Impact of mouse tracheal basal cell expansion medium on formation and metabolic characteristics of tracheospheres
小鼠气管基底细胞扩增培养基对气管球形成及代谢特性的影响
| 期刊: | BMC Molecular and Cell Biology | 影响因子: | 2.700 |
| 时间: | 2025 | 起止号: | 2025 Oct 20;26(1):31 |
| doi: | 10.1186/s12860-025-00554-8 | ||
文献解析
1. 领域背景与文献
文献英文标题:Impact of mouse tracheal basal cell expansion medium on formation and metabolic characteristics of tracheospheres;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:呼吸系统干细胞与类器官研究。
气道类器官是当前肺脏研究的核心模型体系,领域发展关键节点包括:2009年研究证实气道基底细胞是小鼠气管和人气道上皮的成体干细胞,奠定了气管球培养的细胞理论基础;2016年双SMAD信号抑制技术的建立,实现了上皮基底细胞的长期体外扩增,极大推动了基底细胞相关研究的开展;2019年以来,气道类器官被广泛应用于肺损伤修复、肺部疾病建模、呼吸道病毒感染机制解析及个性化药物筛选等方向。当前该领域的研究热点包括类器官培养体系的优化、基底细胞分化调控机制的解析、利用类器官模拟特发性肺纤维化等难治性肺部疾病的病理过程。该领域尚未解决的核心问题是,不同实验室采用的基底细胞扩增培养方案存在较大异质性,其对后续3D类器官的表型、功能的影响尚未得到系统性阐明,导致不同研究间的结果可比性较差,难以实现培养体系的标准化。
现有研究已证实培养基组分可显著调控干细胞的干性维持、代谢状态及分化潜能,但针对气道基底细胞扩增培养基的头对头比较研究较为缺乏,无法明确培养基引入的实验变量对后续实验结果的影响。本研究针对这一研究空白,通过对比三种已被广泛使用的小鼠气管基底细胞扩增培养基,明确扩增阶段培养基组分对后续3D气管球形成、分化及分子特征的调控效应,为气道类器官培养体系的标准化提供实验依据,同时为肺纤维化类器官研究的方案选择提供参考,具有重要的方法学指导价值。
2. 文献综述解析
作者的评述逻辑按照类器官研究的方法学异质性维度展开,分别从培养方案的差异、培养基组分的功能效应、现有评价方法的局限性三个方面梳理现有研究进展。
现有研究的关键结论包括:气道基底细胞具有成体干细胞特性,可在3D培养条件下自组装形成包含基底细胞、纤毛细胞和分泌细胞的气管球,可较好模拟体内气道上皮的结构与功能;不同物种、不同组织来源的气道基底细胞培养方案存在明显差异,基础培养基配方、添加因子组合、培养环境条件均会影响细胞的干性维持与分化潜能;在间充质干细胞、肠道类器官等其他培养体系中已证实,培养基组成会显著改变细胞的代谢与分化表型,进而影响实验结果的可靠性。现有技术的优势在于,气管球培养体系可重现体内气道上皮的生理功能,适用于分化机制研究、药物毒性筛选等场景;基于机器学习的类器官图像分析技术可实现无损伤、高通量的表型量化,降低人工计数带来的操作者误差;转录组、代谢组联合分析可系统解析类器官的分子特征,为表型差异提供机制层面的解释。现有研究的局限性在于,缺乏对不同基底细胞扩增培养基效应的系统性头对头比较,无法量化培养基引入的实验变量大小;多数研究依赖终点的分子生物学检测(如单细胞RNA测序、免疫荧光染色),检测成本较高且无法实现对类器官生长的连续监测;针对气管球的标准化评价体系尚未建立,不同实验室的实验结果难以进行横向比较。
本研究的创新价值体现在三个方面:首次系统性对比三种已报道的小鼠气管基底细胞扩增培养基对后续3D气管球表型的影响,明确了扩增阶段培养基组分可显著改变气管球的形成效率、分化状态、代谢谱及转录组特征;证实扩增培养基的差异会导致特发性肺纤维化相关信号通路的激活状态改变,为肺纤维化类器官研究的培养方案选择提供了直接参考;建立了基于图像分析、代谢组检测的低成本、高通量气管球评价体系,可替代部分高成本的终点检测方法,为类器官培养的标准化提供了新的评价思路。
3. 研究思路总结与详细解析
本研究的整体目标是明确小鼠气管基底细胞扩增阶段的培养基组分对后续3D气管球形成、分化及分子特征的影响,核心科学问题是扩增期培养基如何通过调控基底细胞的干性、代谢及分化潜能,改变后续气管球的表型与分子特征,技术路线遵循“小鼠气管基底细胞分离→三种培养基平行扩增→统一3D气管球培养→多维度表型检测(图像分析、实时荧光定量PCR、代谢组、转录组)→数据整合分析→结论”的闭环逻辑,所有分组均排除了细胞分离、3D培养阶段的混杂变量,仅保留扩增阶段培养基的单一变量差异。
3.1 小鼠气管基底细胞分离与扩增培养
本环节的核心目标是获得同质的原代小鼠气管基底细胞,并在三种不同培养基中完成平行扩增,排除细胞分离过程的混杂变量。实验采用8-12周龄C57BL/6NJ小鼠(n=9),通过蛋白酶灌注法分离气管上皮细胞,将分离得到的细胞充分混匀后平均分为3组,分别接种于胶原蛋白包被的T75培养瓶中,使用三种培养基培养至汇合度,培养时长约10天。三种培养基的配方差异为:培养基1为添加霍乱毒素、胰岛素、转铁蛋白、牛垂体提取物、表皮生长因子、地塞米松的无血清培养基;培养基2在基础组分中添加5%胎牛血清、视黄酸,调整了生长因子的工作浓度;培养基3在培养基2的基础上额外添加ALK2抑制剂DMH-1、TGF-β受体抑制剂A-83-01、ROCK抑制剂Y27632。实验结果显示三组细胞均成功扩增至足够用于后续3D培养的细胞量,镜下观察显示三组细胞均呈现典型的基底细胞上皮样形态,扩增阶段未观察到明显的形态学差异(文献未明确提供该阶段的量化统计数据)。实验所用关键产品:Sigma的蛋白酶14(货号p-5147)、Gibco的DMEM/F12基础培养基、Corning的胶原蛋白凝胶(货号354236);其余试剂未明确提及品牌,领域常规使用细胞培养级添加因子、抗生素类试剂。
3.2 3D气管球培养与形态学分析
本环节的核心目标是在统一的3D培养条件下,比较不同扩增培养基来源的基底细胞的气管球形成能力及形态特征。实验将扩增后的三组基底细胞消化为单细胞悬液,统一使用Pneumacult ALI培养基重悬,与基质胶(Matrigel)按1:1混合后接种于Transwell小室的预包被基质上,37℃固化后于气液界面条件下培养,分别在培养第4、7、12、19天进行明场成像,使用OrgaQuant深度学习算法对气管球进行识别与计数,通过自定义MatLab算法分析气管球的面积、大小分布特征,采用单因素方差分析与Tukey事后检验比较组间差异。实验结果对应明场成像图(图2)与量化分析图(图3),培养第12天时,培养基2、3组的气管球总占比面积显著高于培养基1组(n=3,P<0.05),培养第19天时培养基3组的总占比面积显著高于其余两组(n=3,P<0.001);累积分布函数分析显示,培养基2、3组的气管球尺寸更大,第12天的1-曲线下面积(1-AUC)显著高于培养基1组(n=3,P<0.005),第19天培养基3组的1-AUC最高。上述结果提示扩增阶段使用含血清及信号通路抑制剂的培养基可提升基底细胞的气管球形成能力,促进更大尺寸气管球的生成。
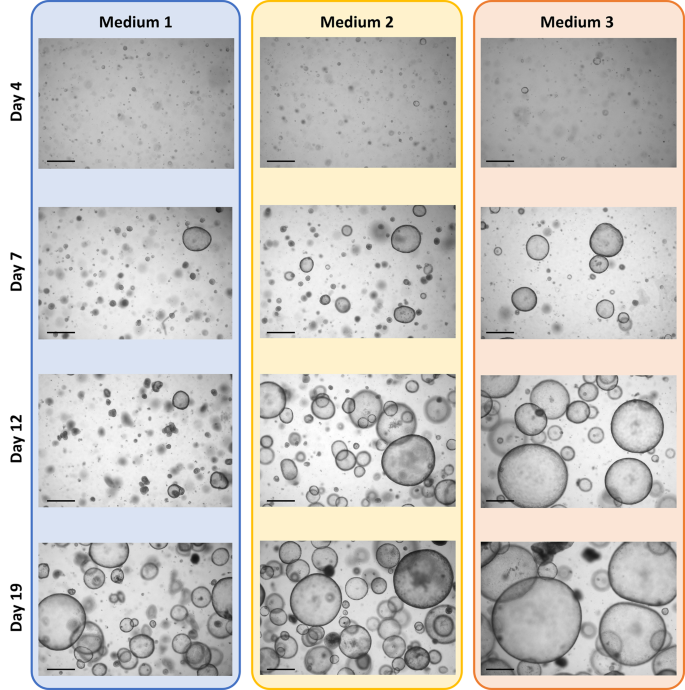
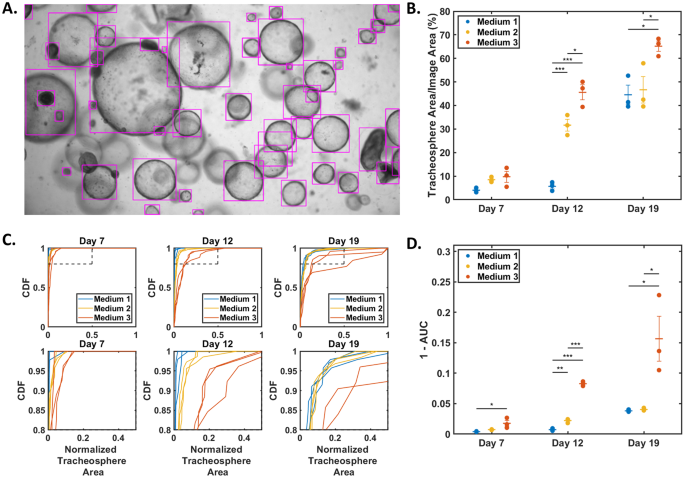
实验所用关键产品:Stemcell Technologies的Pneumacult ALI培养基(货号05001)、Corning的基质胶(货号356231)、Corning的12mm Transwell小室(货号3401)、Olympus的IX70光学显微镜;文献未提及OrgaQuant算法的商业授权情况,领域常规使用开源深度学习工具进行类器官图像分析。
3.3 气管球分化状态的基因表达检测
本环节的核心目标是明确不同扩增培养基对气管球细胞分化与增殖状态的影响。实验分别在3D培养第14天和第21天收集气管球样本,提取总RNA后反转录为cDNA,采用实时荧光定量PCR(qPCR)检测基底细胞标志物角蛋白5、纤毛细胞标志物叉头框蛋白J1、分泌细胞标志物分泌球蛋白1A1、增殖标志物Ki-67的表达水平,以管家基因作为内参,采用单因素方差分析比较组间表达差异。实验结果对应实时荧光定量PCR结果图(图4),第14天时培养基2、3组的叉头框蛋白J1、分泌球蛋白1A1表达水平显著高于培养基1组(n=3,P<0.01),而Ki-67表达水平显著低于培养基1组(n=3,P<0.001);第21天时三组的叉头框蛋白J1表达无显著差异,培养基2组的分泌球蛋白1A1表达仍显著高于其余两组(n=3,P<0.05),三组角蛋白5的表达在两个时间点均无显著差异。上述结果提示扩增阶段使用含血清的培养基可促进基底细胞在3D培养中更早分化为纤毛细胞和分泌细胞,而无血清的培养基1组细胞增殖状态维持更久。

实验所用关键产品:Corning的细胞回收液(货号354253)、Qiagen的RNeasy RNA提取试剂盒(货号74104)、BioRad的SYBR Green实时荧光定量PCR试剂;引物序列未明确提及品牌,领域常规使用商业化合成的实时荧光定量PCR引物。
3.4 气管球的代谢组特征分析
本环节的核心目标是解析不同扩增培养基来源的气管球的代谢谱差异,探索低成本的类器官状态监测指标。实验收集3D培养第14天的条件培养基,采用液相色谱-质谱联用技术进行靶向代谢组分析,检测中心碳代谢、氨基酸代谢相关的代谢物丰度,采用单因素方差分析筛选差异代谢物,通过Ingenuity Pathway Analysis(IPA)进行代谢通路富集分析,同时采用乳酸检测试剂盒测定条件培养基中的乳酸浓度。实验结果对应代谢组热图与通路分析图(图5),培养基2、3组的条件培养基中糖酵解中间体(己糖磷酸、丙酮酸、乳酸)、三羧酸循环(TCA循环)中间体(富马酸、苹果酸、草酰乙酸、柠檬酸)的丰度显著高于培养基1组(n=3,P<0.05),而组氨酸、丝氨酸、谷氨酸等氨基酸的丰度显著低于培养基1组;通路分析显示两组间差异最显著的代谢通路为氨基酸合成与降解通路、葡萄糖代谢通路、尿素循环通路。上述结果提示培养基2、3组的气管球能量代谢更活跃,糖酵解和三羧酸循环通量更高,而培养基1组的氨基酸周转速率更高。
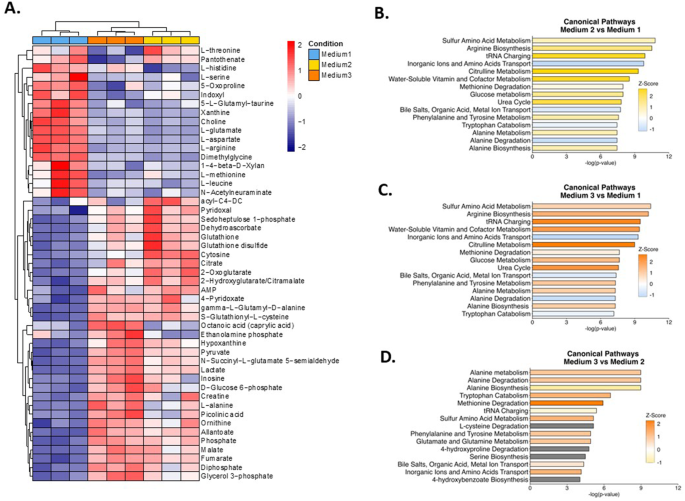
实验所用关键产品:Eton Bioscience的L-乳酸检测试剂盒;代谢组检测由科罗拉多大学医学院代谢组学平台完成,文献未提及具体色谱、质谱试剂品牌,领域常规使用色谱级有机溶剂、质谱级代谢物标准品。
3.5 气管球的转录组特征分析
本环节的核心目标是从转录组层面明确扩增培养基对气管球基因表达与信号通路的调控效应。实验提取3D培养第14天的气管球总RNA,进行bulk RNA测序,采用STAR软件比对测序读段,DESeq2软件分析差异表达基因(筛选标准:校正后P<0.05,log2倍数变化绝对值>1.5),通过主成分分析评估组间表达谱差异,采用IPA进行信号通路富集分析,并比对已发表的特发性肺纤维化异常基底样细胞特征基因集。实验结果对应转录组分析图(图6、图7),主成分分析显示三组样本的表达谱各自聚类,培养基2和3组的表达谱更相似,与培养基1组沿第一主成分(解释83.3%变异)明显分离;培养基1与2、3组的差异表达基因分别为7437个和8643个,而培养基2和3组间仅2176个差异基因;通路富集分析显示,与培养基1组相比,培养基2、3组的肝纤维化、特发性肺纤维化信号通路显著上调(Z值为正,校正后P<0.05),伤口愈合、成纤维细胞信号通路也存在激活;特发性肺纤维化相关基因的表达存在组间差异,如I型胶原α1链、Wnt10b在培养基1组高表达,而V型胶原α3链、VI型胶原α1链、Wnt5a、角蛋白17在培养基2、3组高表达,其中角蛋白17是异常基底样细胞的标志性基因。上述结果提示扩增培养基可显著调控气管球的纤维化相关信号通路激活状态,不同培养基的类器官模型适用于不同的研究场景。
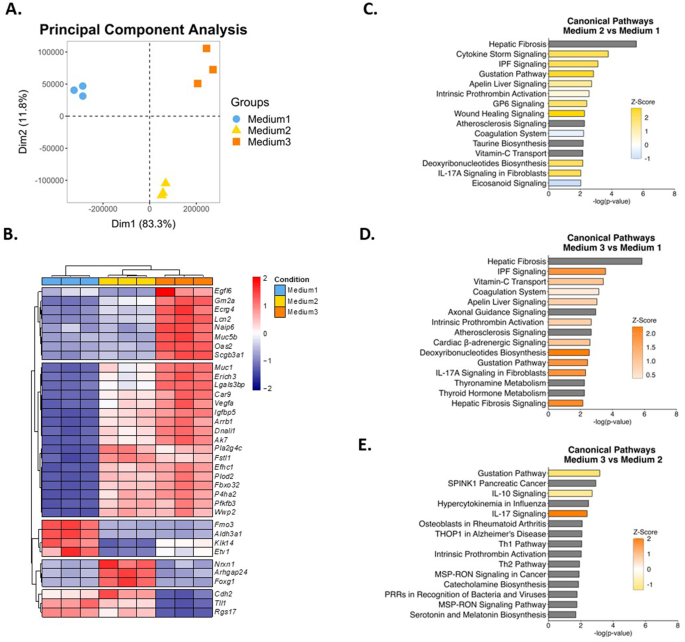
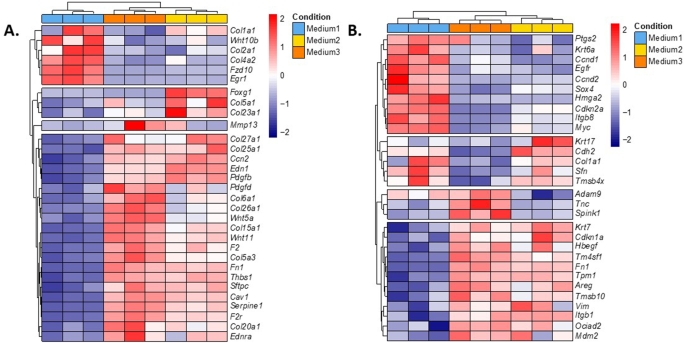
实验所用关键产品:Novogene提供RNA测序文库构建与测序服务;分析使用的R包(DESeq2、pheatmap等)均为开源工具,文献未明确提供测序试剂品牌,领域常规使用商业化RNA建库试剂盒与高通量测序平台。
4. Biomarker研究及发现成果
本研究涉及的Biomarker分为两类,一类是用于评价气管球功能状态的Biomarker,包括代谢物标志物和分化相关基因标志物,另一类是与肺纤维化相关的分子Biomarker,整体筛选遵循“表型差异检测→分子组学筛选→功能通路关联”的完整逻辑链条。
对于功能状态类Biomarker,其来源为3D培养的条件培养基与气管球组织,验证方法包括实时荧光定量PCR检测基因表达、质谱检测代谢物丰度。其中条件培养基中的乳酸浓度在第14天可有效区分培养基1组与培养基2、3组(组间差异P<0.05),三羧酸循环中间体的丰度与气管球的分化程度呈正相关,无需裂解样本即可实现动态检测;分化相关基因标志物中,叉头框蛋白J1、分泌球蛋白1A1的表达水平在第14天的组间差异倍数可达3倍以上(n=3,P<0.01),可准确反映气管球的分化成熟状态。对于纤维化相关Biomarker,其来源为气管球组织,验证方法为RNA测序,其中角蛋白17在培养基3组的表达水平显著高于其余两组,与已报道的特发性肺纤维化异常基底样细胞特征一致,V型胶原α3链、VI型胶原α1链等胶原基因在培养基2、3组的表达上调倍数可达2倍以上(校正后P<0.05)。
核心成果方面,功能状态Biomarker可用于气管球培养的质量控制:条件培养基中的乳酸、三羧酸循环中间体丰度可作为无损伤监测气管球分化状态的代谢标志物,无需裂解样本即可实现动态检测,适合大规模类器官培养的高通量筛选;叉头框蛋白J1、分泌球蛋白1A1的表达水平可反映扩增培养基对基底细胞分化潜能的影响,第14天的表达差异可预测后续气管球的成熟速度。纤维化相关Biomarker的结果显示,不同扩增培养基可导致气管球的特发性肺纤维化相关信号通路激活状态差异,角蛋白17、V型胶原α3链等基因的表达水平可作为评价气管球纤维化相关表型的指标,其中培养基3组的角蛋白17高表达提示该培养体系可能更适用于模拟特发性肺纤维化的异常基底细胞表型;值得注意的是,不同培养基导致的纤维化相关基因表达谱存在异质性,无单一Biomarker可全面反映培养基的效应,需结合多基因特征判断。本研究所有组学数据均经过多重检验校正,差异结果的统计学显著性均满足P<0.05的标准。
推测:本研究发现的培养基对纤维化通路的调控效应,提示在利用气管球开展特发性肺纤维化相关研究时,需严格控制扩增培养基的选择,避免引入实验偏倚,确保研究结果的可靠性。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。