Functional heterogeneity of cancer-associated fibroblasts with distinct neoadjuvant immunotherapy plus chemotherapy response in esophageal squamous cell carcinoma
食管鳞状细胞癌新辅助免疫治疗联合化疗反应不同的癌相关成纤维细胞的功能异质性
| 期刊: | Biomarker Research | 影响因子: | 9.500 |
| 时间: | 2024 | 起止号: | 2024 Sep 27;12(1):113. |
| doi: | 10.1186/s40364-024-00656-z | 研究方向: | 肿瘤 |
| 疾病类型: | 食管癌 | 细胞类型: | 成纤维细胞 |
文献解析
1. 领域背景与文献引入
文献英文标题:Functional heterogeneity of cancer-associated fibroblasts with distinct neoadjuvant immunotherapy plus chemotherapy response in esophageal squamous cell carcinoma;发表期刊:Biomarker Research;影响因子:未公开;研究领域:食管鳞状细胞癌肿瘤微环境与新辅助免疫联合化疗响应。
食管鳞状细胞癌(ESCC)是全球第六大癌症死因,占食管癌的85%,5年生存率仅15-25%。近年来,新辅助免疫联合化疗(neoICT,如替雷利珠单抗联合卡铂+白蛋白紫杉醇)显著提高了ESCC患者的病理完全缓解(pCR)率,但仍有近半数患者响应率低或出现耐药。肿瘤微环境(TME)的异质性是治疗响应差异的核心因素,其中癌相关成纤维细胞(CAFs)作为TME的主要 stromal 细胞,参与细胞外基质(ECM)重塑、免疫抑制及药物耐药,但ESCC患者neoICT后CAFs的功能异质性及与治疗响应的关系尚不明确。因此,解析neoICT后TME中CAFs的动态变化及功能表型,对揭示治疗耐药机制、提高ESCC患者的治疗响应具有重要意义。本研究针对这一空白,通过单细胞RNA测序(scRNA-seq)和多重免疫荧光(mfIHC),系统解析了ESCC患者neoICT前后TME的细胞组成变化,重点阐明了CAFs的功能亚型与治疗响应的关联及机制。
2. 文献综述解析
作者对现有研究的分类维度主要围绕CAFs的异质性及功能:
1. CAFs的亚型分类:现有研究将CAFs分为肌成纤维细胞CAFs(myCAFs,表达ACTA2、FAP)、炎症性CAFs(iCAFs,表达IL6、CCL2)、抗原呈递CAFs(apCAFs)等,但ESCC中CAFs的亚型鉴定及功能研究不足;
2. CAFs的功能:myCAFs通过分泌胶原蛋白(如COL1A1)重塑ECM,形成物理屏障阻碍T细胞浸润;iCAFs通过分泌炎症因子(如IL6)招募 immunosuppressive细胞(如M2巨噬细胞),促进免疫抑制;
3. 现有研究的局限性:多基于细胞系或动物模型,缺乏ESCC患者neoICT前后CAFs的单细胞水平动态分析,且CAFs与T细胞相互作用介导治疗耐药的机制尚未阐明。
本研究的创新点在于:
- 首次在ESCC患者中,通过scRNA-seq解析了neoICT前后CAFs的功能异质性;
- 鉴定出与治疗耐药相关的CAFs亚型(CD248+机械响应CAFs、IL6+CCL2+免疫调节CAFs);
- 揭示了CAFs与T细胞通过TIGIT-NECTIN2相互作用介导免疫抑制的机制,为靶向CAFs提高neoICT响应提供了新靶点。
3. 研究思路总结与详细解析
3.1 整体框架
研究目标:解析ESCC患者neoICT后TME的动态变化,尤其是CAFs的功能表型与治疗响应的关系。
核心科学问题:CAFs亚型如何介导neoICT耐药?
技术路线:临床样本收集→scRNA-seq分析TME细胞组成→CAFs亚型鉴定→功能机制研究(轨迹分析、转录因子调控)→CAFs与T细胞相互作用分析→mfIHC临床验证→生存分析。
3.2 临床样本收集与单细胞RNA测序
实验目的:获取neoICT前后的ESCC样本,进行单细胞转录组分析。
方法细节:纳入18例ESCC患者,收集41份样本(17份治疗前内镜活检,24份治疗后手术切除),其中6例为配对样本;样本经sCelLive™组织保存液保存,酶解成单细胞悬液(用Singleron PythoN™组织解离系统),通过10x Genomics平台进行scRNA-seq;数据过滤标准:基因数200-前2%、UMI数前2%、线粒体含量<50%。
结果解读:共获得232710个高质量细胞,平均每个细胞检测到1343个基因、4782个UMI;细胞类型注释显示,TME包含上皮细胞、单核吞噬细胞、成纤维细胞、T细胞等11种细胞类型。
产品关联:实验所用关键产品:Singleron的sCelLive™组织保存液、sCelLive™组织解离液;10x Genomics单细胞测序平台;抗体:ADH1B(Proteintech,Cat#19899-1)、CD248(Abcam,Cat#ab204914)等。
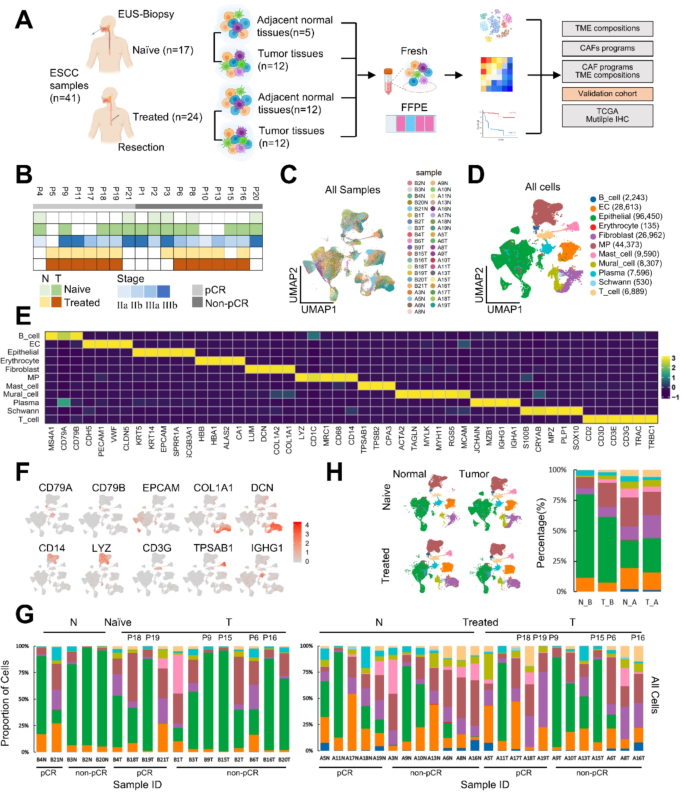
3.3 肿瘤微环境细胞类型鉴定与动态变化分析
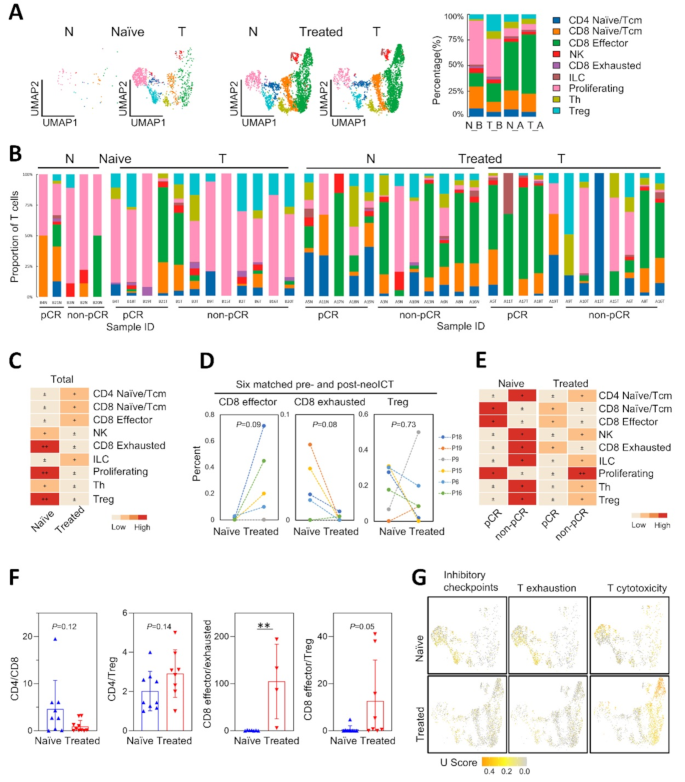
实验目的:分析neoICT前后TME细胞组成的变化。
方法细节:用Cell-ID和SynEcoSys™(基于CellMakerDB、PanglaoDB)注释细胞类型;用STARTRAC-dist分析细胞类型的富集程度;用Mann-Whitney U检验和Wilcoxon配对检验比较治疗前后的差异。
结果解读:
- neoICT后,上皮细胞比例降低(P<0.05),成纤维细胞、免疫细胞(如cDC2)比例升高(P<0.05);
- 单核吞噬细胞中,MT1G+M2巨噬细胞(促肿瘤)在non-pCR组富集(P<0.05),与不良预后相关(TCGA生存分析P=5.02e-05);
- 内皮细胞中,静脉EC比例升高(P<0.05),毛细血管EC和增殖EC比例降低(P<0.05)。
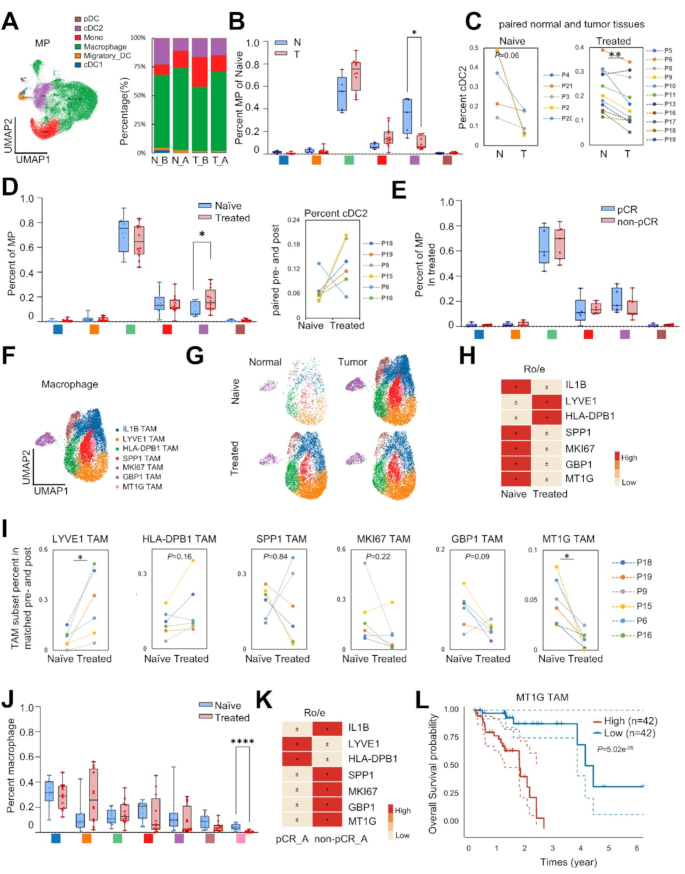
3.4 癌相关成纤维细胞亚型的鉴定与功能解析
实验目的:鉴定ESCC中CAFs的亚型及功能。
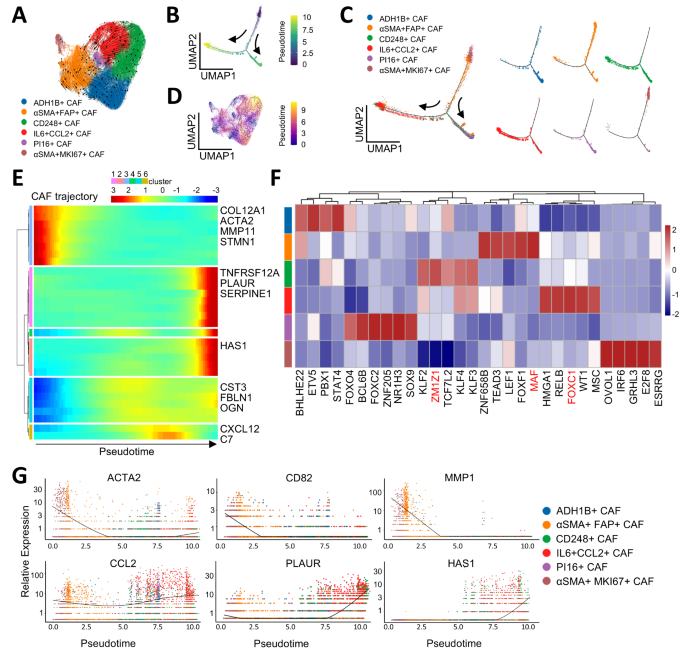
方法细节:对26962个成纤维细胞进行无监督聚类;基于差异基因表达(如ADH1B、CD248、IL6)和GO分析(ECM组织、炎症反应)定义亚型;用Monocle2/3进行轨迹分析,鉴定CAFs的分化路径;用转录因子(TF)分析解析调控网络。
结果解读:
- CAFs亚型鉴定:6种亚型,包括2种稳态样CAFs(ssl-CAFs:ADH1B+、PI16+)、3种机械响应CAFs(mr-CAFs:αSMA+FAP+、αSMA+MKI67+、CD248+)、1种免疫调节CAFs(im-CAFs:IL6+CCL2+);
- 动态变化:neoICT后,αSMA+FAP+mr-CAFs比例降低(P<0.05),CD248+mr-CAFs和IL6+CCL2+im-CAFs比例升高(P<0.05);
- 功能机制:
- CD248+mr-CAFs:表达CD248、S100A4等机械响应基因,位于肿瘤巢周围,形成物理屏障阻碍CD8+T细胞浸润;
- IL6+CCL2+im-CAFs:表达IL6、CCL2等炎症基因,诱导免疫抑制;
- 轨迹分析:αSMA+FAP+mr-CAFs分化为CD248+mr-CAFs和IL6+CCL2+im-CAFs,转录因子MAF调控αSMA+FAP+mr-CAFs,ZMIZ1调控CD248+mr-CAFs,FOXC1调控IL6+CCL2+im-CAFs。
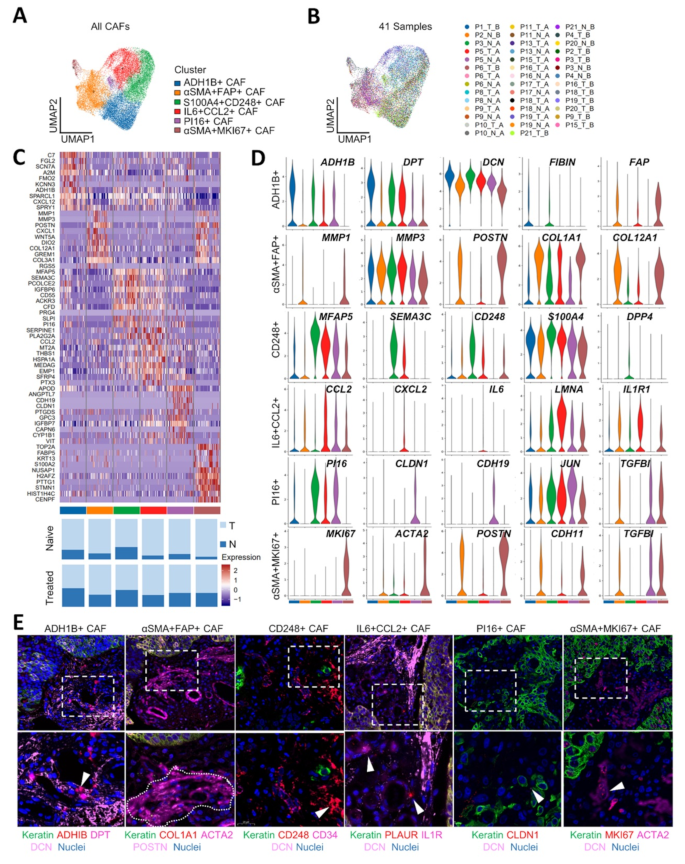
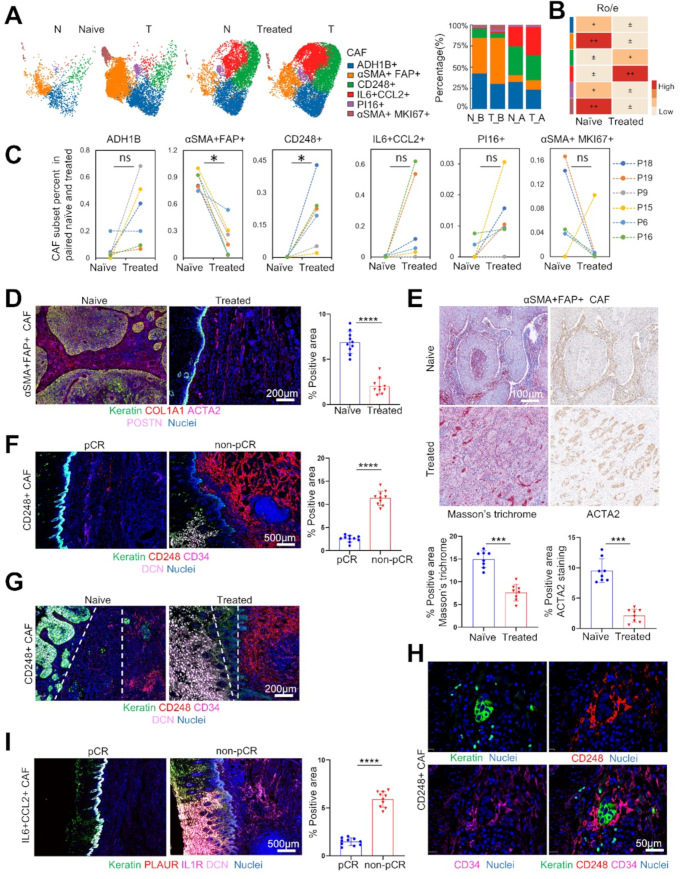
3.5 癌相关成纤维细胞与T细胞相互作用机制研究
实验目的:解析CAFs与T细胞的相互作用及对免疫抑制的影响。
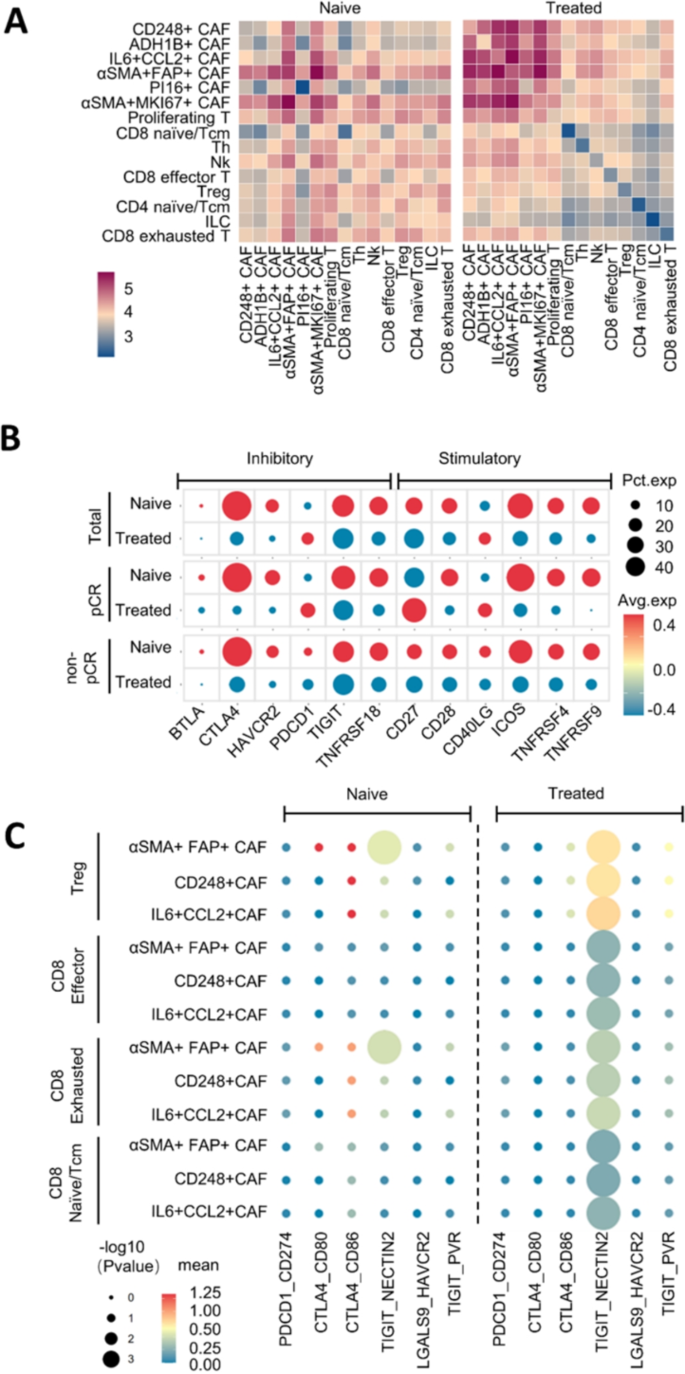
方法细节:用CellPhoneDB分析CAFs与T细胞的配体-受体对;用mfIHC验证配体(NECTIN2)和受体(TIGIT)的表达;比较pCR与non-pCR组的相互作用差异。
结果解读:
- 相互作用变化:neoICT后,CTLA4-CD86/80相互作用降低,TIGIT-NECTIN2相互作用增强;
- 关键机制:CD248+mr-CAFs和IL6+CCL2+im-CAFs高表达NECTIN2,与T细胞表面TIGIT结合;non-pCR组中,Tregs与CAFs的TIGIT-NECTIN2相互作用显著高于pCR组(P<0.05),促进免疫抑制;
- 次要机制:PDCD1/CD274相互作用较弱,不是主要的免疫抑制通路。
3.6 临床样本验证与生存分析
实验目的:验证CAFs亚型与治疗响应的关系。
方法细节:对10例患者的FFPE样本进行mfIHC染色,检测CAFs标志物(αSMA、FAP、CD248、IL6)的表达;用ImageJ量化染色强度;用TCGA数据库分析CAFs基因 signature 与生存的关系。
结果解读:
- 临床验证:neoICT后,αSMA+FAP+mr-CAFs比例降低(P<0.0001),CD248+mr-CAFs和IL6+CCL2+im-CAFs比例升高(P<0.0001);non-pCR组CD248+mr-CAFs和IL6+CCL2+im-CAFs比例显著高于pCR组(P<0.0001);
- 生存分析:αSMA+FAP+mr-CAFs基因 signature 与多种癌症(如BLCA、KIRC)的不良预后相关(P<0.05)。
4. Biomarker研究及发现成果解析
4.1 Biomarker定位
本研究涉及的Biomarker包括:
- CAFs亚型:CD248+机械响应CAFs(mr-CAFs)、IL6+CCL2+免疫调节CAFs(im-CAFs);
- T细胞抑制性 checkpoint:TIGIT(表达于T细胞表面)。
筛选逻辑:scRNA-seq聚类→差异基因表达→临床样本mfIHC验证→生存分析关联;
验证逻辑:单细胞水平鉴定→组织水平量化→治疗响应关联→机制验证。
4.2 研究过程详述
- 来源:ESCC患者的肿瘤组织样本;
- 验证方法:scRNA-seq检测基因表达,mfIHC检测蛋白水平,CellPhoneDB分析相互作用;
- 特异性与敏感性:
- CD248+mr-CAFs:non-pCR组比例显著高于pCR组(n=10,P<0.0001);
- IL6+CCL2+im-CAFs:non-pCR组比例显著高于pCR组(n=10,P<0.0001);
- TIGIT:non-pCR组T细胞表达水平显著高于pCR组(P<0.05);
- 功能关联:
- CD248+mr-CAFs:形成物理屏障,阻碍CD8+T细胞浸润和药物递送;
- IL6+CCL2+im-CAFs:通过IL6诱导治疗耐药;
- TIGIT-NECTIN2:CAFs表达NECTIN2与T细胞TIGIT结合,促进免疫抑制;
- 创新性:首次在ESCC中鉴定出CD248+mr-CAFs作为机械响应亚型,揭示其与T细胞通过TIGIT-NECTIN2相互作用介导耐药。
4.3 核心成果提炼
- CD248+mr-CAFs:作为ESCC患者neoICT耐药的 Biomarker,其高表达与non-pCR相关(P<0.0001),可通过靶向CD248破坏物理屏障,提高T细胞浸润;
- IL6+CCL2+im-CAFs:作为免疫抑制 Biomarker,其高表达与non-pCR相关(P<0.0001),可通过IL6抑制剂降低炎症反应;
- TIGIT:作为T细胞抑制性 checkpoint,其与NECTIN2的相互作用是免疫抑制的关键,靶向TIGIT可恢复T细胞功能。
本研究为ESCC患者neoICT的个性化治疗提供了新的 Biomarker 和靶点,具有重要的临床转化价值。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。