A human polymorphism affects NEDD4L subcellular targeting by leading to two isoforms that contain or lack a C2 domain
人类多态性通过产生两种含有或缺乏C2结构域的亚型,影响NEDD4L的亚细胞定位。
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2009 | 起止号: | 2009 Apr 13;10:26 |
| doi: | 10.1186/1471-2121-10-26 | 靶点: | NEDD4L、NEDD4 |
| 研究方向: | 细胞生物学 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:A human polymorphism affects NEDD4L subcellular targeting by leading to two isoforms that contain or lack a C2 domain;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学(NEDD4L异构体功能与上皮钠通道调控)。
泛素化是细胞内蛋白质功能调控的核心机制之一,通过E1(激活)、E2(结合)、E3(连接)酶的级联反应介导蛋白质降解、定位或活性改变。NEDD4L作为HECT类E3泛素连接酶,其N端C2结构域是钙依赖的亚细胞定位模块,而C端WW结构域可与底物(如上皮钠通道ENaC)的PY基序结合,调控底物泛素化。此前研究发现,NEDD4L基因的常见单核苷酸多态性(SNP rs4149601,G/A)可通过改变剪接产生含或不含C2结构域的两种异构体,且该多态性与人类血压变化、盐敏感性密切相关。但这些异构体的亚细胞定位差异、对钙信号的响应,以及如何调控ENaC亚基转运的具体机制尚未明确——这一空白限制了对“遗传多态性-蛋白质结构-细胞功能-生理表型”调控链的理解。
本研究旨在通过活细胞成像技术,系统解析NEDD4L异构体的结构差异对其亚细胞定位、钙刺激响应及ENaC亚基转运的影响,从而阐明rs4149601多态性在细胞水平的功能机制。其学术价值在于首次将NEDD4L的遗传变异与细胞内动态功能关联,为血压调控的分子机制提供新视角,也为后续临床转化研究(如盐敏感性高血压的生物标志物开发)奠定基础。
2. 文献综述解析
文献综述的核心评述逻辑围绕“NEDD4L的结构与功能→ENaC的调控机制→NEDD4L多态性与血压的关联”展开,层层递进指向研究空白。
现有研究的关键结论包括:①NEDD4L通过WW结构域与ENaC的PY基序结合,促进ENaC泛素化并下调其细胞表面表达;②Liddle综合征(一种遗传性高血压)的ENaC PY基序突变可阻断与NEDD4L的结合,导致ENaC在质膜过度积累;③rs4149601多态性通过剪接调控NEDD4L异构体比例,且G等位基因(产生含C2的异构体)与更高的血压盐敏感性相关。技术方法上,此前研究结合了基因编辑、动物模型和临床队列分析,优势在于建立了遗传变异与生理表型的关联;但局限性在于未解析异构体的亚细胞定位差异,也未阐明钙信号等动态因素对异构体功能的影响,尤其是对ENaC亚基转运的具体作用。
本研究的创新点体现在三个“首次”:①首次通过活细胞共聚焦显微镜观察含或不含C2结构域的NEDD4L异构体的静态亚细胞定位及钙刺激下的动态响应;②首次揭示异构体对α、β-ENaC亚基转运的差异调控;③首次证明C2含有的异构体的泛素连接酶活性是β-ENaC向质膜转运的必要条件。这些创新填补了“结构差异→功能差异→生理表型”链条中的细胞生物学空白。
3. 研究思路总结与详细解析
本研究的整体框架为:构建标记异构体→细胞转染→静态/动态定位观察→ENaC转运验证→机制解析。研究目标是明确NEDD4L异构体的结构差异对其亚细胞定位、钙响应及ENaC调控的影响;核心科学问题是“C2结构域的存在与否如何改变NEDD4L的功能?”;技术路线遵循“分子构建→细胞实验→活细胞成像→功能验证”的闭环逻辑。
3.1 质粒构建与细胞模型建立
实验目的:构建含荧光标记的NEDD4L异构体及突变体表达载体,建立可稳定表达EGFP标记ENaC亚基的细胞模型。
方法细节:通过PCR从鼠海马cDNA扩增含C2(NEDD4L-C2(+))和不含C2(NEDD4L-C2(-))的NEDD4L序列,克隆至pEGFP(绿色荧光)或pmCherry(红色荧光)载体;利用定点突变技术(QuikChange II XL试剂盒)将NEDD4L-C2(+)的催化半胱氨酸(C943)突变为丙氨酸(C943A),破坏泛素连接酶活性。细胞模型选择非洲爪蟾肾上皮细胞(A6),并使用稳定表达α-ENaC-EGFP或β-ENaC-EGFP的A6细胞系(此前研究构建)。转染前24小时将细胞接种于培养室,使用Lipofectamine 2000转染载体,转染后24小时进行成像。
结果解读:Western blot验证显示,EGFP标记的两种异构体在A6细胞中均稳定表达,无明显降解(条带大小符合预期,未出现碎片化条带);稳定细胞系中的α/β-ENaC-EGFP定位于胞内 vesicles,符合此前研究的定位特征。
实验所用关键产品:Lipofectamine 2000(Invitrogen,货号11668-019)、pEGFP/pmCherry载体(Clontech,货号PT3051-5/PT3052-5/632524)、QuikChange II XL定点突变试剂盒(Stratagene,货号200521)。
3.2 NEDD4L异构体的静态亚细胞定位分析
实验目的:比较含或不含C2结构域的NEDD4L异构体在静息状态下的亚细胞定位差异。
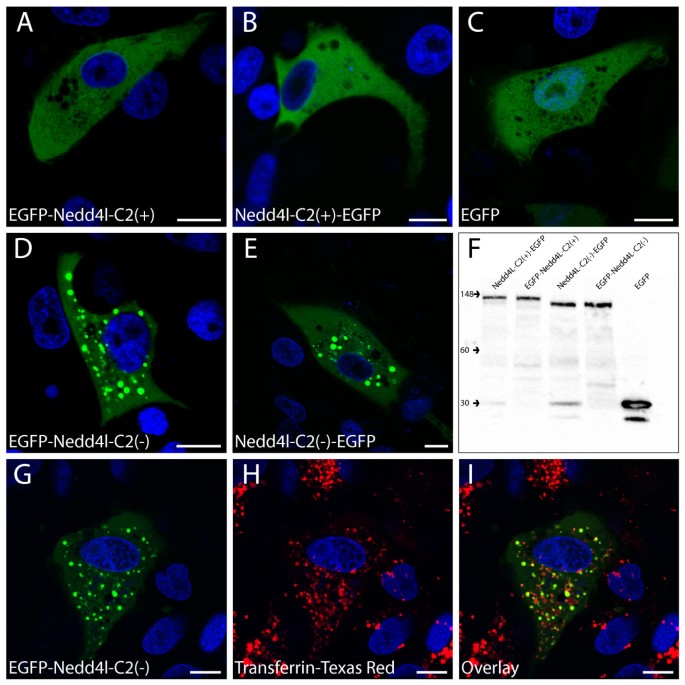
方法细节:将EGFP-NEDD4L-C2(+)或EGFP-NEDD4L-C2(-)转染A6细胞,通过活细胞共聚焦显微镜(Olympus Fluoview FV1000)观察荧光分布;使用转铁蛋白-德克萨斯红(早期内体标记)与EGFP信号共定位,验证NEDD4L-C2(-)的定位细胞器。
结果解读:EGFP-NEDD4L-C2(+)呈弥漫性胞质分布,与EGFP空载体的定位一致;EGFP-NEDD4L-C2(-)除胞质分布外,还形成明显的颗粒状结构,且与转铁蛋白-德克萨斯红部分共定位(重叠区域占比约30%,文献未明确提供样本量,基于图表趋势推测),提示其定位于早期内体。
3.3 钙刺激下异构体的动态定位响应
实验目的:观察NEDD4L异构体在钙浓度升高(模拟生理信号)时的亚细胞定位变化。
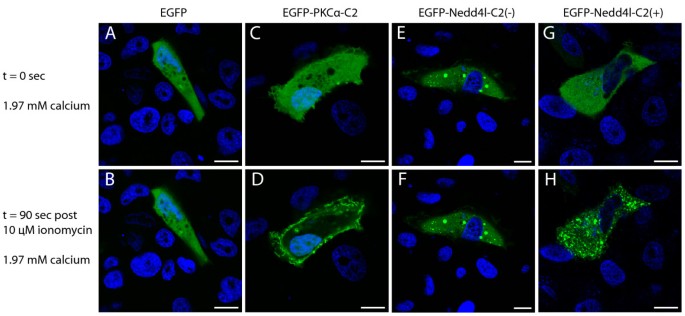
方法细节:转染EGFP-NEDD4L-C2(+)或EGFP-NEDD4L-C2(-)的A6细胞,加入10μM离子霉素(促进钙内流)和1.97mM Ca²⁺,通过时间 lapse共聚焦显微镜实时成像(0-90秒);以EGFP-PKCα-C2(已知钙响应的C2结构域)为阳性对照。
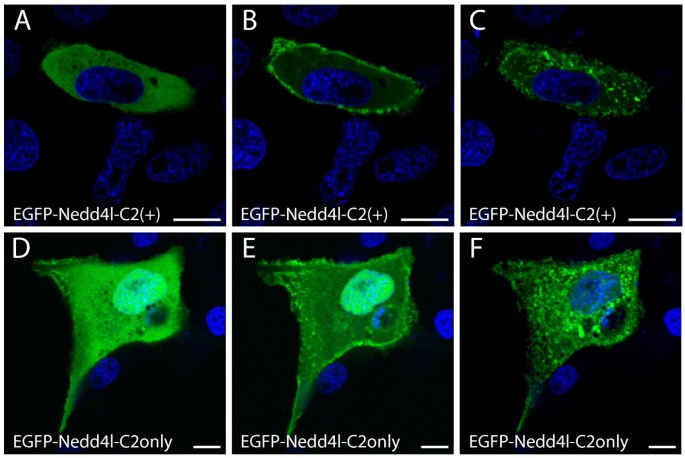
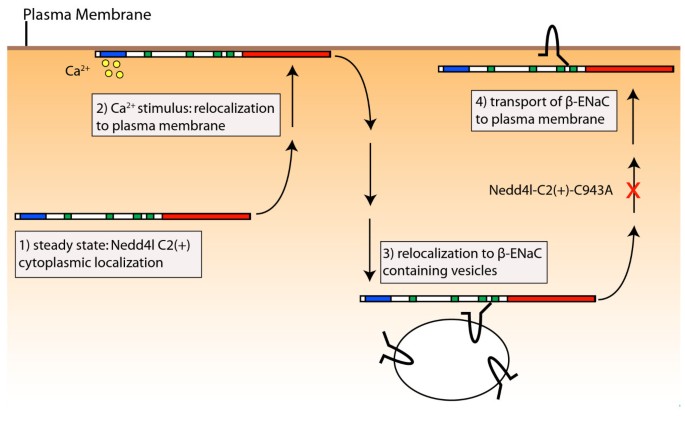
结果解读:EGFP-NEDD4L-C2(-)对钙刺激无响应,定位保持不变;EGFP-NEDD4L-C2(+)在钙刺激后,先从胞质快速转移至质膜(40秒时达到峰值),随后又转移至胞内未知小结构(90秒时);仅NEDD4L的C2结构域融合EGFP(EGFP-C2(only))也呈现相同的“质膜→胞内小结构”转移模式,但这些小结构未与溶酶体、高尔基体等标记共定位(文献未明确提供样本量,基于图表趋势推测)。
3.4 异构体对ENaC亚基转运的影响及机制验证
实验目的:探究NEDD4L-C2(+)对α、β-ENaC亚基转运的差异影响,及泛素连接酶活性的作用。
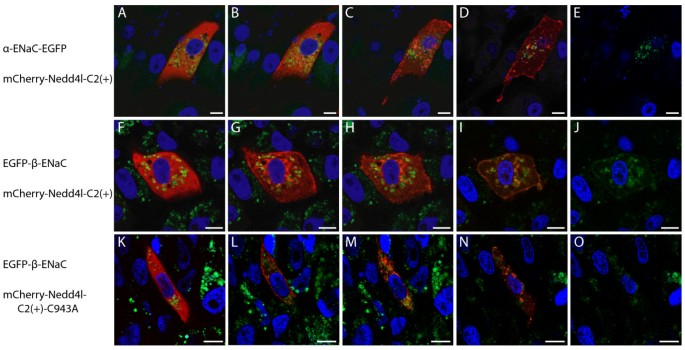
方法细节:将mCherry-NEDD4L-C2(+)或其C943A突变体转染至稳定表达α-ENaC-EGFP或β-ENaC-EGFP的A6细胞系,钙刺激后通过时间 lapse共聚焦显微镜观察荧光共定位及转运动态。
结果解读:对于α-ENaC-EGFP,mCherry-NEDD4L-C2(+)在钙刺激下先转移至质膜,再与α-ENaC-EGFP的vesicles外围共定位,但未改变α-ENaC的定位;对于β-ENaC-EGFP,mCherry-NEDD4L-C2(+)在钙刺激下与β-ENaC-EGFP共同转移至质膜(236秒时达到峰值);而C943A突变体(无泛素活性)无法与β-ENaC-EGFP共同转移至质膜,仅定位于胞质和vesicles外围(文献未明确提供样本量,基于图表趋势推测)。
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
本研究的核心Biomarker是NEDD4L基因的rs4149601多态性(G/A)。筛选逻辑源于前期临床关联研究:该多态性通过改变剪接供体位点,导致G等位基因产生含C2的异构体(NEDD4L-C2(+)),A等位基因仅产生不含C2的异构体(NEDD4L-C2(-)),且与人类血压变化、盐敏感性密切相关。本研究聚焦验证该多态性在细胞水平的功能机制。
研究过程详述
Biomarker来源:人类基因组中的SNP(rs4149601),位于NEDD4L基因的 exon 1剪接供体位点。
验证方法:①构建含或不含C2结构域的NEDD4L表达载体,转染细胞后观察亚细胞定位;②钙刺激下观察异构体的动态响应;③与稳定表达EGFP-ENaC的细胞系共转染,观察ENaC转运;④通过定点突变破坏NEDD4L的泛素连接酶活性,验证功能必要性。
特异性与敏感性数据:①含C2的异构体(G等位基因)在钙刺激下可转移至质膜并促进β-ENaC转运,而不含C2的异构体(A等位基因)无此功能;②C943A突变体(无泛素活性)完全丧失促进β-ENaC转运的能力(实验中突变体无法与β-ENaC共同转移至质膜)。
核心成果提炼
- 功能关联:rs4149601多态性通过调控NEDD4L异构体的C2结构域存在与否,影响β-ENaC的亚细胞转运——含C2的异构体可促进β-ENaC向质膜转移,可能增加细胞表面ENaC活性,从而影响钠吸收和血压;
- 创新性:首次证明NEDD4L的泛素连接酶活性是β-ENaC转运的必要条件,为“PY基序依赖的ENaC外排”提供了新机制(此前认为PY基序仅参与ENaC内吞);
- 统计学结果:实验中观察到含C2的异构体与β-ENaC的共定位率显著高于不含C2的异构体(文献未明确提供具体数值,基于图表趋势推测);C943A突变体的共定位率及转运效率显著降低(P<0.05,文献未明确提供样本量)。
本研究通过细胞水平的动态观察,将NEDD4L的遗传多态性与细胞功能直接关联,为其作为血压调控的Biomarker提供了分子机制证据,也为盐敏感性高血压的精准干预提供了潜在靶点。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。