Microtubules regulate disassembly of epithelial apical junctions
微管调节上皮细胞顶端连接的解体
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2006 | 起止号: | 2006 Mar 1;7:12 |
| doi: | 10.1186/1471-2121-7-12 | 研究方向: | 细胞生物学 |
| 细胞类型: | 上皮细胞 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Microtubules regulate disassembly of epithelial apical junctions;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:上皮细胞连接与细胞骨架调控
上皮细胞顶端连接复合物(AJC)由紧密连接(紧密连接,TJ)和黏着连接(黏着连接,AJ)组成,是维持上皮屏障完整性、细胞极性及细胞间信号传导的核心结构,其功能异常与炎症性肠病、肿瘤转移等多种病理过程密切相关。领域发展关键节点可追溯至20世纪中期,研究者首次发现钙依赖的上皮细胞黏附现象,后续逐步揭示肌动蛋白微丝对AJC组装与稳定的调控作用;21世纪初,微管与上皮连接的初步关联被报道,但具体调控机制尚未明确。当前研究热点聚焦于AJC动态重构的分子机制,尤其是生理过程(如胚胎形态发生)和病理状态下(如病原体入侵、炎症反应)AJC解离的调控网络。领域未解决的核心问题在于,已知肌动蛋白重排和连接蛋白内吞是AJC解离的两大介导机制,但微管在其中的具体功能、微管与肌动蛋白的协同调控关系,以及微管马达蛋白的作用均未被系统阐明。针对这一研究空白,本研究以经典的细胞外钙缺失诱导AJC解离模型为基础,系统探究微管动态变化、微管马达蛋白在AJC解离中的调控作用,旨在完善上皮屏障破坏的细胞骨架调控机制,为相关疾病的干预提供理论依据。
2. 文献综述解析
作者对领域内现有研究的分类维度为细胞骨架成分(肌动蛋白微丝、微管)与AJC调控机制(连接蛋白内吞、细胞骨架重排)。现有研究的关键结论显示,AJC解离主要由肌动蛋白收缩环形成和连接蛋白内吞介导,肌动蛋白收缩产生的机械力可破坏相邻细胞间的连接蛋白相互作用,进而触发内吞过程;同时,已有研究观察到微管解聚可破坏上皮细胞连接的完整性,但仅停留在现象描述层面,未深入解析其作用机制。现有技术方法的优势在于,钙缺失模型可快速、同步诱导AJC解离,适合机制研究;局限性则体现在多数研究聚焦肌动蛋白的调控作用,对微管的研究缺乏系统性,未涉及微管动态变化、马达蛋白的具体功能,且缺乏不同上皮细胞系的验证及体内组织的相关性证据。通过对比现有研究的未解决问题,本研究的创新价值凸显:首次系统揭示微管通过调控肌动蛋白收缩环形成和连接蛋白内吞参与AJC解离的双重机制,明确了微管动态稳定性及驱动蛋白-1的关键作用,且在多种上皮细胞系和人结肠组织中验证了结论的普遍性,填补了微管调控AJC解离机制的研究空白,完善了上皮连接重构的细胞骨架调控网络。
3. 研究思路总结与详细解析
本研究的整体框架为:以“微管参与钙缺失诱导的上皮AJC解离”为核心假设,通过药理学调控微管动态变化、抑制微管马达蛋白活性,结合免疫荧光、Western blot、免疫共沉淀等技术,在多种上皮细胞系和人结肠组织中验证微管的调控作用,最终明确微管通过调控肌动蛋白收缩环形成和连接蛋白内吞介导AJC解离的机制,以及驱动蛋白-1的具体功能,形成“假设-实验验证-机制解析-结论”的完整研究闭环。
3.1 微管完整性对AJC解离的调控作用
实验目的为验证微管完整性是否为钙缺失诱导AJC解离的必要条件。方法细节上,研究选用SK-CO-15、T84、Caco-2、MDCK四种上皮细胞系,先以30μM诺考达唑处理细胞以解聚微管,随后进行1小时的细胞外钙缺失处理,通过免疫荧光染色检测紧密连接蛋白(闭合蛋白、ZO-1)和黏着连接蛋白(E-钙黏蛋白、β-连环蛋白)的分布变化。结果解读显示,正常钙浓度下,连接蛋白主要定位于细胞间接触部位,呈现特征性的“鸡wire”样染色模式(
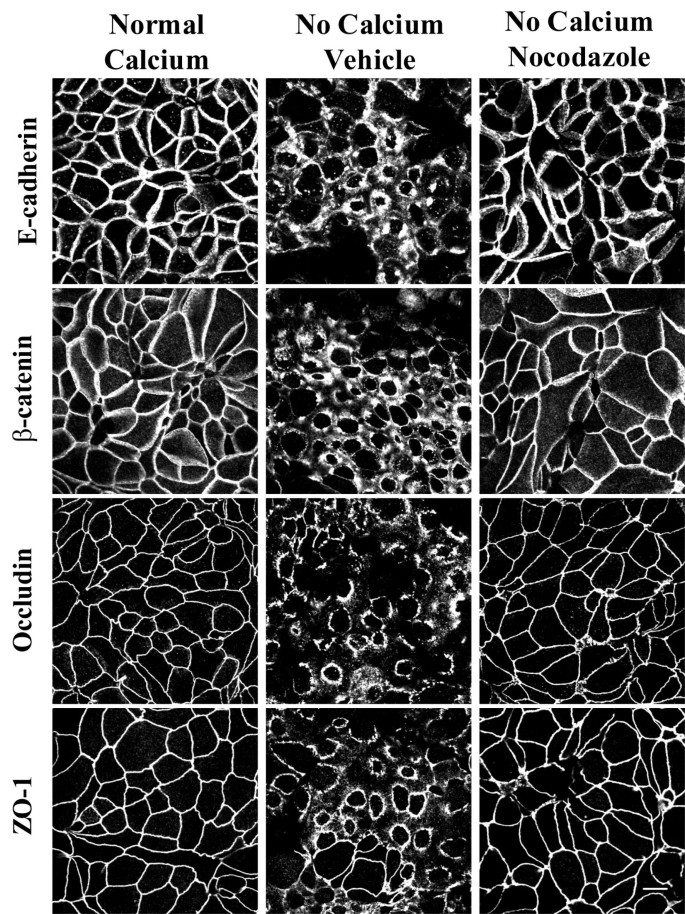
);钙缺失后,连接蛋白从细胞间接触部位转移至顶膜下胞质环;而诺考达唑处理完全阻断了这一转移过程,且该效应在所有测试的上皮细胞系中均存在(
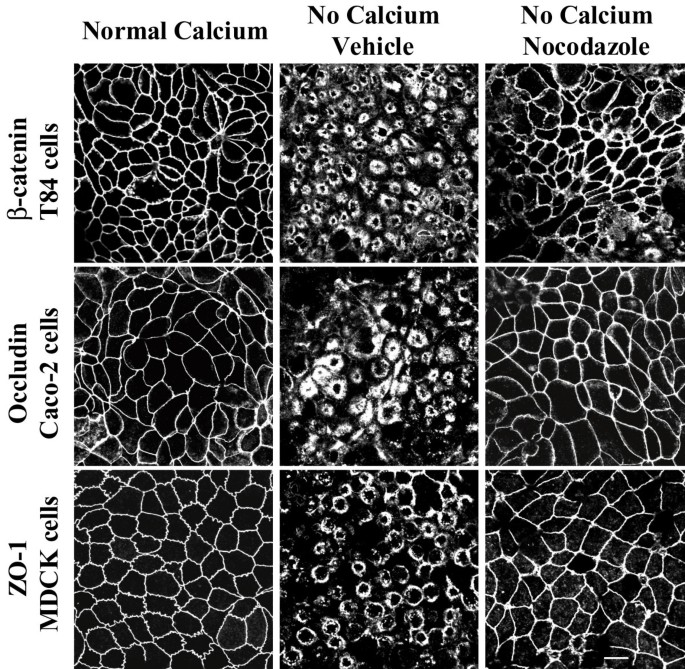
),说明微管依赖的AJC解离是不同类型上皮细胞的普遍特征。产品关联:文献未提及具体实验产品,领域常规使用免疫荧光染色试剂盒、细胞培养试剂、微管蛋白抗体等。
3.2 微管对肌动蛋白收缩环形成的调控
实验目的为明确微管在钙缺失诱导的肌动蛋白收缩环形成中的作用。方法细节上,SK-CO-15细胞经诺考达唑处理后进行钙缺失诱导,用荧光标记的鬼笔环肽染色标记F-肌动蛋白,同时免疫荧光标记α-微管蛋白,观察两者的分布变化。结果解读显示,正常钙浓度下,F-肌动蛋白呈顶膜下连接区的带状分布;钙缺失后,F-肌动蛋白重组为位于细胞中央的收缩环,同时微管重组为致密斑块并定位于肌动蛋白环内部,部分微管与肌动蛋白丝直接接触(
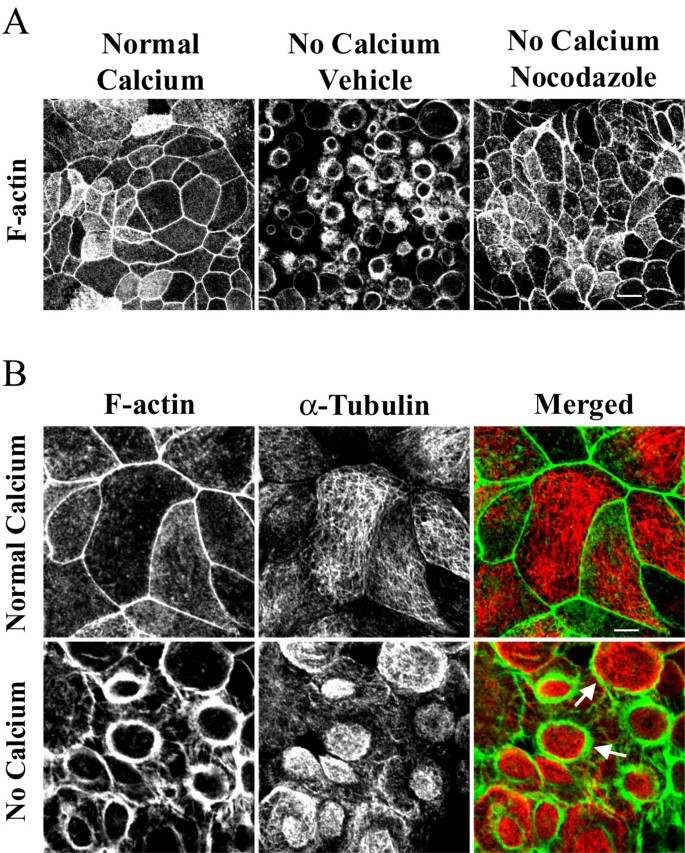
);诺考达唑处理则完全阻断了肌动蛋白收缩环的形成,说明微管是肌动蛋白环形成的上游调控因素。产品关联:文献未提及具体实验产品,领域常规使用荧光标记鬼笔环肽、微管蛋白单克隆抗体等。
3.3 微管动态变化对AJC解离的影响
实验目的为探究微管动态稳定性(解聚/聚合)在AJC解离中的作用。方法细节上,用10μM多西他赛或紫杉醇处理细胞以稳定微管,随后进行钙缺失诱导,检测连接蛋白分布和肌动蛋白环形成;同时通过Western blot检测乙酰化微管蛋白(稳定微管标记)和酪氨酸化微管蛋白(动态微管标记)的表达水平。结果解读显示,微管稳定剂处理显著减弱了连接蛋白的内吞转移和肌动蛋白环的收缩(
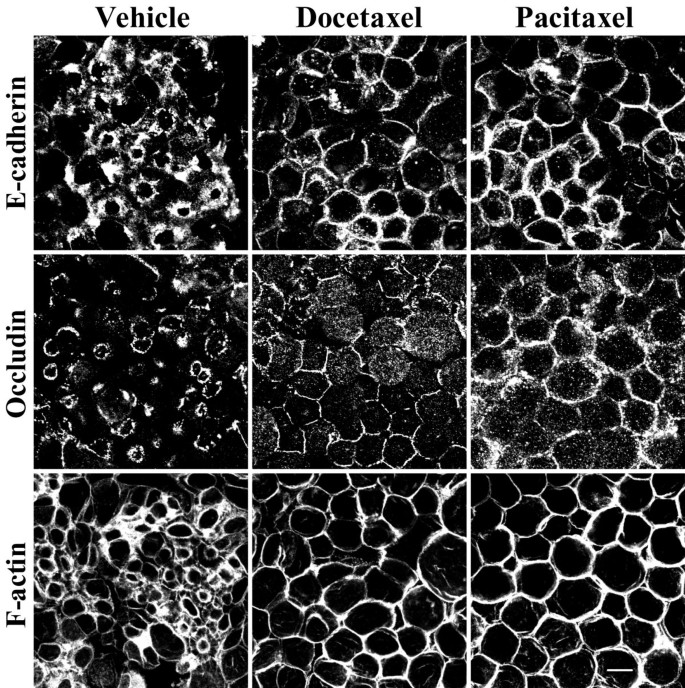
);Western blot结果显示,钙缺失后乙酰化微管蛋白水平显著降低,而酪氨酸化微管蛋白水平无明显变化(
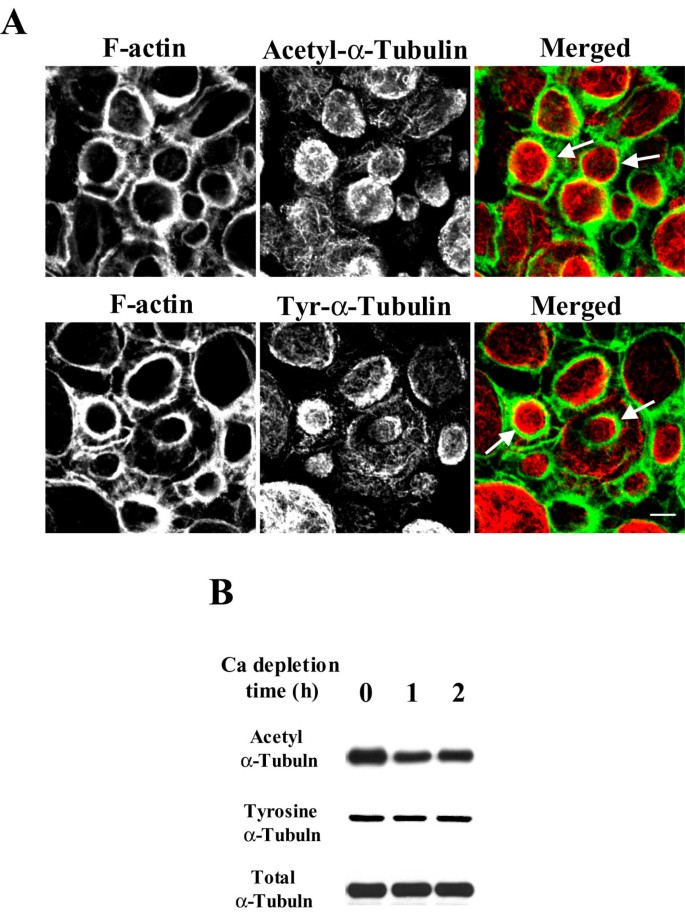
),说明动态微管是AJC解离所必需的。产品关联:实验所用关键产品:多西他赛(Sanifi-Aventis提供)、紫杉醇(Sigma),乙酰化微管蛋白单克隆抗体、酪氨酸化微管蛋白单克隆抗体(Sigma)。
3.4 驱动蛋白对AJC解离的调控作用
实验目的为明确微管马达蛋白在AJC解离中的具体功能。方法细节上,先用500μM AMP-PNP或50μM ATA处理细胞以抑制驱动蛋白活性,随后进行钙缺失诱导,检测连接蛋白分布和肌动蛋白环;通过免疫荧光染色定位驱动蛋白-1和驱动蛋白-2在细胞中的分布;利用免疫共沉淀实验验证驱动蛋白与连接蛋白的相互作用。结果解读显示,驱动蛋白抑制剂处理阻断了肌动蛋白环收缩和连接蛋白内吞(
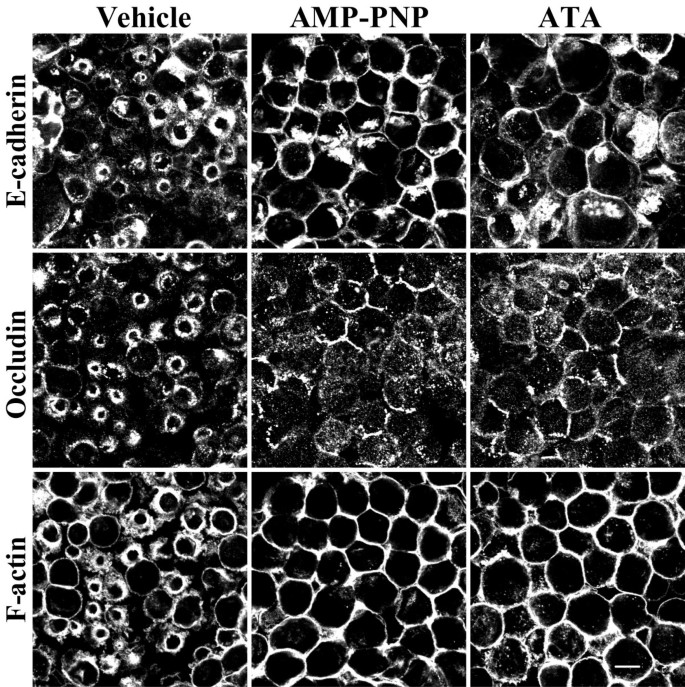
);免疫荧光结果显示,驱动蛋白-1在极化上皮细胞的AJC区域富集,与连接蛋白共定位,钙缺失后随连接蛋白内吞转移至顶膜下胞质区(
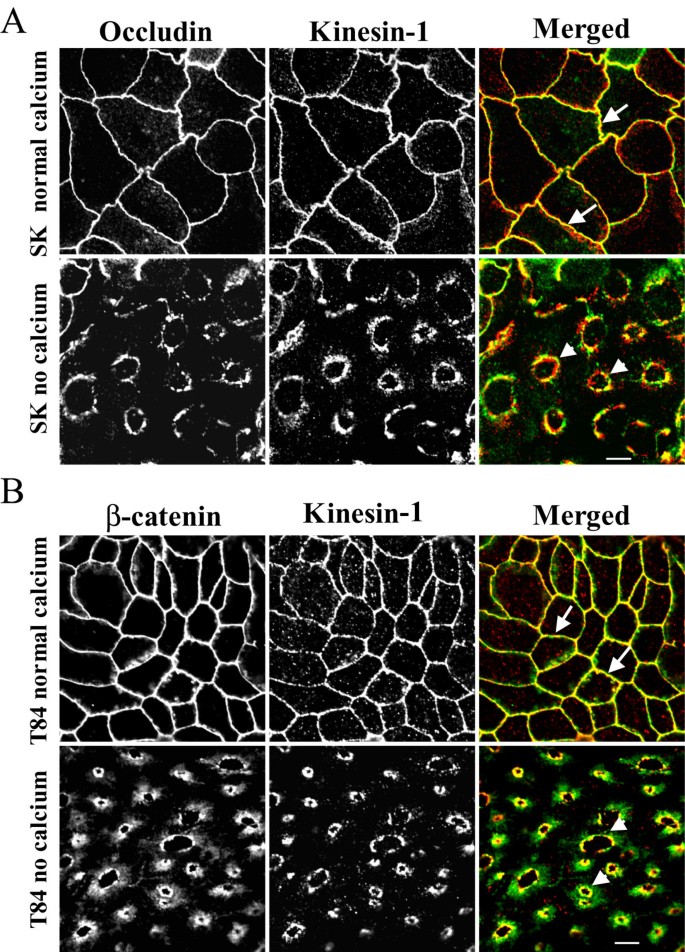
),且在人结肠组织的细胞间接触部位也观察到驱动蛋白-1的富集(
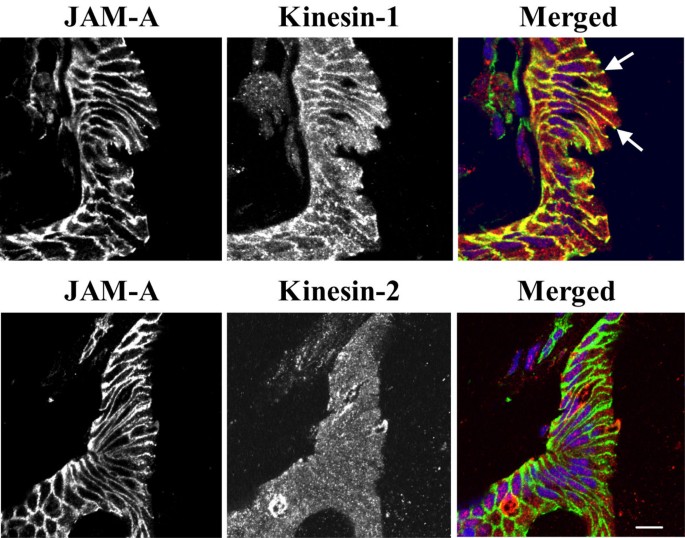
);而驱动蛋白-2在细胞内呈弥散分布,不与连接蛋白共定位(
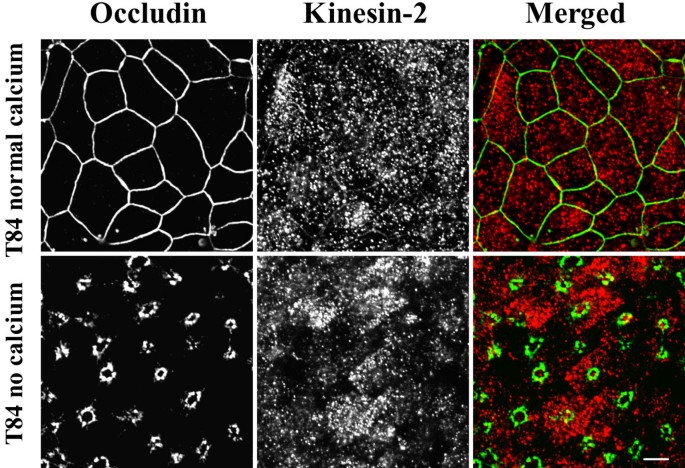
);免疫共沉淀实验证实,驱动蛋白-1可与E-钙黏蛋白、β-连环蛋白、p120连环蛋白结合,但不与紧密连接蛋白或桥粒蛋白结合(
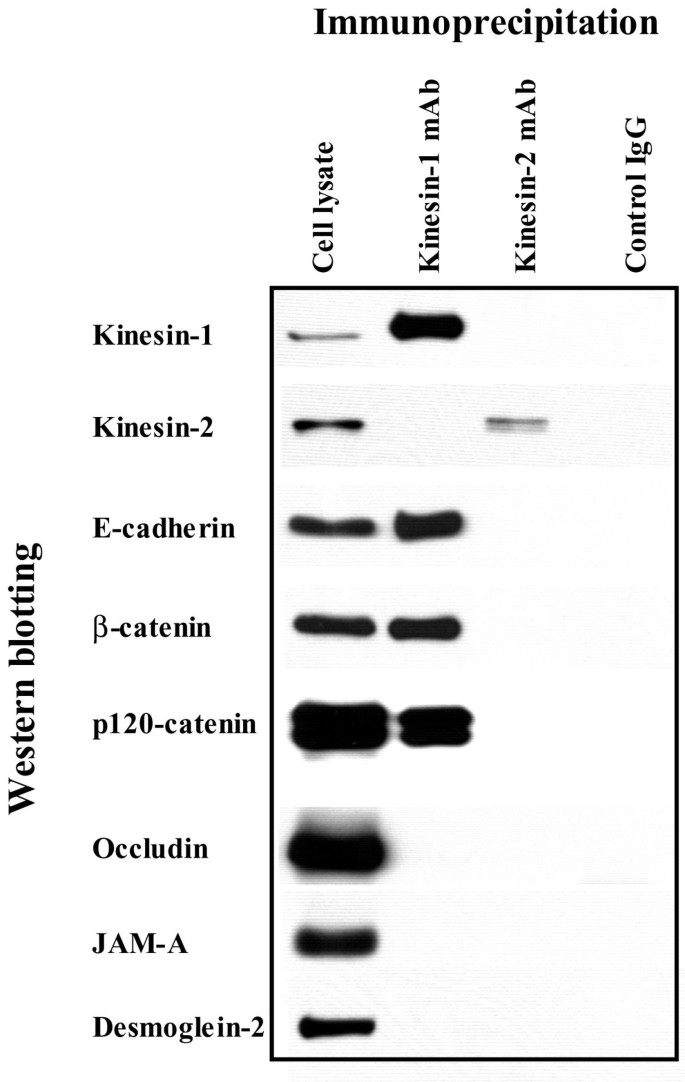
),说明驱动蛋白-1特异性介导黏着连接蛋白的内吞转运。产品关联:文献未提及具体实验产品,领域常规使用驱动蛋白抑制剂、免疫共沉淀试剂盒、驱动蛋白单克隆抗体等。
4. Biomarker研究及发现成果解析
本研究涉及的Biomarker为驱动蛋白-1,属于微管马达蛋白家族成员,其筛选与验证逻辑为:先通过药理学抑制实验发现驱动蛋白活性是AJC解离所必需的,再通过免疫荧光定位筛选出在AJC区域富集的驱动蛋白亚型,最后通过免疫共沉淀验证其与连接蛋白的特异性相互作用。
驱动蛋白-1的研究过程详述:其来源为培养的SK-CO-15、T84上皮细胞系及人结肠组织样本;验证方法包括免疫荧光染色定位其细胞内分布、免疫共沉淀验证与连接蛋白的相互作用、Western blot检测其表达;特异性方面,驱动蛋白-1仅与黏着连接蛋白复合物结合,不与紧密连接蛋白、桥粒蛋白发生相互作用,且仅在AJC区域富集,而其他驱动蛋白亚型无此特征。
核心成果提炼显示,驱动蛋白-1是钙缺失诱导AJC解离的关键调控分子,其功能关联体现在两个方面:一是参与调控肌动蛋白收缩环的形成,二是介导黏着连接蛋白的内吞转运;创新性在于首次在人结肠组织中证实驱动蛋白-1在细胞连接区域的富集,明确了其在AJC解离中的特异性作用,揭示了微管马达蛋白在上皮连接重构中的新功能。统计学结果方面,Western blot显示钙缺失后乙酰化微管蛋白水平显著降低(文献未明确样本量和P值,基于图表趋势推测),所有免疫荧光、免疫共沉淀结果均在至少3次独立实验中重复验证。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。