Aging of mesenchymal stem cell in vitro
间充质干细胞体外衰老
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2006 | 起止号: | 2006 Mar 10;7:14 |
| doi: | 10.1186/1471-2121-7-14 | 研究方向: | 细胞生物学、发育与干细胞 |
| 疾病类型: | 衰老 | 细胞类型: | 干细胞 |
文献解析
1. 领域背景与文献引入
文献英文标题:Aging of mesenchymal stem cell in vitro;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:间充质干细胞体外培养与衰老研究
间充质干细胞(MSC)是具有自我更新能力和多向分化潜能的成体干细胞,自1982年Friedenstein首次从骨髓中分离鉴定以来,其在造血干细胞移植辅助、器官损伤修复、基因治疗等领域的治疗潜力逐渐被证实,成为再生医学的研究热点。领域发展关键节点包括1999年Pittenger等明确间充质干细胞的多向分化能力,2000年后多项临床研究验证其在造血重建中的作用;当前研究热点聚焦于间充质干细胞的体外扩增优化、衰老机制及临床应用时机的选择;未解决的核心问题是间充质干细胞在骨髓中含量极低(仅0.001%-0.01%),必须经过体外扩增才能满足临床需求,但长期体外培养会导致间充质干细胞进入衰老,丢失干细胞特性,而现有研究对间充质干细胞体外衰老的起始时间、关键标记变化规律及最佳临床应用时机尚未形成统一结论。结合领域现状,本研究针对“间充质干细胞体外培养过程中衰老的发生规律及对干细胞功能的影响”这一研究空白,通过系统评估长期培养中间充质干细胞的增殖、端粒、分化及形态学变化,为临床应用的最佳时机提供直接实验依据,具有重要的转化医学价值。
2. 文献综述解析
作者围绕“间充质干细胞的治疗价值→体外扩增的必要性→衰老相关标记的研究现状→现有研究的争议与不足”这一逻辑展开综述,明确了本研究的核心定位。现有研究普遍支持间充质干细胞具有多向分化潜能和临床治疗价值,体外扩增是解决其体内含量极低问题的必需手段;技术方法上,多采用群体倍增数(PD)、端粒长度、分化能力等标记评估细胞衰老,其中端粒缩短被认为是细胞衰老的核心分子机制之一;但现有研究存在明显局限性,不同研究因培养条件差异导致群体倍增数、端粒缩短率的结果不一致,关于供体年龄对间充质干细胞体外衰老的影响结论存在争议,且缺乏对间充质干细胞体外培养全程(从初期到晚期)衰老相关指标的系统动态评估。本研究的创新价值在于,首次系统追踪了间充质干细胞长达120天、10代体外培养过程中的多项衰老相关指标变化,明确了间充质干细胞从培养初期即开始进入亚临床衰老状态,分化能力从第6代开始显著下降,弥补了现有研究对衰老起始时间及分化能力变化细节的不足,为临床应用的早期使用提供了直接实验依据。
3. 研究思路总结与详细解析
本研究以“长期体外培养对间充质干细胞衰老及干细胞特性的影响”为核心科学问题,采用“样本采集→体外长期培养传代→多指标动态检测→统计学分析→结论”的闭环技术路线,系统评估了间充质干细胞在增殖能力、端粒长度、分化潜能、形态学等方面的变化,明确了间充质干细胞体外衰老的规律及临床应用的最佳时机。
3.1 骨髓样本采集与间充质干细胞原代培养体系建立
实验目的:从健康供体骨髓中分离间充质干细胞并建立稳定的长期体外培养体系,为后续衰老评估提供实验材料。方法细节:从11名健康造血干细胞移植供体(年龄2.5-63岁)采集10ml骨髓样本,采用Ficoll密度梯度离心法分离骨髓单个核细胞,将细胞以1×10⁶cells/ml的密度接种于75cm²培养瓶,使用含10%热灭活胎牛血清、青霉素/链霉素的DMEM-LG培养基,置于37℃、5%CO₂的 humidified培养箱中培养,每4天更换完全培养基,当贴壁的成纤维样细胞达90%融合时,用0.25%胰酶-EDTA消化传代,传代密度为1×10⁴cells/ml,持续培养至120天,期间定期收集细胞进行各项检测。实验所用关键产品:Gibco的DMEM-LG培养基、胎牛血清、青霉素/链霉素;Greiner bio-one的75cm²培养瓶;Dako的抗CD44异硫氰酸荧光素(FITC)抗体、抗CD13藻红蛋白(PE)抗体、抗CD34 FITC抗体;Roche的Telo TAGGG端粒长度检测试剂盒;Bio-rad的凝胶成像分析软件。结果解读:原代培养的平均融合时间为15.6天,收获细胞数量平均为17.0×10⁵个;11个样本中9个成功培养100-164天,传代8-10次,2个样本因污染分别在培养63天、95天后终止,传代5、6次;将供体分为<10岁(6人)和23-63岁(5人)两组,经独立样本检验和重复测量方差分析,两组在端粒长度、群体倍增数、收获细胞数及融合时间上均无显著差异(P>0.05),说明供体年龄对本研究范围内的间充质干细胞体外衰老无显著影响。
3.2 间充质干细胞免疫表型稳定性检测
实验目的:验证长期体外培养过程中间充质干细胞表面标志物的表达是否发生变化,明确免疫表型与衰老的关联。方法细节:在第2、4、6、8、10代,取部分间充质干细胞,分别用FITC标记的CD44抗体、PE标记的CD13抗体、FITC标记的CD34抗体进行染色,同时设置同型对照,采用流式细胞术(FCM)检测,用Cellquest软件分析标志物的阳性表达率。结果解读:各代次间充质干细胞均高表达CD44和CD13,低表达或几乎不表达CD34,经重复测量方差分析,不同代次间三种标志物的表达率无显著差异(P>0.05),说明间充质干细胞的免疫表型在体外衰老过程中保持相对稳定,不能作为衰老的早期标记。
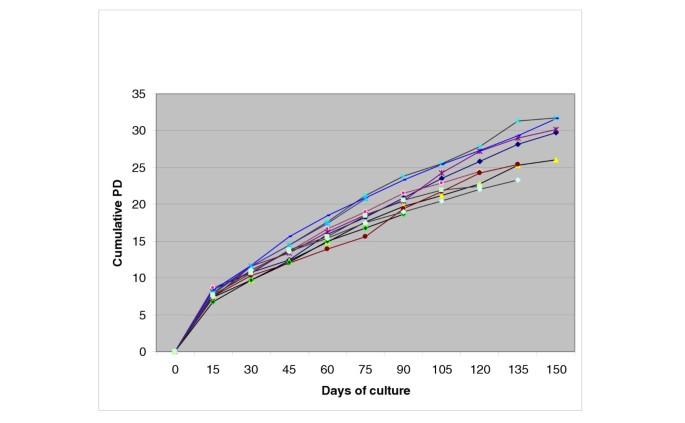
3.3 增殖能力与生长动力学分析
实验目的:评估长期培养中间充质干细胞的增殖潜能变化,明确衰老过程中的增殖规律。方法细节:通过计算每代细胞的群体倍增数(PD),公式为logN/log2(N为融合时细胞数与接种细胞数的比值),绘制不同供体的长期生长曲线,同时在每次换液时观察细胞形态学变化并记录。结果解读:第1代间充质干细胞的平均群体倍增数为7.7,随着传代次数增加,群体倍增数逐渐下降,第10代平均群体倍增数降至1.2,增殖能力显著降低(n=9,P<0.05);长期生长曲线显示不同供体的间充质干细胞增殖潜能存在个体差异,但整体均呈逐渐下降趋势;培养后期(>120天)细胞出现典型的Hayflick细胞衰老形态:细胞大小和形态不均一,细胞质出现颗粒状结构,培养基中出现细胞碎片,部分细胞出现空泡化、变圆并从培养瓶壁脱落,这些形态学变化与细胞衰老的经典模型一致。
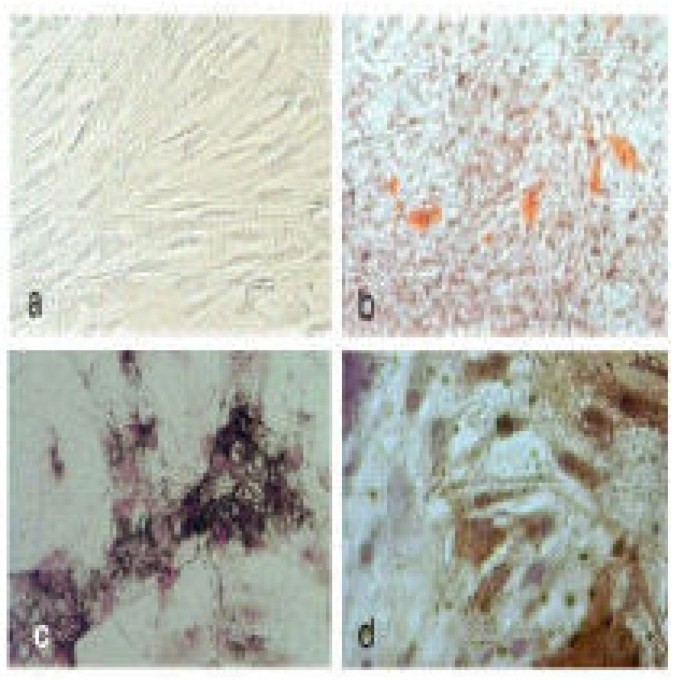
3.4 多向分化潜能动态评估
实验目的:明确长期体外培养对间充质干细胞向脂肪细胞和骨细胞分化能力的影响,比较两种分化潜能对衰老的敏感性。方法细节:在第2、4、6、8、10代,将间充质干细胞分别接种于诱导培养基中:脂肪分化培养基含0.5μM氢化可的松、0.5μM异丁基甲基黄嘌呤、60μM吲哚美辛、10μg/ml胰岛素,培养2-3周后用油红O染色鉴定;骨分化培养基含0.1μM地塞米松、10μM β-甘油磷酸钠、50μM抗坏血酸,培养2-3周后用Von Kossa染色和碱性磷酸酶染色鉴定。结果解读:第4代及之前的所有样本均能成功向脂肪细胞和骨细胞分化;从第6代开始,间充质干细胞的分化能力逐渐下降,第6代有10%的样本失去脂肪分化潜能,第8代50%的样本失去脂肪分化潜能,第10代60%的样本失去脂肪分化潜能(n=5,P<0.05);骨分化潜能的下降相对较晚,第8代有25%的样本失去骨分化潜能,第10代20%的样本失去骨分化潜能(n=5,P<0.05);同一培养板中,脂肪分化阳性细胞的比例显著低于骨分化阳性细胞,说明间充质干细胞的脂肪分化潜能对体外衰老更为敏感。
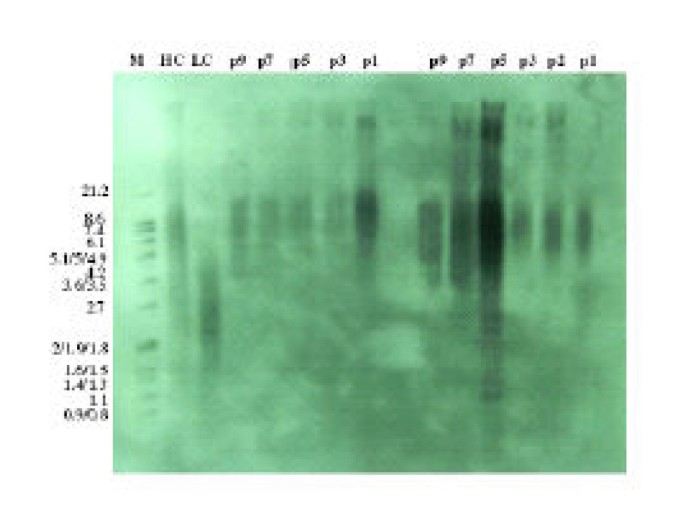
3.5 端粒长度变化检测
实验目的:明确长期体外培养中间充质干细胞端粒长度的变化规律,验证端粒缩短与细胞衰老的关联。方法细节:在第1、3、5、7、9代,采用Southern印迹法(Southern blot)检测端粒长度:提取细胞基因组DNA,用RsaI和HinfI限制性内切酶消化,经0.8%琼脂糖凝胶电泳分离后转移至尼龙膜,与地高辛标记的端粒重复序列探针杂交,用碱性磷酸酶标记的抗地高辛抗体结合,通过化学发光底物CDP-Star显影,用Bio-rad软件计算平均端粒限制性片段(TRF)长度。结果解读:第1代间充质干细胞的平均端粒长度为9.19Kbp,随着传代次数增加,端粒长度逐渐缩短,第9代平均端粒长度降至8.7Kbp,培养120天后端粒长度共缩短约0.44Kbp,平均每两代端粒缩短约100bp(n=9,P<0.05);不同供体的初始端粒长度存在个体差异,但端粒缩短的趋势一致,说明端粒缩短是间充质干细胞体外衰老的核心分子标记之一。
4. Biomarker研究及发现成果解析
本研究以“间充质干细胞体外衰老的关键Biomarker及变化规律”为核心,通过动态检测增殖类、分子类、功能类、形态学四类Biomarker,明确了间充质干细胞体外衰老的起始时间、变化规律及临床应用的最佳时机。
Biomarker定位:本研究涉及的Biomarker包括增殖类Biomarker(群体倍增数)、分子类Biomarker(端粒长度)、功能类Biomarker(多向分化潜能)、形态学Biomarker(细胞大小、细胞质颗粒、细胞碎片);筛选/验证逻辑是基于经典细胞衰老模型(Hayflick模型)和现有研究中的衰老标记,通过长期体外培养的动态检测,验证这些Biomarker与间充质干细胞体外衰老的关联,构建完整的衰老评估体系。
研究过程详述:Biomarker的来源为体外培养的间充质干细胞;验证方法包括群体倍增数计算(细胞计数法)、端粒长度Southern印迹法、分化能力的组织化学染色法、形态学观察法;特异性与敏感性数据:群体倍增数从第1代的7.7降至第10代的1.2(n=9,P<0.05),端粒长度从第1代的9.19Kbp降至第9代的8.7Kbp(n=9,P<0.05),脂肪分化潜能从第4代的100%降至第10代的40%(n=5,P<0.05),骨分化潜能从第4代的100%降至第10代的80%(n=5,P<0.05),形态学异常从培养第3个月开始逐渐出现,第4个月后显著增多。
核心成果提炼:本研究的核心成果包括:1. 明确间充质干细胞从体外培养初期即开始进入亚临床衰老状态,并非从培养后期才开始;2. 首次证明间充质干细胞的脂肪分化潜能比骨分化潜能对体外衰老更为敏感,分化能力从第6代开始显著下降;3. 供体年龄在2.5-63岁范围内对间充质干细胞的体外衰老无显著影响;4. 端粒长度缩短、群体倍增数下降、分化能力丢失是间充质干细胞体外衰老的关键标记,其中端粒长度可作为定量评估衰老的分子标记。这些成果的创新性在于系统揭示了间充质干细胞体外衰老的全程变化规律,为临床应用中间充质干细胞的早期使用(建议在第6代之前)提供了直接实验依据,避免因衰老导致的治疗效果下降;同时为间充质干细胞体外扩增的优化策略提供了参考方向,如通过优化培养条件延缓衰老进程。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。