Glycosaminoglycans modulate C6 glioma cell adhesion to extracellular matrix components and alter cell proliferation and cell migration
糖胺聚糖调节C6胶质瘤细胞与细胞外基质成分的黏附,并改变细胞增殖和迁移。
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2005 | 起止号: | 2005 Aug 19;6:31 |
| doi: | 10.1186/1471-2121-6-31 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Glycosaminoglycans modulate C6 glioma cell adhesion to extracellular matrix components and alter cell proliferation and cell migration;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:神经肿瘤学(胶质瘤分子调控)。
胶质母细胞瘤是临床最常见的恶性胶质瘤亚型,对现有治疗手段具有高度耐药性,多数患者在确诊后1年内死亡,预后极差。领域共识:细胞外基质成分可调控肿瘤细胞的分化、增殖、形态及黏附行为,其与肿瘤细胞的相互作用参与肿瘤进展的早期步骤,可能导致基因组不稳定并积累突变,进而促进肿瘤恶性表型的发展。现有研究已证实胶质瘤细胞的黏附能力与侵袭行为密切相关,但糖胺聚糖在胶质瘤细胞与细胞外基质相互作用中的特异性调控机制,尤其是不同细胞外基质成分下的功能差异尚未得到系统阐明。针对这一研究空白,本研究旨在通过体外实验明确糖胺聚糖对C6胶质瘤细胞黏附、增殖及迁移行为的调控作用,为胶质瘤恶性进展的分子机制提供新的实验依据。
2. 文献综述解析
作者以细胞外基质成分类型、糖胺聚糖功能差异为分类维度,系统评述了胶质瘤领域中细胞外基质与肿瘤细胞相互作用的研究进展。现有研究已证实细胞外基质中的IV型胶原、层粘连蛋白、纤连蛋白均可调控胶质瘤细胞的黏附与侵袭行为,糖胺聚糖的硫酸化修饰状态影响肿瘤细胞的增殖能力;部分研究采用C6胶质瘤细胞系作为体内外模型,该模型在形态学和恶性表型上与胶质母细胞瘤高度相似,具有实验重复性好、可控性强的优势,但此前的研究多聚焦于单一细胞外基质成分或单一糖胺聚糖的作用,未系统分析不同糖胺聚糖对不同细胞外基质成分介导的胶质瘤细胞功能的特异性调控,也未区分糖胺聚糖在细胞黏附初始阶段与已黏附阶段的作用差异。本研究的创新价值在于首次系统揭示了肝素、硫酸软骨素等糖胺聚糖对C6胶质瘤细胞与不同细胞外基质成分黏附、增殖及迁移的特异性调控模式,明确了糖胺聚糖仅在细胞黏附的初始阶段发挥调控作用,且其功能效应依赖于细胞外基质的组成,填补了领域内关于糖胺聚糖在胶质瘤细胞-基质相互作用中特异性调控机制的研究空白。
3. 研究思路总结与详细解析
本研究的核心目标是阐明糖胺聚糖对C6胶质瘤细胞与细胞外基质相互作用的特异性调控机制,核心科学问题为不同类型的糖胺聚糖如何根据细胞外基质成分的差异调控胶质瘤细胞的黏附、增殖及迁移行为,技术路线遵循“假设提出→体外实验验证→功能效应分析→结论总结”的闭环逻辑。
3.1 细胞外基质成分对C6胶质瘤细胞黏附的剂量效应研究
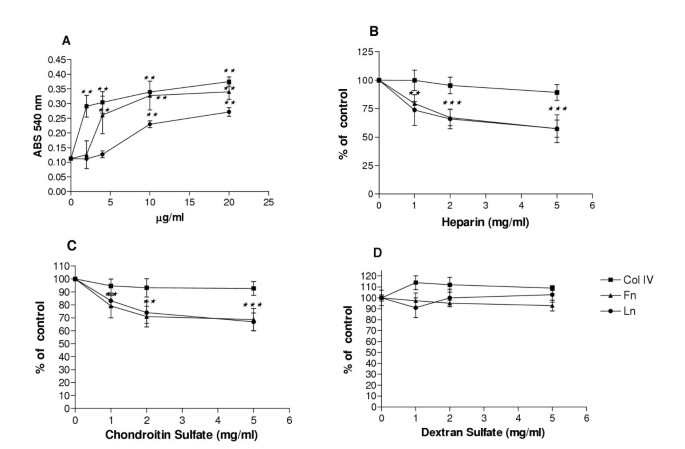
实验目的是明确不同细胞外基质成分(IV型胶原、层粘连蛋白、纤连蛋白)对C6胶质瘤细胞黏附能力的影响及剂量依赖关系。方法细节为采用不同浓度(2μg/ml至20μg/ml)的细胞外基质蛋白包被96孔板,接种C6胶质瘤细胞后在标准培养条件下孵育2小时,去除未黏附细胞后用结晶紫染色,通过酶标仪检测540nm处的吸光度值量化细胞黏附率。结果解读显示,三种细胞外基质成分均以剂量依赖方式促进C6细胞的黏附,其中IV型胶原的黏附促进作用最强,在2μg/ml浓度时黏附率较对照组提升160%(n=4,P<0.0001),当浓度达到10μg/ml时进入平台期,此时IV型胶原使黏附率提升203%,纤连蛋白提升193%,层粘连蛋白提升105%,且层粘连蛋白在所有浓度下的黏附促进作用均弱于另外两种成分。
文献未提及具体实验产品,领域常规使用细胞外基质蛋白试剂、结晶紫染色试剂盒、酶标仪等实验材料与仪器。
3.2 糖胺聚糖对C6胶质瘤细胞初始黏附的特异性调控
实验目的是探究肝素、硫酸软骨素、硫酸葡聚糖三种多糖对C6胶质瘤细胞与不同细胞外基质成分黏附的调控作用。方法细节为在接种C6细胞的同时加入不同浓度(1mg/ml至5mg/ml)的糖胺聚糖或硫酸葡聚糖,孵育2小时后检测细胞黏附率;同时设置细胞已黏附后添加多糖的实验,检测细胞脱离率。结果解读显示,肝素和硫酸软骨素均以剂量依赖方式抑制C6细胞与层粘连蛋白、纤连蛋白的黏附,5mg/ml浓度时肝素对两种基质的黏附抑制率均为42%(n=4,P<0.0001),硫酸软骨素对层粘连蛋白的抑制率为33.2%、对纤连蛋白为31.4%,但两者均不影响细胞与IV型胶原的黏附;硫酸葡聚糖对所有细胞外基质成分介导的黏附均无显著影响;此外,三种多糖均不会导致已黏附的C6细胞脱离基质,提示糖胺聚糖仅在细胞黏附的初始阶段发挥调控作用。
文献未提及具体实验产品,领域常规使用糖胺聚糖标准品、细胞黏附检测试剂盒等。
3.3 糖胺聚糖对C6胶质瘤细胞增殖的调控作用
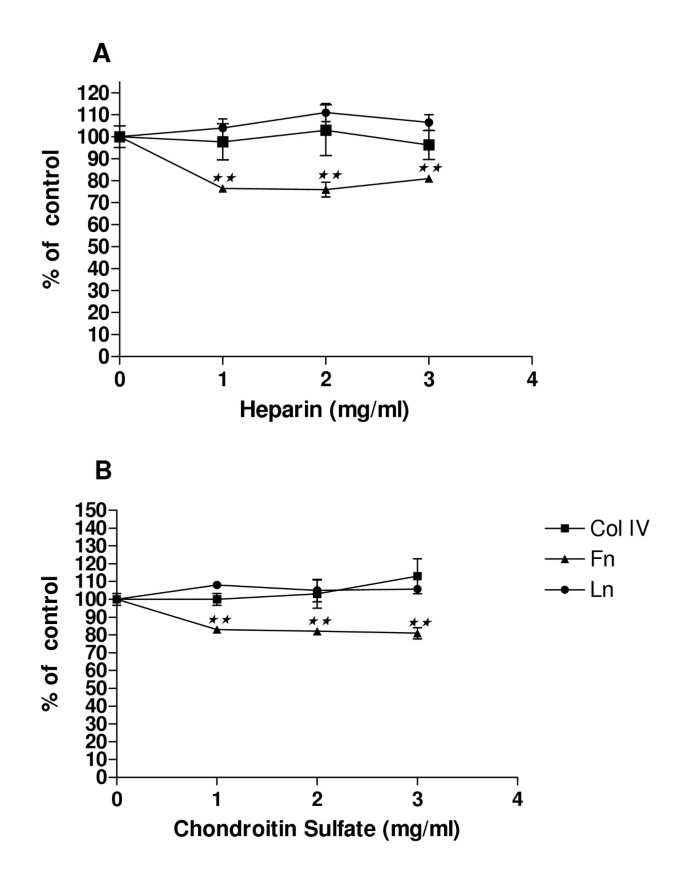
实验目的是明确糖胺聚糖对不同细胞外基质成分上C6胶质瘤细胞增殖能力的影响。方法细节为用10μg/ml的细胞外基质蛋白包被96孔板,接种C6细胞并加入不同浓度(1mg/ml至3mg/ml)的肝素或硫酸软骨素,培养2天后采用噻唑蓝(MTT)比色法检测细胞增殖率。结果解读显示,肝素和硫酸软骨素仅显著抑制纤连蛋白包被板上的C6细胞增殖,抑制率分别为24%和20%(n=3,P<0.001),但对IV型胶原或层粘连蛋白上的细胞增殖无明显影响。
文献未提及具体实验产品,领域常规使用MTT试剂盒、细胞培养试剂等。
3.4 糖胺聚糖对C6胶质瘤细胞迁移的调控作用
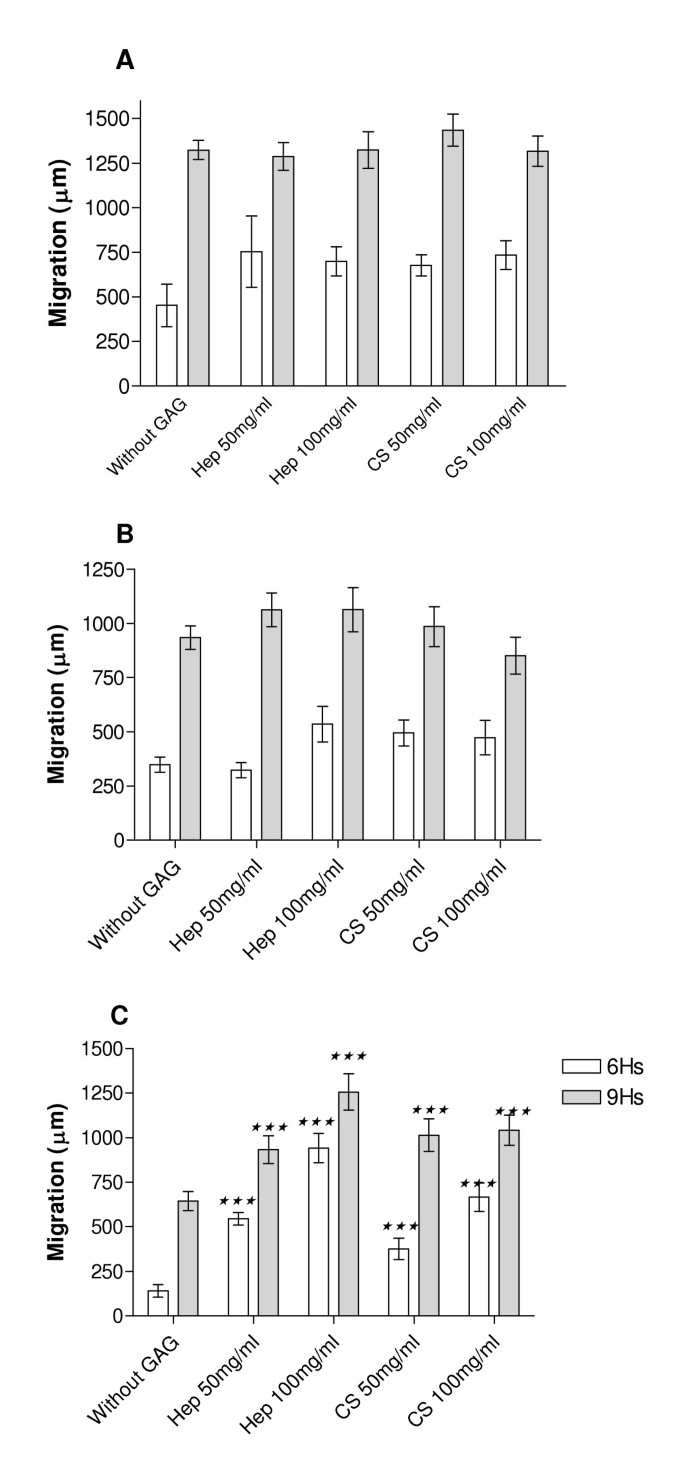
实验目的是研究糖胺聚糖对不同细胞外基质成分上C6胶质瘤细胞迁移能力的影响。方法细节为采用单层细胞迁移实验,将培养至汇合的C6细胞盖玻片转移至包被有10μg/ml细胞外基质蛋白的35mm孔中,加入不同浓度(50mg/ml、100mg/ml)的肝素或硫酸软骨素,分别在0小时、6小时、9小时检测细胞迁移出盖玻片的比例。结果解读显示,肝素和硫酸软骨素均不影响C6细胞在IV型胶原或纤连蛋白上的迁移,但显著促进细胞在层粘连蛋白上的迁移,6小时时50mg/ml肝素使迁移率提升222%,100mg/ml肝素提升567%(n=3,P<0.0001),硫酸软骨素50mg/ml使迁移率提升166%,100mg/ml提升373%。
文献未提及具体实验产品,领域常规使用细胞迁移实验装置、倒置显微镜成像系统等。
4. Biomarker研究及发现成果
本研究中涉及的生物标志物为糖胺聚糖(肝素、硫酸软骨素),属于细胞外基质调控分子,其筛选与验证逻辑为通过体外黏附实验筛选出具有黏附调控作用的糖胺聚糖,再通过增殖实验、迁移实验验证其对胶质瘤细胞功能的特异性调控效应。
研究过程详述显示,该生物标志物为外源性添加的标准糖胺聚糖分子,验证方法包括体外细胞黏附实验、噻唑蓝(MTT)比色法增殖实验、单层细胞迁移实验;特异性数据显示,肝素和硫酸软骨素仅对层粘连蛋白、纤连蛋白介导的C6细胞黏附具有抑制作用,对IV型胶原介导的黏附无影响;仅抑制纤连蛋白包被基质上的细胞增殖,仅促进层粘连蛋白包被基质上的细胞迁移,具有明确的基质依赖性特异性;敏感性数据方面,糖胺聚糖对黏附、增殖及迁移的调控作用均呈现剂量依赖效应,高浓度下的调控效应更为显著。核心成果提炼为首次发现糖胺聚糖可根据细胞外基质成分的不同,特异性调控胶质瘤细胞的黏附、增殖及迁移行为,提示糖胺聚糖及相关蛋白聚糖可作为胶质瘤恶性进展的潜在调控靶点,为胶质瘤的抗侵袭治疗提供新的研究方向;所有实验结果均标注了样本量及统计学显著性,如5mg/ml肝素对层粘连蛋白介导黏附的抑制率为42%(n=4,P<0.0001),100mg/ml肝素使层粘连蛋白上的细胞迁移率提升567%(n=3,P<0.0001)。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。