Dynamic assembly, localization and proteolysis of the Bacillus subtilis SMC complex
枯草芽孢杆菌SMC复合物的动态组装、定位和蛋白水解
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2005 | 起止号: | 2005 Jun 29;6:28 |
| doi: | 10.1186/1471-2121-6-28 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Dynamic assembly, localization and proteolysis of the Bacillus subtilis SMC complex;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细菌染色体动力学(枯草芽孢杆菌SMC复合物的动态组装、定位调控及蛋白水解机制)。
结构维持染色体(Structural Maintenance of Chromosomes, SMC)蛋白是一类高度保守的染色体动力学关键因子,广泛参与染色体凝聚、分离、修复等过程。在细菌中,枯草芽孢杆菌(Bacillus subtilis)的SMC蛋白与辅助因子ScpA(kleisin家族)、ScpB形成三元复合物,对染色体的正确排列和分离至关重要。此前研究已明确该复合物定位于核质的双极中心,但ScpA/ScpB亚复合物的动态组装机制、SMC定位的生理调控因素(如ATP酶活性、DNA复制、染色体超螺旋)及SMC蛋白的降解调控(转录后水平)等核心问题尚未解决。本文针对这些空白,系统研究了SMC复合物的动态组装、定位依赖及蛋白水解机制,为细菌染色体动力学的多层调控提供了关键实验证据。
2. 文献综述解析
作者对现有研究的评述逻辑围绕“SMC复合物的组成-功能-定位-调控未知”展开,将领域研究分为三类:
1. 组成与功能:明确SMC需与ScpA、ScpB形成复合物才能发挥染色体凝聚和分离功能,但未解析ScpA/ScpB亚复合物的动态相互作用;
2. 亚细胞定位:发现复合物定位于核质双极中心,但缺乏对定位依赖的生理因素(如DNA复制、拓扑结构)的深入研究;
3. 调控机制:已知SMC在稳定期快速降解,但未明确降解的分子机制(转录 vs 转录后)及参与的蛋白酶。
现有研究的局限性在于:(1)未阐明ScpA/ScpB亚复合物如何动态组装并招募到SMC;(2)SMC定位的具体调控网络不清晰;(3)SMC降解的转录后调控机制未知。
本文的创新价值在于:首次揭示ScpA/ScpB亚复合物的动态组装模式及向SMC的招募过程;明确SMC定位依赖ATP酶活性、持续DNA复制和染色体超螺旋;发现SMC通过ClpX和LonA蛋白酶实现转录后降解;并通过原子力显微镜(AFM)观察到SMC体外形成“玫瑰花结”结构,为体内双极中心的形成提供了结构基础。
3. 研究思路总结与详细解析
3.1 整体框架
本文以“体外分子互作→体内功能验证→定位调控→降解机制→结构解析”为核心逻辑,逐步验证以下科学问题:
- ScpA与ScpB如何形成亚复合物并招募到SMC?
- SMC的ATP酶活性、DNA复制及染色体超螺旋如何调控其定位?
- SMC的降解是转录还是转录后调控?依赖哪些蛋白酶?
- SMC的体外高级结构是否解释体内中心形成?
3.2 ScpA/ScpB亚复合物的体外动态组装分析
实验目的:探究ScpA与ScpB的相互作用及亚复合物的形成模式。
方法细节:采用分析凝胶过滤(Superdex 200 10/300 GL柱,Amersham-Pharmacia Biotech)和蔗糖梯度离心(5-20%蔗糖溶液)分离蛋白复合物,结合SDS-PAGE(Coomassie染色或银染)鉴定组分。
结果解读:
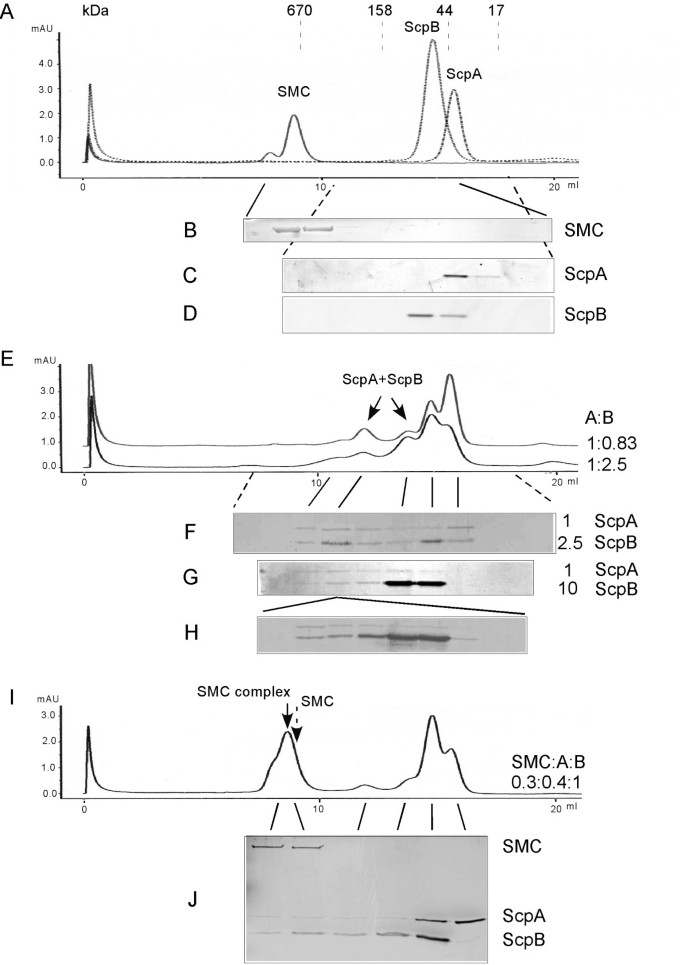
- ScpA以单体为主(洗脱峰16.2 ml,对应35 kDa),ScpB以二聚体为主(洗脱峰15.0 ml,对应65 kDa);
- 两者混合后形成至少两种稳定亚复合物:110 kDa(ScpA单体+ScpB二聚体)和210 kDa(ScpA二聚体+ScpB二聚体×2),且为动态可逆(将210 kDa复合物二次凝胶过滤,仍保持相同洗脱模式);
- 细胞提取物中,ScpB存在于低分子量(游离二聚体,1.8S)和高分子量(与ScpA结合,12-13S)组分,支持体内存在ScpA/ScpB亚复合物。
产品关联:凝胶过滤柱为Amersham-Pharmacia Biotech产品;蔗糖梯度离心使用常规实验室设备;SDS-PAGE试剂为领域常规使用(如Bio-Rad的凝胶和染色液)。
3.3 SMC与ScpA/ScpB复合物的形成验证
实验目的:明确SMC是否通过结合ScpA/ScpB亚复合物形成功能复合物。
方法细节:将纯化的SMC(0.3 nmol)与ScpA(0.4 nmol)、ScpB(1 nmol)共同孵育后,通过分析凝胶过滤分离,SDS-PAGE检测复合物组分。
结果解读:
- SMC单独存在时为二聚体(洗脱峰对应690 kDa,实际分子量~260 kDa,因长 coil-coil 结构导致凝胶过滤表观分子量偏大);
- 加入ScpA+ScpB后,SMC峰向更大分子量(780 kDa)偏移,且ScpA/ScpB的210 kDa亚复合物峰显著减少,说明ScpA/ScpB亚复合物被特异性招募到SMC,形成三元复合物。
产品关联:SMC、ScpA、ScpB的纯化采用Ni柱亲和层析(原文未提具体品牌,领域常规使用Qiagen或GE Healthcare的Ni-NTA树脂);SDS-PAGE用了银染试剂盒(如Thermo Scientific的Pierce Silver Stain)。
3.4 SMC ATP酶突变体的功能与定位分析
实验目的:探究SMC的ATP酶活性对功能和定位的影响。
方法细节:
1. 突变体构建:通过定点突变(Stratagene QuikChange试剂盒)构建Walker A(K37I,ATP结合缺陷)和C基序(S1090R,ATP水解缺陷)突变体,整合到染色体amy位点;
2. 功能验证:检测突变体在smc缺失背景下的生长表型(温度敏感性);
3. 定位分析:将突变体融合GFP,通过荧光显微镜观察亚细胞定位。
结果解读:
- 突变体在smc缺失背景下表现为温度敏感(仅37℃可生长,23℃以下无法生长),说明ATP结合和水解均为SMC功能必需;
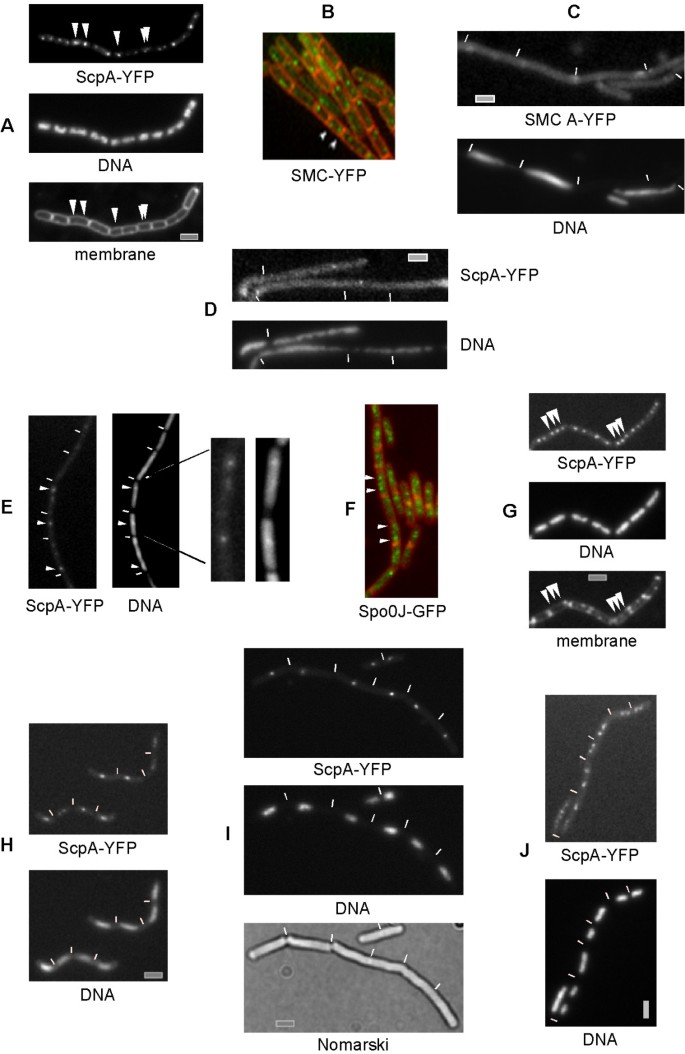
- GFP融合体在细胞内弥散分布(无离散焦点),且ScpA-YFP也无法形成双极焦点,证明ATP酶活性是复合物定位的前提。
产品关联:定点突变试剂盒为Stratagene产品;荧光显微镜为常规设备(如Zeiss Axio Observer,原文未提具体品牌);GFP抗体为领域常规使用(如Roche的Anti-GFP抗体)。
3.5 SMC定位的生理依赖因素分析
实验目的:研究DNA复制、染色体超螺旋对SMC定位的调控。
方法细节:
1. 抑制DNA复制:使用dnaB温度敏感突变体(42℃阻断复制起始),观察ScpA-YFP定位;
2. 抑制染色体超螺旋:用萘啶酸(200 ng/ml)或新生霉素(10 μg/ml)抑制拓扑异构酶(gyrase),减少染色体负超螺旋,检测SMC-YFP/ScpA-YFP定位。
结果解读:
- 抑制复制:30分钟后细胞伸长为丝状体,SMC焦点集中于细胞中心(复制机器位置);恢复25℃培养后,双极定位快速恢复,说明定位依赖持续DNA复制;
- 抑制超螺旋:>80%细胞仅含单个弥散焦点,荧光强度显著减弱;而原点结合蛋白Spo0J-GFP的双极定位受影响较小(45%细胞仍保持),说明SMC定位依赖染色体负超螺旋。
产品关联:抑制剂萘啶酸、新生霉素为Sigma-Aldrich产品;荧光染色用了DAPI(Sigma)和FM4-64(Thermo Fisher)。
3.6 SMC的转录后降解调控分析
实验目的:明确SMC降解的调控层次(转录 vs 转录后)及参与的蛋白酶。
方法细节:
1. 转录水平:通过引物延伸(Qiagen RNeasy提取RNA,Super Script II反转录)检测不同生长阶段(指数期→稳定期)的smc mRNA水平;
2. 蛋白水平:Western blot(Eurogentec的SMC抗体)检测对应阶段的SMC蛋白量;
3. 蛋白酶依赖:在clpX(ClpP辅助因子)、lonA(Lon蛋白酶)突变体中检测稳定期SMC水平。
结果解读:
- 转录后调控:smc mRNA水平在指数期到稳定期无显著变化,但SMC蛋白在稳定期快速降解(指数期高表达,稳定期不可检测);
- 翻译抑制实验:指数期加氯霉素(抑制翻译)后SMC稳定,晚期指数期加氯霉素则快速降解,说明稳定期SMC更易被水解;
- 蛋白酶依赖:clpX或lonA突变体中,稳定期SMC仍可检测,说明降解依赖ClpX和LonA;
- DNA保护作用:DNase处理细胞提取物使SMC更易降解,提示DNA结合能保护SMC免受水解。
产品关联:RNA提取用了Qiagen RNeasy试剂盒;反转录酶为Invitrogen的Super Script II;SMC抗体为Eurogentec定制。
3.7 SMC的体外高级结构解析
实验目的:观察SMC的体外结构,解释体内双极中心的形成机制。
方法细节:采用原子力显微镜(AFM,Digital Instruments Multimode Nanoscope IIIa)在溶液中观察纯化SMC的结构(浓度~0.1 μg/μl,HEPES缓冲液)。
结果解读:
- SMC形成“玫瑰花结”样超结构:核心直径~40 nm,从核心延伸出多条~40 nm长的臂(对应SMC的coil-coil结构);
- 该结构由多个SMC二聚体组装而成,Walker A突变体可部分形成,C基序突变体无法形成,说明依赖ATP酶活性;
- 推测该结构是体内双极中心的基础,通过结合DNA环实现染色体凝聚。
产品关联:AFM为Digital Instruments产品;悬臂为OLYMPUS的OMCL TR800PSA(0.68 N/m)。
4. Biomarker研究及发现成果解析
本文聚焦于枯草芽孢杆菌SMC复合物的分子调控机制,未涉及生物标志物(Biomarker)的筛选、验证或功能分析(如疾病诊断、预后预测的分子标记)。因此,本部分无相关成果。

特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。