Protein-trap version 2.1: screening for expressed proteins in mammalian cells based on their localizations
Protein-trap 2.1 版:基于定位筛选哺乳动物细胞中表达的蛋白质
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2004 | 起止号: | 2004 Feb 2;5:8 |
| doi: | 10.1186/1471-2121-5-8 | 研究方向: | 细胞生物学 |
文献解析
1. 领域背景与文献引入
文献英文标题:Protein-trap version 2.1: screening for expressed proteins in mammalian cells based on their localizations.;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学-蛋白质亚细胞定位与功能筛选
蛋白质亚细胞定位是决定其生物学功能的核心因素之一,早期研究依赖特异性抗体对单个蛋白进行定位分析,但该方法需针对每个蛋白制备专属抗体,成本高、通量极低,无法满足大规模蛋白功能筛选需求。20世纪90年代后,基因捕获(gene-trap)技术兴起,通过报告基因标记内源基因,可实现基于基因表达水平的高通量筛选,但该技术仅关注转录调控,无法检测蛋白定位变化这一关键功能调控方式。蛋白捕获(protein-trap)技术的出现填补了这一空白,最初在果蝇模型中采用绿色荧光蛋白(GFP)作为标签,实现了基于蛋白定位的筛选,但GFP分子量较大(约239个氨基酸),可能干扰靶蛋白的正常折叠与定位,且针对哺乳动物细胞的高效蛋白捕获系统仍存在缺失,缺乏预筛选步骤导致实验效率低下。针对上述领域痛点,本文开发了适用于哺乳动物细胞的蛋白捕获v2.1系统,通过优化标签大小与筛选流程,为基于蛋白亚细胞定位的功能研究提供了高效、低干扰的新工具。
2. 文献综述解析
作者以技术发展的时间线与应用场景为核心逻辑,系统梳理了蛋白定位研究领域的三类关键技术:传统抗体检测、基因捕获与早期蛋白捕获技术。传统抗体检测技术可直接观察蛋白的天然定位,是蛋白定位研究的金标准,但该方法需针对每个靶蛋白制备特异性抗体,通量极低,无法实现大规模筛选;基因捕获技术通过报告基因标记内源基因的转录起始位点,可高通量筛选基因表达调控事件,但仅能反映转录水平变化,无法检测蛋白定位、翻译后修饰等转录后调控过程;早期蛋白捕获技术(如果蝇中的GFP标签系统)实现了基于蛋白定位的筛选,但GFP大标签易干扰蛋白功能,且未针对哺乳动物细胞优化,缺乏预筛选步骤导致实验效率不足,同时无法兼容分泌蛋白的筛选。
通过对比现有技术的局限性,本文的创新价值凸显:一是采用仅43个氨基酸的myc表位标签替代GFP,显著降低标签对靶蛋白功能的干扰;二是在载体中加入嘌呤霉素抗性筛选盒,实现对整合阳性细胞的预筛选,将蛋白捕获效率提升至约10%;三是系统兼容细胞内蛋白与分泌蛋白的定位筛选,填补了哺乳动物细胞中分泌蛋白定位筛选工具的空白,为全面解析蛋白亚细胞定位与功能的关联提供了技术支撑。
3. 研究思路总结与详细解析
本研究的核心目标是开发适用于哺乳动物细胞的高效蛋白捕获系统,实现基于蛋白亚细胞定位的高通量功能筛选;核心科学问题为如何在哺乳动物细胞中实现低干扰、高效率的内源蛋白表位标记,同时支持细胞内与分泌蛋白的定位分析;技术路线遵循“载体构建→系统验证→功能应用”的闭环逻辑:首先构建包含myc表位标签与嘌呤霉素筛选盒的EpiTag逆转录病毒载体,然后在人肺癌细胞中验证载体的整合效率、标签标记的准确性与蛋白全长表达特性,最后将系统应用于缺氧诱导的蛋白转位筛选,验证其功能筛选能力。
3.1 EpiTag载体构建与整合效率验证
实验目的:构建适用于哺乳动物细胞的蛋白捕获载体,验证载体的单拷贝整合效率与标签标记的分子原理。
方法细节:构建EpiTag逆转录病毒载体,该载体包含loxP序列侧翼的嘌呤霉素抗性盒,以及带有剪接供体/受体序列的myc表位迷你外显子;将载体包装为逆转录病毒后感染人肺癌细胞NCI-H1299,通过嘌呤霉素筛选获得抗性克隆;采用Southern blot技术(XbaI酶切基因组DNA)检测每个克隆的载体整合拷贝数。
结果解读:Southern blot结果显示,约80%的抗性克隆为单拷贝整合(图1C),说明载体能高效实现基因组单位点整合,减少多拷贝整合对靶基因表达的干扰;载体原理验证显示,当载体整合到内源基因内含子时,细胞表达截短蛋白但通过内部核糖体进入位点(IRES)表达嘌呤霉素抗性基因,获得筛选抗性;经Cre重组酶切除嘌呤霉素抗性盒后,内源基因转录产物将myc表位迷你外显子剪接至成熟mRNA中,实现靶蛋白的myc标签标记(图1A、B)。
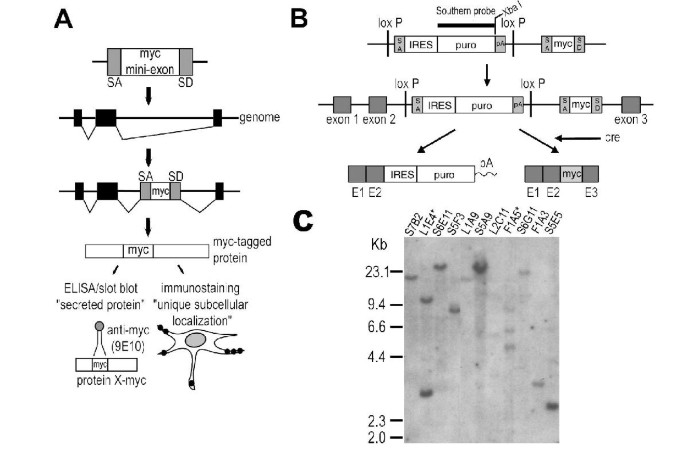
实验所用关键产品:9E10抗myc表位抗体(Developmental Studies Hybridoma Bank)、Cre重组酶逆转录病毒载体、嘌呤霉素抗性盒(来源于Clonetech pIRESpuro载体)。
3.2 内源蛋白表位标记与定位准确性验证
实验目的:验证EpiTag系统能有效标记细胞内与分泌蛋白,且标记后的蛋白能正确反映天然亚细胞定位。
方法细节:对5670个嘌呤霉素抗性克隆进行Cre重组酶处理,采用9E10抗体免疫染色检测细胞内蛋白的定位,采用双抗体夹心ELISA检测分泌蛋白;通过3"-RACE技术鉴定标记蛋白的身份;采用共染色技术(DAPI染核、FITC-鬼笔环肽染细胞骨架、Mitotracker Green FM染线粒体、靶蛋白特异性抗体)验证标记蛋白的定位准确性。
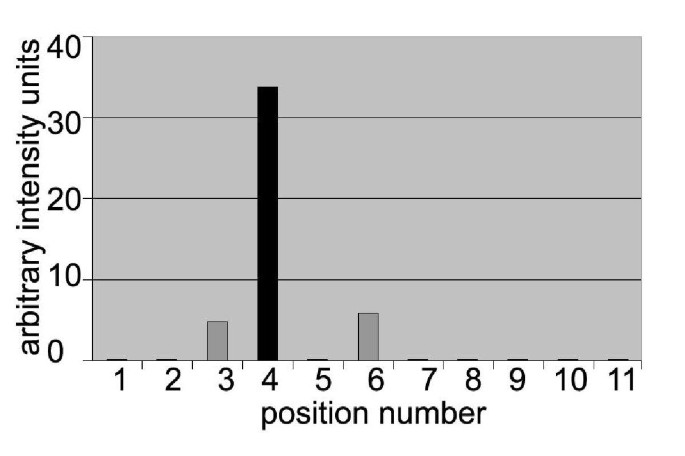
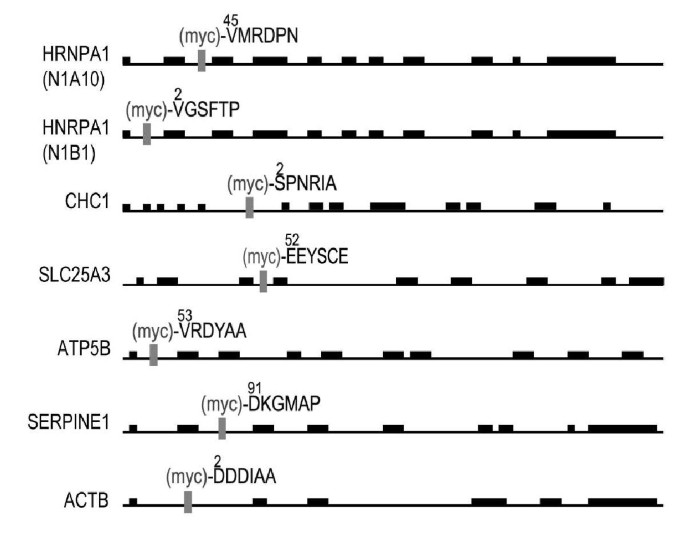
结果解读:约10%的克隆检测到myc标签蛋白的阳性信号,其中包括核蛋白(如异质核糖核蛋白A1)、细胞骨架蛋白(β-肌动蛋白)、线粒体蛋白(F1-β-ATP酶),共染色结果显示标记蛋白与天然蛋白的亚细胞定位完全一致(图2);同时筛选到1个分泌蛋白纤溶酶原激活物抑制剂-1(PAI-1),ELISA检测到显著高于背景的信号(图3);3"-RACE结果显示,myc表位迷你外显子准确插入靶基因的外显子-外显子边界,确保标签融合不破坏蛋白的开放阅读框(图4)。
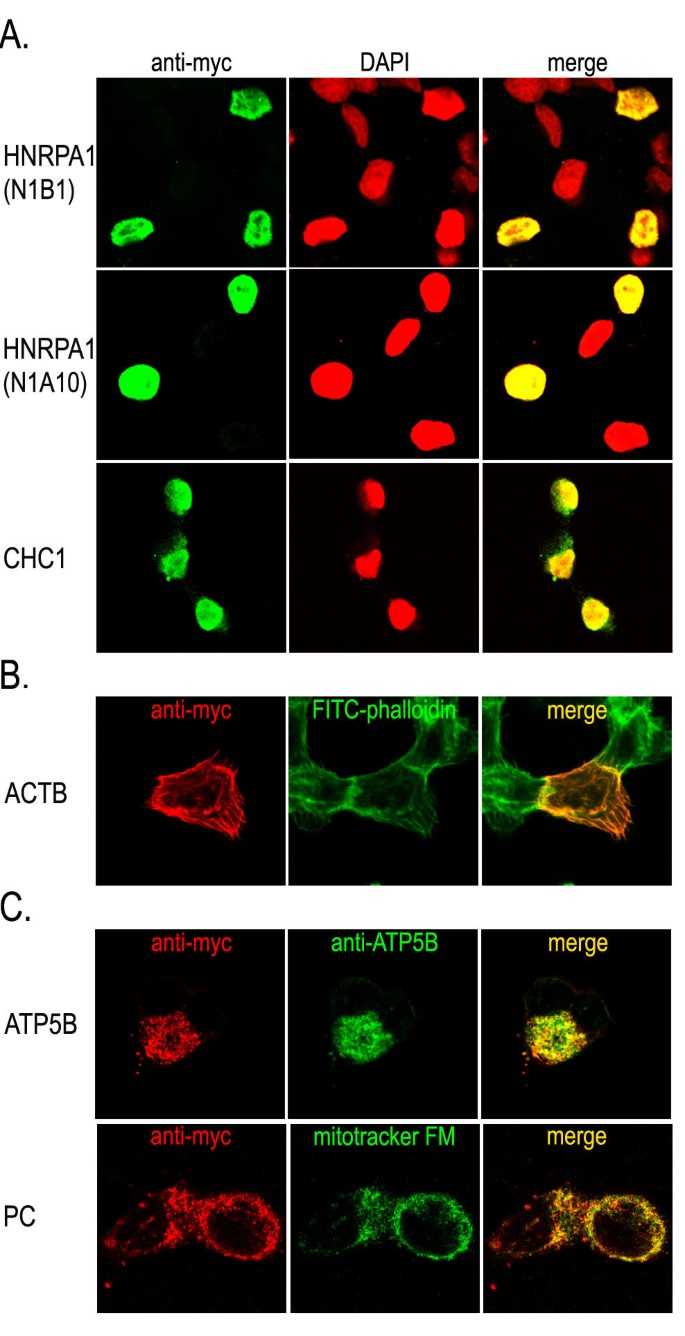
实验所用关键产品:Cy3标记驴抗小鼠IgG(Jackson ImmunoResearch)、Mitotracker Green FM(Molecular Probes)、抗ATP5B特异性抗体、兔抗Ep2表位多克隆抗体(用于ELISA检测)。
3.3 标记蛋白的全长表达验证
实验目的:验证myc标签标记后的靶蛋白以全长形式表达,确保标签融合不导致蛋白截短或功能缺失。
方法细节:选取标记的F1-β-ATP酶(ATP5B)与β-肌动蛋白克隆,分别提取Cre重组酶处理前后的细胞裂解液,进行蛋白质免疫印迹(Western blot)分析;先用抗myc抗体检测标签蛋白,再用靶蛋白特异性抗体检测内源蛋白与标记蛋白的分子量差异。
结果解读:Cre处理后的细胞裂解液中检测到myc标签蛋白条带,其分子量比内源蛋白大3-4kDa,与myc表位标签的分子量一致;靶蛋白特异性抗体能同时识别内源蛋白与标记蛋白,说明标记蛋白为全长融合形式,标签融合未导致蛋白截短(图5)。
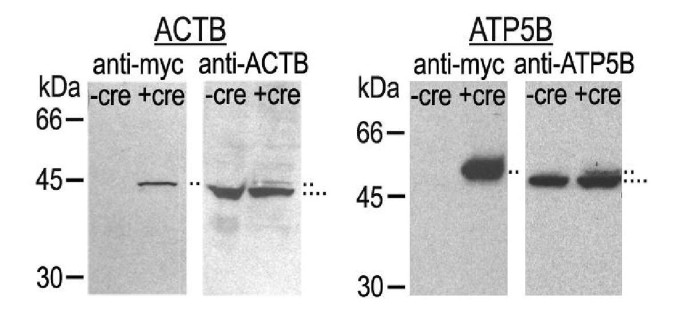
实验所用关键产品:兔抗myc多克隆抗体(Cell Signaling Technology)、ECL化学发光检测系统(Amersham)、Hybond-C Extra硝酸纤维素膜(Amersham)。
3.4 缺氧诱导的蛋白转位筛选应用
实验目的:验证蛋白捕获v2.1系统可用于筛选响应胞外信号发生亚细胞定位变化的功能蛋白。
方法细节:将嘌呤霉素抗性克隆铺于96孔板,经Cre重组酶处理后分为两组,分别在常氧(95%空气/5%CO₂)与缺氧(95%N₂/5%CO₂)条件下培养18小时;采用免疫荧光染色观察蛋白定位变化,采用Western blot验证蛋白表达水平的稳定性。
结果解读:筛选到真核翻译起始因子1A(EIF1A),常氧下其在细胞质呈斑片状分布,缺氧下转变为类似肌动蛋白细胞骨架的纤维状分布(图6B);Western blot结果显示,常氧与缺氧条件下EIF1A的表达水平与分子量一致,说明定位变化是蛋白转位而非降解或翻译后修饰导致(图6C)。
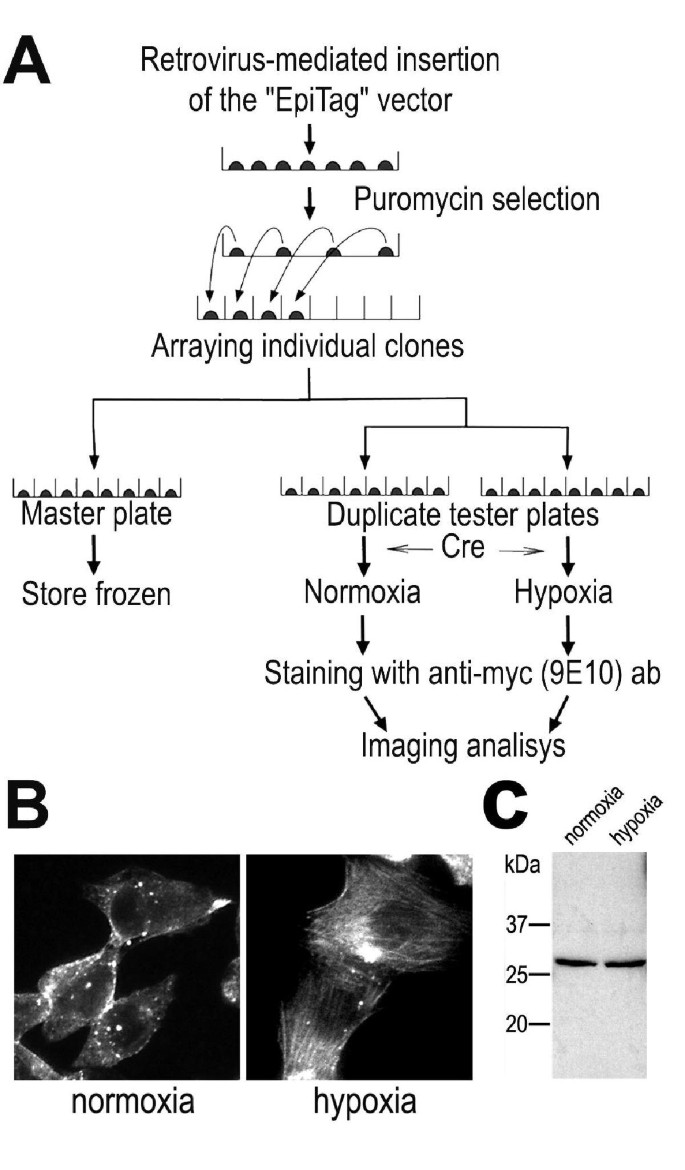
文献未提及具体实验产品,领域常规使用缺氧培养箱、激光共聚焦显微镜等仪器。
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
本文涉及的Biomarker为响应缺氧发生亚细胞定位变化的真核翻译起始因子1A(EIF1A),筛选与验证逻辑遵循“标签库构建→信号诱导筛选→身份鉴定→功能验证”的完整链条:首先通过EpiTag系统构建人肺癌细胞的内源蛋白myc标签库,然后在常氧与缺氧条件下筛选定位变化的蛋白,通过3"-RACE鉴定蛋白身份,最后通过Western blot验证蛋白表达水平的稳定性,确认定位变化为转位导致。
研究过程详述
该Biomarker为人肺癌细胞NCI-H1299的内源蛋白,验证方法包括免疫荧光染色观察亚细胞定位变化,以及Western blot验证蛋白表达水平;特异性方面,EIF1A在常氧与缺氧条件下的表达水平与分子量无显著差异,但亚细胞定位特异性从胞质斑片状转变为纤维状,文献未提供敏感性相关数据;样本量方面,共筛选5670个嘌呤霉素抗性克隆,获得1个阳性克隆(文献未提供P值)。
核心成果提炼
EIF1A是首次被发现响应缺氧发生胞质转位的翻译起始因子,其定位变化可能参与缺氧条件下的翻译调控网络,为缺氧应答的非转录调控机制提供了新的研究方向;同时,本研究验证的多种亚细胞定位明确的蛋白(如核蛋白、线粒体蛋白、分泌蛋白)可作为蛋白定位研究的参考Biomarker,为后续蛋白功能研究提供了定位对照。该成果不仅拓展了蛋白捕获技术的应用场景,也为解析缺氧诱导的细胞功能重塑机制提供了新的线索。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。