A functional endosomal pathway is necessary for lysosome biogenesis in Drosophila
功能性内体途径是果蝇溶酶体生物发生的必要条件
| 期刊: | BMC Cell Biology | 影响因子: | |
| 时间: | 2016 | 起止号: | 2016 Nov 16;17(1):36. |
| doi: | 10.1186/s12860-016-0115-7 | 研究方向: | 信号转导 |
文献解析
1. 领域背景与文献引入
文献英文标题:A functional endosomal pathway is necessary for lysosome biogenesis in Drosophila;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学(溶酶体生物发生与内体通路调控)
溶酶体是真核细胞中负责大分子降解的核心细胞器,1950年代由诺贝尔奖得主Christian de Duve首次发现,领域共识:溶酶体生物发生受转录因子EB(TFEB)的系统性调控,同时依赖内体通路与生物合成通路的紧密整合,新合成的溶酶体蛋白通过甘露糖-6-磷酸受体(MPR)或LIMP-2等途径转运至溶酶体。当前领域研究热点集中于溶酶体生物发生的两种核心模型——成熟模型(内体逐步转化为溶酶体)与囊泡运输模型(溶酶体为预存囊泡,通过囊泡融合获取组分),以及内体通路与自噬通路的交叉调控机制。目前未解决的核心问题包括:体内层面缺乏系统性证据明确内体通路各成熟环节对溶酶体生物发生的必要性,两种模型的体内验证数据相对匮乏,且内体通路与自噬交叉调控的结论存在细胞模型间的矛盾。
作者此前研究发现去泛素化酶UBPY参与果蝇溶酶体生物发生,而UBPY的已知核心功能集中于内体通路的受体分选,因此提出假设:内体通路的整体完整性是溶酶体生物发生的必要前提。本研究通过在果蝇脂肪体细胞中特异性阻断内体通路不同成熟阶段,系统性验证该假设,旨在为溶酶体生物发生的成熟模型提供体内实验证据,同时明确内体通路与自噬功能的关联机制,为溶酶体储存疾病的发病机制研究提供新视角。
2. 文献综述解析
作者的综述逻辑按三个核心维度展开:溶酶体生物发生的调控网络、内体通路的功能节点与分子机制、内体通路与自噬通路的交叉调控。
现有研究成果总结显示,溶酶体生物发生方面,已明确TFEB通过调控约500个靶基因实现对溶酶体生成与自噬的系统性调控,溶酶体蛋白的转运存在MPR依赖与非依赖两条平行通路;内体通路方面,Rab家族GTP酶(Rab5、Rab4、Rab7)与ESCRT复合物分别调控内体的早期融合、循环分选与晚期多泡体形成,是内体成熟的核心功能节点;内体与自噬的交叉方面,部分哺乳动物细胞模型研究显示Rab5参与自噬体的早期形成,而ESCRT突变体中则出现自噬体积累的表型,现有研究的优势在于细胞模型中的分子机制解析较为深入,局限性在于体内实验证据不足,尤其是缺乏对整个内体通路各环节的系统性阻断研究,无法明确内体通路完整性对溶酶体生物发生的必要性。
本研究的创新价值在于,首次在体内模型(果蝇脂肪体)中系统性阻断内体通路的不同成熟阶段,明确内体通路的完整性是溶酶体生物发生的必要条件,为溶酶体生物发生的成熟模型提供了关键体内实验支持;同时解决了内体通路与自噬交叉调控的部分矛盾,证明在体内模型中内体通路阻断会导致自噬通量阻滞而非自噬体形成缺陷,为后续相关研究提供了体内实验的参考标准。
3. 研究思路总结与详细解析
本研究的整体框架为:以“内体通路完整性是溶酶体生物发生必要条件”为核心科学问题,通过FLPout技术在果蝇脂肪体细胞中特异性阻断内体通路不同成熟环节,利用溶酶体与自噬标志物检测表型变化,最终验证内体通路对溶酶体生物发生及自噬功能的必要性,形成“假设-体内模型构建-表型检测-结论”的完整研究闭环。
3.1 内体通路阻断模型构建与验证
实验目的为构建果蝇脂肪体细胞内体通路不同阶段的特异性阻断模型,并验证各环节的阻断效率。方法细节上,采用FLPout转基因技术,在少量脂肪体细胞中特异性表达靶向内体通路关键组分的dsRNA或显性负突变体,包括阻断内体出芽的Shibire显性负突变体ShiK44A、阻断早期内体融合的Rab5 dsRNA、阻断内体循环的Rab4显性负突变体Rab4SN、阻断多泡体形成的Chmp1 dsRNA,以及作为阳性对照的阻断晚期内体-溶酶体融合的Rab7显性负突变体Rab7TN;通过液相内吞标记物Texas Red-avidin的摄取实验验证内体通路的阻断效果。结果解读显示,表达上述突变体或dsRNA的细胞中,Texas Red-avidin的内吞或转运过程出现显著缺陷(文献未明确提供样本量,基于图表趋势推测),证明内体通路各环节被有效阻断。产品关联:文献未提及具体实验产品,领域常规使用果蝇转基因品系、荧光标记内吞探针类试剂。
3.2 溶酶体生物发生缺陷检测
实验目的为检测内体通路阻断后溶酶体的形态与功能变化。方法细节上,采用GFP标记的溶酶体相关膜蛋白1(LAMP1)作为溶酶体形态标志物,通过免疫组化(IHC)检测内源性组织蛋白酶L(溶酶体核心水解酶)的分布与表达水平;利用ImageJ软件定量分析GFP-LAMP1囊泡的大小及组织蛋白酶L的荧光相对强度。结果解读显示,野生型细胞中GFP-LAMP1标记出大的核周溶酶体及胞质中均匀分布的小囊泡,而内体通路阻断的细胞中GFP-LAMP1囊泡大小显著减小(文献未明确提供样本量,P<0.0001);同时组织蛋白酶L的荧光强度在阻断细胞中显著降低(文献未明确提供样本量,P<0.0001),表明溶酶体的形态发生与功能成熟均出现严重缺陷。
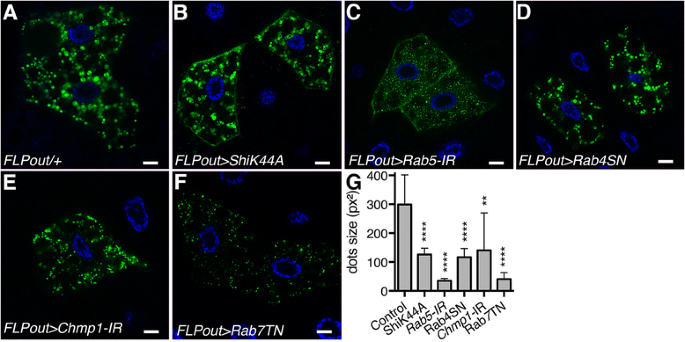
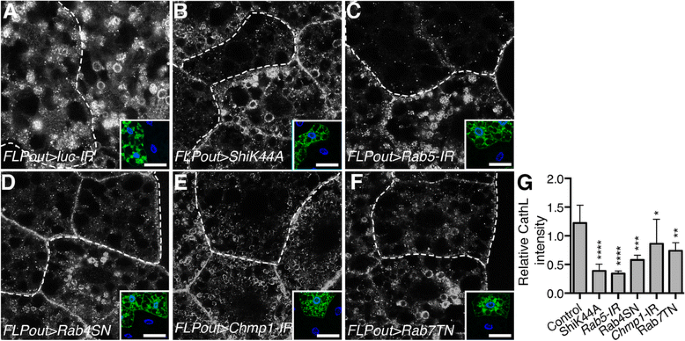
产品关联:实验所用关键产品:抗组织蛋白酶L抗体(Abcam,货号ab133641);其余未提及产品,领域常规使用GFP融合蛋白转基因品系、免疫组化荧光二抗类试剂。
3.3 自噬通量阻滞检测
实验目的为检测内体通路阻断对自噬功能的影响。方法细节上,采用GFP标记的Atg8a作为自噬体标志物,GFP-mCherry-Atg8a串联荧光标记物作为自噬通量检测工具,通过免疫组化检测自噬底物Ref(2)P(果蝇p62同源物)的积累情况;利用ImageJ软件定量分析GFP-Atg8a囊泡数量、GFP与mCherry信号的Pearson共定位系数及Ref(2)P聚集物的大小。结果解读显示,内体通路阻断的细胞中,即使在喂食的基础状态下也出现大量GFP-Atg8a阳性自噬体(文献未明确提供样本量,P<0.0001);GFP-mCherry-Atg8a的共定位系数显著升高(文献未明确提供样本量,P<0.0001),表明自噬体无法与溶酶体融合形成自溶酶体,自噬通量出现阻滞;同时Ref(2)P聚集物的大小显著增加(文献未明确提供样本量,P<0.0001),进一步验证自噬降解功能受损。
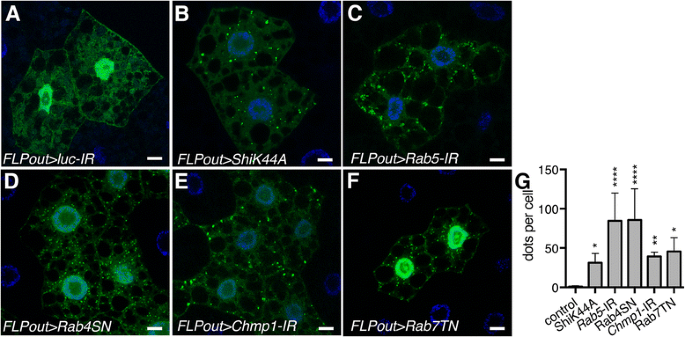
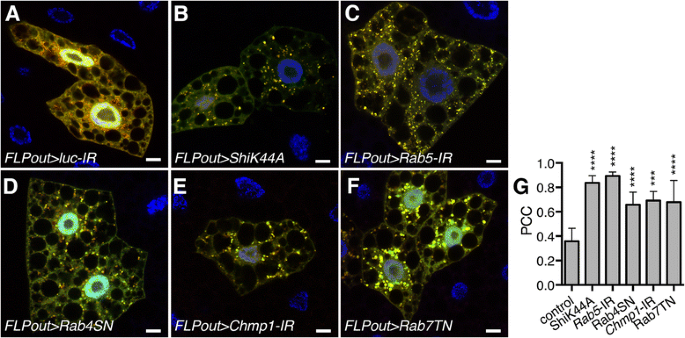
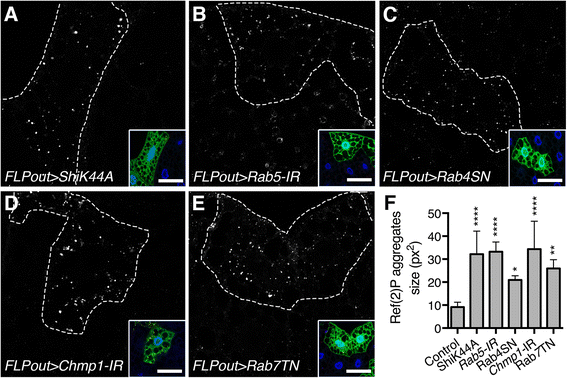
产品关联:文献未提及具体实验产品,领域常规使用自噬标志物转基因品系、抗p62同源物抗体类试剂。
4. Biomarker研究及发现成果解析
本研究未涉及传统疾病诊断或预后生物标志物,而是鉴定了内体通路的核心功能组分(Shibire、Rab5、Rab4、Chmp1、Rab7)作为溶酶体生物发生与自噬功能的调控型Biomarker,筛选逻辑为:基于内体通路已知的成熟阶段功能节点,在体内模型中系统性阻断各节点功能,通过溶酶体与自噬标志物的表型变化验证其调控作用。
研究过程详述显示,这些Biomarker均为内体通路的固有功能蛋白,验证方法为在果蝇脂肪体细胞中通过dsRNA或显性负突变体阻断其功能,利用免疫组化与荧光标记技术检测溶酶体标志物(LAMP1、组织蛋白酶L)与自噬标志物(Atg8a、Ref(2)P)的变化;特异性方面,每个Biomarker的阻断均特异性对应内体通路的某一成熟阶段,且均导致一致的溶酶体生物发生缺陷表型,敏感性方面,即使在少量细胞中阻断目标蛋白功能,也能检测到显著的表型变化(文献未明确提供具体敏感性数值)。
核心成果提炼显示,这些内体通路组分是溶酶体生物发生的必要调控因子,其功能缺失会直接导致溶酶体形态与功能异常,并进一步引发自噬通量阻滞;创新性在于首次在体内模型中系统性验证了内体通路各成熟环节对溶酶体生物发生的必要性,为溶酶体生物发生的成熟模型提供了关键体内实验证据;统计学结果显示,各阻断组与对照组的表型差异均具有极显著性(P<0.0001),证明结论的可靠性。该成果为溶酶体储存疾病的研究提供了新方向,提示内体通路功能异常可能是此类疾病的潜在发病机制之一。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。