ADP-ribosyltransferase PARP11 suppresses Zika virus in synergy with PARP12
ADP-核糖基转移酶PARP11与PARP12协同抑制寨卡病毒
| 期刊: | Cell and Bioscience | 影响因子: | 6.100 |
| 时间: | 2021 | 起止号: | 2021 Jun 29;11(1):116. |
| doi: | 10.1186/s13578-021-00628-y | 研究方向: | 微生物学 |
文献解析
1. 领域背景与文献引入
文献英文标题:ADP-ribosyltransferase PARP11 suppresses Zika virus in synergy with PARP12;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:病毒免疫学(寨卡病毒先天免疫调控)
寨卡病毒于1947年在乌干达首次分离,近70年保持低流行状态,2015年起在太平洋岛屿、巴西等地区爆发,被世界卫生组织列为国际关注的突发公共卫生事件。寨卡病毒感染可导致成人吉兰-巴雷综合征,孕妇感染可引发胎儿小头畸形、宫内生长受限等严重出生缺陷,目前尚无获批的疫苗或特异性抗病毒药物。领域共识:先天免疫中的I型干扰素(IFN-I)及干扰素刺激基因(ISGs)是宿主抵抗病毒感染的核心防线,ISGs通过多种分子机制抑制病毒复制。现有研究已发现部分聚腺苷二磷酸核糖聚合酶(PARP)家族成员(如PARP12、PARP13)具有抗病毒功能,但PARP11的抗病毒作用存在争议,此前研究显示其通过降解I型干扰素受体1(IFNAR1)促进水泡性口炎病毒(VSV)和单纯疱疹病毒1型(HSV-1)复制,但其在寨卡病毒感染中的作用尚未明确,且PARP家族成员间的协同抗病毒机制仍待阐明。本研究旨在探究PARP11在寨卡病毒感染中的功能及作用机制,为寨卡病毒的防治提供潜在靶点。
2. 文献综述解析
本文综述部分围绕寨卡病毒的流行危害、先天免疫ISGs的抗病毒作用、PARP家族成员的功能争议三个维度展开,系统梳理了领域内研究现状,明确了PARP11在寨卡病毒感染中的研究空白。
现有研究已证实寨卡病毒的全球流行趋势及严重临床危害,且明确I型干扰素诱导的ISGs是抑制寨卡病毒复制的关键因素,其中PARP12已被证实通过PARP酶活性介导寨卡病毒非结构蛋白1(NS1)和非结构蛋白3(NS3)的ADP-核糖基化,进而促进其泛素化降解。同时,研究发现PARP家族成员的抗病毒功能存在多样性,部分成员依赖自身PARP酶活性,部分则不依赖,但PARP11的功能存在矛盾报道,此前研究显示其通过下调IFNAR1蛋白水平抑制干扰素信号通路,从而促进VSV和HSV-1复制,但其在寨卡病毒感染中的作用尚未被探究。现有研究的局限性在于,对PARP11在不同病毒感染中的功能差异机制缺乏理解,且未揭示PARP家族成员间的协同抗病毒作用。本研究的创新价值在于,首次发现PARP11是寨卡病毒感染诱导的ISG,具有显著的抗寨卡病毒功能,且该功能不依赖自身PARP酶活性,而是通过与PARP12协同促进病毒NS1和NS3蛋白降解,解决了PARP11功能争议的问题,拓展了PARP家族的抗病毒调控网络。
3. 研究思路总结与详细解析
本研究以“PARP11是否为抗寨卡病毒的ISG及其作用机制”为核心科学问题,采用“功能验证-机制探究-协同作用分析”的技术路线,通过细胞模型构建、分子生物学实验及蛋白相互作用分析,系统阐明了PARP11协同PARP12抑制寨卡病毒的分子机制。
3.1 PARP11作为干扰素刺激基因的诱导验证
实验目的:确认PARP11是否为I型干扰素及寨卡病毒感染诱导的ISG。方法细节:构建IFNAR1敲除的HEK293T和A549细胞系,分别用重组人IFN-α(1000 U/mL)、IFN-β(20 ng/mL)处理24小时,或用寨卡病毒感染不同时间点,通过实时荧光定量PCR(qRT-PCR)检测PARP11的mRNA水平,通过蛋白质免疫印迹(Western blotting)检测蛋白表达,并进行灰度值定量分析。结果解读:在野生型细胞中,IFN处理和寨卡病毒感染后,PARP11的mRNA和蛋白水平均显著上调,其中IFN-α处理后HEK293T细胞中PARP11 mRNA水平升高约3倍(n=3,P<0.001),寨卡感染48小时后A549细胞中蛋白水平升高约2.5倍(n=3,P<0.01);而在IFNAR1敲除细胞中,PARP11的表达无明显变化。这表明PARP11是依赖IFNAR1信号通路的ISG。
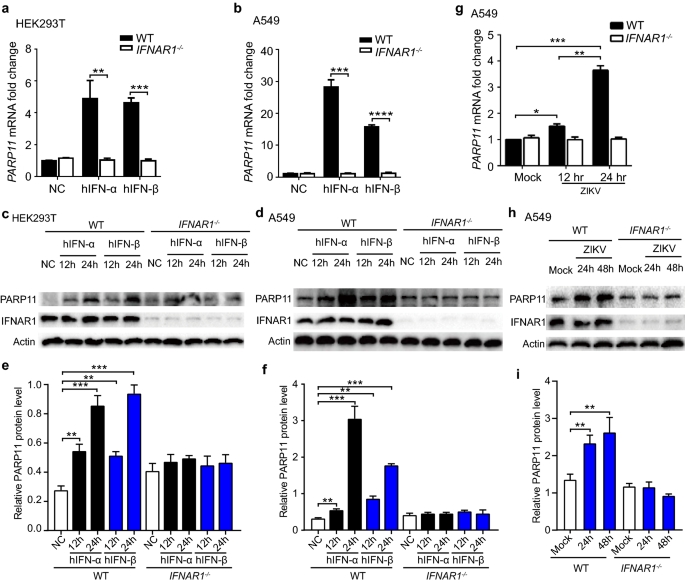
产品关联:实验所用关键产品包括PureLink RNA提取试剂盒(赛默飞世尔)、One Step PrimeScript RT-PCR试剂盒(Takara)、兔抗PARP11抗体(Finetest)等。
3.2 PARP11抗寨卡病毒的功能验证
实验目的:明确PARP11对寨卡病毒复制的调控作用。方法细节:通过CRISPR/Cas9系统构建PARP11敲除的A549细胞系,同时构建PARP11过表达的A549细胞系,感染寨卡病毒后,采用空斑实验检测细胞上清中的病毒滴度,实时荧光定量PCR检测细胞内的病毒RNA水平,并绘制病毒生长曲线。结果解读:过表达PARP11的细胞中,寨卡病毒滴度降低约10倍(n=3,P<0.0001),病毒RNA水平降低约4倍(n=3,P<0.001);而敲除PARP11的细胞中,病毒滴度和RNA水平均显著升高,病毒生长速率明显加快。这证实PARP11具有显著的抗寨卡病毒功能。
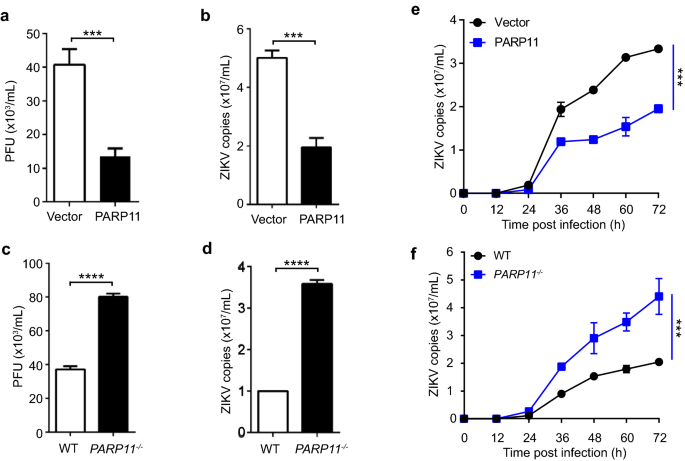
产品关联:空斑实验使用BHK-21细胞,实时荧光定量PCR使用SYRB Green qPCR mix(TransGen Biotec),CRISPR/Cas9系统采用sgRNA表达载体及Cas9质粒。
3.3 PARP11抗寨卡病毒不依赖IFNAR1蛋白水平调控
实验目的:探究PARP11是否通过调控IFNAR1蛋白水平发挥抗寨卡病毒功能。方法细节:用寨卡病毒和VSV分别感染野生型和PARP11敲除的A549细胞,蛋白质免疫印迹检测IFNAR1蛋白水平及细胞内的ADP-核糖化水平,并进行灰度值定量分析。结果解读:寨卡病毒感染后,野生型和PARP11敲除细胞中的IFNAR1蛋白水平均无明显变化,而VSV感染后IFNAR1水平显著降低;同时,野生型细胞在寨卡感染后ADP-核糖化水平显著升高(n=3,P<0.01),但PARP11敲除细胞中无明显变化。这表明PARP11抗寨卡病毒功能不依赖IFNAR1蛋白水平调控,可能通过调控细胞内的ADP-核糖化发挥作用。
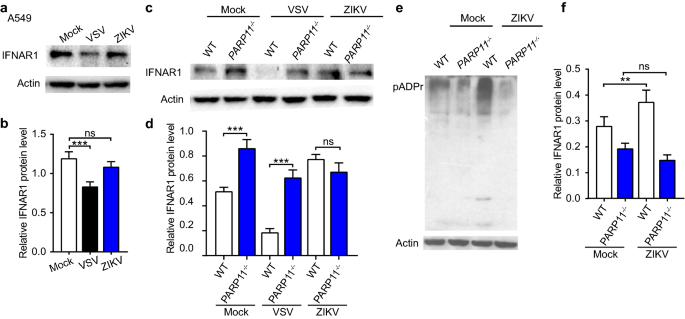
产品关联:使用小鼠抗聚ADP-核糖抗体(GeneTex)检测ADP-核糖化水平。
3.4 PARP11抗寨卡病毒不依赖自身PARP酶活性
实验目的:验证PARP11的PARP酶活性是否参与其抗寨卡病毒功能。方法细节:构建PARP11的全长、WWE域缺失、PARP域缺失及酶活性失活(G205A)突变体,转染HeLa细胞后感染寨卡病毒,空斑实验检测病毒滴度,蛋白质免疫印迹验证突变体的表达。结果解读:全长PARP11和酶活性失活突变体均能显著抑制寨卡病毒复制,病毒滴度降低约5倍(n=3,P<0.001),而WWE域缺失或PARP域缺失的突变体无明显抑制作用。这表明PARP11的抗寨卡病毒功能不依赖自身PARP酶活性,但需要完整的WWE域和PARP域结构。
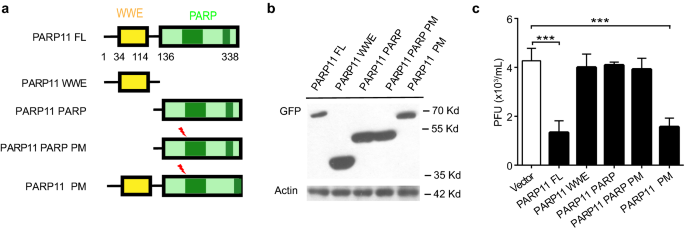
产品关联:采用定点突变技术构建酶活性失活突变体,使用抗GFP抗体(Abcam)验证突变体表达。
3.5 PARP11协同PARP12促进寨卡病毒蛋白降解
实验目的:探究PARP11与PARP12在抗寨卡病毒中的协同作用。方法细节:在野生型、PARP11敲除、PARP12敲除及双敲除的HEK293T细胞中,共转染寨卡病毒NS1/NS3与PARP12、PARP11质粒,蛋白质免疫印迹检测NS1/NS3蛋白水平;同时在PARP11过表达和敲除的A549细胞中感染寨卡病毒,检测内源NS1/NS3蛋白水平。结果解读:PARP11与PARP12共转染时,NS1和NS3蛋白水平显著降低(n=3,P<0.05至P<0.001),且该降解作用在PARP11或PARP12敲除细胞中显著减弱;过表达PARP11的A549细胞中内源NS1/NS3水平降低约40%(n=3,P<0.01),敲除PARP11则升高约60%(n=3,P<0.001)。这表明PARP11与PARP12协同促进寨卡病毒NS1和NS3蛋白的降解。
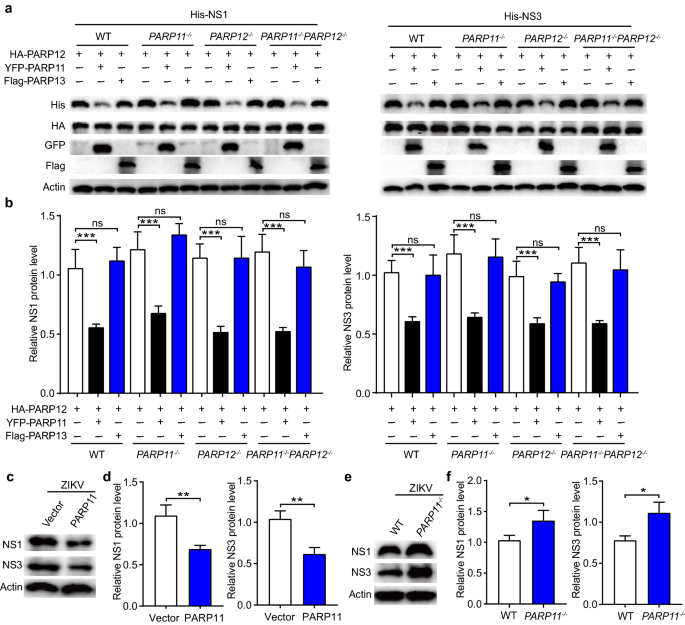
产品关联:使用免疫沉淀实验验证蛋白相互作用,采用抗HA、His标签抗体(Sigma-Aldrich)。
3.6 PARP11抗寨卡病毒功能主要依赖PARP12
实验目的:明确PARP11的抗寨卡病毒功能是否依赖PARP12的存在。方法细节:在野生型和PARP12敲除的A549细胞中,分别过表达PARP11,感染寨卡病毒后,空斑实验检测病毒滴度,实时荧光定量PCR检测病毒RNA水平;同时在PARP12敲除的HEK293T细胞中,转染PARP11野生型及酶活性失活突变体,检测NS1/NS3蛋白水平。结果解读:过表达PARP11在野生型细胞中显著抑制寨卡病毒复制,但在PARP12敲除细胞中的抑制作用显著减弱(病毒滴度仅降低约2倍,n=3,P<0.01);PARP11在PARP12敲除细胞中对NS1/NS3的降解效率也显著低于野生型细胞(n=3,P<0.001)。这表明PARP11的抗寨卡病毒功能主要依赖PARP12的存在。
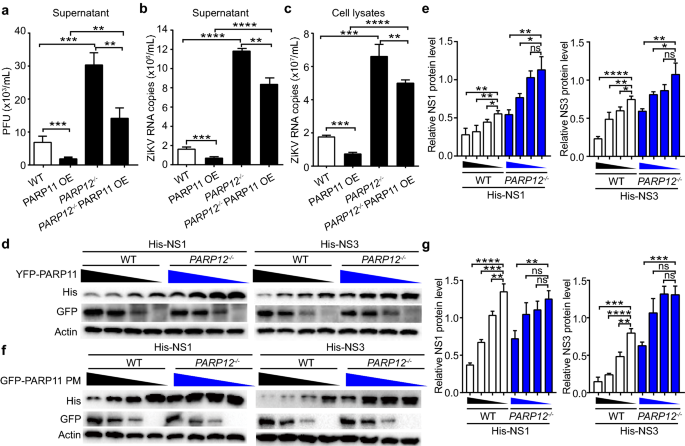
产品关联:使用PARP12敲除的A549细胞系,构建方法为CRISPR/Cas9系统。
3.7 PARP11与PARP12的相互作用结构域验证
实验目的:明确PARP11与PARP12相互作用的关键结构域。方法细节:构建PARP11的WWE域、PARP域突变体及PARP12的锌指结构域(ZnF)、WWE域、PARP域突变体,通过免疫沉淀实验检测相互作用;同时在Vero细胞中共转染PARP11和PARP12的荧光标记质粒,免疫荧光共定位实验观察两者的亚细胞定位。结果解读:免疫沉淀实验显示,PARP11通过WWE域与PARP12的WWE域相互作用,而PARP12通过PARP域与寨卡病毒NS1蛋白相互作用;免疫荧光共定位实验显示,PARP11与PARP12在细胞内共定位。这表明两者通过WWE域形成复合物,协同调控病毒蛋白的降解。
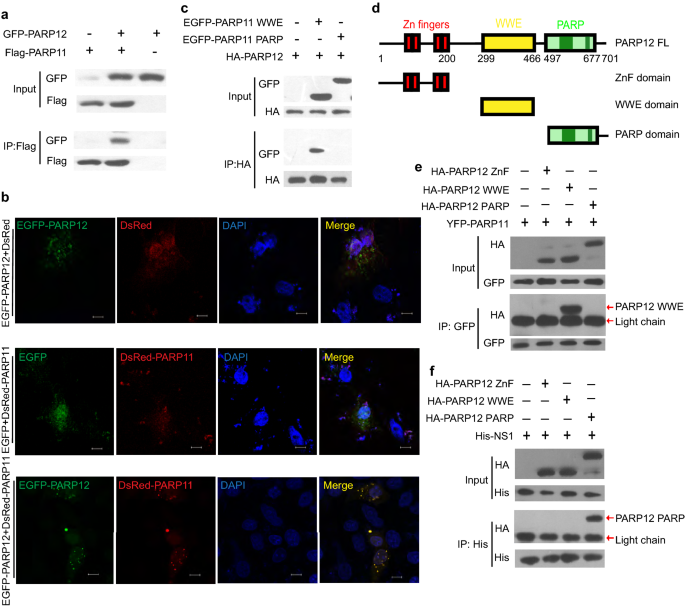
产品关联:使用共聚焦显微镜(Carl Zeiss LSM700)进行免疫荧光成像,采用抗Flag、GFP抗体(Sigma-Aldrich、Abcam)进行免疫沉淀。
4. Biomarker研究及发现成果
本研究发现的关键Biomarker为ADP-核糖基转移酶PARP11,作为新的抗寨卡病毒ISG,其通过与PARP12协同作用抑制寨卡病毒复制,具有潜在的抗病毒治疗靶点价值。
PARP11是I型干扰素和寨卡病毒感染诱导的ISG,筛选逻辑为:首先通过IFN处理和病毒感染验证其诱导表达,然后通过功能实验验证其抗寨卡病毒活性,接着通过机制实验阐明其与PARP12的协同作用及结构基础。PARP11来源于宿主细胞内源性表达,验证方法包括实时荧光定量PCR检测mRNA水平、蛋白质免疫印迹检测蛋白水平、空斑实验检测病毒滴度、免疫沉淀实验检测蛋白相互作用等。特异性方面,PARP11仅在寨卡病毒感染中表现出抗病毒功能,与在VSV和HSV-1感染中的促病毒作用不同;敏感性方面,过表达PARP11可使寨卡病毒滴度降低约10倍(n=3,P<0.0001),敲除PARP11则使病毒滴度显著升高。核心成果提炼:PARP11作为抗寨卡病毒ISG,通过与PARP12的WWE域相互作用,协同促进寨卡病毒NS1和NS3蛋白的降解,从而抑制病毒复制;该发现首次阐明了PARP11在寨卡病毒感染中的抗病毒功能,解决了其在不同病毒感染中的功能争议,拓展了PARP家族的协同抗病毒机制;统计学结果显示,所有实验数据均来自至少3次独立重复,P值<0.05至<0.0001,具有显著统计学意义。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。