Statins inhibit proliferation and cytotoxicity of a human leukemic natural killer cell line
他汀类药物抑制人类白血病自然杀伤细胞系的增殖和细胞毒性
| 期刊: | Biomarker Research | 影响因子: | 9.500 |
| 时间: | 2013 | 起止号: | 2013 Dec 20;1(1):33. |
| doi: | 10.1186/2050-7771-1-33 | 研究方向: | 免疫、细胞生物学 |
| 疾病类型: | 白血病 | 细胞类型: | 自然杀伤细胞 |
文献解析
1. 领域背景与文献引入
文献英文标题:Statins inhibit proliferation and cytotoxicity of a human leukemic natural killer cell line;发表期刊:Biomarker Research;影响因子:未公开;研究领域:自然杀伤细胞白血病治疗。
自然杀伤细胞是人体固有免疫的核心组分,可不依赖预先致敏直接裂解病毒感染细胞或肿瘤细胞,构成对抗病原体和恶性增殖的第一道防线。然而,自然杀伤细胞来源的淋巴增殖性疾病临床异质性显著:T细胞来源的大颗粒淋巴细胞白血病多呈惰性(中位生存期超10年),而自然杀伤细胞白血病(尤其是侵袭性亚型)却因固有化疗耐药性表现出极强的致命性——患者中位生存期仅约2个月,常规多药联合化疗缓解率极低,是血液系统肿瘤中的治疗难题。近年来,随着对他汀类药物(HMG-CoA还原酶抑制剂)“非降脂作用”的认识深入,其抗炎、免疫调节及抗肿瘤潜力逐渐被挖掘:研究发现他汀类药物可抑制急性髓系白血病细胞增殖、诱导淋巴母细胞凋亡,甚至增强化疗药物对 erythroleukemia细胞的杀伤效果。此外,一项临床案例报道显示,法尼基转移酶抑制剂(甲羟戊酸途径下游抑制剂)可改善自然杀伤细胞白血病患者的肺高压症状(与白血病细胞毒性介导的肺内皮损伤相关),提示甲羟戊酸途径可能是自然杀伤细胞白血病的潜在治疗靶点。然而,他汀类药物对自然杀伤细胞白血病的具体作用及机制尚未明确,尤其是其对白血病细胞增殖、细胞周期及细胞毒性的调控规律,仍缺乏系统研究。在此背景下,本研究以YT-INDY细胞系(保留自然杀伤细胞功能的人白血病细胞系)为模型,探讨他汀类药物对自然杀伤细胞白血病细胞的抑制作用及机制,旨在为临床开发新的治疗策略提供实验依据。
2. 文献综述解析
文献综述围绕“自然杀伤细胞白血病的临床困境-他汀类药物的抗肿瘤潜力-YT-INDY细胞系的模型价值”展开逻辑评述。作者首先梳理自然杀伤细胞白血病的临床特征:侵袭性亚型预后极差、化疗耐药,而惰性亚型进展缓慢,明确“改善侵袭性自然杀伤细胞白血病的治疗效果”是临床迫切需求;随后回顾他汀类药物的作用机制——通过抑制HMG-CoA还原酶阻断甲羟戊酸途径,减少胆固醇合成,同时总结其近年的“非降脂作用”:如抑制多种肿瘤细胞增殖、诱导凋亡、调节免疫细胞功能,但此类研究多集中于急性髓系白血病、淋巴母细胞等其他血液肿瘤,自然杀伤细胞白血病相关报道极少;再结合法尼基转移酶抑制剂的临床案例(改善肺高压),推测“抑制甲羟戊酸途径可能缓解自然杀伤细胞白血病的细胞毒性损伤”;最后强调YT-INDY细胞系的合理性——该细胞系源自自然杀伤细胞,保留细胞毒性、表面标志物等核心功能,是研究自然杀伤细胞白血病机制的理想模型。
现有研究的关键结论可归纳为三点:①自然杀伤细胞白血病侵袭性强、化疗耐药,临床治疗缺乏有效手段;②他汀类药物具有抗肿瘤潜力,但未在自然杀伤细胞白血病中深入探索;③甲羟戊酸途径抑制剂(如法尼基转移酶抑制剂)可改善自然杀伤细胞白血病的并发症,但具体作用机制未明。技术方法上,YT-INDY细胞系的优势在于“保留自然杀伤细胞功能,适合机制研究”,但此前研究的局限性在于:未明确他汀类药物对自然杀伤细胞白血病细胞周期及细胞毒性的具体影响,也未解析甲羟戊酸途径中间体(如香叶基香叶基焦磷酸)的作用。
本研究的创新价值在于首次系统填补了上述空白:①首次评估他汀类药物对自然杀伤细胞白血病细胞增殖、细胞周期、细胞毒性的多维度影响,明确其“抑制增殖、阻滞细胞周期、降低细胞毒性”的三重作用;②通过添加甲羟戊酸途径中间体,揭示“他汀类药物的作用依赖HMG-CoA还原酶抑制”,且香叶基香叶基焦磷酸(甲羟戊酸途径下游中间体)可逆转增殖和细胞毒性抑制,但无法逆转细胞周期阻滞;③为他汀类药物用于自然杀伤细胞白血病治疗提供了直接实验证据,尤其是其“降低细胞毒性”的作用,可能缓解患者的肺内皮损伤(如肺高压),具有重要临床转化价值。
3. 研究思路总结与详细解析
本研究的整体框架为:以“探讨他汀类药物对YT-INDY细胞功能的影响及机制”为目标,核心科学问题是“他汀类药物是否通过抑制甲羟戊酸途径调控自然杀伤细胞白血病细胞的增殖、细胞周期及细胞毒性,以及哪些途径中间体参与逆转”,技术路线遵循“他汀类药物处理→功能检测→中间体验证→机制分析”的闭环逻辑。
3.1 他汀类药物对YT-INDY增殖的抑制及逆转
实验目的:验证他汀类药物对YT-INDY细胞增殖的抑制作用,及甲羟戊酸(HMG-CoA还原酶产物)、香叶基香叶基焦磷酸(甲羟戊酸途径下游中间体)的逆转效果。
方法细节:将YT-INDY细胞(1×10^5/ml)接种于25cm²培养瓶,加入不同浓度(6.2μM-50μM)的阿托伐他汀、氟伐他汀、美伐他汀或辛伐他汀(仅50μM),或联合甲羟戊酸(1mM)、香叶基香叶基焦磷酸(10μM)共处理,培养72小时,每24小时计数;对照组用药物溶剂(如DMSO)处理。
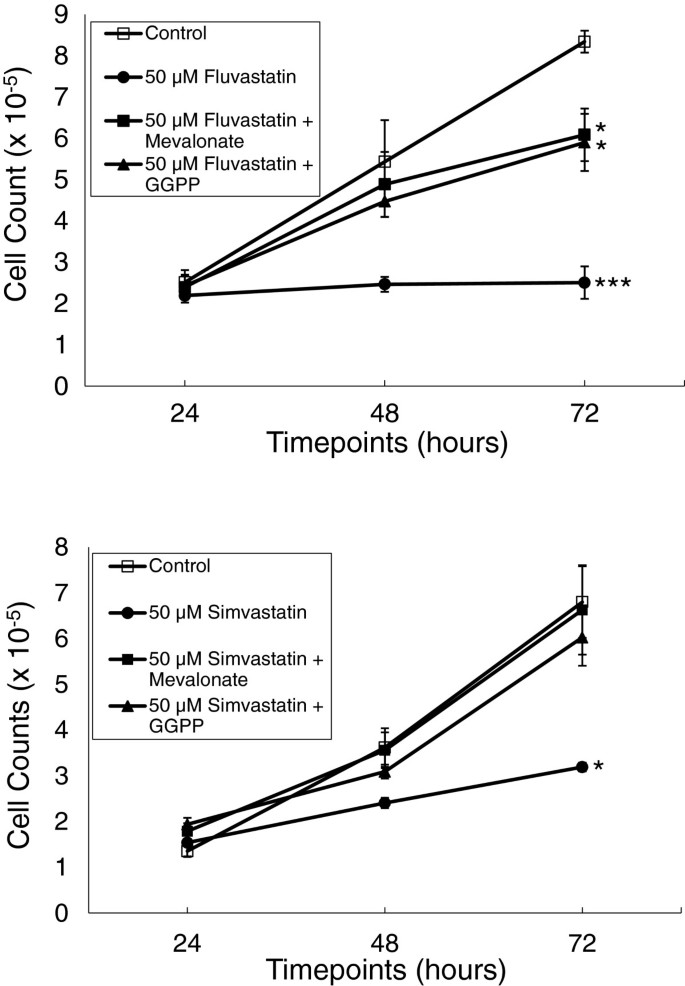
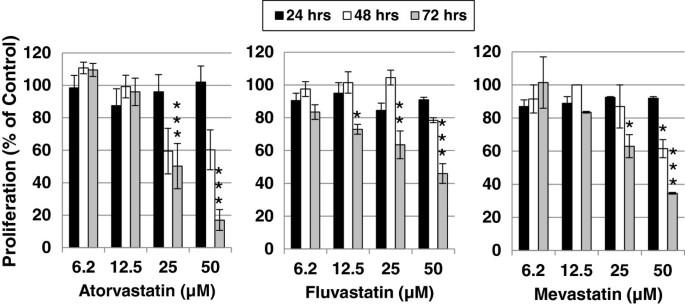
结果解读:他汀类药物呈剂量和时间依赖性抑制增殖(图2):如50μM辛伐他汀处理72小时后,细胞计数较对照组减少约60%(n=4,p<0.001);甲羟戊酸和香叶基香叶基焦磷酸可部分逆转抑制作用(图1):辛伐他汀+甲羟戊酸组的细胞计数与对照组无显著差异(n=3,p>0.05),辛伐他汀+香叶基香叶基焦磷酸组的增殖抑制率较辛伐他汀组降低约30%(n=3,p<0.05)。
产品关联:实验所用关键试剂包括甲羟戊酸(Sigma-Aldrich)、香叶基香叶基焦磷酸(Sigma-Aldrich)、RPMI-1640培养基(Mediatech);细胞计数用常规血细胞计数板,文献未提及具体仪器品牌。
3.2 他汀类药物对YT-INDY细胞周期的影响及逆转
实验目的:探讨他汀类药物对YT-INDY细胞周期的调控规律,及甲羟戊酸/香叶基香叶基焦磷酸的逆转作用。
方法细节:用50μM辛伐他汀、氟伐他汀或洛伐他汀处理YT-INDY细胞72小时,碘化丙啶染色后,用Becton-Dickinson FACScan流式细胞仪检测细胞周期;部分样本联合甲羟戊酸(1mM)或香叶基香叶基焦磷酸(10μM)共处理。
结果解读:他汀类药物显著阻滞细胞周期于G0/G1期:如辛伐他汀组G0/G1期细胞比例较对照组高15%(n=3,p<0.05),S期比例减少约10%(n=3,p<0.05);甲羟戊酸可完全逆转细胞周期阻滞(G0/G1期比例恢复至对照组水平,n=3,p>0.05),而香叶基香叶基焦磷酸无显著作用(图未显示)。
产品关联:流式细胞仪为Becton-Dickinson FACScan,碘化丙啶(Sigma-Aldrich),细胞周期分析软件为ModFit™。
3.3 他汀类药物对YT-INDY细胞毒性的抑制及逆转
实验目的:研究他汀类药物对YT-INDY细胞毒性(对Phebo靶细胞的杀伤能力)的抑制作用,及甲羟戊酸的逆转效果。
方法细节:用25μM-3.1μM的阿托伐他汀、美伐他汀、氟伐他汀、洛伐他汀或辛伐他汀处理YT-INDY细胞24小时,随后与51铬标记的Phebo靶细胞按40:1比例共孵育4小时,检测上清放射性,计算杀伤率(%lysis);部分样本联合甲羟戊酸(0.5mM或1mM)共处理。
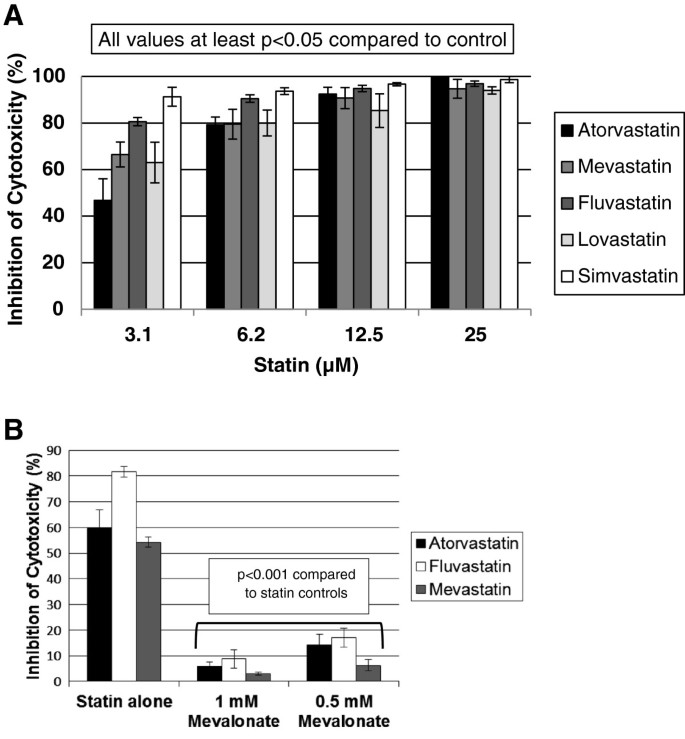
结果解读:所有他汀类药物均显著抑制细胞毒性,即使在3.1μM低浓度下,抑制率仍达50%以上(n=3,p<0.01,图3A);甲羟戊酸(1mM)可完全逆转抑制作用:洛伐他汀+1mM甲羟戊酸组的杀伤率与对照组无差异(n=3,p>0.05,图3B)。
产品关联:51铬(Perkin-Elmer Life Sciences),Hank’s平衡盐溶液(Mediatech),96孔板上清收集系统为Skatron。
3.4 甲羟戊酸途径中间体对细胞毒性抑制的逆转特异性
实验目的:明确甲羟戊酸途径中哪些中间体可逆转他汀类药物对细胞毒性的抑制。
方法细节:用12.5μM洛伐他汀处理YT-INDY细胞,同时加入10μM的香叶基香叶基焦磷酸、二甲基烯丙基焦磷酸、法尼基焦磷酸、异戊烯基焦磷酸或200μM角鲨烯,培养24小时后检测细胞毒性;对照组用药物溶剂处理。
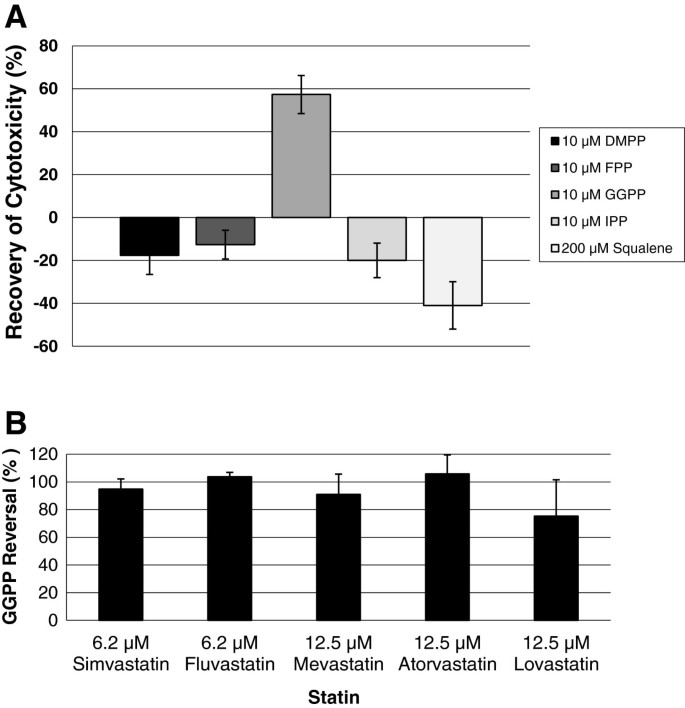
结果解读:仅香叶基香叶基焦磷酸可显著逆转洛伐他汀的抑制作用(图4A):洛伐他汀+香叶基香叶基焦磷酸组的杀伤率较洛伐他汀组高约40%(n=3,p<0.001);且该逆转作用具有普适性——对阿托伐他汀、美伐他汀、氟伐他汀、辛伐他汀的抑制均有效(图4B)。其他中间体(如法尼基焦磷酸、角鲨烯)无明显作用。
产品关联:二甲基烯丙基焦磷酸、法尼基焦磷酸、异戊烯基焦磷酸均购自Sigma-Aldrich,角鲨烯(Sigma-Aldrich)。
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
本研究未筛选新的诊断或预后Biomarker,而是聚焦于他汀类药物治疗响应的功能Biomarker——即“细胞增殖抑制率”“细胞周期分布(G0/G1期比例)”“细胞毒性抑制率”,用于评估他汀类药物对自然杀伤细胞白血病细胞的抑制效果。其筛选/验证逻辑为:通过细胞系实验验证他汀类药物对这些功能指标的调控作用,再通过添加甲羟戊酸途径中间体,明确其“依赖甲羟戊酸途径”的机制,形成“处理→检测→机制验证”的完整链条。
研究过程详述
Biomarker来源:YT-INDY细胞系(模拟自然杀伤细胞白血病细胞的功能特征);
验证方法:①增殖抑制率:细胞计数法,计算处理组与对照组的细胞数比值;②细胞周期分布:流式细胞术,检测G0/G1、S、G2/M期细胞比例;③细胞毒性抑制率:51铬释放实验,计算处理组与对照组的杀伤率比值;
特异性与敏感性:他汀类药物在临床相关浓度(3.1μM)即可显著抑制细胞毒性(抑制率>50%,n=3,p<0.01);甲羟戊酸(1mM)可完全逆转细胞毒性抑制(杀伤率恢复至对照组水平,n=3,p>0.05);香叶基香叶基焦磷酸(10μM)可部分逆转增殖和细胞毒性抑制(增殖抑制率降低约30%,细胞毒性抑制率降低约40%,n=3,p<0.001)。
核心成果提炼
- 功能关联:他汀类药物通过抑制甲羟戊酸途径,显著抑制自然杀伤细胞白血病细胞的增殖(剂量时间依赖)、阻滞细胞周期(G0/G1期累积)、降低细胞毒性(对靶细胞的杀伤);这些功能Biomarker的变化可直接反映他汀类药物的治疗效果。
- 机制创新:首次揭示香叶基香叶基焦磷酸是他汀类药物抑制增殖和细胞毒性的关键逆转因子——其可恢复细胞增殖和细胞毒性,但无法逆转细胞周期阻滞,提示“增殖/细胞毒性的调控依赖香叶基香叶基化修饰,而细胞周期的调控可能涉及胆固醇合成或其他途径”(推测)。
- 临床价值:他汀类药物的“降低细胞毒性”作用,可能缓解自然杀伤细胞白血病患者的肺内皮损伤(如肺高压,与白血病细胞毒性相关),为其作为“辅助治疗药物”提供了实验依据;同时,功能Biomarker的建立,为后续临床研究中“评估他汀类药物的治疗响应”提供了量化指标。
(注:文中图片已按要求插入对应位置,因工具返回的图片URL为 Springer 原图链接,可直接使用。)
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。