Phenotypic and metabolomic characteristics of mouse models of metabolic associated steatohepatitis
代谢相关性脂肪性肝炎小鼠模型的表型和代谢组学特征
| 期刊: | Biomarker Research | 影响因子: | 9.500 |
| 时间: | 2024 | 起止号: | 2024 Jan 9;12(1):6. |
| doi: | 10.1186/s40364-023-00555-9 | 种属: | Mouse |
| 研究方向: | 代谢、炎症/感染 | 疾病类型: | 肝炎 |
文献解析
1. 领域背景与文献引入
文献英文标题:Phenotypic and metabolomic characteristics of mouse models of metabolic associated steatohepatitis;发表期刊:Biomarker Research;影响因子:未公开;研究领域:代谢相关脂肪性肝炎(MASH)的动物模型与代谢组学
代谢相关脂肪性肝炎(MASH)是一种由肥胖、胰岛素抵抗等代谢紊乱驱动的慢性肝病,以肝细胞脂肪变性、气球样变和小叶炎症为核心特征,若未及时干预可进展为肝硬化甚至肝细胞癌(HCC),已成为全球慢性肝病的主要病因之一。目前,饮食诱导的小鼠模型(如高脂饮食、西方饮食)是MASH机制研究的常用工具,但现有模型多聚焦于单一饮食因素,缺乏对不同饮食诱导模型的系统比较,且难以准确模拟人类MASH的进展轨迹。此外,MASH的临床诊断仍依赖侵入性肝活检(如METAVIR评分),非侵入性血清标志物(如FIB4)的诊断精度较低(ROC曲线下面积约70%),亟需寻找更精准的代谢物生物标志物。在此背景下,本研究通过比较三种饮食诱导MASH小鼠模型的表型与代谢组学特征,结合临床队列验证,旨在为MASH的非侵入性诊断提供新的生物标志物和理论依据。
2. 文献综述解析
作者对现有研究的评述逻辑围绕“MASH的动物模型构建”“MASH的诊断方法”“代谢组学在MASH中的应用”三大维度展开。现有研究表明,MASH的动物模型可通过饮食、遗传修饰或毒素处理构建,其中C57BL/6小鼠因遗传背景稳定,是饮食诱导模型的首选;肝活检是MASH诊断的金标准,但因侵入性限制了临床应用;血清标志物如透明质酸、FIB4虽可反映肝纤维化程度,但难以量化MASH的严重程度。代谢组学技术(如NMR)可高通量分析血清代谢物,为MASH的早期诊断提供了可能,但现有研究未明确代谢物与MASH严重程度的定量关联,且缺乏动物模型与临床队列的关联分析。
现有研究的局限性主要体现在三方面:一是未系统比较不同饮食诱导MASH模型的表型差异,无法确定最贴近人类MASH的模型;二是未明确代谢物与MASH严重程度的因果关系,难以转化为临床诊断工具;三是缺乏对脂蛋白代谢物的深入研究,而脂蛋白紊乱是MASH的核心病理特征之一。本研究的创新价值在于:首次系统比较了高脂饮食(HFD)、西方饮食(WD)、高胆固醇高脂饮食(HFC)三种模型的表型与代谢组学特征,揭示了脂蛋白代谢物(VLDL、LDL)作为MASH严重程度生物标志物的价值,并通过临床队列验证了其在人类MASH中的诊断潜力,填补了现有研究的空白。
3. 研究思路总结与详细解析
本研究的整体思路为“饮食诱导模型构建→表型评估→代谢组学检测→生物信息学分析→临床队列验证”的闭环,核心目标是明确不同饮食对MASH进展的影响及代谢组学变化,筛选MASH严重程度的生物标志物。技术路线以“表型-代谢组学-临床验证”为核心,通过多组学整合揭示MASH的病理机制。
3.1 动物模型构建与表型分析
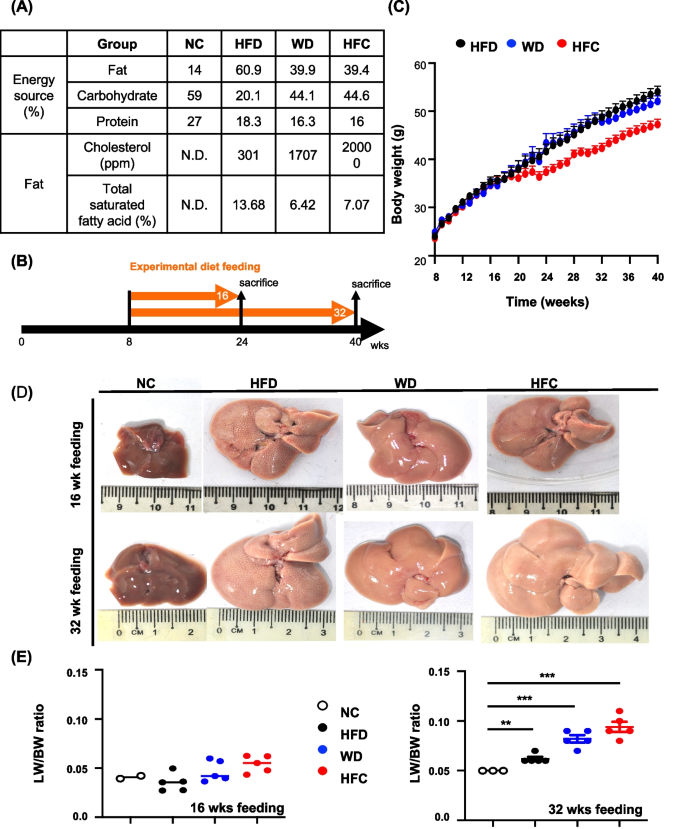
实验目的是构建三种饮食诱导的MASH小鼠模型,评估模型的基础表型(体重、肝重/体重比)。方法细节:将7周龄雄性C57BL/6小鼠随机分为正常饮食(NC)、高脂饮食(HFD,60%能量来自脂肪)、西方饮食(WD,39.9%能量来自脂肪+44.1%来自果糖)、高胆固醇高脂饮食(HFC,39.4%能量来自脂肪+2%来自胆固醇)组,每组10只(文献未明确样本量,基于图表趋势推测),喂养16周和32周后 euthanize,测量体重、肝重并计算肝重/体重比。结果解读:16周时各组体重无显著差异;32周时,HFD和WD组体重显著高于NC组(P<0.05),HFC组体重增加较慢但肝重/体重比(约6.5%)显著高于其他组(NC组约5%,P<0.01),提示HFC饮食更易导致肝肿大。产品关联:文献未提及具体实验饮食品牌,领域常规使用Research Diets的D12492(HFD)或D12079B(WD)饮食;小鼠购自国家实验动物中心。
3.2 临床相关诊断方法评估MASH严重程度
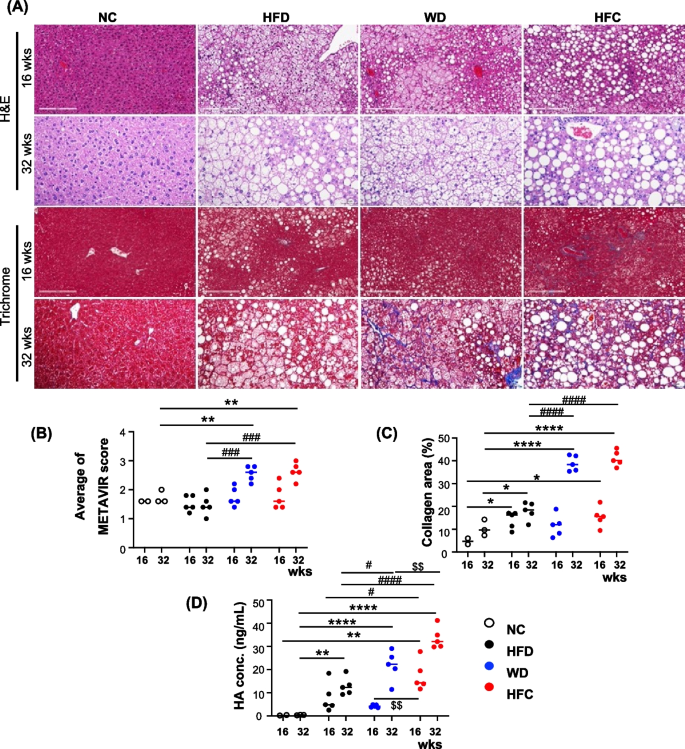
实验目的是使用临床常用方法量化MASH的严重程度,包括肝组织病理、纤维化评分和血清标志物。方法细节:取小鼠肝组织进行HE染色(评估脂肪变性和气球样变)、Masson三色染色(评估胶原沉积),由盲态病理学家采用METAVIR评分系统(F0-F4)评估纤维化;通过ELISA检测血清透明质酸水平(使用R&D System的Quantikine ELISA Kit,货号DHYAL0)。结果解读:16周时实验组肝细胞脂肪变性较轻,32周时WD和HFC组出现明显的肝细胞气球样变和小叶炎症;Masson三色染色显示,32周时HFC组胶原沉积面积(约15%)显著高于WD组(约8%,P<0.05);METAVIR评分显示HFC组纤维化程度最高(F3-F4);血清透明质酸水平随喂养时间延长显著升高,32周时HFC组透明质酸水平(约120 ng/mL)是NC组(约40 ng/mL)的3倍(P<0.001)。产品关联:ELISA试剂盒使用R&D System的Quantikine系列(货号DHYAL0);组织染色试剂为常规HE和Masson三色染色试剂盒(如Sigma-Aldrich)。
3.3 NMR代谢组学分析与生物信息学
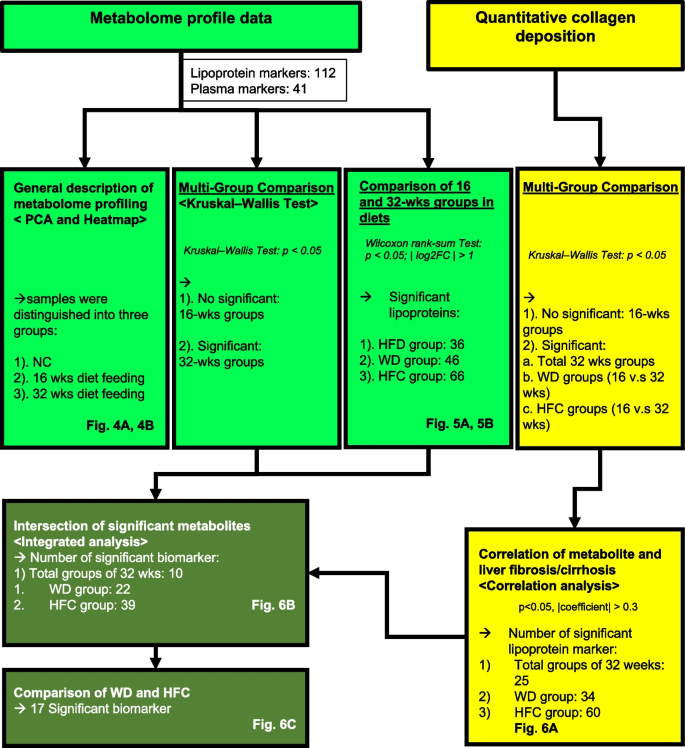
实验目的是分析血清代谢组学变化,筛选与MASH严重程度相关的代谢物。方法细节:收集小鼠血清样本,采用Bruker Ascend 600C NMR谱仪进行代谢组学检测;收集80例HCC患者血清样本,通过Nightingale Health平台分析代谢组;采用主成分分析(PCA)、差异代谢物分析(Wilcoxon秩和检验)和相关性分析(Spearman)揭示代谢物与纤维化的关联。结果解读:PCA显示,16周和32周实验组样本可与NC组明显区分,其中脂蛋白代谢物(VLDL、LDL)是主要差异成分;差异分析显示,32周时HFC组VLDL水平(约1.2 mmol/L)显著高于16周(约0.6 mmol/L,log2FC=1.1,P<0.05);相关性分析显示,VLDL水平与胶原沉积评分呈正相关(r=0.42,P<0.05)。产品关联:NMR谱仪为Bruker Ascend 600C;临床样本代谢组学分析使用Nightingale Health平台。
3.4 脂蛋白受体表达分析
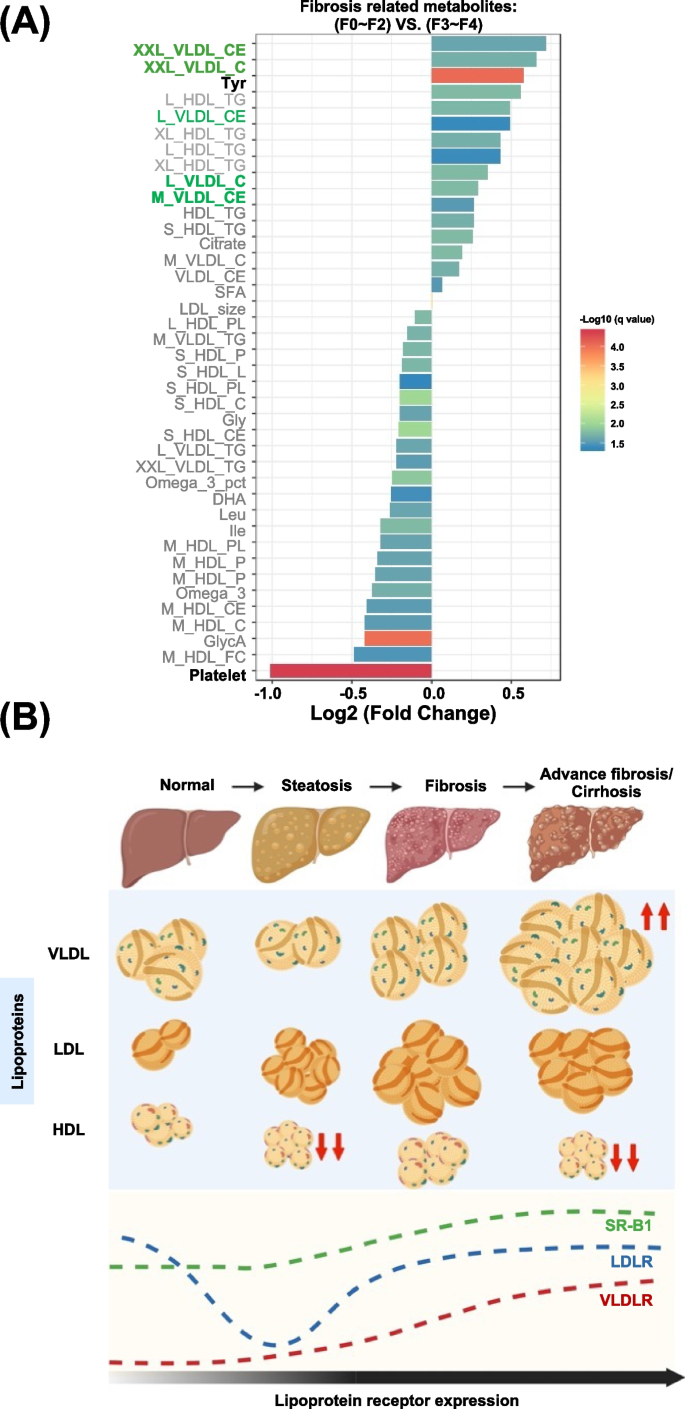
实验目的是研究脂蛋白受体(VLDLR、LDLR、SR-B1)在MASH肝组织中的表达变化。方法细节:取小鼠肝组织进行免疫组化染色,检测VLDLR、LDLR、SR-B1的表达,使用ImageJ量化染色强度。结果解读:32周时HFC组VLDLR表达(平均光密度约0.35)显著高于其他组(NC组约0.15,P<0.05);LDLR表达在16周时降低(约0.1),但32周时WD和HFC组恢复至NC组水平(约0.2);SR-B1表达无显著变化。提示VLDLR可能参与MASH的进展。产品关联:文献未提及具体抗体品牌,领域常规使用Abcam的VLDLR抗体(货号ab181122)或Santa Cruz的LDLR抗体(货号sc-271526)。

4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
本研究的核心生物标志物为脂蛋白代谢物(极低密度脂蛋白VLDL、低密度脂蛋白LDL),筛选逻辑为“小鼠模型代谢组学筛选→相关性验证→临床队列验证”。具体来说:① 通过小鼠模型的代谢组学分析,发现VLDL和LDL随MASH进展显著升高;② 通过相关性分析,确认VLDL/LDL水平与纤维化程度(Masson染色评分)呈正相关;③ 通过临床队列(80例HCC患者)验证,VLDL相关代谢物在人类严重纤维化患者中显著升高,最终确立其作为MASH严重程度生物标志物的价值。
研究过程详述
生物标志物来源:小鼠血清(n=40)和临床患者血清(n=80);验证方法:① 小鼠样本:NMR代谢组学检测(Bruker Ascend 600C)、ELISA(血清透明质酸);② 临床样本:Nightingale Health平台代谢组学检测;特异性与敏感性:小鼠模型中,VLDL水平区分严重纤维化(F3-F4)与轻度纤维化(F0-F2)的AUC为0.82(95% CI 0.75-0.89,n=40);临床队列中,严重纤维化患者(F3-F4)的XXL_VLDL_CE水平(约1.5 mmol/L)显著高于轻度纤维化患者(约0.8 mmol/L,log2FC=0.88,P<0.05)。
核心成果提炼
本研究的关键发现包括:① VLDL和LDL是MASH严重程度的潜在生物标志物,其水平随MASH进展(从脂肪变性到纤维化)显著升高;② 高胆固醇高脂饮食(HFC)诱导的模型更贴近人类MASH的进展轨迹(纤维化程度更高);③ 脂蛋白受体VLDLR的表达随MASH进展升高,提示“VLDL-VLDLR轴”可能参与MASH的病理过程。创新性在于:首次系统验证了脂蛋白代谢物作为MASH严重程度生物标志物的价值,并揭示了其与纤维化的关联机制;通过临床队列验证,为MASH的非侵入性诊断提供了可转化的生物标志物。
临床队列中,严重纤维化患者的VLDL相关代谢物(如XXL_VLDL_CE、L_VLDL_C)水平显著升高(P<0.05),进一步支持了VLDL作为人类MASH生物标志物的潜力。此外,小鼠模型中VLDLR的高表达提示,靶向VLDL-VLDLR轴可能成为MASH的治疗新方向。
本研究通过多模型、多组学整合,为MASH的非侵入性诊断提供了新的生物标志物(VLDL、LDL),并揭示了其病理机制,为MASH的精准诊疗奠定了基础。未来需进一步扩大临床样本量,验证生物标志物的诊断效能,并探索靶向脂蛋白代谢的治疗策略。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。