Transient activation of YAP/TAZ confers resistance to morusin-induced apoptosis
YAP/TAZ的瞬时激活赋予细胞对莫鲁辛诱导的细胞凋亡的抵抗力
| 期刊: | BMC Molecular and Cell Biology | 影响因子: | 2.400 |
| 时间: | 2025 | 起止号: | 2025 Jan 20;26(1):4. |
| doi: | 10.1186/s12860-025-00531-1 | 靶点: | YAP、TAZ |
| 研究方向: | 细胞生物学、表观遗传 | ||
文献解析
1. 领域背景与文献
文献英文标题:Morusin induces transient YAP activation to confer resistance to apoptosis in cancer cells;发表期刊:BMC Cancer;影响因子:4.6(2023年);研究领域:肿瘤学、天然产物抗肿瘤机制、Hippo信号通路研究。
Hippo信号通路是进化保守的细胞调控通路,核心通过MST1/2-LATS1/2激酶级联调控效应分子YAP/TAZ的活性,当通路激活时,LATS1/2磷酸化YAP/TAZ使其滞留胞质并降解,抑制细胞增殖、促进凋亡;当通路异常失活时,YAP/TAZ入核激活靶基因表达,促进细胞增殖、存活,与多种肿瘤的发生发展密切相关。领域发展关键节点:1995年在果蝇中首次发现Hippo通路核心组分,2003年明确其在哺乳动物中的同源调控机制,近年来YAP/TAZ的非经典调控通路及在肿瘤免疫微环境中的作用成为研究热点。当前研究热点方向包括YAP/TAZ的翻译后修饰调控、非经典通路对其活性的影响、YAP/TAZ抑制剂的开发及临床应用、天然产物对Hippo通路的调控作用等。未解决的核心问题:天然产物抗肿瘤过程中肿瘤细胞的逃逸机制尚未完全阐明,尤其是YAP/TAZ在其中的具体调控网络及非经典通路的参与。
桑皮素是从桑树中提取的天然黄酮类化合物,已被证明通过抑制STAT3、调控PI3K/Akt、JNK、ERK等通路诱导多种肿瘤细胞凋亡,但肿瘤细胞可通过自噬、应激颗粒形成抵抗其诱导的凋亡。针对这一研究空白,本文聚焦Hippo通路YAP/TAZ在桑皮素诱导的凋亡抵抗中的作用,解析其调控机制,为提升桑皮素的抗肿瘤疗效提供新的策略,具有重要的学术价值与临床转化潜力。
2. 文献综述解析
作者从Hippo通路的核心调控机制、YAP/TAZ在肿瘤中的功能、桑皮素的抗肿瘤作用及研究局限性三个维度系统梳理了领域内现有研究,明确了本文的研究切入点与创新方向。
现有研究已阐明Hippo通路的经典调控机制,即MST1/2激活LATS1/2,磷酸化YAP/TAZ使其滞留胞质降解,而YAP/TAZ的异常激活可通过促进细胞增殖、诱导免疫抑制微环境、增强肿瘤转移能力等参与多种肿瘤的进展;桑皮素作为天然抗肿瘤化合物,已被证明可通过抑制STAT3信号通路、调控PI3K/Akt、JNK、ERK等多条通路诱导前列腺癌、肾癌、卵巢癌等多种肿瘤细胞凋亡,但同时肿瘤细胞可通过自噬、应激颗粒形成等机制抵抗桑皮素诱导的凋亡,降低其抗肿瘤疗效。现有研究的技术方法优势在于已明确桑皮素的多条作用通路及Hippo通路的核心调控网络,为后续机制研究奠定了基础;但局限性在于缺乏对桑皮素诱导肿瘤细胞凋亡抵抗的具体机制研究,尤其是YAP/TAZ在其中的调控作用及非经典Hippo通路的参与情况尚未明确。
通过对比现有研究的未解决问题,本文首次发现桑皮素通过非经典Hippo通路诱导YAP瞬时激活,介导应激颗粒形成从而产生凋亡抵抗;进一步解析了LATS1/2、MINK1、MAPK通路在YAP瞬时激活及失活过程中的调控作用,明确了YAP/TAZ在桑皮素诱导的凋亡抵抗中的核心功能,为桑皮素联合YAP/TAZ抑制剂提升抗肿瘤疗效提供了理论依据,填补了天然产物抗肿瘤逃逸机制研究的空白。
3. 研究思路总结与详细解析
本研究以“桑皮素诱导YAP瞬时激活介导肿瘤细胞凋亡抵抗”为核心科学问题,采用“假设-实验验证-机制解析-功能验证”的闭环技术路线,通过细胞模型、分子生物学实验、功能学检测等多种方法,系统解析了YAP/TAZ在桑皮素诱导的凋亡抵抗中的作用及调控机制,研究逻辑严谨、证据充分。
3.1 桑皮素诱导YAP激活的验证
实验目的:明确桑皮素是否能诱导YAP激活及激活的时间、剂量效应特征,为后续机制研究奠定基础。方法细节:选取A549、HepG2、HEK293A、HCT116、HeLa等多种肿瘤细胞系,分别用不同浓度的桑皮素处理3小时,或用30μM桑皮素处理0-24小时,通过免疫印迹(Western Blot)技术检测YAP在S127位点的磷酸化水平,qPCR检测YAP下游靶基因CTGF、CYR61的mRNA表达水平,免疫荧光染色及核质分离技术检测YAP的亚细胞定位。结果解读:免疫印迹结果显示,桑皮素以剂量依赖方式诱导YAP S127去磷酸化(n=3,P<0.01),处理3小时时去磷酸化水平达到峰值,随后逐渐恢复磷酸化状态;qPCR结果显示,CTGF、CYR61的mRNA水平在处理1-3小时显著升高(n=3,P<0.001),随后逐渐下降;免疫荧光及核质分离结果显示,YAP在桑皮素处理后迅速入核,3小时时核定位比例最高(n=3,P<0.001),随后逐渐回到胞质。以上结果表明桑皮素可诱导YAP瞬时激活,表现为去磷酸化、核定位及转录活性升高,且该激活过程具有时间和剂量依赖性。

产品关联:实验所用关键产品:Cell Signaling Technology的抗磷酸化YAP(13008)、抗YAP(17074)抗体,BD Biosciences的抗G3BP(611126)抗体,Chengdu Biopurify的桑皮素(BP0961),Bio-Rad的iQ™ SYBR Green Supermix,Zeiss LSM 700共聚焦显微镜等。
3.2 YAP激活的调控机制解析
实验目的:明确桑皮素诱导YAP激活是否依赖经典Hippo通路,及参与YAP激活与失活的调控激酶。方法细节:用30μM桑皮素处理HCT116细胞不同时间,通过免疫印迹检测经典Hippo通路上游分子MST1/2、MOB1、SAV1的磷酸化水平;通过siRNA敲低HCT116细胞的LATS1/2,检测桑皮素处理后YAP的磷酸化恢复情况;构建过表达野生型及组成型激活型(T187E)HA-MINK1的HCT116细胞系,检测桑皮素处理后YAP的磷酸化变化;用MEK1抑制剂PD98059预处理HCT116细胞,检测桑皮素处理后YAP的磷酸化及核定位情况。结果解读:免疫印迹结果显示,桑皮素处理不影响经典Hippo通路上游分子MST1/2、MOB1、SAV1的磷酸化水平,说明YAP激活不依赖经典Hippo通路;敲低LATS1/2后,桑皮素诱导的YAP再磷酸化过程被抑制,说明LATS1/2参与YAP的失活过程;过表达组成型激活型MINK1可延长YAP的激活时间,抑制其再磷酸化;MEK1抑制剂处理也可抑制YAP的再磷酸化,且过表达组成型激活型MINK1可降低ERK的磷酸化水平,说明MINK1、MAPK通路参与YAP的失活调控。以上结果表明桑皮素通过非经典Hippo通路诱导YAP瞬时激活,LATS1/2、MINK1、MAPK通路共同调控YAP的激活与失活过程。
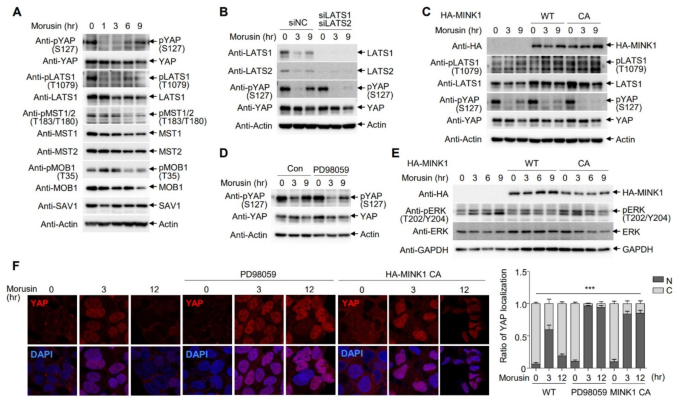
产品关联:实验所用关键产品:iNtRON Biotechnology的Muta-Direct™定点突变试剂盒、Maxime™ RT-PCR PreMix,Invitrogen的Lipofectamine 3000转染试剂、Lipofectamine™ RNAiMAX转染试剂,Roche的HA-HRP抗体(12013819001),GeneTex的抗TAZ(GTX134857)抗体等。
3.3 YAP/TAZ对桑皮素诱导应激颗粒形成的影响
实验目的:明确YAP/TAZ是否参与桑皮素诱导的应激颗粒形成,解析其在凋亡抵抗中的间接作用途径。方法细节:通过siRNA敲低A549、HCT116细胞的YAP/TAZ,用30μM桑皮素处理0-9小时,通过免疫荧光染色检测应激颗粒标记蛋白G3BP1的点状结构,统计形成应激颗粒的细胞比例。结果解读:免疫荧光结果显示,敲低YAP/TAZ后,桑皮素诱导的G3BP1点状结构显著减少,各时间点形成应激颗粒的细胞比例降低约70%(n=3,P<0.001),说明YAP/TAZ是桑皮素诱导应激颗粒形成的关键调控因子,应激颗粒的形成依赖于YAP/TAZ的激活。
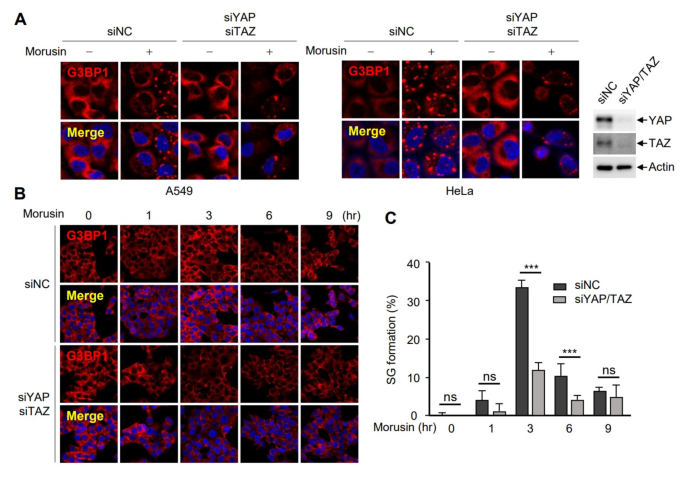
产品关联:实验所用关键产品:Santa Cruz Biotechnology的抗YAP(sc-101199)抗体,MyBioSource的抗LATS2(MBS7600942)抗体,Bethyl Laboratories的抗actin(A700-057)、抗GAPDH(A700-103)抗体等。
3.4 YAP/TAZ介导桑皮素诱导的凋亡抵抗验证
实验目的:明确YAP/TAZ是否直接介导桑皮素诱导的肿瘤细胞凋亡抵抗,验证其功能作用。方法细节:通过siRNA敲低HEK293A、HeLa细胞的YAP/TAZ,用不同浓度桑皮素处理6小时或用50μM桑皮素处理不同时间,通过免疫印迹检测凋亡标志物PARP、caspase-3的切割水平及抗凋亡蛋白Bcl-2、Bcl-xL的表达水平;在过表达组成型激活型MINK1的HCT116细胞中检测桑皮素处理后凋亡标志物的变化;用MTT法检测敲低YAP/TAZ或过表达组成型激活型MINK1后细胞的活力变化。结果解读:免疫印迹结果显示,敲低YAP/TAZ后,桑皮素处理的细胞中PARP、caspase-3的切割水平显著升高(n=3,P<0.01),Bcl-2、Bcl-xL的表达水平降低,说明凋亡被显著促进;过表达组成型激活型MINK1的细胞中,PARP、caspase-3的切割水平降低,且敲低YAP/TAZ可逆转MINK1的抗凋亡作用;MTT结果显示,敲低YAP/TAZ后细胞活力显著降低(n=3,P<0.001),过表达组成型激活型MINK1后细胞活力显著升高(n=3,P<0.001)。以上结果表明YAP/TAZ是桑皮素诱导的肿瘤细胞凋亡抵抗的核心调控因子,其激活可通过介导应激颗粒形成及上调抗凋亡蛋白表达抑制凋亡。
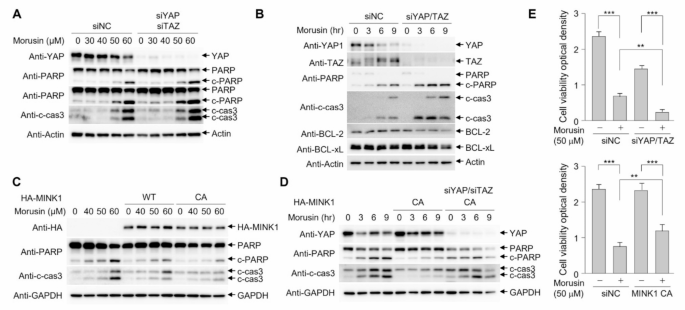
产品关联:实验所用关键产品:Roche的Cell Viability Assay Kit(11465007001),Merck Millipore的抗tubulin(05-829)抗体,Cell Signaling Technology的抗PARP(9542)、抗cleaved-caspase3(9661)抗体等。
4. Biomarker研究及发现成果
本文将YAP/TAZ鉴定为桑皮素诱导肿瘤细胞凋亡抵抗的功能Biomarker,系统解析了其筛选、验证过程及功能价值,为桑皮素的临床应用提供了新的靶点与策略。
YAP/TAZ属于转录共激活因子类Biomarker,其筛选逻辑为:首先通过检测桑皮素处理后YAP的激活特征(去磷酸化、核定位、转录活性升高)初步确定其参与桑皮素诱导的细胞应答,然后通过敲低和过表达实验验证其在应激颗粒形成、凋亡抵抗中的核心功能,最后解析其调控机制明确其作用网络。验证逻辑遵循“分子水平检测→细胞功能验证→机制解析”的完整链条,确保了Biomarker的可靠性。
Biomarker来源为肿瘤细胞内的内源性蛋白,验证方法包括免疫印迹检测YAP的磷酸化水平及凋亡标志物的表达、qPCR检测YAP下游靶基因的表达、免疫荧光检测YAP的亚细胞定位及应激颗粒形成、MTT检测细胞活力等。特异性与敏感性:敲低YAP/TAZ可使桑皮素诱导的肿瘤细胞凋亡率显著升高,过表达组成型激活型MINK1延长YAP激活时间可使凋亡率显著降低(n=3,P<0.001),说明YAP/TAZ对桑皮素诱导的凋亡具有高度的调控特异性与敏感性。
YAP/TAZ是桑皮素诱导肿瘤细胞凋亡抵抗的关键功能Biomarker,其瞬时激活可通过介导应激颗粒形成及上调抗凋亡蛋白表达抑制桑皮素诱导的凋亡;本文首次发现桑皮素通过非经典Hippo通路诱导YAP瞬时激活,解析了LATS1/2、MINK1、MAPK通路在其中的调控作用,创新性地阐明了YAP/TAZ介导天然产物抗肿瘤逃逸的具体机制。该Biomarker的功能关联明确,即作为桑皮素诱导凋亡抵抗的核心调控因子,其活性状态直接影响桑皮素的抗肿瘤疗效;统计学结果显示所有实验均重复3次,差异具有统计学意义(P<0.05、P<0.01或P<0.001)。此外,本文提出桑皮素联合YAP/TAZ抑制剂的治疗策略,为提升天然产物的抗肿瘤疗效提供了新的方向,具有重要的临床转化潜力。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。