Using RNA-seq to identify suitable housekeeping genes for hypoxia studies in human adipose-derived stem cells
使用 RNA-seq 识别适合人类脂肪干细胞缺氧研究的管家基因
| 期刊: | BMC Molecular and Cell Biology | 影响因子: | 2.400 |
| 时间: | 2023 | 起止号: | 2023 Apr 17;24(1):16. |
| doi: | 10.1186/s12860-023-00475-4 | 研究方向: | 发育与干细胞 |
| 细胞类型: | 干细胞 | ||
文献解析
1. 领域背景与文献
文献英文标题:Identification of stable housekeeping genes for hypoxia studies in human adipose-derived stem cells;发表期刊:BMC Molecular and Cell Biology;影响因子:4.606(2022年);研究领域:干细胞生物学与缺氧调控
内参基因(管家基因)是基因表达定量分析的核心参考,需在不同实验条件下维持稳定表达,才能准确反映靶基因的表达变化。缺氧模型作为模拟缺血性疾病、肿瘤微环境等生理病理状态的重要工具,被广泛应用于生命科学研究,但部分经典内参基因如GAPDH、PGK1的启动子区域含有缺氧反应元件(HRE),会受缺氧诱导因子-1(HIF-1)通路调控,导致表达稳定性下降,进而影响定量结果的准确性。目前针对人脂肪来源干细胞(hADSC)缺氧研究的稳定内参基因仍存在争议,不同研究的结论不一致,缺乏统一的方法学标准,这是该领域亟待解决的核心问题。本研究旨在通过RNA测序高通量筛选结合qRT-PCR多算法验证,系统鉴定hADSC在缺氧条件下的稳定内参基因,填补该细胞模型方法学的空白,为后续hADSC缺氧相关研究提供可靠的定量基础。
2. 文献综述解析
作者对领域内现有研究的分类维度主要围绕“内参基因稳定性验证方法”和“不同细胞/实验条件下的内参基因适用性”展开。现有研究中,经典内参基因如GAPDH、ACTB等在常规培养条件下应用广泛,但其表达稳定性依赖于细胞的基础代谢状态,在缺氧环境中因受HIF-1通路的直接或间接调控,表达水平会发生显著变化,无法满足定量分析的要求;部分研究提出RPL13A、TBP等基因可作为缺氧研究的内参,但这些结论多基于肿瘤细胞或其他干细胞模型,在hADSC中的验证数据较为匮乏。从技术方法来看,qRT-PCR结合GeNorm、NormFinder等算法是目前内参基因稳定性验证的金标准,但传统筛选方法存在候选基因范围窄、样本量小的局限性,且缺乏针对hADSC缺氧模型的系统筛选流程。本研究的创新点在于首次整合RNA测序高通量技术和多算法验证体系,对78个文献报道的候选内参基因进行全面评估,精准锁定hADSC缺氧条件下的稳定内参基因,不仅解决了该细胞模型的方法学瓶颈,也为其他干细胞缺氧研究的内参筛选提供了可借鉴的技术范式。
3. 研究思路总结与详细解析
本研究的整体框架为:以“筛选hADSC缺氧条件下的稳定内参基因”为核心目标,围绕“哪些内参基因在hADSC缺氧环境中不受调控、表达稳定”这一科学问题,构建“文献筛选候选内参→RNA测序高通量分析表达稳定性→qRT-PCR验证→多算法评估稳定性→靶基因验证内参可靠性”的完整研究闭环,确保结果的科学性和可靠性。
3.1 细胞模型构建与RNA样本制备
实验目的:构建hADSC常氧与缺氧培养模型,提取高质量RNA用于后续转录组测序和qRT-PCR验证。
方法细节:选取5例不同供体的hADSC(传代5-8代),培养至80%-90%汇合度后,分别置于常氧(37℃、5% CO₂、21% O₂)和缺氧(37℃、15% CO₂、<0.1% O₂)条件下培养48h;采用RNeasy Plus Micro试剂盒提取总RNA,通过2100 Bioanalyzer检测RNA完整性(RNA Integrity Number, RIN≥8.0)和纯度(A260/280比值为1.8-2.0),确保样本符合测序和qRT-PCR要求。
结果解读:成功获得10份(5例供体×2种条件)高质量RNA样本,所有样本的RIN值和纯度均达到实验标准,为后续转录组分析和基因定量提供了可靠的材料基础。
产品关联:实验所用关键产品:Lonza/ZenBio的人脂肪来源干细胞系、Gibco的Dulbecco改良 Eagle培养基、Qiagen的RNeasy Plus Micro试剂盒、Agilent的2100 Bioanalyzer。
3.2 RNA测序与高通量候选基因筛选
实验目的:通过转录组测序分析,从78个文献候选内参基因中筛选出缺氧条件下表达稳定的基因。
方法细节:采用Illumina TruSeq® Stranded mRNA试剂盒构建测序文库,分别使用HiSeq 2500和NovaSeq 2500平台进行单端测序;利用FastQC和Trimmomatic进行数据质控和修剪,通过HISAT2将reads比对至人类参考基因组(GrCh38),使用featureCounts进行基因计数;通过DESeq2分析常氧与缺氧组的差异表达,计算每个候选内参基因的变异系数(Coefficient of Variation, CV)和对数二倍变化(Log 2 Fold Change, L2FC),筛选CV≤0.15且L2FC接近0的基因。
结果解读:转录组分析共鉴定出2800个差异表达转录本,主成分分析(PCA)显示常氧与缺氧组的转录组特征存在显著差异;78个候选内参基因中,15个基因的CV≤0.15,进一步结合L2FC筛选出8个表达变异最小的基因,其中ALAS1、RRP1、GUSB、POLR2B为排名前4的候选基因。
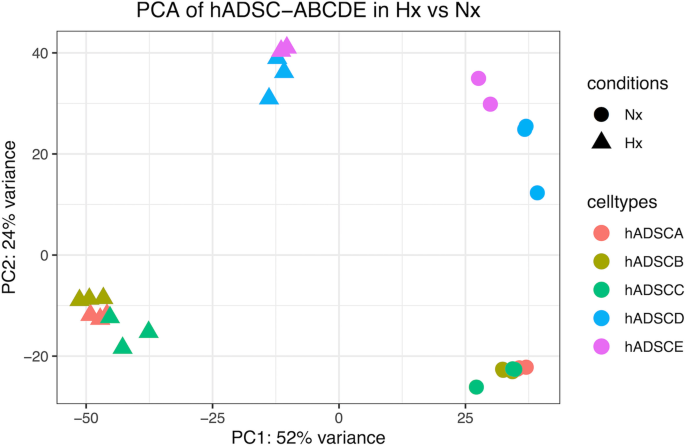
产品关联:实验所用关键产品:Illumina的TruSeq® Stranded mRNA试剂盒、HiSeq 2500/NovaSeq 2500测序平台、DESeq2生物信息学分析软件。
3.3 qRT-PCR验证与内参稳定性评估
实验目的:验证候选内参基因在hADSC中的表达稳定性,排除低表达或不稳定的基因。
方法细节:选取排名前4的候选基因(ALAS1、RRP1、GUSB、POLR2B)及经典内参基因18S、PGK1,采用TaqMan探针法进行qRT-PCR;利用GeNorm(几何平均法)、NormFinder(模型方差估计法)、BestKeeper(两两相关法)、ΔCt法及RefFinder(加权排名几何平均法)多算法分析Ct值的稳定性,评估每个候选基因的表达稳定性。
结果解读:POLR2B在部分hADSC中未检测到表达,GUSB在多数hADSC中的Ct值过高(表达量极低),均不适合作为内参基因;18S和RRP1的表达稳定性在所有算法中排名前两位,其中18S的Ct值约为20(高表达水平),RRP1的Ct值约为30(中低表达水平),可覆盖不同表达丰度的靶基因定量需求。
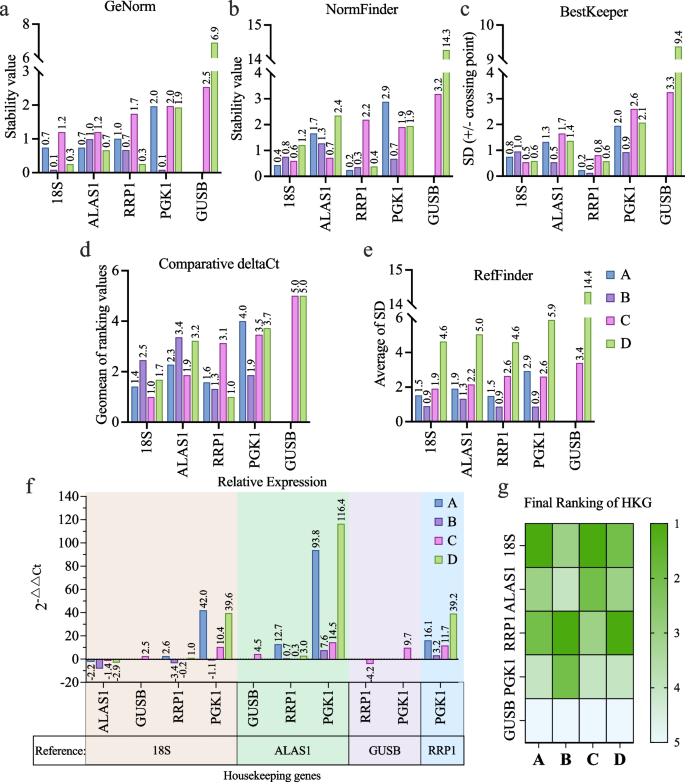
产品关联:实验所用关键产品:Qiagen的RT² Omniscript反转录试剂盒、Thermo Fisher的TaqMan Assay探针、Bio-Rad的CFX Real-Time PCR检测系统、RefFinder在线分析工具。
3.4 靶基因验证内参可靠性
实验目的:验证筛选出的内参基因在靶基因定量分析中的准确性和可靠性。
方法细节:选取已知的缺氧响应基因VEGFA作为靶基因,分别以18S、RRP1及两者的几何均值作为内参,计算缺氧组相对常氧组的VEGFA表达倍数,评估不同内参对定量结果的影响。
结果解读:VEGFA在缺氧组中显著上调,以18S为内参时上调6.8±1.4倍,以RRP1为内参时上调12±0.6倍,两者联合使用(几何均值)时上调9.5±1.0倍,结果稳定且符合缺氧调控的生物学规律,证明18S和RRP1作为内参基因的可靠性。
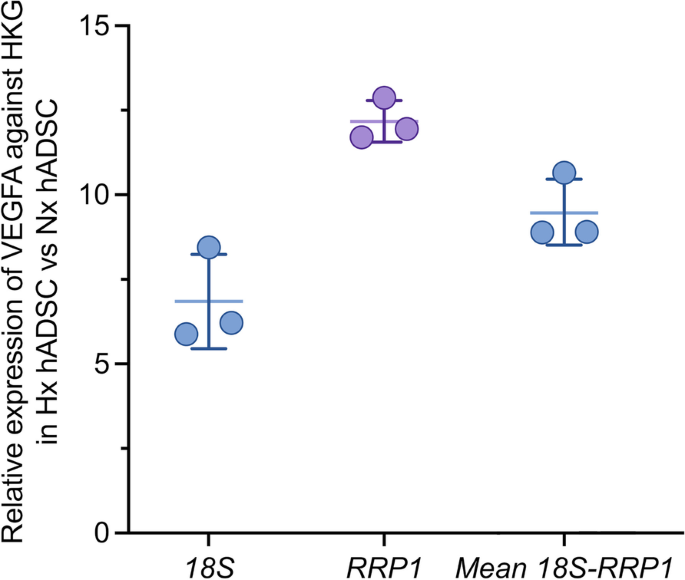
产品关联:文献未提及具体实验产品,领域常规使用qRT-PCR相关的反转录酶、荧光探针及实时定量PCR仪。
4. Biomarker研究及发现成果
本研究筛选的Biomarker为18S核糖体RNA和RRP1基因,属于“表达稳定型参考Biomarker”,其筛选逻辑为“文献候选基因库构建→RNA测序高通量筛选→qRT-PCR验证→多算法稳定性评估→靶基因功能验证”的完整链条,确保Biomarker的可靠性和适用性。
Biomarker定位:18S是核糖体小亚基的核心组成部分,参与蛋白质翻译的基础过程,其表达量与细胞的核糖体数量正相关,理论上不受缺氧等环境因素的调控;RRP1编码核糖体RNA加工蛋白1,主要参与核仁发生后期的调控,是细胞基础生命活动必需的基因。两者的筛选过程严格遵循“低变异系数、无显著差异表达”的标准,确保在hADSC常氧与缺氧条件下的表达稳定性。
研究过程详述:Biomarker的来源为hADSC的总RNA样本,验证方法为qRT-PCR结合多算法分析;18S和RRP1在5例hADSC的常氧与缺氧组中,变异系数均≤0.15,对数二倍变化接近0,表达稳定性显著高于GAPDH、PGK1等经典内参基因;RefFinder综合排名显示,18S和RRP1的稳定性评分分别为1.0和1.2(评分越接近1越稳定),远高于其他候选基因。
核心成果提炼:18S和RRP1可单独或联合作为hADSC缺氧研究的内参基因,联合使用时(采用几何均值)能更准确地平衡不同表达丰度靶基因的定量误差;首次明确GAPDH、PGK1等经典内参基因因受缺氧调控,不适合用于hADSC缺氧研究;该成果为hADSC缺氧相关的基因表达定量提供了标准化方法,同时也为其他干细胞缺氧研究的内参筛选提供了技术参考。本研究未针对内参基因的临床应用数据进行报道,后续可进一步探索其在hADSC临床转化研究中的价值。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。