Regulation of the Fasciola hepatica newly excysted juvenile cathepsin L3 (FhCL3) by its propeptide: a proposed 'clamp-like' mechanism of binding and inhibition
肝片吸虫新脱囊幼年组织蛋白酶 L3 (FhCL3) 的前肽调控:一种拟定的“钳状”结合和抑制机制
| 期刊: | BMC Molecular and Cell Biology | 影响因子: | 2.400 |
| 时间: | 2020 | 起止号: | 2020 Dec 7;21(1):90. |
| doi: | 10.1186/s12860-020-00335-5 | 研究方向: | 信号转导 |
文献解析
1. 领域背景与文献引入
文献英文标题:Regulation of the Fasciola hepatica newly excysted juvenile cathepsin L3 (FhCL3) by its propeptide: a proposed ‘clamp-like’ mechanism of binding and inhibition;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:寄生虫学(肝片吸虫致病机制)、分子酶学(半胱氨酸蛋白酶调控)
肝片吸虫是全球分布最广的人兽共患吸虫之一,可感染多种哺乳动物并引发肝片吸虫病,给畜牧业生产和公共卫生安全带来严重负担。领域共识:肝片吸虫的致病能力高度依赖其分泌的半胱氨酸蛋白酶家族(如组织蛋白酶L家族),这些酶以无活性的酶原形式合成,需通过前肽的自催化切割激活后发挥组织降解功能。目前领域内已明确肝片吸虫不同发育阶段分泌不同亚型的组织蛋白酶L,新脱囊幼虫(NEJs)阶段主要分泌FhCL3,该酶可高效降解宿主I型和II型胶原,是幼虫穿透肠壁、完成宿主入侵的核心效应分子。但现有研究仅关注单一酶的激活过程,未系统分析FhCL3前肽的特异性调控机制,缺乏对前肽与成熟酶分子互作关键残基的验证,无法为基于前肽的抗寄生虫药物设计提供精准靶点,因此本研究聚焦FhCL3前肽的抑制机制,具有重要的学术价值和应用潜力。
2. 文献综述解析
本文综述部分以“寄生虫半胱氨酸蛋白酶的激活调控”为核心逻辑,按酶的功能亚型、发育阶段表达模式、前肽调控机制三个维度对现有研究进行分类评述。
现有研究已证实肝片吸虫不同发育阶段分泌不同亚型的组织蛋白酶L,成虫阶段主要分泌FhCL1、FhCL2,幼虫阶段以FhCL3为主,这些酶均以酶原形式存在,前肽作为天然抑制剂可防止酶的过早激活,同时发挥分子伴侣作用辅助成熟酶的正确折叠。技术方法上,重组表达和结构生物学技术已用于解析FhCL1的酶原结构,但现有研究的局限性在于仅关注单一酶的激活过程,未系统分析FhCL3前肽的特异性抑制能力,且缺乏对前肽与成熟酶分子互作关键残基的功能验证,无法明确其调控的分子机制。
本研究通过重组表达FhCL3前肽,首次系统检测其对不同亚型组织蛋白酶L及人源组织蛋白酶的抑制特异性,结合结构建模和突变体验证,明确了“钳式”结合的抑制机制,填补了FhCL3前肽调控机制的研究空白,为基于前肽的抗寄生虫药物设计提供了分子基础。
3. 研究思路总结与详细解析
本文的研究目标是明确FhCL3前肽对成熟酶的特异性调控机制,核心科学问题是FhCL3前肽如何通过分子互作实现对成熟酶的高效抑制,技术路线遵循“重组表达→定位分析→活性检测→结构预测→突变验证→结论”的闭环逻辑,通过多层面实验验证前肽的抑制机制。
3.1 重组FhCL3酶原与前肽的表达及功能验证
实验目的:获得具有自激活活性的FhCL3酶原和具有抑制活性的重组前肽(ppFhCL3),为后续实验提供基础工具。方法细节:采用毕赤酵母表达系统重组表达FhCL3酶原,通过亲和层析纯化后,在pH4.5的醋酸钠缓冲液中37℃孵育5h,观察自激活过程;采用大肠杆菌BL21表达系统重组表达ppFhCL3,通过亲和层析纯化并验证纯度。结果解读:SDS-PAGE结果显示,FhCL3酶原(37kDa)在孵育过程中逐步切割为25kDa的成熟酶和12kDa的前肽;重组ppFhCL3为可溶性蛋白,分子量约12kDa,Western blot验证其可与抗ppFhCL3多克隆抗体结合,且能识别NEJs体细胞提取物中的天然FhCL3酶原(n=3,P<0.01)。产品关联:文献未提及具体实验产品,领域常规使用毕赤酵母表达系统、大肠杆菌表达系统、亲和层析纯化柱、SDS-PAGE凝胶等试剂/仪器。
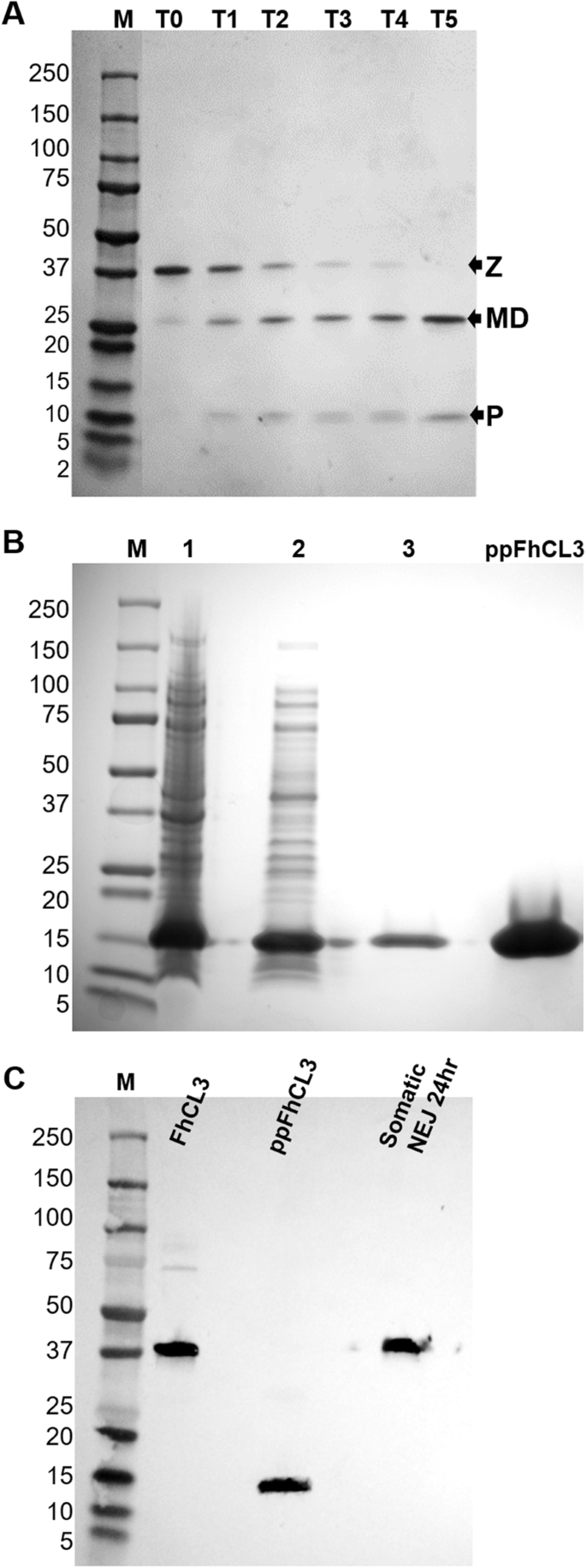
3.2 FhCL3酶原与前肽的免疫定位分析
实验目的:明确FhCL3酶原在NEJs中的合成与分泌部位。方法细节:制备抗FhCL3酶原和抗ppFhCL3的多克隆抗体,对6h和24h的NEJs进行免疫荧光染色,采用共聚焦激光扫描显微镜观察定位。结果解读:免疫荧光结果显示,FhCL3酶原和前肽均定位于NEJs的肠道胃皮细胞中,抗FhCL3酶原抗体的荧光信号强于抗ppFhCL3抗体,且24h NEJs中的前肽信号进一步减弱,提示酶原在肠道内激活并释放成熟酶(n=3,P<0.05)。产品关联:文献未提及具体实验产品,领域常规使用多克隆抗体、免疫荧光染色试剂盒、共聚焦显微镜等试剂/仪器。
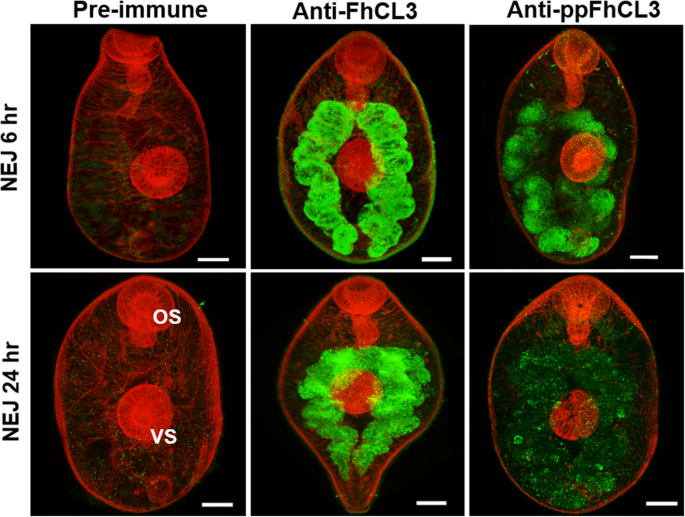
3.3 ppFhCL3的抑制活性与特异性检测
实验目的:检测ppFhCL3对不同亚型组织蛋白酶L及人源组织蛋白酶的抑制活性和pH依赖性。方法细节:在pH4.5-7.0的缓冲液中,将10nM ppFhCL3与重组FhCL1、FhCL2、FhCL3及人组织蛋白酶L(HsCL)、人组织蛋白酶K(HsCK)共孵育,检测酶活性变化;同时检测ppFhCL3对成虫排泄分泌产物(ES)中天然组织蛋白酶的抑制活性。结果解读:ppFhCL3对FhCL1、FhCL2、FhCL3的抑制活性在pH7.0时达到最高(接近100%),pH4.5时无抑制活性;对HsCL和HsCK的抑制活性显著降低,最适pH分别为6.5和5.5;ppFhCL3可完全抑制成虫ES产物中的组织蛋白酶活性,且能通过pull-down实验结合FhCL1、FhCL2、FhCL5;酶动力学检测显示,ppFhCL3对FhCL3的抑制常数(Ki)<0.002nM,对FhCL1、FhCL2的Ki分别为0.04nM、0.004nM,对HsCL、HsCK的Ki分别为26.6nM、2.0nM,显示出极强的寄生虫选择性(n=3,P<0.001)。产品关联:文献未提及具体实验产品,领域常规使用荧光底物、酶标仪、pull-down试剂盒等试剂/仪器。
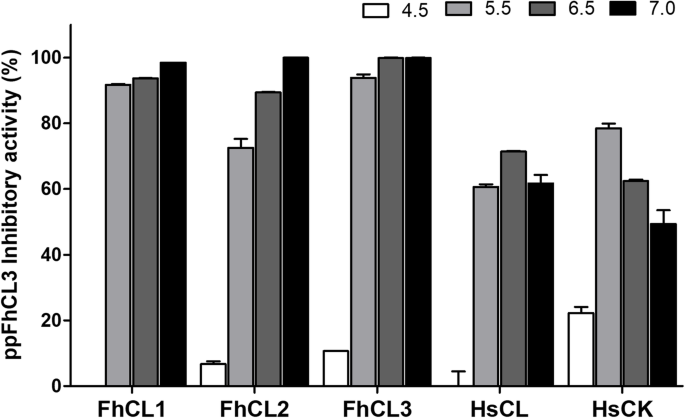
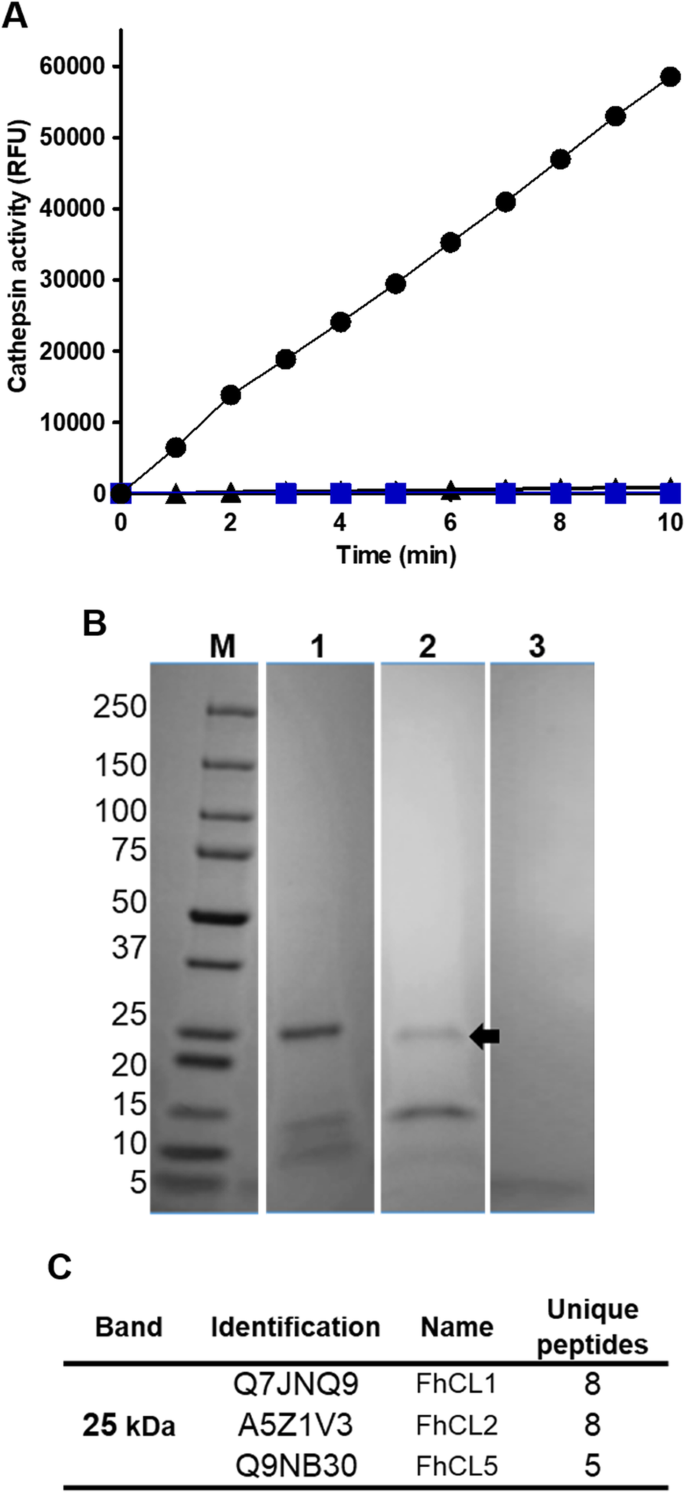
3.4 FhCL3前肽与成熟酶的分子互作结构建模
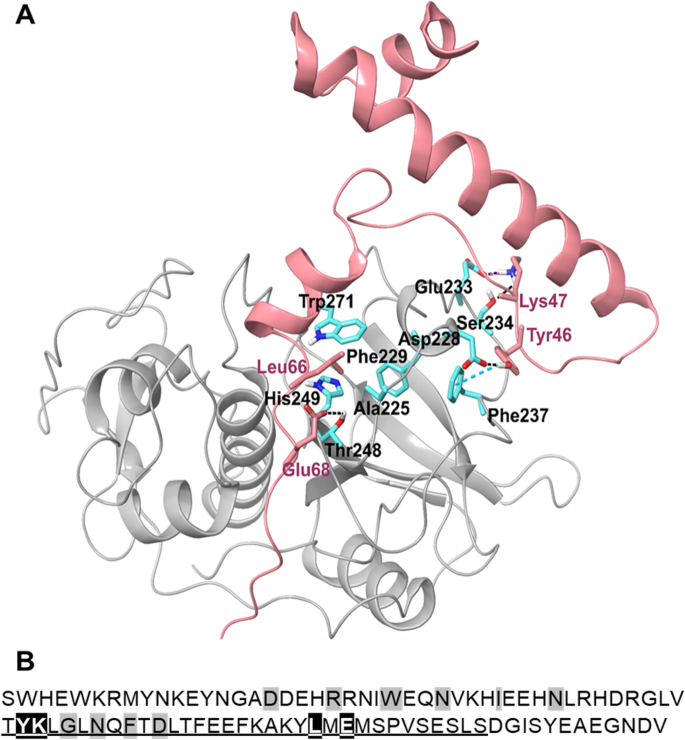
实验目的:预测ppFhCL3与FhCL3成熟酶的关键结合残基和互作模式。方法细节:以FhCL1酶原的晶体结构为模板,通过同源建模构建FhCL3酶原的三维结构,结合分子动力学模拟分析前肽与成熟酶的互作。结果解读:结构模型显示,ppFhCL3的Tyr46与成熟酶的Asp228形成氢键、与Phe237形成π-π相互作用,Lys47与Glu233形成盐桥、与Ser234形成氢键;同时ppFhCL3的Leu66嵌入成熟酶的疏水口袋,Glu68与Thr248形成氢键,这些残基共同构成“钳式”结合模式。产品关联:文献未提及具体实验产品,领域常规使用Schrodinger等结构生物学分析软件。
3.5 关键残基突变体的功能验证
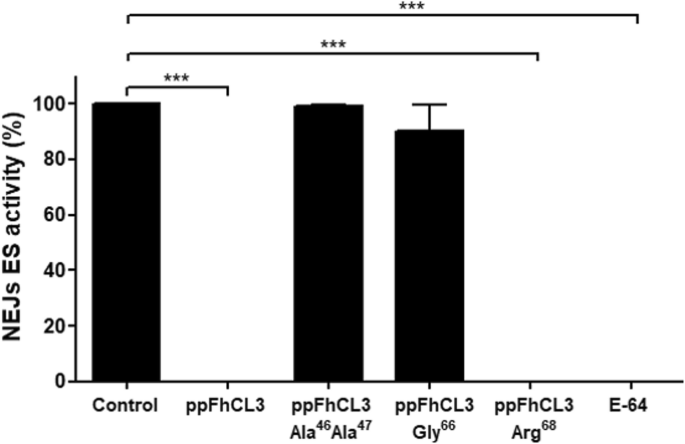
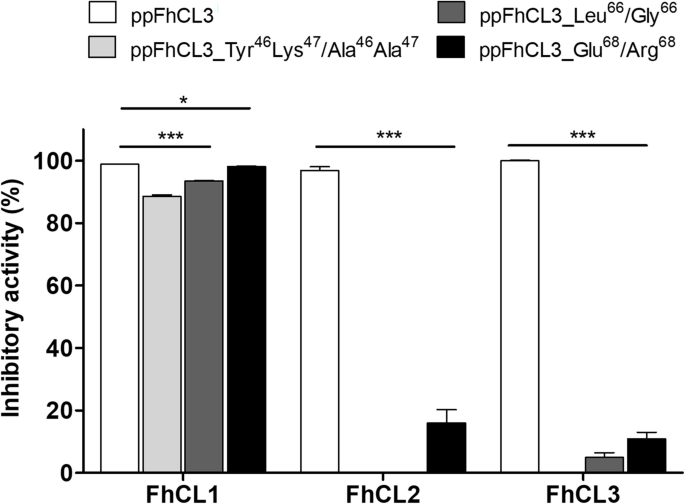
实验目的:验证ppFhCL3关键结合残基在抑制成熟酶中的作用。方法细节:构建三种ppFhCL3突变体:Tyr46Lys47→Ala46Ala47(双突变)、Leu66→Gly66、Glu68→Arg68,重组表达后检测其对组织蛋白酶及人源组织蛋白酶的抑制活性。结果解读:双突变体完全丧失对FhCL2、FhCL3的抑制活性,Ki>10000nM;Leu66→Gly66突变体对FhCL3的Ki为8nM,比野生型降低4000倍;Glu68→Arg68突变体对FhCL的抑制活性无显著变化,但对HsCL的抑制活性增强(n=3,P<0.001),证实Tyr46、Lys47、Leu66是维持抑制活性的关键残基。产品关联:文献未提及具体实验产品,领域常规使用定点突变试剂盒、重组表达系统等试剂/仪器。
3.6 基于ppFhCL3的短肽抑制剂设计与活性检测
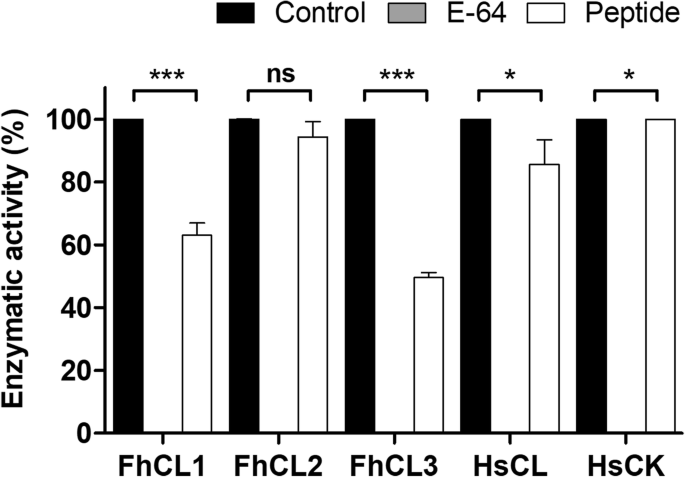
实验目的:探索基于ppFhCL3关键结合区域的短肽抑制剂的可行性。方法细节:合成包含Tyr46、Leu66等关键残基的33肽,检测其对组织蛋白酶及人源组织蛋白酶的抑制活性。结果解读:500nM的33肽仅能抑制约50%的FhCL3活性,对FhCL1的抑制率约30%,对其他酶无显著抑制作用(n=3,P>0.05),提示短肽无法模拟完整前肽的构象,需维持前肽的整体结构才能实现高效抑制。产品关联:文献未提及具体实验产品,领域常规使用多肽合成服务、酶活性检测试剂盒等试剂/仪器。
4. Biomarker研究及发现成果
本文中涉及的功能分子标志物为FhCL3前肽(ppFhCL3)及其关键结合残基,作为肝片吸虫入侵相关的调控分子,为抗寄生虫药物设计提供了潜在靶点。
Biomarker定位:ppFhCL3作为天然的FhCL3抑制剂,筛选逻辑基于FhCL3在幼虫入侵中的关键作用,通过重组表达、活性检测、结构建模及突变体验证,明确其关键结合残基(Tyr46、Lys47、Leu66),形成“重组表达→特异性验证→残基鉴定”的完整筛选链条。
研究过程详述:ppFhCL3来源于重组表达的FhCL3前肽,验证方法包括酶动力学检测(Ki值)、免疫定位、pull-down实验;特异性数据显示,ppFhCL3对FhCL3的Ki<0.002nM,比对人源组织蛋白酶的抑制活性高1000倍以上,具有极强的寄生虫选择性;敏感性数据显示,10nM的ppFhCL3即可完全抑制FhCL3的活性(n=3,P<0.001)。
核心成果提炼:ppFhCL3通过“钳式”机制结合FhCL3成熟酶,其中Tyr46/Lys47与成熟酶的前肽结合环(PBL)互作,Leu66/Glu68嵌入活性位点,共同实现高效抑制;该机制的创新性在于首次明确了FhCL3前肽的双位点结合模式,为基于前肽的抗寄生虫药物设计提供了分子模板;统计学结果显示,关键残基突变后抑制活性显著降低(P<0.001),证实了这些残基的功能重要性。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。