Novel hepatocyte growth factor (HGF) binding domains on fibronectin and vitronectin coordinate a distinct and amplified Met-integrin induced signalling pathway in endothelial cells
纤维连接蛋白和玻璃连接蛋白上的新型肝细胞生长因子 (HGF) 结合域协调内皮细胞中独特且扩增的 Met-整合素诱导信号通路
| 期刊: | BMC Cell Biology | 影响因子: | |
| 时间: | 2005 | 起止号: | 2005 Feb 17;6(1):8. |
| doi: | 10.1186/1471-2121-6-8 | 研究方向: | 免疫、细胞生物学 |
| 细胞类型: | 内皮细胞 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Novel hepatocyte growth factor (HGF) binding domains on fibronectin and vitronectin coordinate a distinct and amplified Met-integrin induced signalling pathway in endothelial cells;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:血管生物学/内皮细胞信号转导。
血管生成是成年机体血管修复与再生的关键过程,依赖内皮细胞从原有血管迁移、增殖及循环内皮祖细胞的招募分化,由生长因子(如VEGF、HGF)与细胞外基质(ECM)的协同信号调控。领域发展关键节点包括:1980s发现VEGF的促血管生成作用;1990s证实整合素与生长因子受体的协同信号;2000s揭示VEGF与纤连蛋白(FN)结合增强信号的机制。当前研究热点集中于生长因子-ECM复合物的形成及信号调控,但肝细胞生长因子(HGF)作为重要促血管生成因子,其与ECM的具体结合模式、体内存在形式及对Met(HGF受体)-整合素信号的调控机制尚未明确——这是领域未解决的核心问题。
本研究针对“HGF与ECM的相互作用及对内皮细胞信号与功能的影响”这一空白,旨在阐明HGF与FN、玻连蛋白(VN)的结合域、复合物的体内存在及对Met-整合素信号通路的调控机制。其学术价值在于首次揭示HGF-ECM复合物通过Ras依赖途径增强Met-整合素信号的新机制,为血管生成相关疾病(如心肌梗死、肿瘤 angiogenesis)的治疗提供潜在靶点。
2. 文献综述解析
文献综述以“生长因子-ECM相互作用的研究进展”为核心逻辑,按“经典生长因子(VEGF、PDGF)与ECM的协同作用→HGF的促血管生成作用及机制空白”的脉络展开评述。
现有研究的关键结论包括:① VEGF、PDGF等生长因子与ECM(如FN)结合可增强受体信号,促进内皮细胞迁移;② 整合素与生长因子受体(如VEGFR-2、PDGFR)的物理关联是信号协同的结构基础;③ HGF通过Met受体促进血管生成,但与ECM的相互作用及信号放大机制未明。技术方法的优势在于利用固相结合实验、表面等离子体共振(SPR)等技术解析分子相互作用,但局限性是缺乏对HGF与ECM具体结合域及体内复合物功能的研究。
本研究的创新价值在于:① 发现HGF与FN、VN的新结合域(FN的70kDa N端与40kDa C端片段);② 证实HGF-FN/VN复合物在体内(血小板上清)存在;③ 揭示复合物通过促进Met与整合素(α5β1、αvβ3)结合,激活Ras依赖的PI3K-Akt通路,增强内皮细胞迁移——填补了HGF促血管生成机制的关键空白。
3. 研究思路总结与详细解析
3.1 整体框架
研究目标:探究HGF与FN、VN的结合模式及对内皮细胞Met-整合素信号通路、迁移/增殖功能的调控。
核心科学问题:① HGF与ECM的结合域及体内存在形式;② HGF-ECM复合物如何调控Met-整合素信号;③ 信号通路与内皮细胞功能(迁移、增殖)的关联。
技术路线:体外分子互作实验→体内复合物验证→细胞功能分析→信号通路解析→整合素作用验证,形成“分子-细胞-体内”的闭环验证体系。
3.2 HGF与ECM结合域的鉴定
实验目的:明确HGF与哪些ECM分子结合及具体结合域位置。
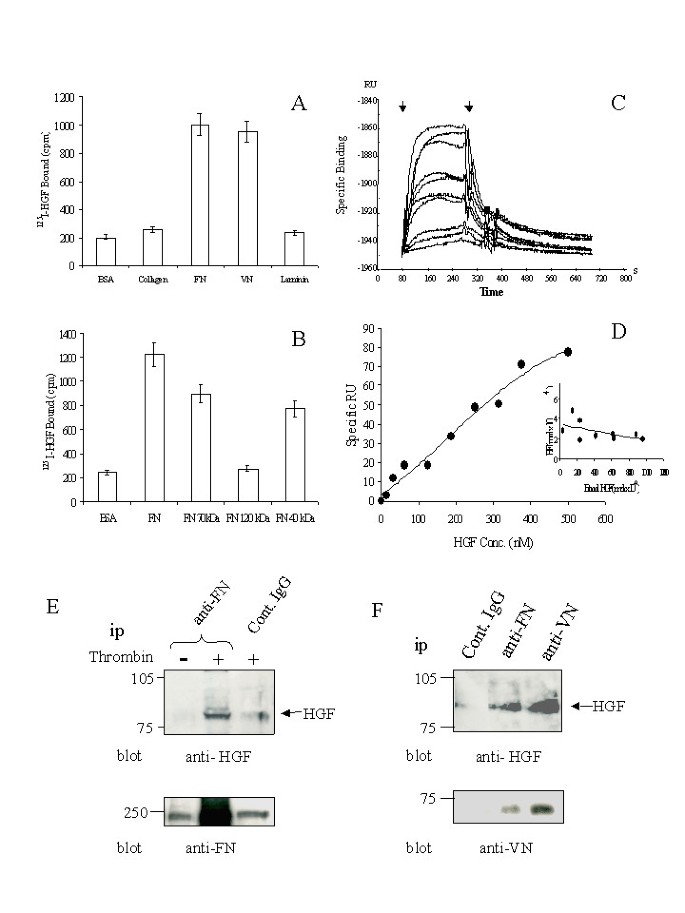
方法细节:① 固相放射性配体结合实验:将125I标记的HGF与固定在塑料孔的ECM(FN、VN、胶原-1、层粘连蛋白)孵育,检测结合水平;② FN蛋白酶解片段结合实验:用FN的70kDa N端、120kDa中间、40kDa C端片段替代完整FN,重复结合实验;③ SPR实时分析:将FN的70kDa片段固定在传感器芯片,注入不同浓度HGF,记录结合动力学。
结果解读:① HGF特异性结合FN和VN(结合水平显著高于胶原-1、层粘连蛋白);② FN的70kDa N端与40kDa C端是HGF结合域(120kDa片段无结合);③ SPR显示HGF与70kDa片段的平衡解离常数(Kd)约为300nM(单位点模型),或15nM(高亲和力)与4μM(低亲和力)的两位点模型。
产品关联:实验所用关键试剂包括Sigma的ECM蛋白、Gibco的FN蛋白酶解片段、PerkinElmer的125I标记HGF。
3.3 体内HGF-ECM复合物的验证
实验目的:证实HGF-FN/VN复合物在体内的存在。
方法细节:用凝血酶刺激血小板(促脱颗粒),收集上清后用抗FN、抗VN抗体免疫沉淀,通过Western blot检测沉淀复合物中的HGF。
结果解读:凝血酶刺激的血小板上清中,抗FN或抗VN抗体可沉淀出HGF(未刺激组或对照IgG组无明显信号),证实体内存在HGF-FN/VN复合物。
产品关联:实验所用关键试剂包括Santa Cruz的HGF抗体、Chemicon的FN/VN抗体。

(图1E、F)
3.4 HGF-ECM复合物对内皮细胞迁移的调控
实验目的:探究HGF-ECM复合物对内皮细胞迁移的影响及整合素的作用。
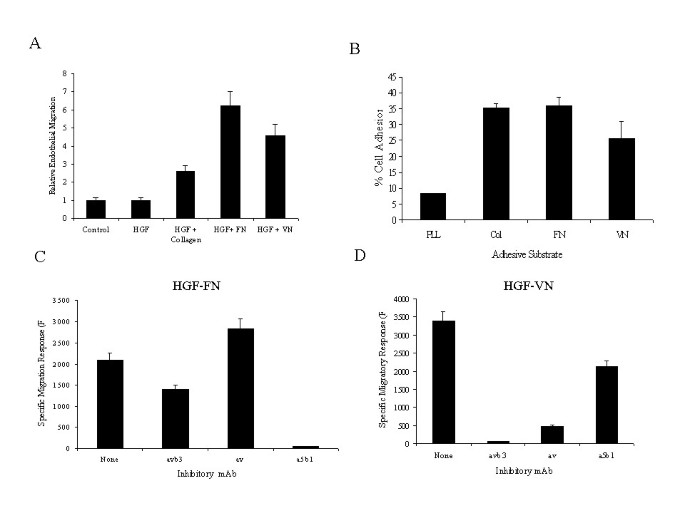
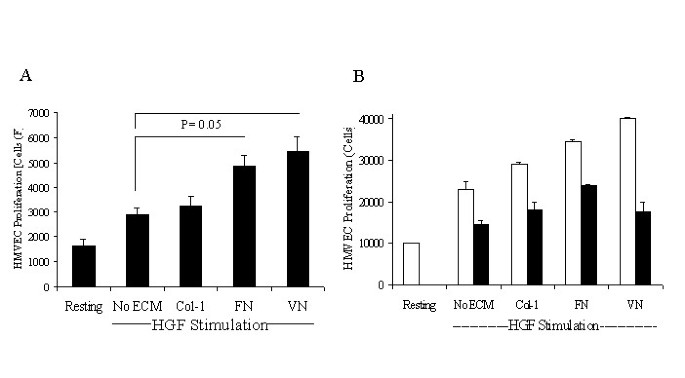
方法细节:① 迁移实验:用Calcein AM标记的人皮肤微血管内皮细胞(HMVEC),在FN/VN/胶原-1包被的Transwell小室中,用HGF单独或与ECM共刺激,检测3小时后的迁移水平;② 整合素阻断实验:用抗α5β1(JBS5)、抗αvβ3(LM609)抗体预处理细胞,重复迁移实验。
结果解读:① HGF单独无明显迁移(与基础水平无差异);与FN/VN共刺激时,迁移水平较基础提高4-5倍(显著高于HGF+胶原-1组的2倍);② 抗α5β1抗体完全阻断HGF-FN诱导的迁移,抗αvβ3抗体显著抑制HGF-VN诱导的迁移——证实整合素α5β1、αvβ3分别介导HGF-FN、HGF-VN的迁移信号。
产品关联:实验所用关键试剂包括BD Bioscience的Fluorblok Transwell小室、Clonetics的HMVEC细胞系。
3.5 Met-整合素的物理关联及信号通路激活
实验目的:解析HGF-ECM复合物对Met-整合素结合及下游信号的影响。
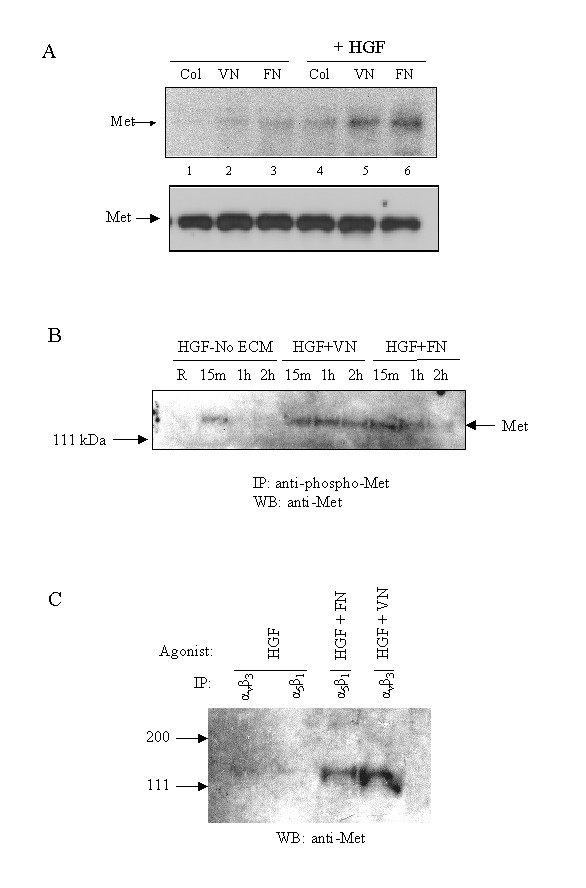
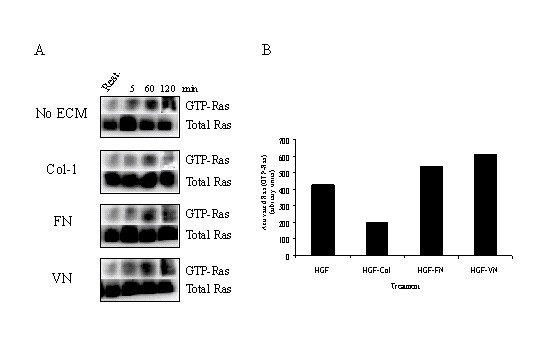
方法细节:① 免疫沉淀:用抗整合素(α5β1、αvβ3、α2β1)抗体沉淀HGF/ECM刺激后的HMVEC lysate,检测Met的共沉淀水平;② Western blot:检测Erk1/2(Map激酶通路)、Akt(PI3K通路)的磷酸化水平;③ Ras pull-down:用Ras结合域(RBD)-琼脂糖沉淀GTP-Ras,检测Ras激活水平。
结果解读:① HGF-FN/VN刺激后,Met与α5β1、αvβ3的结合显著增强(HGF单独或HGF+胶原-1组无此现象);② HGF-FN/VN诱导Erk1/2、Akt的持续磷酸化(HGF单独组磷酸化在1小时后减弱);③ Ras激活水平较HGF单独组高2倍,且持续至120分钟——证实复合物通过促进Met-整合素结合,激活Ras依赖的双重信号通路。
产品关联:实验所用关键试剂包括Cell Signaling的磷酸化Erk/Akt抗体、Upstate的RBD-琼脂糖。
3.6 信号通路与细胞功能的关联验证
实验目的:明确迁移、增殖依赖的信号通路。
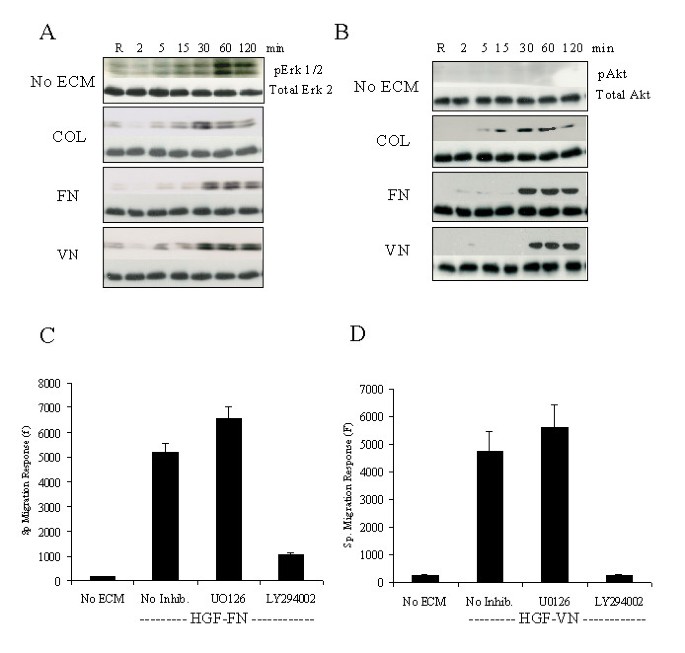
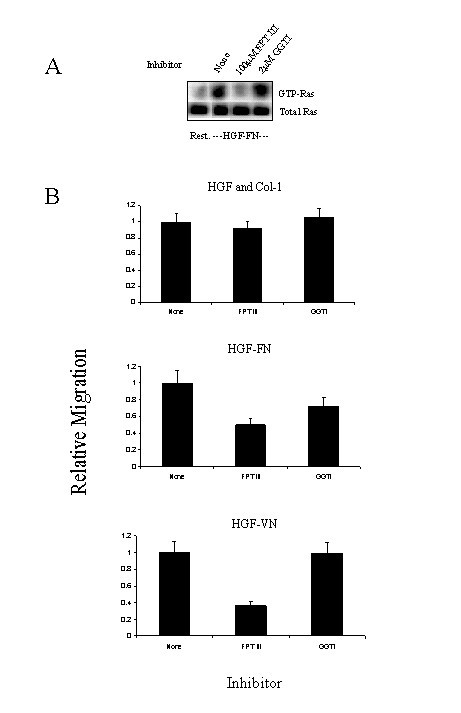
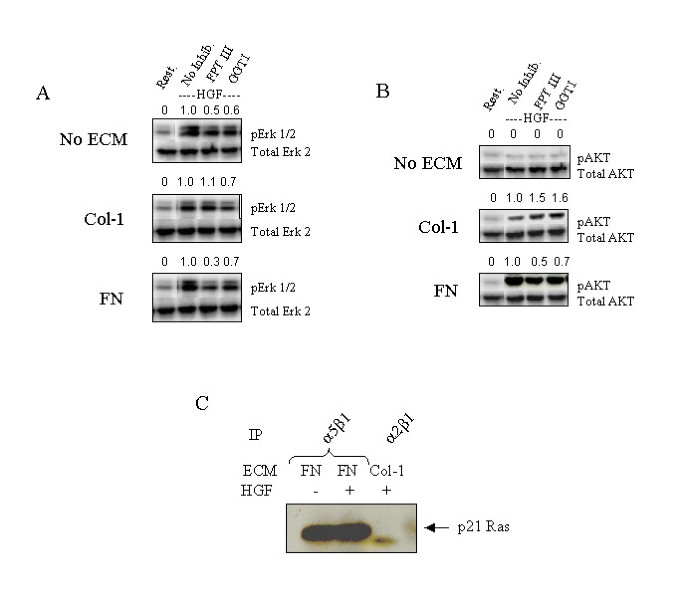
方法细节:① 迁移抑制实验:用PI3K抑制剂LY294002、MEK抑制剂U1026预处理细胞,检测HGF-FN/VN诱导的迁移;② 增殖抑制实验:用U1026预处理细胞,检测HGF/ECM刺激后的细胞增殖(CyQuant法);③ Ras抑制实验:用法尼基转移酶抑制剂FPT-III预处理细胞,检测Ras激活及迁移水平。
结果解读:① LY294002完全抑制HGF-FN/VN诱导的迁移(U1026无影响)——证实迁移依赖PI3K通路;② U1026显著抑制HGF/ECM诱导的增殖(抑制率50%-80%)——证实增殖依赖Map激酶通路;③ FPT-III抑制Ras激活及迁移(HGF+胶原-1组无影响)——证实HGF-FN/VN的迁移信号是Ras依赖的。
产品关联:实验所用关键试剂包括Sigma的LY294002、U1026抑制剂。
4. Biomarker研究及发现成果解析
本研究虽未聚焦于“诊断/预后型Biomarker”的筛选,但揭示了HGF-FN/VN复合物作为“功能型生物分子复合物”的潜在 Biomarker 价值——其体内存在(如血小板上清中的复合物)可能反映血管生成的活跃状态。
4.1 复合物的体内存在验证
研究过程:通过凝血酶刺激血小板释放上清,用抗FN/VN抗体免疫沉淀,Western blot检测HGF的共沉淀水平——证实HGF-FN/VN复合物在体内(血小板脱颗粒上清)存在。
结果: thrombin刺激组的FN/VN免疫沉淀样品中,HGF信号显著高于未刺激组或对照IgG组(n=3,实验重复3次)。
4.2 核心成果提炼
功能关联:HGF-FN/VN复合物通过促进Met-整合素结合,激活Ras依赖的PI3K-Akt通路,增强内皮细胞迁移——是血管生成的关键功能单元。
创新性:① 首次发现HGF与FN、VN的新结合域;② 证实HGF-ECM复合物在体内存在;③ 揭示复合物通过Ras依赖途径增强Met-整合素信号的机制。
4.3 潜在应用价值
尽管未直接鉴定诊断型Biomarker,但HGF-FN/VN复合物的体内水平可能作为血管生成活跃程度的指标(如心肌梗死患者的血小板上清中复合物水平升高),为评估血管修复能力提供参考。
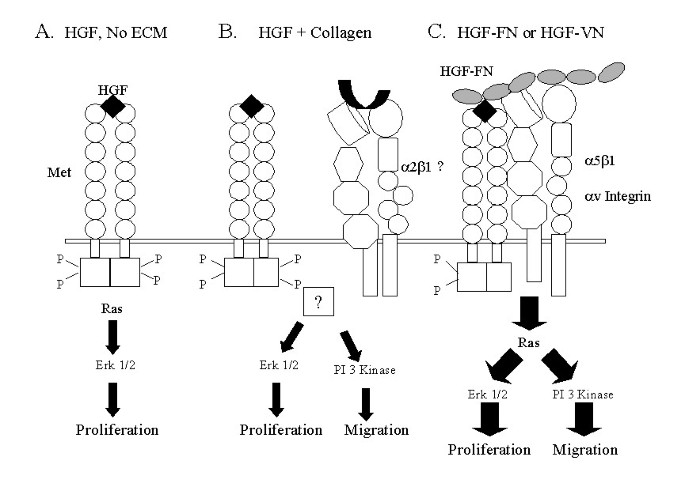
(图9:HGF信号调控机制模型,A:HGF单独激活Met-Erk通路促进增殖;B:HGF+胶原-1激活Ras非依赖的PI3K通路;C:HGF-FN/VN激活Ras依赖的双重通路,增强增殖与迁移)
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。