circCYP24A1 promotes Docetaxel resistance in prostate Cancer by Upregulating ALDH1A3
circCYP24A1 通过上调 ALDH1A3 促进前列腺癌对多西他赛的耐药性
| 期刊: | Biomarker Research | 影响因子: | 9.500 |
| 时间: | 2022 | 起止号: | 2022 Jul 13;10(1):48. |
| doi: | 10.1186/s40364-022-00393-1 | 研究方向: | 肿瘤 |
| 疾病类型: | 前列腺癌 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:circCYP24A1 promotes Docetaxel resistance in prostate Cancer by Upregulating ALDH1A3;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤学-泌尿生殖系统肿瘤(前列腺癌化疗耐药性)
前列腺癌是老年男性群体中发病率最高的恶性肿瘤之一,早期患者通过根治性手术或放疗可获得较好预后,但约15%的高危局限性患者会进展为转移性阶段,需依赖系统治疗维持生存。多西他赛(DTX)是目前转移性激素敏感性前列腺癌(mHSPC)和转移性去势抵抗性前列腺癌(mCRPC)的一线化疗药物,联合雄激素剥夺治疗可显著延长患者生存期,但临床中多数患者会在3年内出现多西他赛耐药,导致治疗失败、预后恶化。当前临床主要依赖肿瘤体积等影像学指标预测多西他赛疗效,但该指标仅基于亚组分析结果,且高/低肿瘤体积的定义存在争议,临床应用价值有限;已有遗传生物标志物可用于预测PARP抑制剂、AKT抑制剂等靶向药物的疗效,但缺乏能有效预测多西他赛耐药的特异性生物标志物。环状RNA(circRNA)因具有独特的闭环结构,比线性RNA更稳定,且在肿瘤发生发展过程中呈现复杂的时空特异性,近年来被证实可通过“海绵吸附miRNA”的方式调控下游基因表达,参与肿瘤增殖、转移及化疗耐药等过程,但circRNA在前列腺癌多西他赛耐药中的具体作用机制尚未明确。
本研究针对前列腺癌多西他赛耐药机制不明、缺乏有效预测生物标志物的核心问题,通过RNA测序技术筛选耐药细胞系中差异表达的circRNA,系统探究circCYP24A1在多西他赛耐药中的生物学功能及分子调控机制,为临床预测化疗反应、开发耐药逆转靶点提供新的理论依据与潜在标志物。
2. 文献综述解析
作者以“临床治疗现状-耐药困境-生物标志物研究缺口-circRNA调控潜力”为核心逻辑,对前列腺癌多西他赛治疗领域的现有研究进行分层梳理。
临床治疗层面,现有研究已证实多西他赛联合雄激素剥夺治疗是转移性前列腺癌的标准一线方案,可显著延长患者总生存期,但约80%的患者会在治疗后3年内出现耐药,成为制约疗效提升的关键瓶颈;现有疗效预测指标中,基于影像学的肿瘤体积分类仅来自两项前瞻性试验的亚组分析,且高/低体积的定义尚未达成共识,临床应用存在局限性;前列腺特异性抗原(PSA)虽可反映治疗反应,但需在治疗后数周期才能检测到变化,无法指导初始治疗方案的制定。生物标志物研究层面,目前已鉴定出可预测PARP抑制剂、AKT抑制剂疗效的遗传标志物,但针对多西他赛耐药的特异性生物标志物研究仍处于空白状态。circRNA研究层面,已有研究证实circRNA可通过调控miRNA表达参与多种肿瘤的化疗耐药过程,如circRNA-SORE通过稳定YBX1蛋白促进肝癌索拉非尼耐药,circAKT3通过miR-198/PI3KR1轴促进胃癌顺铂耐药,但circRNA在前列腺癌多西他赛耐药中的调控作用尚未见报道。
通过对比现有研究的未解决问题,本研究的创新价值凸显:首次鉴定出在前列腺癌多西他赛耐药细胞及组织中高表达的circCYP24A1,系统阐明其通过“海绵吸附miR-1301-3p上调ALDH1A3表达、激活PI3K/AKT/mTOR通路”的耐药调控机制,并证实circCYP24A1可作为独立预测因子用于多西他赛化疗反应的早期评估,填补了前列腺癌多西他赛耐药circRNA标志物及机制研究的空白。
3. 研究思路总结与详细解析
本研究以“揭示circRNA在前列腺癌多西他赛耐药中的调控机制、鉴定有效预测生物标志物”为核心目标,围绕“circCYP24A1如何调控前列腺癌多西他赛耐药性”的科学问题,构建“耐药细胞系构建→差异circRNA筛选→功能验证→机制探究→临床验证”的完整技术路线,通过体外细胞实验、体内动物实验及临床样本分析的多层次验证,明确circCYP24A1的耐药调控作用及临床应用价值。
3.1 多西他赛耐药前列腺癌细胞系构建与验证
实验目的:构建稳定的多西他赛耐药前列腺癌细胞系,为后续circRNA筛选及功能研究提供细胞模型。
方法细节:采用逐步递增药物浓度的方法诱导DU145细胞产生耐药性,初始以2nM多西他赛处理细胞2天,收集存活细胞传代培养,待细胞适应后逐步将药物浓度提升至100nM,最终在10nM多西他赛培养基中维持培养;通过CCK-8实验检测细胞对多西他赛的敏感性,通过裸鼠异种移植模型验证细胞的体内耐药性,通过流式细胞术检测细胞凋亡率及细胞周期分布。
结果解读:CCK-8实验显示,耐药细胞系(DU145-DR)的多西他赛半数抑制浓度(IC50)为122.3nM,是亲本DU145细胞的21.46倍(n=3,P<0.001);体内实验中,DU145-DR细胞形成的肿瘤对多西他赛治疗的反应性显著低于亲本细胞;流式细胞术结果显示,经20nM多西他赛处理后,DU145-DR细胞的凋亡率显著低于亲本细胞,G2/M期细胞比例显著降低(n=3,P<0.001),成功构建具有稳定耐药性的前列腺癌细胞系。
产品关联:实验所用关键产品:YEASEN的MycAway™ Plus-Color One-Step支原体检测试剂盒、MCE的多西他赛试剂、Vazyme的CCK-8试剂盒、BD的流式细胞术凋亡检测试剂盒。
3.2 差异表达circRNA筛选与circCYP24A1鉴定
实验目的:筛选多西他赛耐药细胞中差异表达的circRNA,鉴定参与耐药调控的关键circRNA分子。
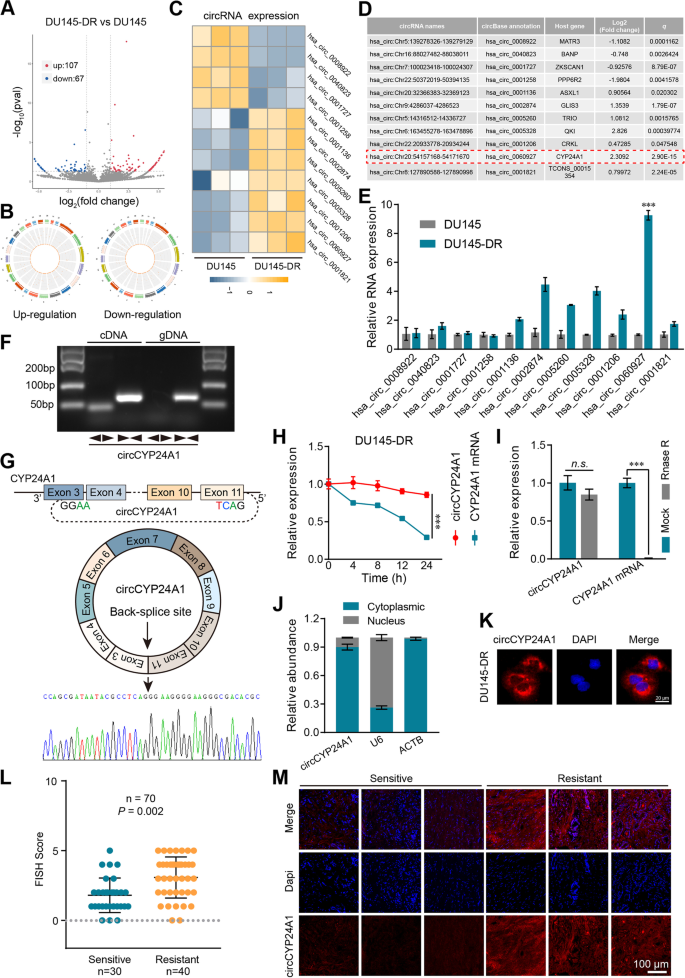
方法细节:提取DU145-DR和亲本细胞的总RNA,采用RiboMinus试剂盒去除核糖体RNA后构建测序文库,通过Illumina HiSeq 2000平台进行RNA测序;利用TopHat2软件将测序数据比对至人类hg38参考基因组,筛选差异表达circRNA(筛选标准:fold-change>2或<-2,P<0.05);通过qRT-PCR验证候选circRNA的表达水平;采用PCR扩增、Sanger测序验证circCYP24A1的环状结构,通过RNase R酶切实验和放线菌素D转录抑制实验验证其稳定性,通过核质分离实验和荧光原位杂交(FISH)检测其亚细胞定位;收集70例前列腺癌患者的组织样本,通过FISH检测circCYP24A1的临床表达特征。
结果解读:RNA测序共鉴定出107个上调circRNA和67个下调circRNA,qRT-PCR验证显示circCYP24A1(hsa_circ_0060927)在耐药细胞中的上调幅度最显著;PCR扩增结果显示,仅在cDNA样本中可扩增出circCYP24A1的特异性条带,gDNA样本中无扩增,Sanger测序进一步验证了其环化连接位点;RNase R酶切实验显示,circCYP24A1的残留量显著高于线性CYP24A1 mRNA(n=3,P<0.001),放线菌素D实验显示circCYP24A1的半衰期显著长于线性mRNA;核质分离和FISH实验显示,circCYP24A1主要定位于细胞质中;临床样本FISH结果显示,多西他赛耐药患者的circCYP24A1表达水平显著高于敏感患者(n=70,P=0.002)。
产品关联:实验所用关键产品:Vazyme的TRIzol总RNA提取试剂、Qiagen的RiboMinus Eukaryote试剂盒、Illumina的HiSeq 2000测序平台、Bersinbio的FISH试剂盒。
3.3 circCYP24A1调控多西他赛耐药性的功能验证
实验目的:验证circCYP24A1在前列腺癌多西他赛耐药中的生物学功能。
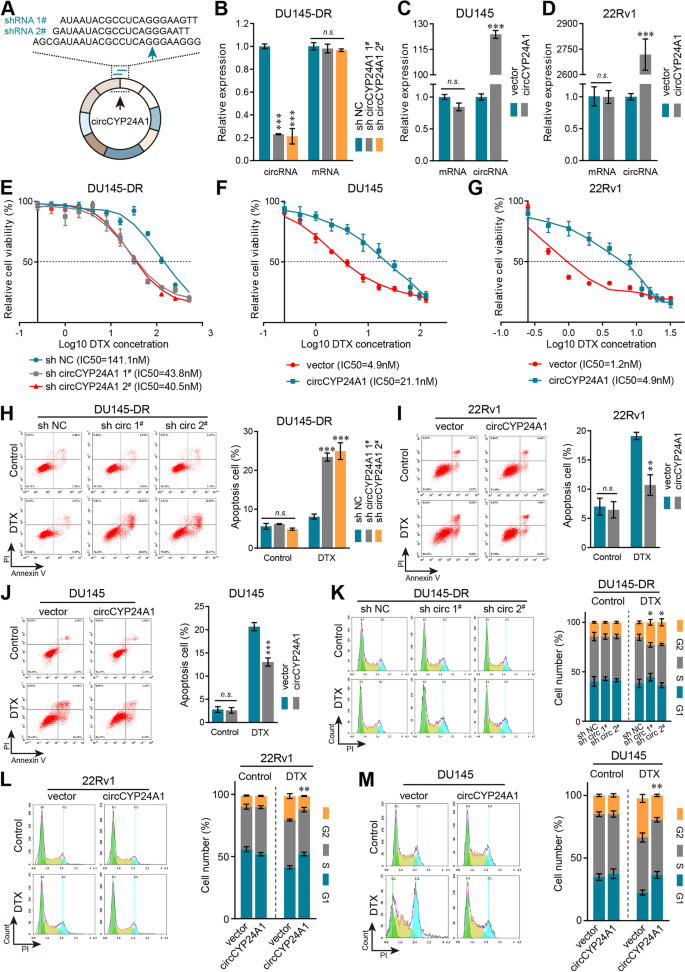
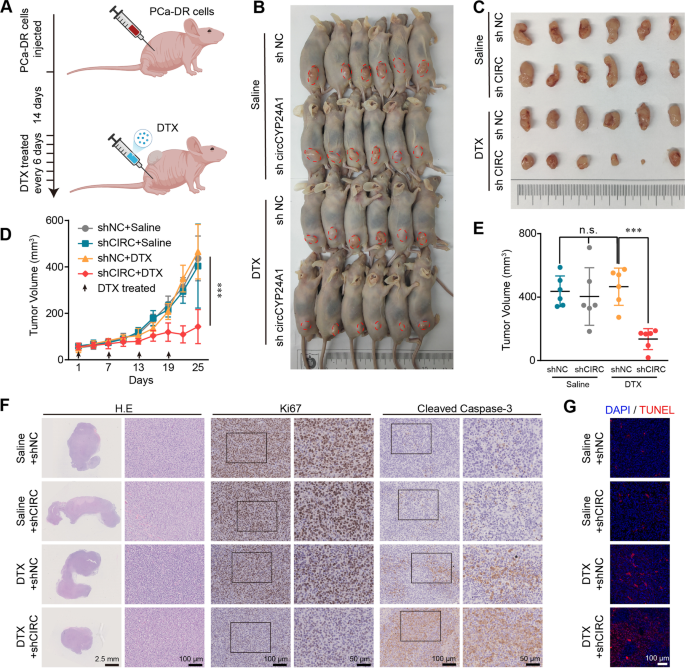
方法细节:在DU145-DR细胞中通过慢病毒转染shRNA敲低circCYP24A1表达,在DU145和22Rv1细胞中转染过表达质粒上调circCYP24A1表达;通过CCK-8实验检测细胞对多西他赛的敏感性,通过流式细胞术检测细胞凋亡率及细胞周期分布;构建裸鼠异种移植模型,将敲低circCYP24A1的DU145-DR细胞接种于裸鼠皮下,待肿瘤形成后给予多西他赛治疗,定期测量肿瘤体积,实验终点取肿瘤组织进行免疫组化(IHC)和TUNEL实验,检测肿瘤细胞的增殖与凋亡情况。
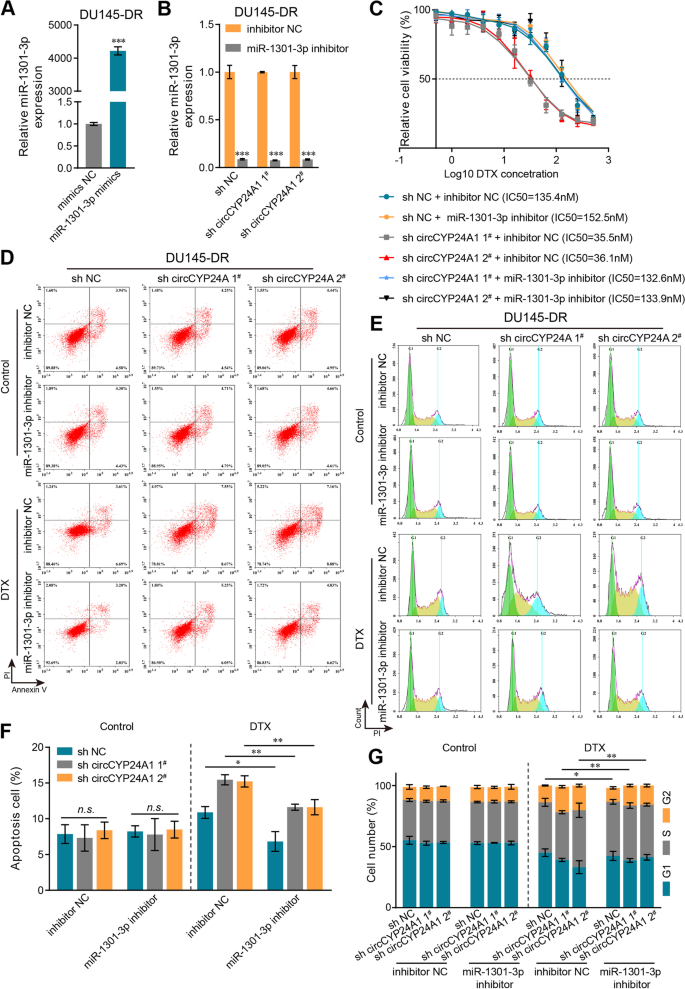
结果解读:CCK-8实验显示,敲低circCYP24A1可显著降低DU145-DR细胞的多西他赛IC50,上调circCYP24A1可显著增加DU145和22Rv1细胞的IC50(n=3,P<0.001);流式细胞术结果显示,敲低circCYP24A1可显著增加多西他赛诱导的细胞凋亡率及G2/M期细胞比例,上调circCYP24A1则产生相反效应(n=3,P<0.001);体内实验显示,敲低circCYP24A1联合多西他赛治疗组的肿瘤体积显著小于其他组(n=6,P<0.001),IHC结果显示该组肿瘤组织中Cleaved caspase 3表达显著升高、Ki67表达显著降低,TUNEL实验显示凋亡细胞比例显著增加,证实circCYP24A1可抑制前列腺癌细胞对多西他赛的化学敏感性。
产品关联:实验所用关键产品:GenePharma的shRNA慢病毒及过表达质粒、Vazyme的CCK-8试剂盒、BD的流式细胞术细胞周期检测试剂盒、Servicebio的免疫组化试剂盒、Roche的TUNEL凋亡检测试剂盒。
3.4 circCYP24A1调控多西他赛耐药的分子机制探究
实验目的:阐明circCYP24A1调控前列腺癌多西他赛耐药的分子机制。
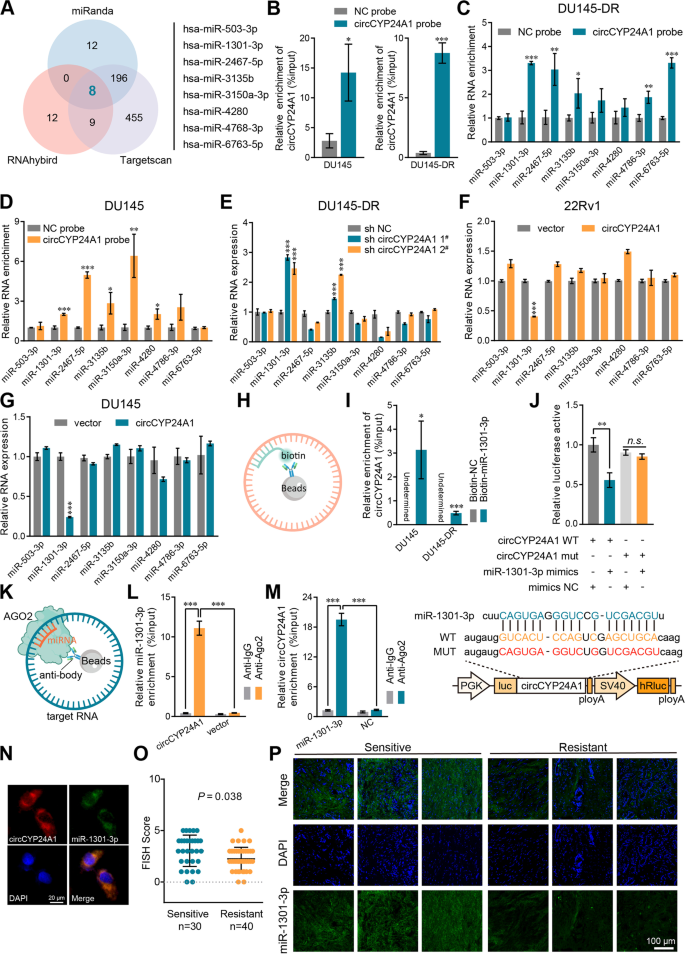
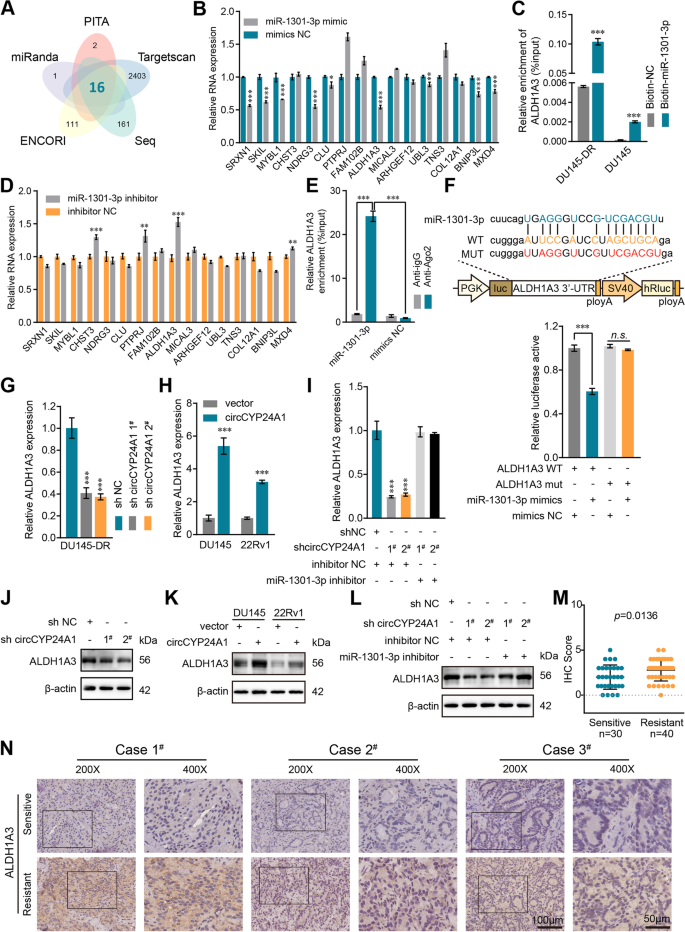
方法细节:通过miRanda、RNAhybird、TargetScan三个数据库预测circCYP24A1的潜在结合miRNA,采用RNA pull-down实验和RNA免疫沉淀(RIP)实验验证circCYP24A1与miR-1301-3p的相互作用,通过双荧光素酶报告实验验证结合位点的特异性;通过PITA、miRanda、TargetScan、ENCORI四个数据库预测miR-1301-3p的潜在靶基因,结合RNA测序结果筛选出ALDH1A3作为候选靶基因,采用RNA pull-down、RIP及双荧光素酶报告实验验证miR-1301-3p与ALDH1A3的相互作用;通过qRT-PCR和Western blot检测circCYP24A1、miR-1301-3p对ALDH1A3表达的调控作用;通过Western blot检测PI3K/AKT/mTOR信号通路的激活情况。
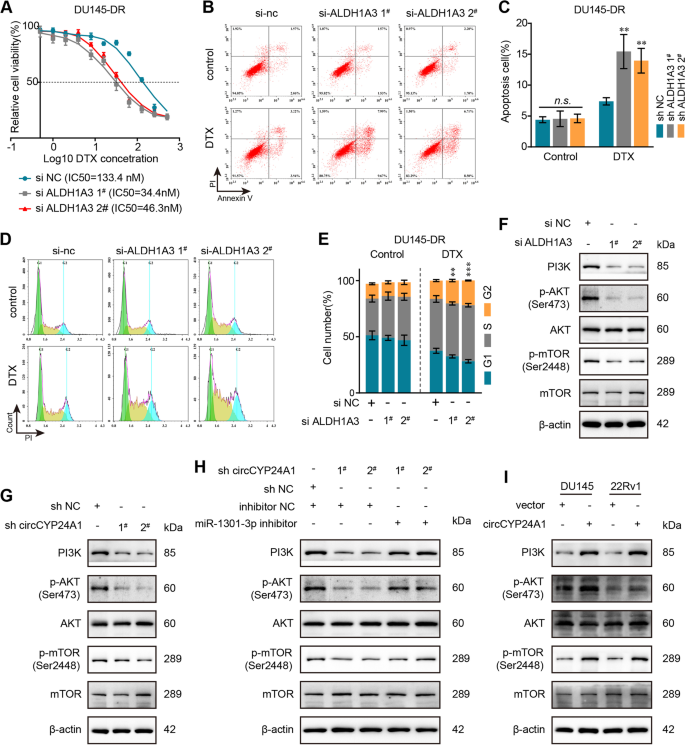
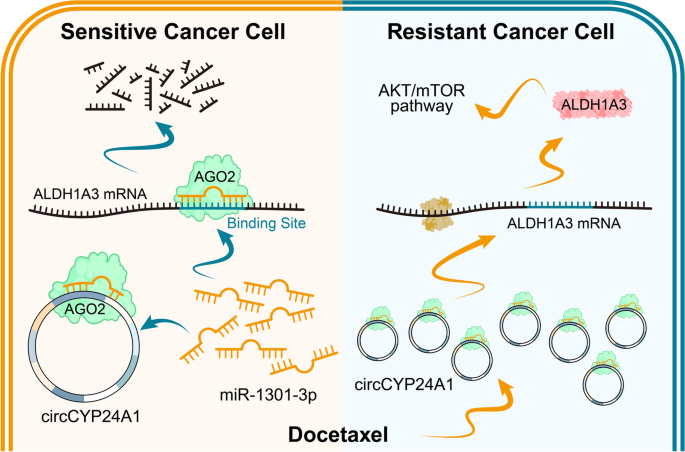
结果解读:RNA pull-down实验显示,miR-1301-3p在circCYP24A1探针的富集产物中显著上调,RIP实验显示circCYP24A1与miR-1301-3p共定位于AGO2复合物中;双荧光素酶报告实验显示,miR-1301-3p可显著降低含circCYP24A1野生型结合位点的报告基因荧光活性(n=3,P<0.001),突变结合位点后该效应消失;敲低circCYP24A1可显著上调miR-1301-3p表达,上调circCYP24A1则显著下调miR-1301-3p表达(n=3,P<0.001);RNA pull-down和双荧光素酶报告实验证实miR-1301-3p可直接结合ALDH1A3的3"UTR区域(n=3,P<0.001);敲低circCYP24A1可显著下调ALDH1A3的mRNA和蛋白表达,该效应可被miR-1301-3p抑制剂逆转(n=3,P<0.001);Western blot结果显示,敲低circCYP24A1或ALDH1A3可显著抑制PI3K/AKT/mTOR通路的激活,上调circCYP24A1则显著激活该通路,证实circCYP24A1通过海绵吸附miR-1301-3p上调ALDH1A3表达,进而激活PI3K/AKT/mTOR通路促进多西他赛耐药。
产品关联:实验所用关键产品:GenePharma的生物素化RNA探针、Bersinbio的RNA pull-down试剂盒及RIP试剂盒、Vazyme的双荧光素酶报告系统、CST的AGO2抗体。
3.5 circCYP24A1作为化疗反应预测因子的临床验证
实验目的:验证circCYP24A1作为前列腺癌多西他赛化疗反应预测因子的临床价值。
方法细节:收集70例接受新辅助多西他赛治疗的前列腺癌患者的组织样本,通过FISH检测circCYP24A1表达,通过IHC检测ALDH1A3表达,通过qRT-PCR检测miR-1301-3p表达;采用单因素和多因素logistic回归分析circCYP24A1表达与化疗反应的相关性,通过ROC曲线分析其预测效能。
结果解读:单因素分析显示,circCYP24A1高表达、miR-1301-3p低表达、ALDH1A3高表达及治疗后PSA水平升高与多西他赛耐药显著相关(P<0.05);多因素logistic回归分析显示,circCYP24A1是预测多西他赛化疗反应的独立危险因素(OR=0.165;95% CI:0.038–0.723;P=0.017);相关性分析显示,circCYP24A1表达与miR-1301-3p表达呈负相关(R=-0.45,P<0.001),与ALDH1A3表达呈正相关(R=0.39,P<0.001),验证了分子机制的临床相关性。
产品关联:实验所用关键产品:GenePharma的FISH探针、Servicebio的IHC试剂盒。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究鉴定的核心Biomarker为环状RNA circCYP24A1,属于非编码RNA类生物标志物;其筛选与验证逻辑为“耐药细胞系RNA测序筛选差异circRNA→细胞及动物实验验证耐药调控功能→分子实验解析调控机制→临床样本验证预测价值”,形成完整的“基础研究-临床转化”证据链。
研究过程详述
circCYP24A1的来源为前列腺癌患者的肿瘤组织样本;验证方法包括:通过FISH检测临床样本中circCYP24A1的表达水平,通过qRT-PCR检测细胞中circCYP24A1的表达,通过CCK-8、流式细胞术验证其对多西他赛敏感性的调控作用,通过裸鼠异种移植模型验证体内功能,通过单因素和多因素logistic回归分析其与化疗反应的相关性;特异性与敏感性方面,临床样本中多西他赛耐药患者的circCYP24A1表达水平显著高于敏感患者(P=0.002),多因素分析显示其作为独立预测因子的比值比(OR)为0.165(95% CI:0.038–0.723;P=0.017),ROC曲线分析显示其具有较好的预测效能(文献未明确AUC、敏感性及特异性具体数值,基于图表趋势推测)。
核心成果提炼
circCYP24A1作为前列腺癌多西他赛耐药的预后标志物,其高表达提示患者对多西他赛治疗的反应性较差,风险比OR=0.165(95% CI:0.038–0.723;P=0.017);其创新性在于首次在前列腺癌多西他赛耐药中鉴定出circCYP24A1这一关键调控分子,阐明其“海绵吸附miR-1301-3p上调ALDH1A3、激活PI3K/AKT/mTOR通路”的耐药机制,并证实其可作为独立预测因子用于化疗反应的早期评估;与传统PSA标志物相比,circCYP24A1可在治疗前通过组织样本检测,能够为初始治疗方案的制定提供依据,具有更高的临床应用价值。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。