一、 研究背景:尼帕病毒——公共卫生的持久威胁
尼帕病毒(Nipah virus, NiV)是一种属于副黏病毒科(Paramyxoviridae)、亨尼帕病毒属(Henipavirus)的单股负链 RNA 病毒 。其自然宿主为狐蝠属(Pteropus)果蝠,可通过受污染的食物、直接接触受感染动物(如猪、马)或人际传播等方式进入人类群体 。
临床上,NiV 感染可导致急性呼吸系统疾病以及严重的致命性脑炎,病死率高达 40% 至 70% 。由于其高致死率、广泛的宿主范围以及目前尚无获批的特效药物或疫苗,世界卫生组织(WHO)已将其列为需要优先应对的区域性重大威胁 。尤其是在人口稠密的东南亚地区,动物与人类频繁的互动进一步增加了疫情爆发的风险 。
二、 领域现状与研究缺口:口服药物的临床急需
虽然已有部分小分子化合物或单克隆抗体在实验环境中显示出对 NiV 的抑制活性,但尚未有任何药物通过临床验证并获得许可 。
目前研究较多的广谱抗病毒药物包括瑞德西韦(Remdesivir, RDV)、法匹拉韦(T-705)和 4'-氟尿苷(4'-FIU)。其中,RDV 在非人灵长类模型中表现出良好的保护作用,但其给药方式主要依赖静脉注射,在疫情爆发的大规模临床应用中存在局限 。因此,开发一种理化性质稳定、安全性高且具有良好口服生物利用度的小分子药物,是当前抗 NiV 研究领域的核心诉求 。
三、 作者研究思路:从体外效能到体内保护的逻辑架构
本研究主要聚焦于国产口服核苷类前体药物 VV116。VV116 此前已在抗击 SARS-CoV-2 及其他人类冠状病毒中展现出优异的广谱活性,并已获批用于 COVID-19 的临床治疗 。
作者团队构建了层次清晰的研究脉络:
体外效力评估:通过 Vero E6 细胞模型,对比 VV116 及其代谢产物 X1 与多种已知抗病毒药物对不同 NiV 毒株的抑制能力 。
药代动力学(PK)表征:在金仓鼠模型中明确口服 VV116 后的代谢动力学,特别是药物在肺、脑、脾等靶器官中的分布情况 。
体内治疗效果验证:通过建立致死剂量感染的仓鼠模型,从病毒载量、组织病理、生存率及体重变化等维度评价 VV116 的保护效力 。
临床转化建议:结合人体 I 期临床数据,为后续针对 NiV 感染的临床给药方案提供参考建议 。
四、 核心研究环节拆解与实验结果解读
1. 体外抑制活性:跨毒株的高效性
研究者首先在 Vero E6 细胞系中开展了“头对头”的药物活性比对实验。
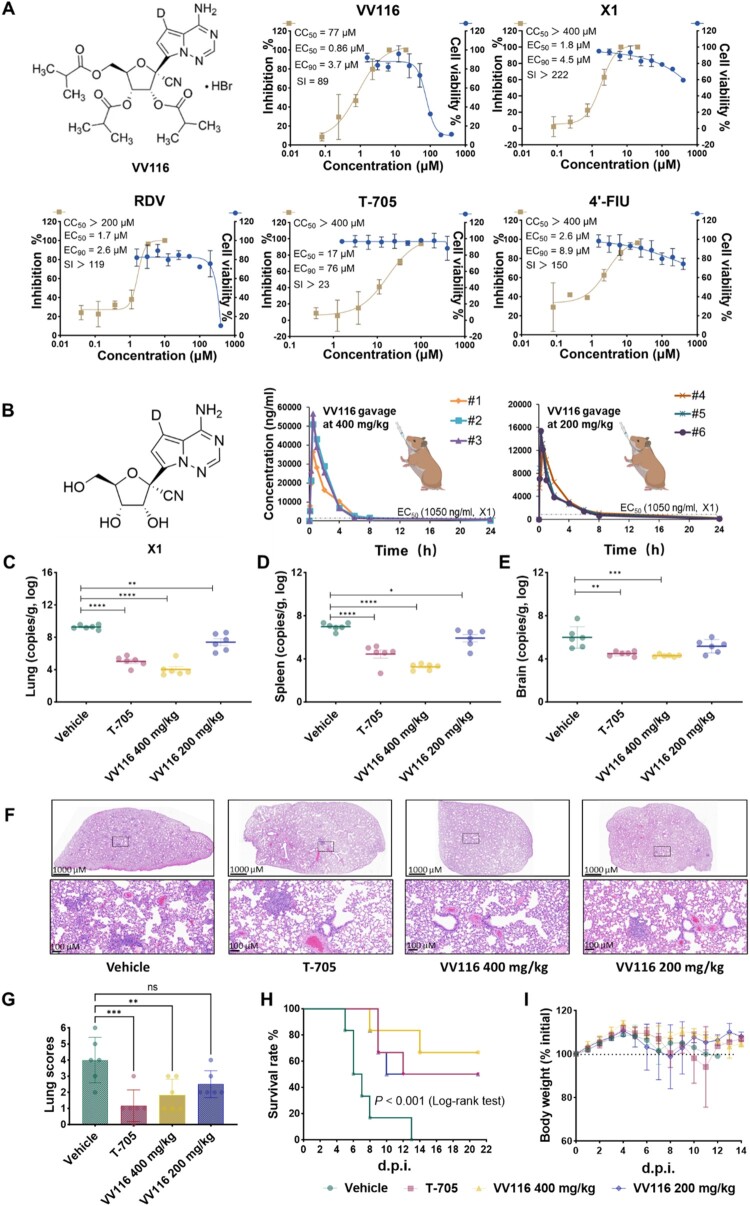
对 NiV-M(马来西亚株)的抑制:VV116 展示了极强的抗病毒潜力,其 $EC_{50}$ 值为 0.86 μM,优于 RDV($1.67 μM$)和 X1($1.8 μM$) 。
对比优势:与法匹拉韦($EC_{50} = 17 μM$)和 4'-FIU($EC_{50} = 2.6 μM$)相比,VV116 的效能显著更高 。
广谱保护力:VV116 同样能有效抑制 NiV-B(孟加拉国株),$EC_{50}$ 为 0.97 μM 。
图 1A 结果分析:实验数据显示,在 Vero E6 细胞中,VV116 呈现出显著的剂量依赖性抑制效果,且其选择性指数(SI = 89)表明在该有效浓度下具有良好的细胞安全性 。
2. 药代动力学(PK):优异的组织穿透性
药物在体内的分布特征是决定其临床价值的关键。
快速吸收与转化:VV116 口服后能迅速转化为母体核苷 X1,在仓鼠体内单次给药 $400 mg/kg$ 后,1 小时内即可达到血药峰浓度 。
靶器官分布:研究发现 X1 广泛分布于肺部和脾脏,其浓度与血浆水平相当 。
突破血脑屏障:虽然脑部药物浓度约为其他器官的 1/20,但考虑到脑部病毒载量通常较低,这一浓度仍足以有效抑制中枢神经系统的病毒复制 。
3. 体内效能评估:显著的病毒抑制与病理改善
在建立致死剂量($1000 LD_{50}$)感染的仓鼠模型后,研究者评估了 VV116 的治疗潜力。
病毒载量下降:
图 1 C-E 结果呈现:在感染后第 4 天,口服 $400 mg/kg$ VV116 的仓鼠,其肺部、脑部和脾脏中的病毒 RNA 拷贝数分别显著降低了约 4、2 和 1.5 个对数级(logs) 。
相比之下,较低剂量的 $200 mg/kg$ 组虽然也能降低病毒载量,但在脑部的抑制效果不如高剂量组明显 。
组织病理学保护:
图 1 F-G 结果分析:溶剂对照组仓鼠表现出严重的肺部病变,包括肺泡壁增厚和血管炎症反应 。而 $400 mg/kg$ VV116 组的肺组织基本保持正常,未见显著异常 。
4. 生存获益与生理稳态
存活率提升:溶剂对照组在感染 13 天后全部死亡 。相比之下,口服 $400 mg/kg$ VV116 组的生存率提升至 66.7%,且所有药物处理组在感染早期均表现出 100% 的存活率 。
图 1 H-I 结果呈现:未治疗组在感染第 4 天开始出现活动减少、食欲下降和体重骤减 。高剂量 VV116 组不仅延缓了发病过程,且在实验终点成功维持了体重高于初始水平 。
五、机制解析与临床前景
基于核苷类似物的共同特征,作者推测 VV116 的活性代谢产物 X1 通过靶向病毒的 RNA 依赖性 RNA 聚合酶(RdRP) 来阻断病毒的 RNA 复制进程 。
本研究的学术价值在于:
临床转化速度快:VV116 的安全性已经在人体中得到验证,这为应对未来的 NiV 突发疫情提供了极具潜力的“现货”治疗方案 。
给药优势:口服给药相比静脉注射更具灵活性,适用于野外、社区等多种复杂环境下的防疫救治 。
临床剂量建议:根据人体 I 期临床数据,建议使用 800 mg 每日两次的给药方案,以维持持续有效的血药浓度来抑制 NiV 。
该研究严谨地证明了口服核苷类药物 VV116 在应对高致死性尼帕病毒感染中的强大效能。从细胞水平的精准抑制到动物模型中显著的生存获益,VV116 不仅展现了其作为治疗候选药物的实力,也为全球防范新发突发传染病贡献了重要的科研参考。
