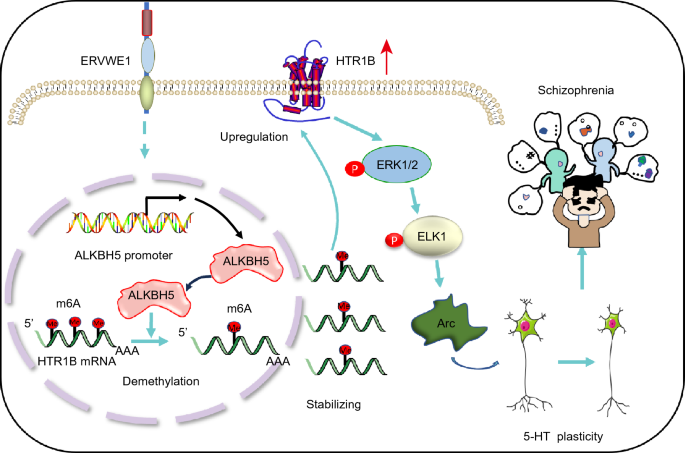
Captive ERVWE1 triggers impairment of 5-HT neuronal plasticity in the first-episode schizophrenia by post-transcriptional activation of HTR1B in ALKBH5-m6A dependent epigenetic mechanisms
捕获的ERVWE1通过ALKBH5-m6A依赖的表观遗传机制,在转录后激活HTR1B,从而引发首发精神分裂症中5-HT神经元可塑性的损伤。
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2023 | 起止号: | 2023 Nov 21;13(1):213 |
| doi: | 10.1186/s13578-023-01167-4 | 靶点: | ALK、5-HT |
| 研究方向: | 表观遗传、神经科学 | 疾病类型: | 精神分裂症 |
文献解析
1. 领域背景与文献引入
文献英文标题:Captive ERVWE1 triggers impairment of 5-HT neuronal plasticity in the first-episode schizophrenia by post-transcriptional activation of HTR1B in ALKBH5-m6A dependent epigenetic mechanisms;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:精神神经科学(精神分裂症发病机制)
精神分裂症是一类以阳性、阴性及认知症状为核心的严重精神疾病,终身患病率约1%,多起病于青壮年期,患者失业率高达80%-90%,给家庭与社会带来沉重负担。领域共识:近年来,基因组关联研究(GWAS)已鉴定出大量与精神分裂症相关的遗传变异,涉及突触蛋白、谷氨酸/多巴胺/5-羟色胺(5-HT)神经递质受体等基因;表观遗传修饰(如DNA甲基化、RNA修饰)与内源性逆转录病毒(HERVs)的病理作用也成为研究热点。当前领域未解决的核心问题包括:精神分裂症中5-HT系统异常与突触可塑性损伤的具体调控机制尚不明确,尤其是HERVs家族成员ERVWE1如何通过表观遗传途径影响5-HT神经元功能;缺乏对ERVWE1介导的转录后调控网络的系统解析。针对上述空白,本研究聚焦ERVWE1在精神分裂症中的作用机制,探究其是否通过ALKBH5介导的N6-甲基腺苷(m6A)表观修饰调控5-HT1B受体(HTR1B),进而影响5-HT神经元可塑性,为精神分裂症的发病机制提供新的分子视角。
2. 文献综述解析
本文综述从精神分裂症的遗传与表观遗传机制、5-HT系统与突触可塑性的关联、HERVs的病理作用三个核心维度梳理现有研究,系统整合多层面研究成果以凸显本研究的创新价值。
现有研究中,GWAS研究已证实突触蛋白、谷氨酸/多巴胺/5-HT受体基因的遗传变异与精神分裂症易感性相关;尸检与临床样本研究显示,精神分裂症患者脑内5-HT受体表达异常,突触可塑性相关蛋白Arc的表达水平改变;HERVs尤其是ERVWE1被证实与精神分裂症发病密切相关,可通过调控神经递质受体、诱导神经炎症、损伤线粒体功能等途径参与疾病进程。技术方法层面,现有研究多采用公共数据库生物信息学分析结合临床样本验证的策略,部分研究辅以细胞或动物模型实验,实现了从人群到细胞层面的初步验证,但仍存在局限性:多数研究聚焦于ERVWE1对单基因或单一通路的调控,缺乏对表观遗传修饰(如m6A)介导的转录后调控机制的探究;对5-HT神经元可塑性损伤的具体分子调控链尚不清晰,未明确ERVWE1与表观遗传修饰、5-HT系统的交互作用。
本研究的创新价值在于,首次揭示ERVWE1通过ALKBH5-m6A依赖的表观遗传途径激活HTR1B-ERK-ELK1-Arc通路,导致5-HT神经元可塑性损伤,填补了ERVWE1调控精神分裂症突触可塑性的表观遗传机制空白;同时通过临床样本多因素分析,证实ALKBH5是精神分裂症的新风险基因,为精神分裂症的Biomarker筛选与治疗靶点开发提供了新方向。
3. 研究思路总结与详细解析
本研究的核心目标是明确ERVWE1调控精神分裂症中5-HT神经元可塑性的分子机制,核心科学问题为ERVWE1是否通过ALKBH5介导的m6A修饰调控HTR1B表达及下游通路,技术路线遵循“公共数据库筛选→临床样本验证→细胞/神经元模型功能实验→表观遗传机制解析→体内功能验证”的闭环逻辑,多层面验证研究假设。
3.1 精神分裂症脑内HTR1B通路异常的生物信息学分析
本环节实验目的为通过公共数据库挖掘精神分裂症患者脑内基因表达与通路异常,筛选关键调控靶点。研究采用GSE53987数据集(含15例精神分裂症患者与19例健康对照的前额叶皮层尸检样本),进行差异表达基因(DEGs)分析、基因本体(GO)与京都基因与基因组百科全书(KEGG)富集分析、相关性分析。结果显示,GO细胞组分分析发现DEGs主要富集于突触结构,GO生物过程分析涉及突触后信号转导、mRNA修饰、5-HT受体信号通路;KEGG分析显示DEGs富集于Ras信号通路、5-HT能突触通路;HTR1B在患者脑内的mRNA表达水平显著高于健康对照(p=0.034,n=15/19);相关性分析显示HTR1B与ERK2、m6A去甲基化酶ALKBH5呈显著正相关(相关系数分别为0.61、0.52,p<0.05),提示HTR1B可能通过m6A修饰与ERK通路参与精神分裂症发病。
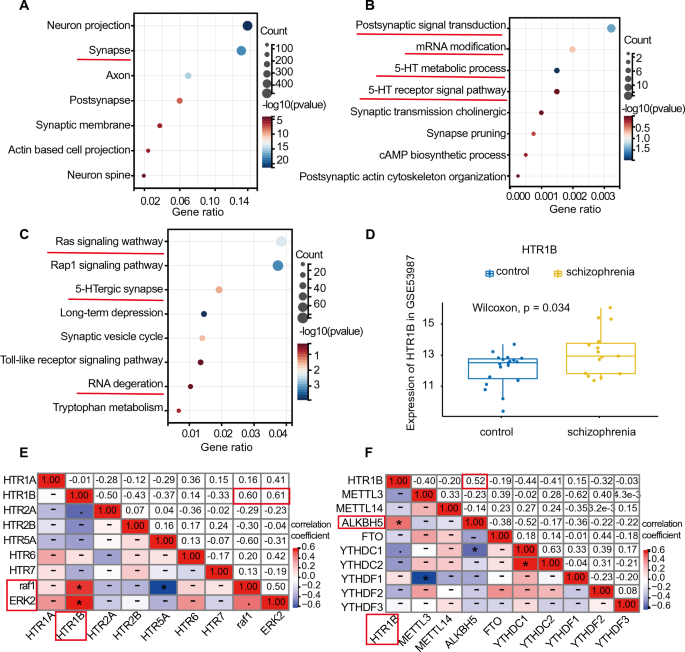
产品关联:文献未提及具体实验产品,领域常规使用生物信息学分析工具(如R语言、DAVID数据库)。
3.2 首发精神分裂症患者外周血关键分子的表达与相关性验证
本环节实验目的为验证临床样本中ERVWE1与HTR1B、Arc、ALKBH5的表达关联,明确潜在风险因素。研究收集44例首发精神分裂症患者与37例健康对照的外周血样本,采用酶联免疫吸附实验(ELISA)检测血浆蛋白水平,实时荧光定量PCR(RT-qPCR)检测全血mRNA水平,进行相关性分析与多因素回归分析。结果显示,患者血浆中HTR1B、Arc、ALKBH5、ERVWE1的蛋白水平均显著高于健康对照(p<0.001),而5-羟色胺、5-羟色胺转运体(SERT)、色氨酸羟化酶-2(TPH2)的蛋白水平显著降低(p<0.001);ERVWE1与HTR1B、Arc、ALKBH5呈强正相关(相关系数分别为0.81、0.77、0.78,p<0.001,n=44);多因素回归分析显示ALKBH5是精神分裂症的独立风险因素。
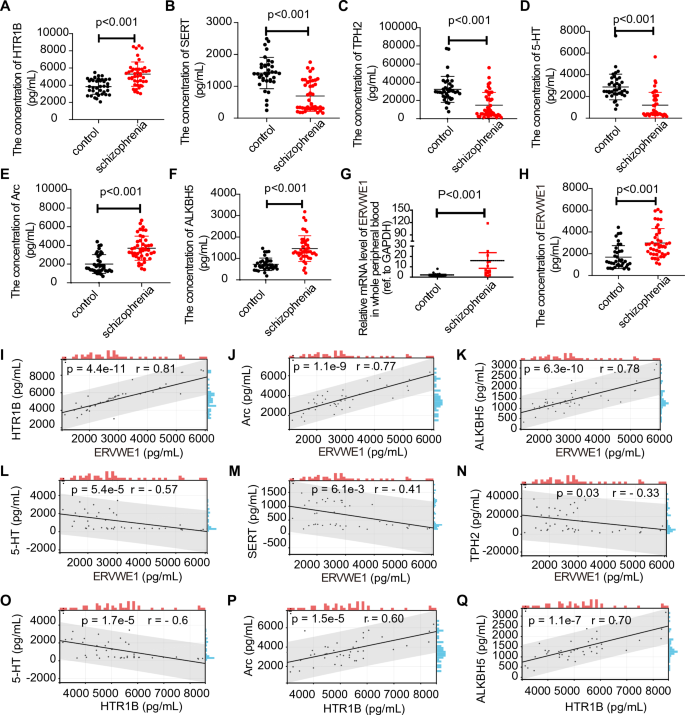
产品关联:文献未提及具体实验产品,领域常规使用ELISA试剂盒、RT-qPCR试剂盒等。
3.3 ERVWE1激活HTR1B-ERK-ELK1-Arc通路的细胞与神经元实验验证
本环节实验目的为验证ERVWE1对HTR1B及下游ERK通路的调控作用。研究在人神经母细胞瘤细胞系SH-SY5Y中转染ERVWE1过表达质粒或HTR1B特异性siRNA,采用蛋白质免疫印迹(Western Blot)检测蛋白表达;分离新生SD大鼠中缝背核(DRN)神经元(经免疫荧光验证含90%以上5-HT神经元),转染ERVWE1质粒后检测相关蛋白表达。结果显示,ERVWE1过表达显著上调SH-SY5Y细胞中HTR1B、磷酸化ERK1/2(p-ERK1/2)、磷酸化ELK1(p-ELK1)、Arc的蛋白水平;敲低HTR1B可完全逆转ERVWE1对下游通路的激活作用;DRN神经元中ERVWE1过表达同样上调上述蛋白水平,免疫荧光染色显示Arc的荧光强度显著增强。
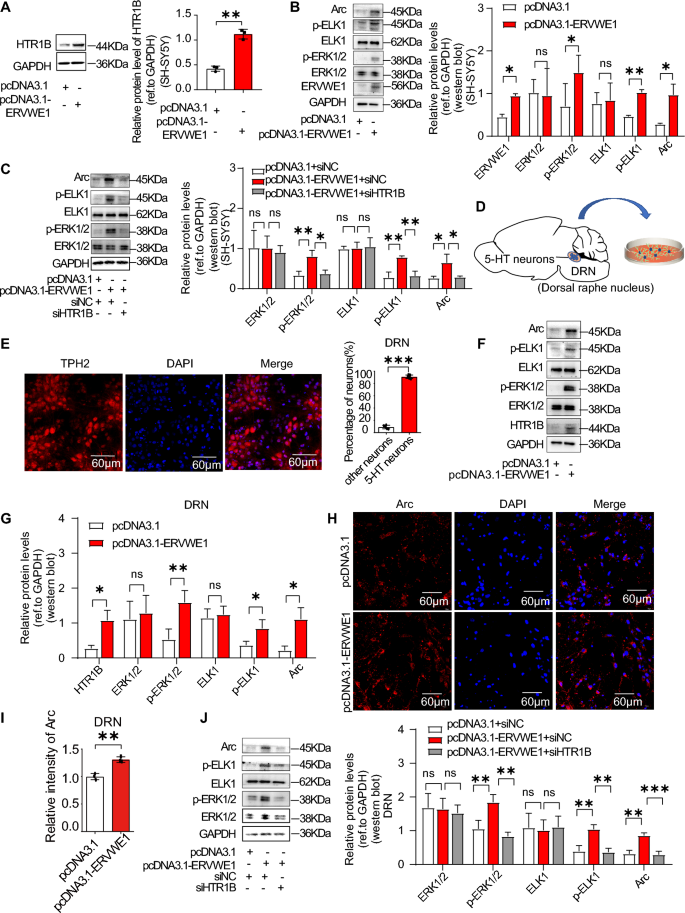
产品关联:文献未提及具体实验产品,领域常规使用细胞转染试剂、蛋白质免疫印迹抗体、免疫荧光试剂等。
3.4 ERVWE1对5-HT神经元可塑性的影响及HTR1B的介导作用
本环节实验目的为探究ERVWE1对5-HT神经元形态与突触可塑性的损伤作用,以及HTR1B在其中的介导功能。研究在DRN神经元中转染ERVWE1过表达质粒或联合转染HTR1B siRNA,采用免疫荧光染色标记微管相关蛋白2(MAP2)以观察神经元形态,标记树突棘以评估突触可塑性,通过Sholl分析、树突棘计数进行量化。结果显示,ERVWE1过表达显著降低5-HT神经元的树突分支数、总树突长度、胞体面积(n=9,p<0.01),以及总树突棘密度(n=15,p<0.001),且四种树突棘亚型(蘑菇型、短粗型、细长型、丝状伪足型)的密度均显著降低;敲低HTR1B可逆转ERVWE1诱导的神经元复杂性降低与树突棘密度减少。
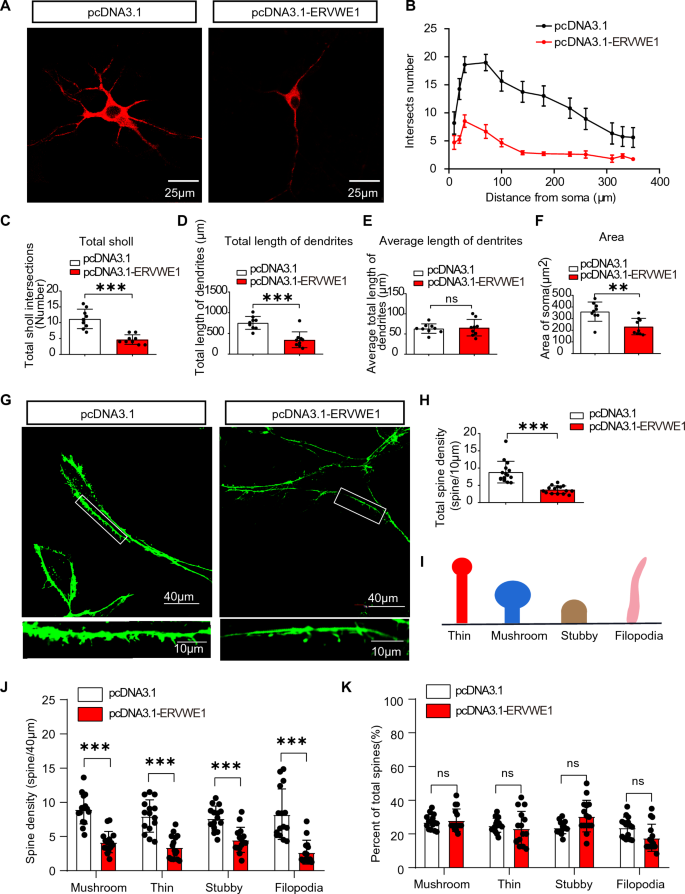
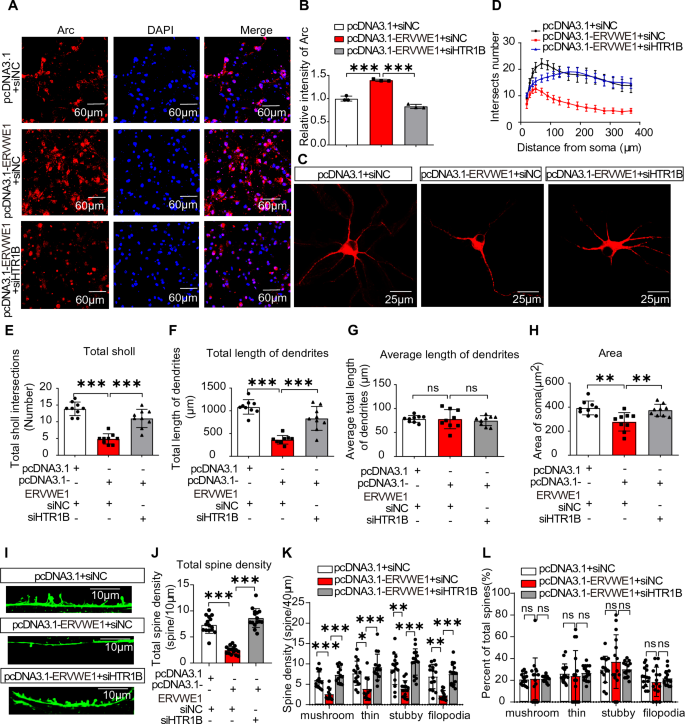
产品关联:文献未提及具体实验产品,领域常规使用共聚焦显微镜、Sholl分析软件等。
3.5 ERVWE1通过ALKBH5调控m6A修饰及HTR1B表达的机制验证
本环节实验目的为明确ERVWE1是否通过ALKBH5介导的m6A修饰调控HTR1B的mRNA稳定性与表达。研究在SH-SY5Y细胞中转染ERVWE1过表达质粒或ALKBH5 siRNA,采用dot blot、RNA甲基化定量试剂盒检测全局m6A水平;通过甲基化RNA免疫沉淀-qPCR(Me-RIP-qPCR)检测HTR1B mRNA的m6A修饰水平;利用放线菌素D处理阻断RNA合成,检测HTR1B mRNA的稳定性;通过双荧光素酶报告实验验证HTR1B编码区(CDS)的m6A修饰位点功能。结果显示,ERVWE1过表达显著降低细胞全局m6A水平,同时上调ALKBH5的mRNA与蛋白表达;敲低ALKBH5可逆转ERVWE1诱导的m6A水平降低与HTR1B上调;Me-RIP-qPCR显示ERVWE1降低HTR1B mRNA的m6A修饰水平,增强其mRNA稳定性;双荧光素酶实验证实HTR1B CDS区的198、572位点为关键m6A修饰位点,ERVWE1通过ALKBH5介导的去甲基化增强HTR1B的表达。
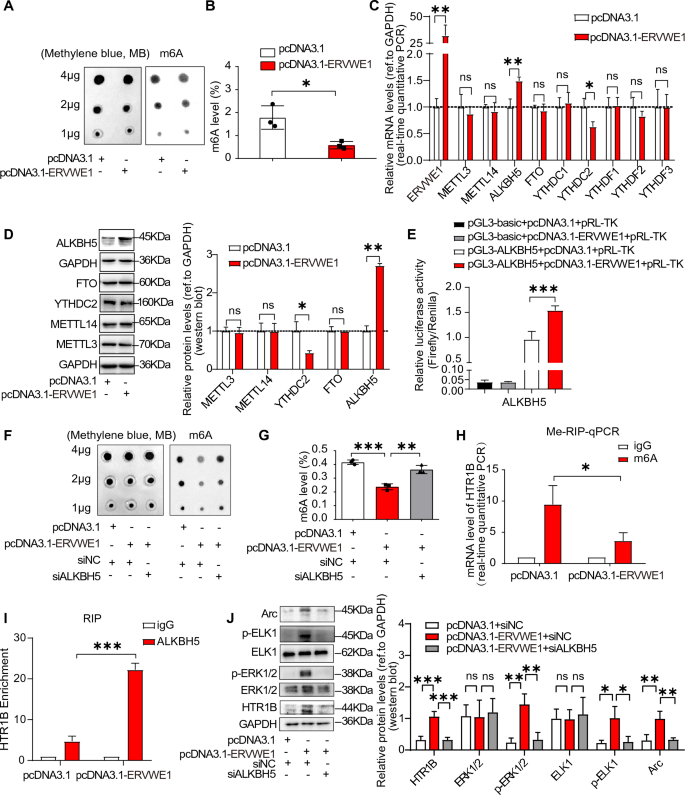
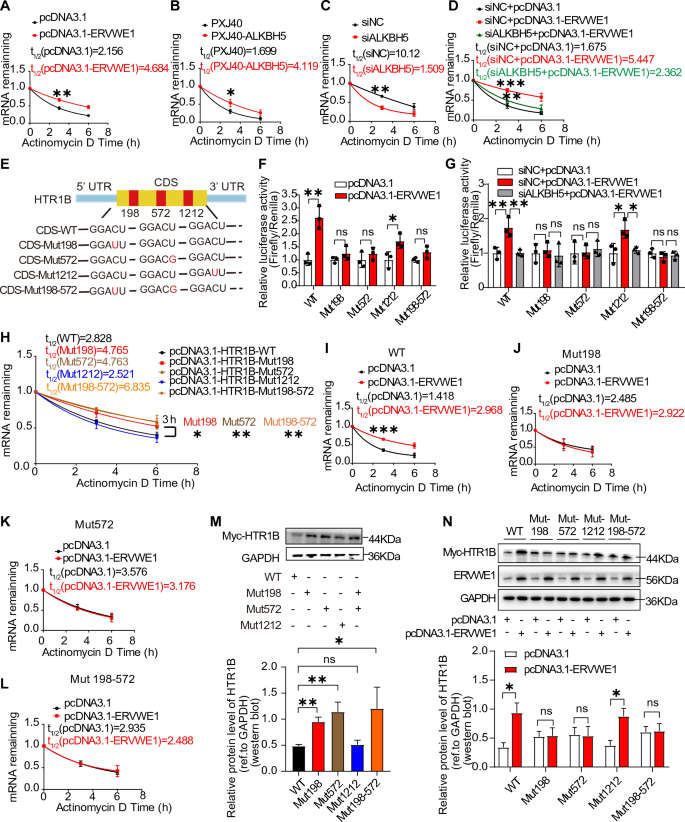
产品关联:文献未提及具体实验产品,领域常规使用m6A甲基化检测试剂盒、Me-RIP试剂盒、双荧光素酶报告系统等。
3.6 ALKBH5介导ERVWE1对5-HT神经元可塑性的损伤作用
本环节实验目的为验证ALKBH5在ERVWE1诱导的5-HT神经元可塑性损伤中的介导作用。研究在DRN神经元中转染ERVWE1过表达质粒或联合转染ALKBH5 siRNA,采用免疫荧光检测Arc的表达,通过Sholl分析、树突棘计数评估神经元可塑性。结果显示,敲低ALKBH5可逆转ERVWE1诱导的Arc表达上调,同时恢复神经元的树突复杂性与树突棘密度,表明ALKBH5是ERVWE1调控5-HT神经元可塑性的关键介导因子。
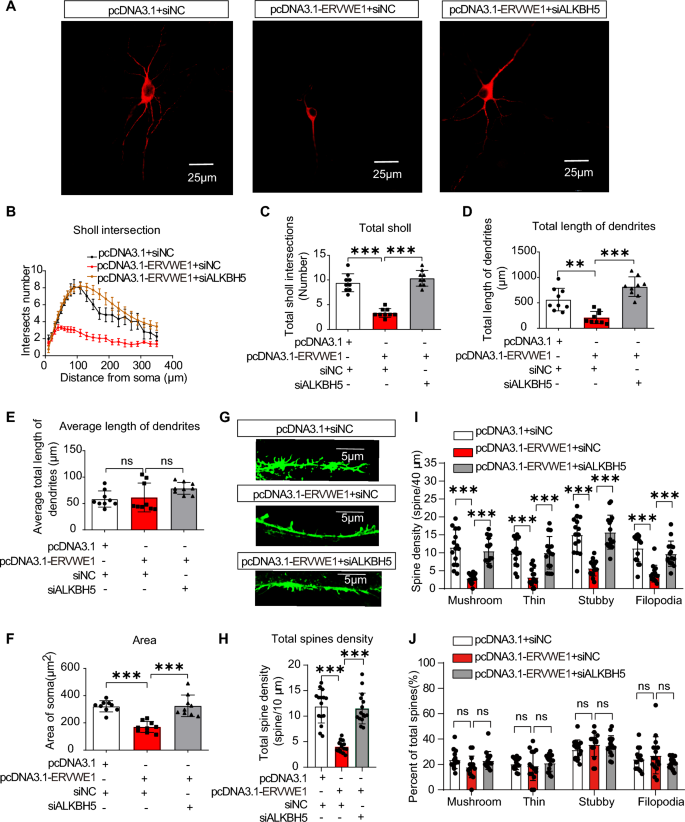
产品关联:文献未提及具体实验产品,领域常规使用免疫荧光试剂、共聚焦显微镜等。
4. Biomarker研究及发现成果解析
本文涉及的Biomarker包括HTR1B、ALKBH5、Arc,筛选与验证逻辑遵循“公共数据库生物信息学筛选→临床样本表达验证→细胞/神经元模型功能验证”的完整链条,确保Biomarker的临床相关性与功能学意义。
Biomarker的来源为首发精神分裂症患者的外周血样本(血浆与全血),验证方法涵盖ELISA检测血浆蛋白水平、RT-qPCR检测mRNA水平、Spearman相关性分析、多因素Logistic回归分析。特异性与敏感性方面,HTR1B血浆水平在患者中显著升高(p<0.001),与ERVWE1呈强正相关(文献未明确提供AUC、敏感性与特异性数据);ALKBH5血浆水平显著升高(p<0.001),多因素回归分析证实其为精神分裂症的独立风险因素(文献未明确提供OR值);Arc血浆水平显著升高(p<0.001),与HTR1B、ERVWE1均呈正相关。
核心成果方面,HTR1B可作为精神分裂症的潜在外周血Biomarker,其功能与5-HT神经元可塑性损伤直接相关;ALKBH5是首次被鉴定的精神分裂症独立风险基因,参与ERVWE1介导的m6A表观遗传调控网络;Arc作为突触可塑性核心蛋白,可反映精神分裂症患者的突触损伤程度。本研究的创新性在于,首次在精神分裂症患者中建立了ERVWE1与表观遗传修饰Biomarker(ALKBH5)、5-HT系统Biomarker(HTR1B)、突触可塑性Biomarker(Arc)的关联网络,为精神分裂症的早期诊断、预后评估及治疗靶点开发提供了新的候选分子。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。