NanoBRET in C. elegans illuminates functional receptor interactions in real time
秀丽隐杆线虫中的 NanoBRET 实时阐明了功能性受体的相互作用
| 期刊: | BMC Molecular and Cell Biology | 影响因子: | 2.400 |
| 时间: | 2022 | 起止号: | 2022 Jan 31;23(1):8. |
| doi: | 10.1186/s12860-022-00405-w | 方法学: | HTRF |
| 研究方向: | 微生物学 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:NanoBRET in C. elegans illuminates functional receptor interactions in real time;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:模式生物(秀丽隐杆线虫)分子细胞生物学、G蛋白偶联受体(GPCR)动态互作与定位研究。
蛋白-蛋白互作是所有生物体生理过程的分子基础,其动态变化、细胞内定位及受体-配体结合的研究是生命科学领域的核心方向,也是药物研发的关键靶点。生物发光共振能量转移(BRET)是研究这些过程的有力工具,其依赖供体酶催化底物产生的能量转移至邻近的荧光受体,无需外源激发光,背景干扰低。传统BRET技术已在体外广泛应用,但体外体系难以模拟体内复杂的生理环境,而体内BRET研究受限于底物生物利用度、信号组织穿透性等问题,在模式生物中的应用极为有限。
现有研究中,新一代纳米生物发光共振能量转移(NanoBRET)技术凭借更小的纳米荧光素酶(Nluc,19kD)标签、150倍于传统荧光素酶的发光强度,成为体外蛋白互作研究的主流工具,但尚未在秀丽隐杆线虫体内建立成熟的应用体系。秀丽隐杆线虫作为经典模式生物,具有完全透明、遗传操作简便的优势,已广泛用于基因功能和发育生物学研究,但现有蛋白互作检测技术如荧光共振能量转移(FRET)、双分子荧光互补(BiFC)均需激光激发,存在背景荧光高、通量低的局限,无法实现实时、无激发的动态蛋白过程监测。因此,本研究旨在建立秀丽隐杆线虫体内NanoBRET体系,填补模式生物体内实时蛋白互作与定位研究的技术空白,为GPCR等重要蛋白的体内功能研究提供新工具。
2. 文献综述解析
作者对领域内现有研究的分类维度为“技术平台发展-体内应用局限-模式生物技术缺口”三层逻辑,系统梳理了BRET技术的发展历程、体内应用的瓶颈,以及秀丽隐杆线虫作为模式生物的技术潜力与现有不足。
现有研究中,体外BRET技术已发展至NanoBRET阶段,其小标签、高发光的特性大幅提升了蛋白融合后的功能保留率与信号强度,可用于检测蛋白互作、构象变化、细胞内转运等多种过程;体内BRET研究主要集中于小鼠等大动物,通过注射标记细胞或配体实现信号检测,但存在组织穿透性差、操作复杂的问题;秀丽隐杆线虫的现有蛋白互作技术以FRET、BiFC为主,这些技术依赖激光激发,易产生光毒性与背景荧光,且无法实现实时动态监测。现有技术的局限性在于,体外研究无法还原体内复杂的蛋白网络与微环境,而线虫现有技术难以满足实时、无激发的动态蛋白过程研究需求,尤其是GPCR这类具有动态转运特性的蛋白。
本研究的创新价值在于,首次将NanoBRET技术拓展至秀丽隐杆线虫体内,通过优化样本处理方法与底物选择,解决了体内BRET的信号强度与稳定性问题,同时建立了旁观者NanoBRET体系用于蛋白定位研究,突破了现有模式生物蛋白互作技术的局限,为GPCR等重要蛋白的体内功能研究提供了可行的技术方案。
3. 研究思路总结与详细解析
本研究的整体框架为“技术体系建立-条件优化-功能验证-拓展应用”闭环,研究目标是构建秀丽隐杆线虫体内NanoBRET体系,核心科学问题是解决体内NanoBRET的信号检测瓶颈并验证其在GPCR研究中的应用,技术路线涵盖融合蛋白线虫株构建、发光信号优化、配体-受体互作检测、受体转运监测四个关键环节。
3.1 供体融合蛋白线虫株构建与发光信号优化
实验目的:构建表达Nluc融合GPCR的稳定转基因秀丽隐杆线虫株,优化体内发光信号的检测条件,为后续NanoBRET实验奠定基础。
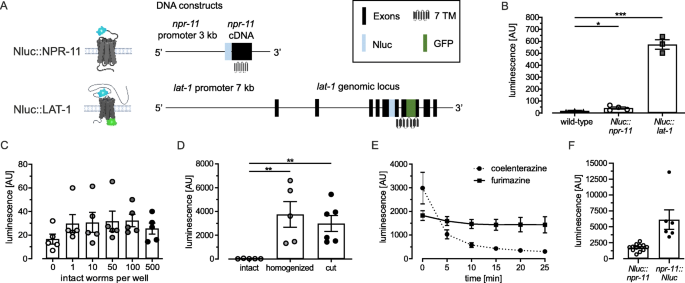
方法细节:通过分子克隆构建Nluc与神经肽受体NPR-11、黏附GPCR LAT-1的N端融合载体,利用显微注射技术将载体导入线虫性腺,获得稳定表达的转基因株;测试不同样本处理方式(完整线虫、体中部切割、机械匀浆)、不同底物(腔肠素H、furimazine)、不同线虫数量对发光信号强度与稳定性的影响,使用酶标仪检测发光信号。
结果解读:Nluc::NPR-11在完整线虫中的发光信号仅为野生型的2倍(n≥3,P<0.01),而切割或匀浆处理后信号提升至3000-4000 AU(n≥3,P<0.001),其中切割处理既能保证线虫细胞完整性,又能有效提升底物利用度;furimazine作为底物的信号稳定性显著优于腔肠素H,25分钟内信号无明显下降;Nluc在GPCR的N端或C端融合均能产生有效发光信号,提示融合位置对蛋白功能影响较小。
产品关联:文献未提及具体实验产品,领域常规使用Promega的NanoLuciferase载体、Sigma-Aldrich的化学试剂、PerkinElmer的酶标仪等。
3.2 荧光标记配体的制备与活性验证
实验目的:制备荧光标记的GPCR配体,验证其结合活性与体内组织分布特性,确保其可用于体内NanoBRET实验。
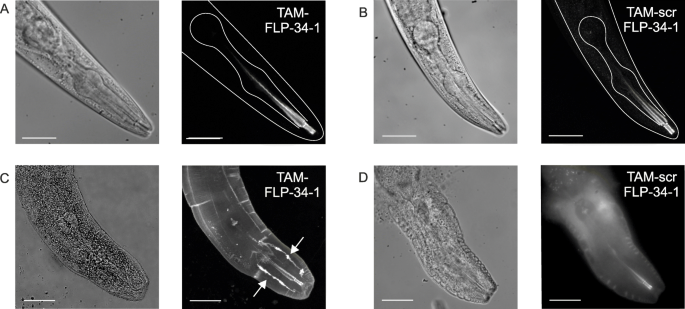
方法细节:采用固相肽合成法制备5(6)-羧基四甲基罗丹明(TAM)标记的FLP-34-1(NPR-11配体)、pLAT-1(LAT-1配体)及其 scrambled 对照肽;在HEK293细胞中通过NanoBRET结合实验验证标记肽的亲和力,通过cAMP报告基因实验验证其激活活性;利用共聚焦显微镜检测标记肽在秀丽隐杆线虫体内的分布。
结果解读:TAM-FLP-34-1在体外与NPR-11的解离常数Kd为388 nM,与未标记肽的抑制常数Ki(107 nM)接近,激活EC50为0.5 nM,与未标记肽活性相当;TAM标记的配体在完整线虫中仅分布于咽腔,而切割后的线虫中可扩散至假体腔,且TAM-FLP-34-1可特异性结合至特定结构,提示切割处理可提升配体的组织可及性;scrambled对照肽无特异性结合与激活活性。
产品关联:文献未提及具体实验产品,领域常规使用MultiSynTech的肽合成仪、Leica的共聚焦显微镜、PerkinElmer的cAMP检测试剂盒等。
3.3 体内配体-受体互作的NanoBRET检测
实验目的:利用优化后的NanoBRET体系,检测秀丽隐杆线虫体内GPCR与配体的特异性互作,验证体系的可靠性。
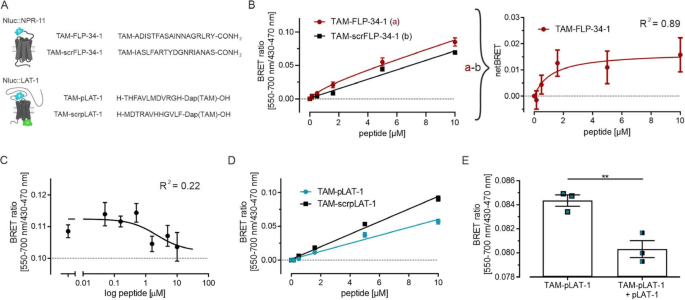
方法细节:将切割后的Nluc::NPR-11、Nluc::LAT-1转基因线虫与不同浓度的TAM标记配体共孵育25分钟,检测BRET信号;进行竞争结合实验,固定TAM标记配体浓度,加入梯度浓度的未标记配体,检测信号变化。
结果解读:TAM-FLP-34-1与NPR-11的体内解离常数Kd为1.4 μM,未标记FLP-34-1的抑制常数Ki为1.1 μM,提示特异性结合;未标记配体可有效置换标记配体,进一步验证了结合的特异性;TAM-pLAT-1与LAT-1的BRET信号随浓度升高持续增加,未达到饱和,Kd>10 μM,且scrambled对照肽也产生较强信号,提示低亲和力互作的检测存在非特异性干扰,需谨慎解读结果。
产品关联:文献未提及具体实验产品,领域常规使用Tecan的酶标仪、Promega的Nano-Glo Live Cell试剂等。
3.4 旁观者NanoBRET体系监测受体动态定位
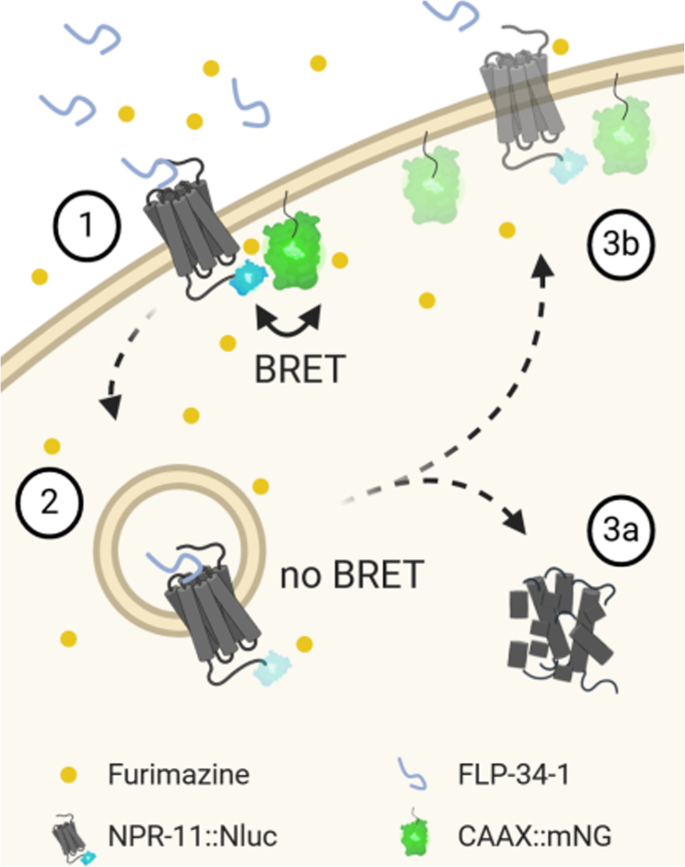
实验目的:建立旁观者NanoBRET体系,实时监测秀丽隐杆线虫体内NPR-11的配体诱导内吞与回收过程,拓展体系的应用范围。
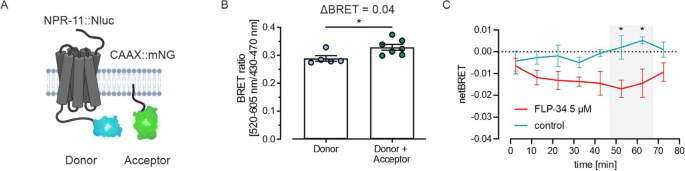
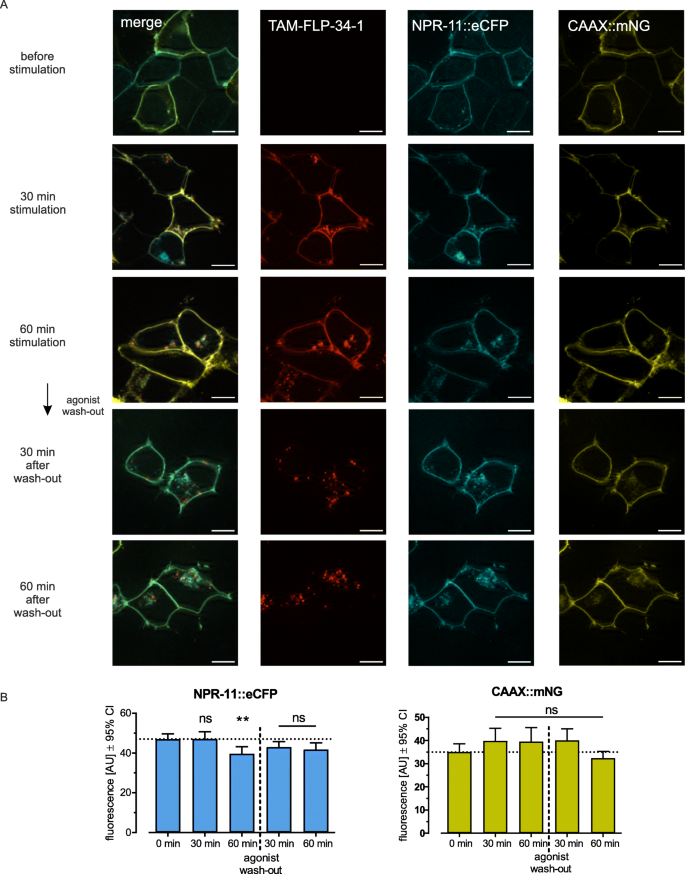
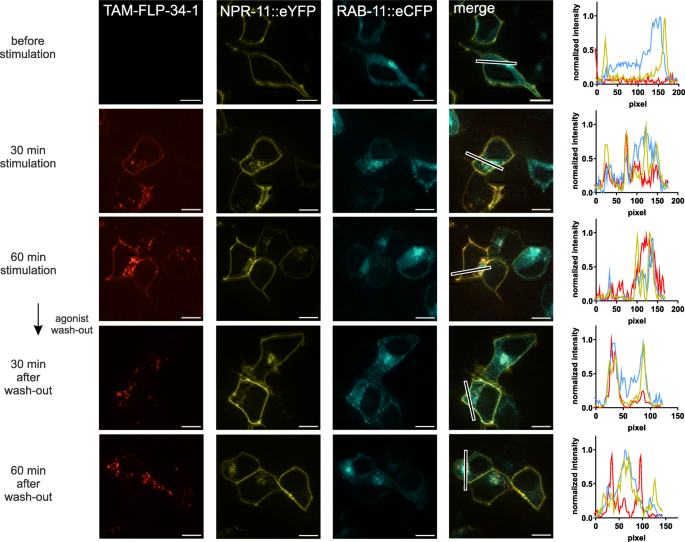
方法细节:构建同时表达NPR-11::Nluc(能量供体)与CAAX::mNG(细胞膜标记,能量受体)的双转基因线虫株;在配体FLP-34-1刺激前后,连续80分钟检测BRET信号变化;在HEK293细胞中通过荧光共定位实验,观察NPR-11与内体标记的共定位情况,验证体内结果。
结果解读:配体刺激后,BRET信号在50-70分钟显著下降(n≥3,P<0.05),提示NPR-11从细胞膜上内吞,与膜标记的距离增加;体外实验显示,NPR-11在配体刺激后与回收内体标记Rab11的共定位增强,而与溶酶体标记的共定位较弱,提示受体主要经历回收过程而非降解;信号在70分钟后逐渐回升,进一步支持受体回收至细胞膜的结论。
产品关联:文献未提及具体实验产品,领域常规使用Zeiss的成像系统、Leica的共聚焦显微镜等。
4. Biomarker研究及发现成果
本研究未涉及传统疾病诊断或预后Biomarker,而是建立了秀丽隐杆线虫体内NanoBRET技术体系作为动态蛋白互作与定位的检测工具,该体系可作为研究GPCR等重要蛋白体内功能的技术Biomarker平台,具有实时、无激发、背景低的优势。
Biomarker定位:本研究建立的线虫体内NanoBRET体系属于技术类Biomarker检测平台,其筛选/验证逻辑为:基于体外成熟的NanoBRET技术,在秀丽隐杆线虫体内优化信号检测条件,通过配体-受体互作实验验证体系的特异性,再拓展至蛋白动态定位研究,形成完整的技术验证闭环。
研究过程详述:该体系的技术来源为体外NanoBRET技术,通过在秀丽隐杆线虫体内构建Nluc融合蛋白转基因株、优化样本处理与底物选择,解决了体内BRET的信号强度与稳定性问题;验证方法包括发光信号优化实验、配体结合特异性实验、受体转运动态监测实验;特异性方面,高亲和力配体-受体对(FLP-34-1/NPR-11)可产生特异性BRET信号,未标记配体可有效置换标记配体,而低亲和力配体-受体对则存在非特异性信号干扰,提示体系对高亲和力互作的检测可靠性更高;时间分辨率方面,可实现80分钟内的连续信号监测,捕捉受体内吞与回收的动态过程。
核心成果提炼:本研究首次在秀丽隐杆线虫体内建立NanoBRET技术体系,实现了实时、无激发的蛋白互作与定位研究,为模式生物体内动态蛋白过程研究提供了新工具;该体系可用于研究GPCR的配体-受体互作与内吞回收,具有时间分辨率高、背景荧光低的优势,弥补了现有线虫蛋白互作技术的不足;研究同时明确了体系的局限性,即对低亲和力互作的检测存在非特异性干扰,需结合其他实验验证结果。该技术平台的建立为后续在模式生物中研究复杂蛋白网络的动态变化奠定了基础,具有重要的学术价值与应用潜力。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。
