GPR116 receptor regulates the antitumor function of NK cells via Gαq/HIF1α/NF-κB signaling pathway as a potential immune checkpoint
GPR116受体通过Gαq/HIF1α/NF-κB信号通路调节NK细胞的抗肿瘤功能,作为一种潜在的免疫检查点。
| 期刊: | Cell and Bioscience | 影响因子: | 6.100 |
| 时间: | 2023 | 起止号: | 2023 Mar 9;13(1):51. |
| doi: | 10.1186/s13578-023-01005-7 | 研究方向: | 细胞生物学、信号转导、肿瘤、免疫/内分泌 |
| 信号通路: | NF-κB | ||
文献解析
1. 领域背景与文献引入
文献英文标题:GPR116 receptor regulates the antitumor function of NK cells via Gαq/HIF1α/NF-κB signaling pathway as a potential immune checkpoint;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:肿瘤免疫治疗(NK细胞免疫检查点及CAR-NK治疗优化)
肿瘤免疫治疗是当前恶性肿瘤治疗的核心前沿方向,嵌合抗原受体T细胞(CAR-T)疗法已在血液系统肿瘤中取得突破性疗效,但存在细胞因子释放综合征(CRS)、神经毒性等严重不良反应,且对实体瘤的治疗效果仍存在瓶颈。自然杀伤(NK)细胞作为先天免疫的核心效应细胞,具有无需抗原预激活、无移植物抗宿主病(GVHD)风险等独特优势,嵌合抗原受体NK(CAR-NK)细胞疗法成为实体瘤免疫治疗的新兴研究热点。G蛋白偶联受体(GPCR)是人类基因组中最大的细胞表面受体家族,约30%的FDA批准药物以其为靶点,黏附GPCR亚家族成员GPR116已被报道参与肺稳态维持、血管内皮功能调控及肿瘤进展等过程,但在免疫细胞尤其是NK细胞中的功能调控作用尚不明确。当前领域的核心研究空白是,缺乏针对NK细胞的特异性免疫检查点靶点以优化CAR-NK治疗效果,因此探究GPR116对NK细胞抗肿瘤功能的调控机制具有重要的学术价值与临床转化意义。
2. 文献综述解析
作者以“GPCR家族药物靶点价值→黏附GPR116非免疫组织功能→NK细胞肿瘤免疫作用→CAR-NK治疗挑战”为逻辑主线,系统梳理领域研究现状,明确GPR116在NK细胞中功能调控的研究空白,为本文研究提供理论依据。
作者首先综述了GPCR作为药物靶点的核心地位,黏附GPCR亚家族的结构特点与组织分布,指出GPR116在肺、血管内皮、肾脏等组织中参与稳态维持与疾病进展,但在免疫细胞中的研究极为有限,仅部分文献推测其可能参与免疫调控。随后,作者阐述了NK细胞在肿瘤免疫监视中的核心作用,其活化受激活型与抑制型受体的平衡调控机制,以及CAR-NK疗法相较于CAR-T的优势与当前面临的疗效瓶颈。现有研究多聚焦于肿瘤细胞自身的GPR116功能,或NK细胞其他免疫检查点(如NKG2A、TIGIT)的调控,尚未涉及GPR116对NK细胞功能的直接调控。本文的创新价值在于,首次将GPR116与NK细胞抗肿瘤功能直接关联,揭示其作为NK细胞负调控免疫检查点的作用,并通过机制研究为CAR-NK治疗优化提供新策略,填补了GPR116在免疫细胞功能调控领域的研究空白。
3. 研究思路总结与详细解析
本文整体研究框架为“体内表型观察→体外功能验证→机制解析→临床转化应用”,核心科学问题是GPR116如何调控NK细胞的抗肿瘤功能,技术路线遵循“假设→实验验证→机制探究→转化应用”的闭环逻辑,通过体内外实验结合信号通路解析,明确GPR116的调控作用及分子机制,并验证其在CAR-NK治疗中的优化效果。
3.1 体内GPR116缺失对NK细胞抗肿瘤功能的影响
实验目的是验证GPR116全局缺失是否通过调控NK细胞功能抑制肿瘤生长。方法上,构建C57BL/6背景的GPR116敲除小鼠,皮下接种PAN02胰腺癌细胞建立移植瘤模型,流式细胞术(FCM)分析肿瘤组织及外周免疫器官中免疫细胞的比例与细胞因子表达水平。结果显示,GPR116敲除小鼠的肿瘤体积与重量显著低于野生型小鼠(n=5,P<0.01),肿瘤组织中NK细胞比例显著升高,且NK细胞中颗粒酶B(GzmB)和干扰素γ(IFNγ)的表达水平显著上调(P<0.001),而CD3+T、CD4+T、CD8+T细胞比例无显著变化,提示GPR116缺失主要通过增强NK细胞功能抑制肿瘤生长。
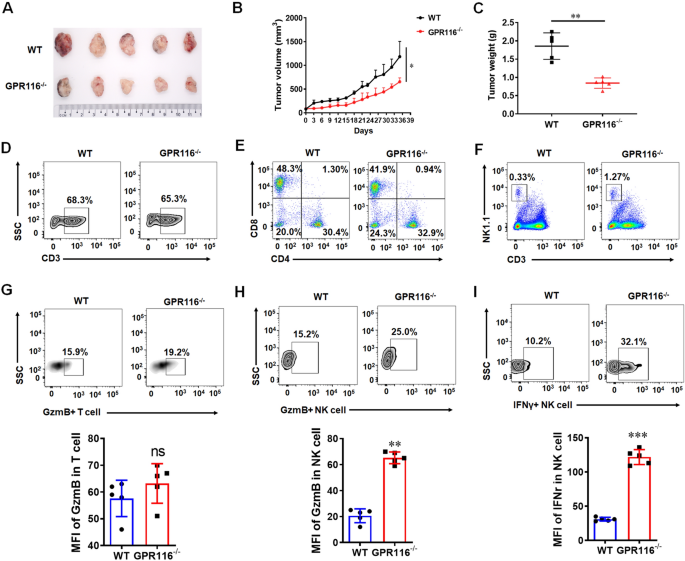
实验所用关键产品:流式抗体(抗小鼠CD3-PE、NK1.1-APC等,品牌Biolegend、eBioscience)、PAN02胰腺癌细胞系(ATCC)、细胞培养试剂(Life Technologies、Gibco)。
3.2 体外GPR116下调对NK细胞杀伤功能的影响
实验目的是明确GPR116与NK细胞活化的相关性及对杀伤功能的直接调控作用。方法上,用重组人IL-15激活NK92细胞,重组小鼠IL-15激活小鼠原代NK细胞,实时定量聚合酶链反应(qRT-PCR)检测GPR116的mRNA表达变化;通过慢病毒介导的shRNA敲低NK92细胞中GPR116的表达,流式细胞术检测其对K562靶细胞的杀伤活性,以及活化标志物CD107a、GzmB、IFNγ的表达。结果显示,NK细胞活化后GPR116的表达显著下调;GPR116敲低的NK92细胞在效靶比2.5:1和5:1时,对K562细胞的杀伤活性显著高于对照组(P<0.01),且CD107a、GzmB、IFNγ的表达水平显著上调(P<0.001),小鼠原代NK细胞敲除GPR116后也呈现类似功能增强效果,证明GPR116与NK细胞活化负相关,下调GPR116可增强NK细胞的杀伤功能。
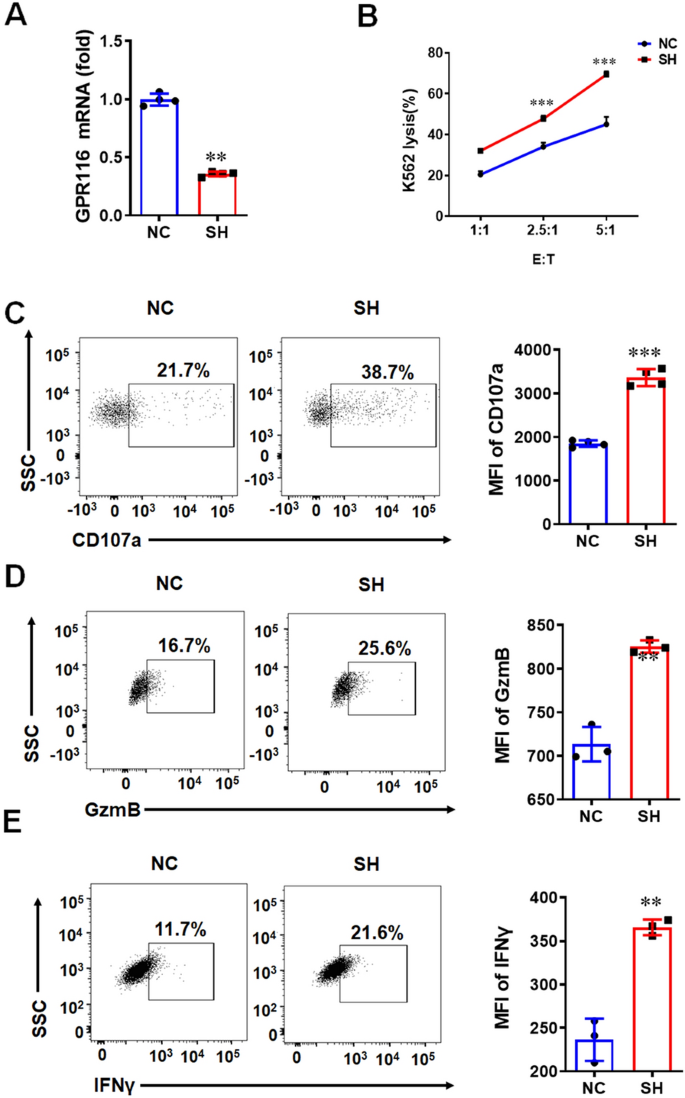
实验所用关键产品:慢病毒载体、qRT-PCR试剂(Takara)、重组IL-15(PeproTech)、流式抗体(抗人CD107a、GzmB等,品牌Invitrogen)。
3.3 GPR116调控NK细胞功能的信号通路解析
实验目的是解析GPR116调控NK细胞功能的下游分子机制。方法上,通过TIMER 2.0数据库分析GPR116与HIF1α的表达相关性;蛋白质免疫印迹(WB)检测GPR116敲低后NK92细胞中HIF1α、NF-κB通路分子(p-P65、总P65)的蛋白表达;使用NF-κB抑制剂QNZ处理细胞,验证NF-κB通路在功能调控中的作用;敲低Gαq表达,验证其作为GPR116下游信号分子的作用。结果显示,GPR116与HIF1α表达呈正相关;GPR116敲低后,NK92细胞中HIF1α表达下调,p-P65表达上调,NF-κB通路活化;抑制NF-κB通路后,GPR116敲低介导的NK细胞杀伤功能增强与细胞因子上调效应被逆转;敲低Gαq后,HIF1α表达下调、p-P65表达上调,NK细胞杀伤功能增强,与GPR116敲低效果一致,证明GPR116通过Gαq/HIF1α/NF-κB信号通路负调控NK细胞功能。
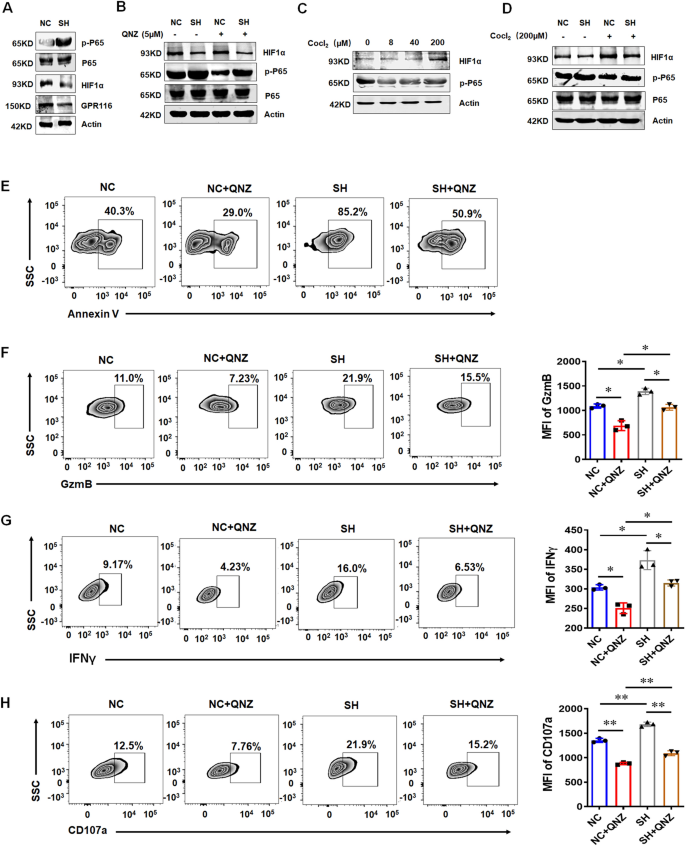
实验所用关键产品:WB抗体(抗HIF1α、p-P65、GPR116等,品牌CST、Abcam)、NF-κB抑制剂QNZ、慢病毒载体用于Gαq敲低。
3.4 GPR116缺失NK细胞的体内抗肿瘤功能验证
实验目的是在体内特异性验证GPR116缺失对NK细胞抗肿瘤功能的增强作用。方法上,给胰腺癌模型小鼠尾静脉注射PBS、野生型NK细胞或GPR116敲除NK细胞,定期监测肿瘤体积,实验终点分析肿瘤重量及肿瘤浸润免疫细胞的比例与功能。结果显示,注射GPR116敲除NK细胞的小鼠肿瘤体积与重量显著低于野生型NK细胞处理组(n=4,P<0.01),肿瘤组织中NK细胞比例显著升高,且GzmB、IFNγ的表达水平显著上调(P<0.001),进一步证实GPR116缺失可增强NK细胞的体内抗肿瘤功能。
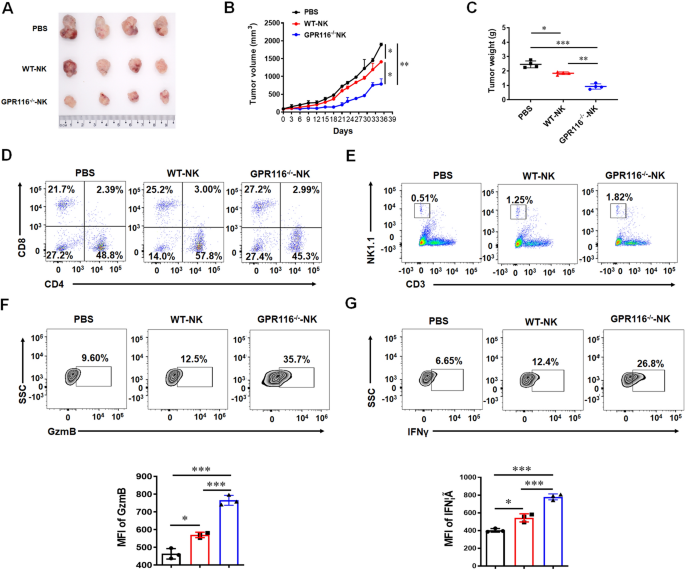
实验所用关键产品:小鼠原代NK细胞分离试剂盒(Invitrogen MagniSort、Miltenyi MACS)、流式抗体(抗小鼠NK1.1、GzmB等)。
3.5 GPR116下调优化NKG2D-CAR-NK细胞的抗肿瘤效果
实验目的是探索GPR116下调在CAR-NK临床转化中的应用价值。方法上,构建靶向NKG2D配体的CAR载体,通过慢病毒转染NK92细胞获得NKG2D-CAR-NK92细胞,同时敲低GPR116表达;流式细胞术检测CAR转染效率与GPR116敲低效果;体外共培养CAR-NK细胞与胰腺癌细胞(PANC28、PANC1、SW1990),检测杀伤活性与活化标志物表达;构建NSG小鼠胰腺癌异种移植模型,尾静脉注射CAR-NK细胞,评估体内治疗效果与安全性。结果显示,GPR116敲低的NKG2D-CAR-NK92细胞对高表达NKG2D配体的PANC28、PANC1细胞的杀伤活性显著高于对照组CAR-NK细胞(P<0.001),CD107a、GzmB表达水平显著上调;体内治疗后,GPR116敲低组小鼠肿瘤体积与重量显著降低(P<0.01),且小鼠体重无显著变化,证明治疗的安全性;机制上,GPR116敲低的CAR-NK细胞中HIF1α表达下调、p-P65表达上调,与之前的机制研究一致。
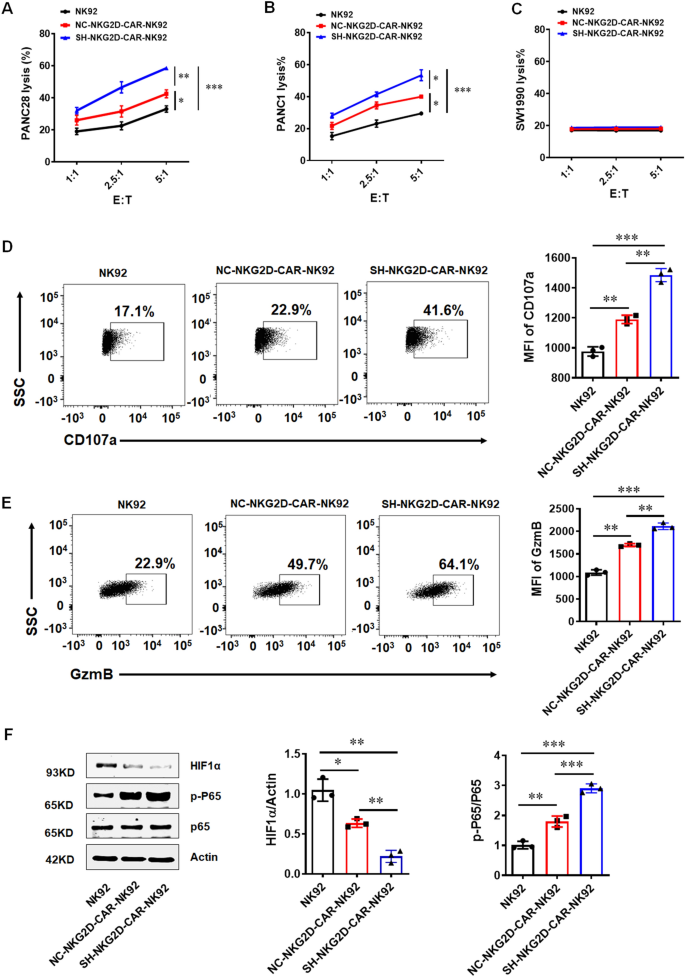
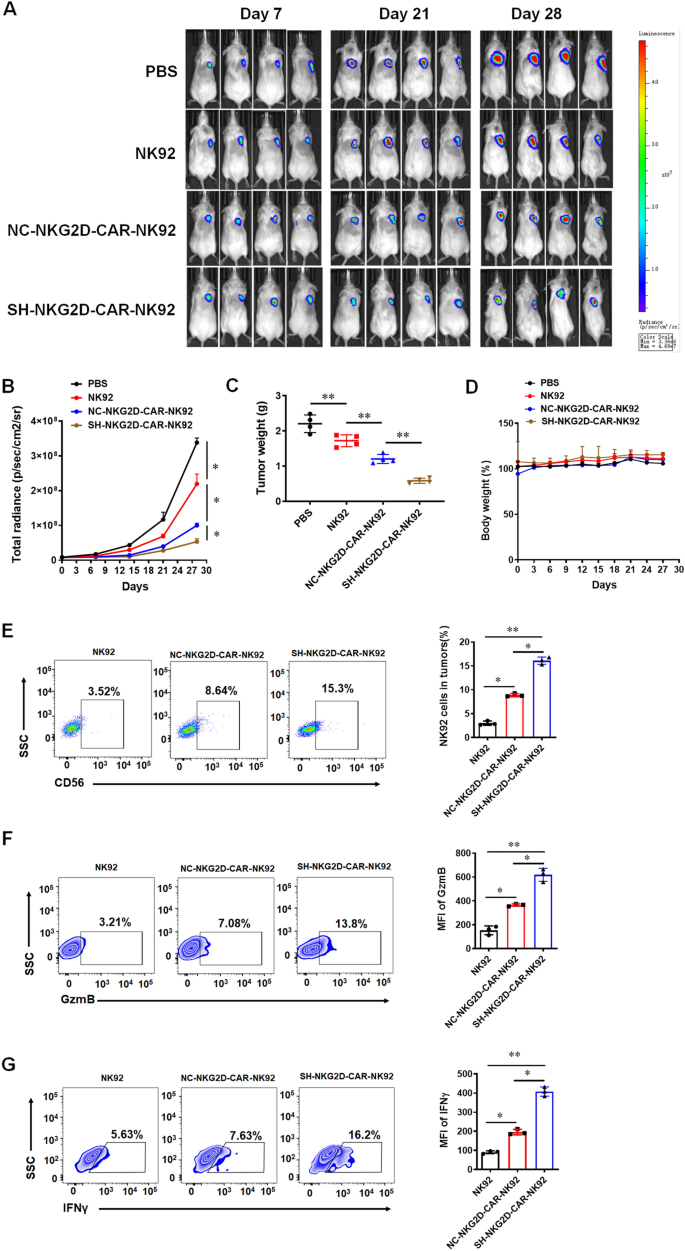
实验所用关键产品:NKG2D-CAR载体、慢病毒载体、流式抗体(抗人NKG2D、CD107a等)、NSG小鼠。
4. Biomarker研究及发现成果解析
本文发现的核心Biomarker为GPR116,属于NK细胞表面的抑制型免疫检查点Biomarker,其筛选与验证逻辑为“体内表型关联→体外功能验证→机制解析→转化应用验证”,通过多层面实验明确其作为NK细胞负调控因子的功能与临床应用潜力。
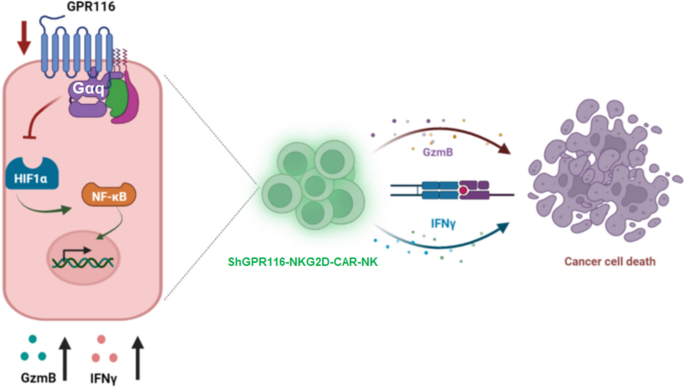
Biomarker定位方面,GPR116是NK细胞表面的黏附GPCR,作为抑制型免疫检查点负调控NK细胞的活化与抗肿瘤功能。筛选与验证逻辑为:首先通过GPR116敲除小鼠的肿瘤模型观察到NK细胞功能增强,随后通过体外NK细胞实验验证GPR116下调对杀伤功能的促进作用,再通过信号通路解析明确其分子机制,最后在CAR-NK细胞中验证其作为靶点的治疗优化效果。研究过程中,GPR116的来源为NK细胞表面受体,验证方法包括qRT-PCR与WB检测表达水平,流式细胞术检测细胞功能,体内肿瘤模型验证抗肿瘤效果;特异性方面,GPR116仅在NK细胞活化后表达下调,且其缺失仅影响NK细胞功能而对T细胞无显著调控作用;敏感性数据未明确提供,但功能实验中各组间差异具有显著统计学意义(P<0.05)。核心成果方面,GPR116通过Gαq/HIF1α/NF-κB信号通路抑制NK细胞的杀伤活性与细胞因子(GzmB、IFNγ)分泌,风险比相关数据未提供,但体内外实验均显示其缺失可显著增强NK细胞抗肿瘤功能;创新性在于首次揭示GPR116作为NK细胞免疫检查点的作用,为CAR-NK治疗优化提供了新的靶点与策略,具有重要的临床转化潜力。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。