ARNTL2 upregulation of ACOT7 promotes NSCLC cell proliferation through inhibition of apoptosis and ferroptosis
ARNTL2 上调 ACOT7 通过抑制细胞凋亡和铁死亡促进 NSCLC 细胞增殖
| 期刊: | BMC Molecular and Cell Biology | 影响因子: | 2.400 |
| 时间: | 2023 | 起止号: | 2023 Mar 31;24(1):14. |
| doi: | 10.1186/s12860-022-00450-5 | 研究方向: | 信号转导、细胞生物学 |
| 细胞类型: | 其它细胞 | 信号通路: | Apoptosis |
文献解析
1. 领域背景与文献引入
文献英文标题:ARNTL2 upregulation of ACOT7 promotes NSCLC cell proliferation through inhibition of apoptosis and ferroptosis;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:非小细胞肺癌分子机制与肿瘤增殖调控。
肺癌是全球范围内癌症相关死亡的首要原因,每年新增病例约200万,其中非小细胞肺癌占所有肺癌病例的85%。尽管靶向治疗(如EGFR抑制剂)和免疫治疗(如PD-1抗体)在部分患者中取得了显著疗效,但仍有大量患者无法获得持久响应,亟需挖掘新的肿瘤驱动基因与潜在治疗靶点。领域共识:昼夜节律基因的失调在多种恶性肿瘤的发生发展中发挥关键调控作用,核心节律基因如Clock、Period家族、Bmal1等的功能已被广泛报道,但其家族另一成员ARNTL2(又称Bmal2)在肿瘤中的作用尤其是非小细胞肺癌细胞增殖的调控机制尚未完全阐明。现有研究仅报道ARNTL2可促进肺腺癌的转移进程,但其调控非小细胞肺癌细胞生长与增殖的分子机制仍处于研究空白,这一现状凸显了本研究的学术必要性,旨在揭示ARNTL2在非小细胞肺癌中的致癌功能及下游调控通路,为开发新型治疗策略提供理论依据。
2. 文献综述解析
作者以昼夜节律基因在肿瘤中的作用、ARNTL2的已知致癌功能、ACOT家族成员的肿瘤调控作用为核心分类维度,系统梳理了领域内现有研究。现有研究关键结论显示,昼夜节律基因的异常表达参与多种肿瘤的进展过程,ARNTL2在肾透明细胞癌、结直肠癌、胰腺癌、乳腺癌中均被证实为致癌基因,可通过调控下游通路促进肿瘤的转移与侵袭;ACOT家族成员作为脂肪酸代谢的关键调控因子,不同成员在不同肿瘤中的作用存在异质性,如ACOT4促进胰腺癌发生,ACOT11在肺腺癌中高表达并促进细胞增殖,ACOT7在乳腺癌、急性髓系白血病、肝细胞癌中发挥癌基因功能。现有研究的技术方法优势在于多结合公共数据库分析与细胞功能实验验证基因的临床相关性与生物学功能,部分研究进一步通过分子机制实验明确调控通路;但局限性也较为明显,多数研究聚焦于ARNTL2对肿瘤转移的调控,对其影响细胞增殖的具体机制研究不足,同时ACOT7在非小细胞肺癌中的上游调控因子及对细胞死亡类型的调控尚未被报道。本研究的创新价值在于首次揭示了ARNTL2通过直接结合ACOT7启动子上调其表达,进而通过抑制非小细胞肺癌细胞的凋亡与铁死亡促进增殖的分子机制,填补了ARNTL2调控非小细胞肺癌细胞增殖机制的空白,同时明确了ACOT7在非小细胞肺癌中的致癌功能及新的调控靶点。
3. 研究思路总结与详细解析
本研究的核心目标是明确ARNTL2在非小细胞肺癌细胞增殖中的作用及分子机制,核心科学问题为ARNTL2如何通过下游靶基因调控非小细胞肺癌细胞的存活与增殖,技术路线遵循“公共数据库筛选→细胞功能验证→分子机制解析→通路rescue验证”的闭环逻辑,全面揭示了ARNTL2/ACOT7轴的致癌功能。
3.1 公共数据库分析与细胞增殖功能验证
实验目的是明确ARNTL2在非小细胞肺癌组织中的表达模式、与患者预后的相关性,以及对非小细胞肺癌细胞增殖的调控作用。方法细节上,基于TCGA数据库分析肺腺癌(LUAD)和肺鳞癌(LUSC)组织中ARNTL2的表达水平,将患者分为高、低表达组进行生存预后分析;检测人永生化正常肺细胞Beas-2B及非小细胞肺癌细胞系A549、H1299、H1975中ARNTL2的表达,选择ARNTL2低表达的H1299细胞进行过表达实验,高表达的A549细胞进行敲低实验,采用CCK8和克隆形成实验检测细胞增殖能力。结果解读显示,TCGA数据库分析表明ARNTL2在LUAD和LUSC组织中的表达显著高于正常组织(LUAD组织n=483,正常组织n=347,P<0.05);LUAD患者中ARNTL2高表达组的总生存期(P=0.00011)和无病生存期(P=0.019)均显著短于低表达组,而LUSC患者中未观察到显著相关性;细胞实验显示,ARNTL2过表达可显著促进H1299细胞的增殖与克隆形成能力(P<0.01),敲低则显著抑制A549细胞的增殖与克隆形成能力(P<0.01),证实ARNTL2是非小细胞肺癌的不良预后标志物并具有促增殖功能。
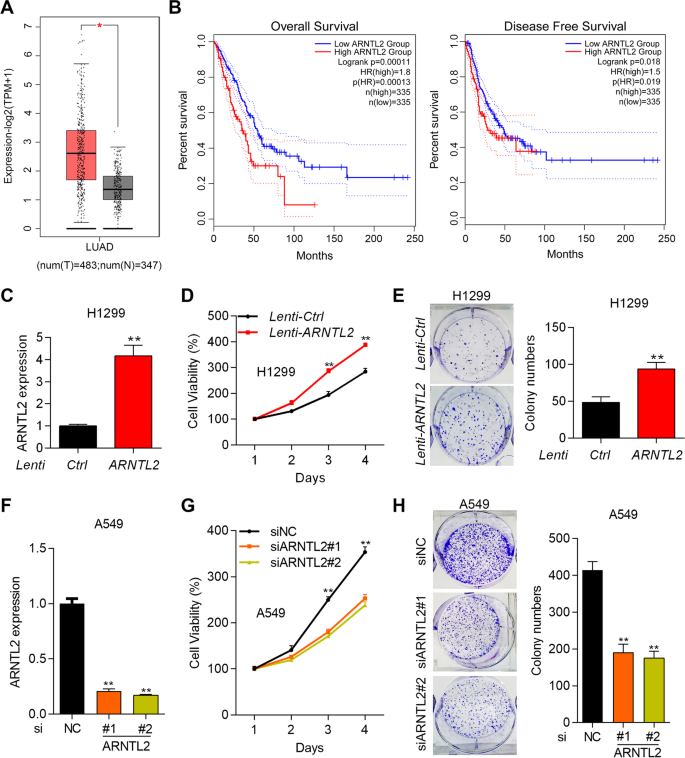
产品关联:实验所用关键产品:Trizol试剂、M-MLV逆转录酶(Promega)、SYBR master mixture(Takara)、CCK-8检测试剂盒(Beyotime)、siRNAs(Hippo Biotechnology)等。
3.2 ARNTL2调控ACOT7的分子机制验证
实验目的是明确ARNTL2是否直接调控ACOT7的转录表达。方法细节上,采用RT-qPCR和免疫印迹实验检测ARNTL2过表达或敲低后ACOT7的mRNA和蛋白表达水平;构建ACOT7启动子的荧光素酶报告载体,通过双荧光素酶报告实验验证ARNTL2对ACOT7启动子活性的影响;构建ARNTL2-Flag表达载体,利用ChIP-qPCR实验验证ARNTL2与ACOT7启动子的直接结合作用;基于TCGA数据库分析ARNTL2与ACOT7的表达相关性及ACOT7与LUAD患者预后的关系。结果解读显示,ARNTL2过表达可显著上调H1299细胞中ACOT7的mRNA和蛋白表达(P<0.01),敲低则显著下调A549细胞中ACOT7的表达(P<0.05);双荧光素酶报告实验表明ARNTL2过表达可增强ACOT7启动子的活性,敲低则降低其活性(P<0.05);ChIP-qPCR实验证实ARNTL2可直接结合ACOT7的启动子序列(P<0.001);TCGA数据库分析显示LUAD患者中ARNTL2与ACOT7的表达呈显著正相关(P<0.0001),ACOT7高表达组的总生存期显著短于低表达组(n=335/组,P=0.00096),证实ARNTL2通过直接结合ACOT7启动子上调其表达,且ACOT7也是LUAD的不良预后标志物。
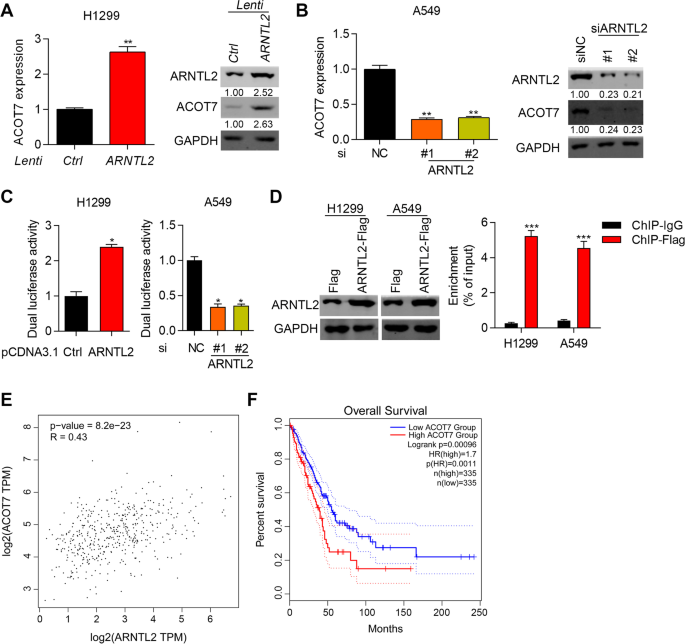
产品关联:实验所用关键产品:ARNTL2抗体(Sigma-Aldrich,SAB2100154)、ACOT7抗体(Proteintech,15972-1-AP)、双荧光素酶报告试剂盒(Promega)、SimpleChIP酶法染色质免疫沉淀试剂盒(Cell Signaling)等。
3.3 ACOT7对非小细胞肺癌细胞增殖与细胞死亡的调控
实验目的是明确ACOT7对非小细胞肺癌细胞增殖、细胞周期及细胞死亡类型的调控作用。方法细节上,在A549细胞中敲低ACOT7,在H1299细胞中过表达ACOT7,采用CCK8和克隆形成实验检测细胞增殖能力;通过PI染色流式细胞术检测细胞周期分布;采用PI/Annexin V染色流式细胞术检测细胞凋亡;利用C-11 BODIPY染色检测脂质ROS水平以评估铁死亡;采用caspase-Glo试剂检测caspase3/7的活性;使用铁死亡抑制剂Ferrostatin-1、凋亡抑制剂Z-VAD-FMK,以及铁死亡诱导剂Erastin、凋亡诱导剂AA2处理细胞,验证ACOT7对细胞死亡的调控作用。结果解读显示,ACOT7敲低可显著抑制A549细胞的增殖与克隆形成(P<0.01),过表达则显著促进H1299细胞的增殖与克隆形成(P<0.05、P<0.01);细胞周期分析显示ACOT7对非小细胞肺癌细胞的周期进程无显著影响;凋亡检测显示ACOT7敲低显著增加Annexin V+PI+细胞比例(P<0.05),过表达则降低该比例(P<0.05),且caspase3/7的活性与ACOT7表达呈负相关;铁死亡检测显示ACOT7过表达可抑制脂质ROS生成,敲低则促进脂质ROS生成(P<0.05、P<0.01);抑制剂与诱导剂实验显示,Ferrostatin-1或Z-VAD-FMK可部分逆转ACOT7敲低诱导的细胞死亡,联合使用可完全逆转;ACOT7过表达可显著挽救Erastin、AA2及联合处理诱导的细胞死亡,证实ACOT7同时抑制非小细胞肺癌细胞的凋亡与铁死亡。
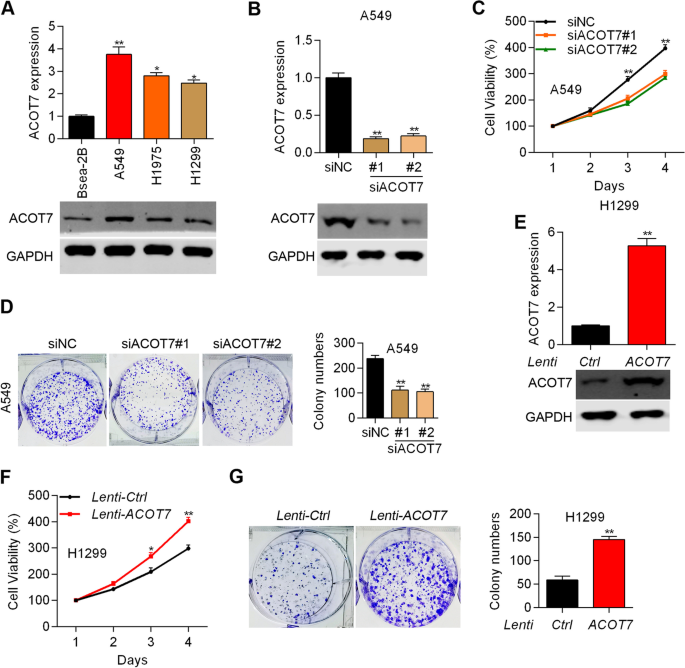
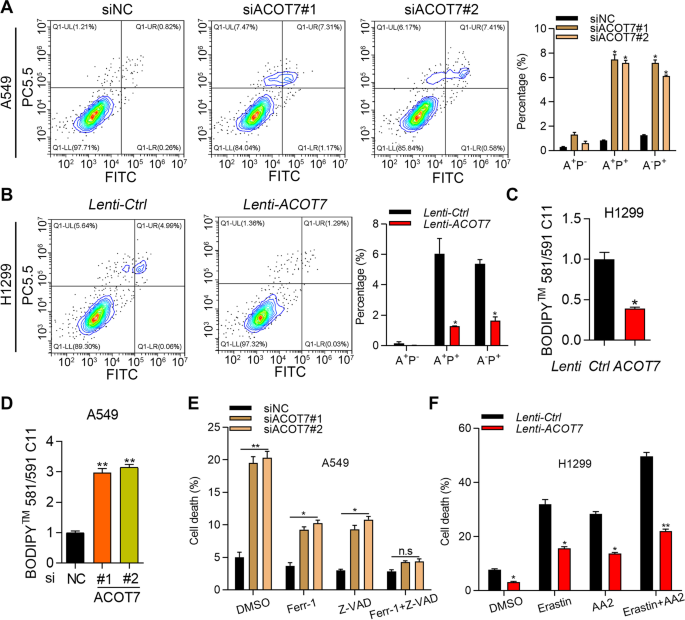
产品关联:实验所用关键产品:PI/Annexin-V染色试剂盒(YEASEN,40302ES20)、C-11 BODIPY染料(Invitrogen)、caspase-Glo试剂(Promega)、Ferrostatin-1(Selleck)、Z-VAD-FMK(Selleck)等。
3.4 ACOT7对脂肪酸代谢的调控及通路rescue验证
实验目的是明确ACOT7对非小细胞肺癌细胞脂肪酸代谢的影响,并验证ARNTL2通过ACOT7调控细胞增殖的核心通路。方法细节上,检测ACOT7过表达或敲低后细胞中MDA(丙二醛)、甘油三酯及多种脂肪酸(棕榈酸、棕榈油酸、硬脂酸、油酸)的水平;在ARNTL2敲低的A549细胞中过表达ACOT7,在ARNTL2过表达的H1299细胞中敲低ACOT7,检测细胞内甘油三酯水平和增殖能力。结果解读显示,ACOT7敲低可显著增加MDA、甘油三酯、油酸和棕榈油酸的水平(P<0.01、P<0.05),过表达则降低这些指标的水平(P<0.05、P<0.01),表明ACOT7调控单不饱和脂肪酸的合成与脂质过氧化过程;Rescue实验显示,ACOT7过表达可逆转ARNTL2敲低导致的甘油三酯水平降低和细胞增殖抑制(P<0.01),ACOT7敲低可逆转ARNTL2过表达导致的甘油三酯水平升高和细胞增殖促进(P<0.05、P<0.01),证实ARNTL2通过上调ACOT7促进非小细胞肺癌细胞增殖的核心通路。
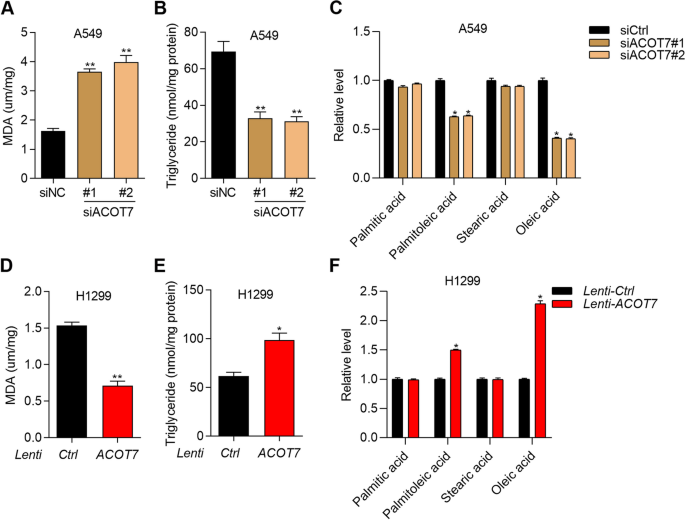
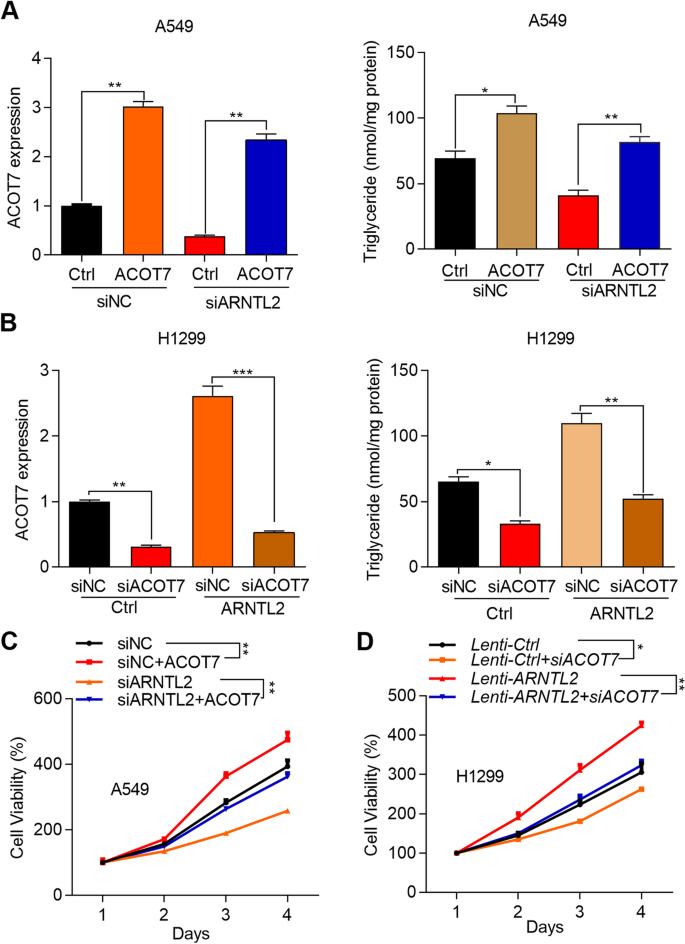
产品关联:实验所用关键产品:MDA检测试剂盒(Beyotime)、甘油三酯检测试剂盒(南京建成)等。
4. Biomarker研究及发现成果解析
本研究涉及的Biomarker为ARNTL2和ACOT7,均属于非小细胞肺癌(尤其是肺腺癌)的预后Biomarker,筛选与验证逻辑遵循“公共数据库筛选→细胞系表达验证→功能实验验证→分子机制验证”的完整链条。Biomarker的来源为TCGA数据库中的临床肿瘤组织样本及体外培养的非小细胞肺癌细胞系,验证方法包括TCGA数据库的生存分析、RT-qPCR与免疫印迹的表达验证、CCK8与克隆形成实验的功能验证、双荧光素酶与ChIP-qPCR的分子机制验证。特异性与敏感性数据方面,ARNTL2在肺腺癌组织中的表达显著高于正常组织(P<0.05),高表达组患者的总生存期和无病生存期显著短于低表达组(P=0.00011、P=0.019);ACOT7与ARNTL2的表达呈显著正相关(P<0.0001),高表达组患者的总生存期显著短于低表达组(P=0.00096),但未提供ROC曲线等特异性与敏感性的具体数值。核心成果提炼显示,ARNTL2和ACOT7均可作为肺腺癌的不良预后Biomarker,风险比(HR)未在原文中明确给出;本研究的创新性在于首次发现ARNTL2/ACOT7轴通过抑制非小细胞肺癌细胞的凋亡与铁死亡、调控脂肪酸代谢促进细胞增殖,为非小细胞肺癌的治疗提供了新的潜在靶点;所有关键实验结果均具有统计学显著性(P<0.05、P<0.01、P<0.0001),TCGA分析的样本量充足(如LUAD组织n=483,生存分析n=335/组),细胞实验结果稳定可靠。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。