The landscape of hervRNAs transcribed from human endogenous retroviruses across human body sites
人体各部位由人类内源性逆转录病毒转录的hervRNA图谱
| 期刊: | Genome Biology | 影响因子: | 9.400 |
| 时间: | 2022 | 起止号: | 2022 Nov 3;23(1):231 |
| doi: | 10.1186/s13059-022-02804-w | 研究方向: | 微生物学 |
文献解析
1. 领域背景与文献引入
文献英文标题:The landscape of hervRNAs transcribed from human endogenous retroviruses across human body sites;发表期刊:Genome Biology;影响因子:17.906(2022年);研究领域:人类基因组学、内源性逆转录病毒功能与疾病关联研究。
人类内源性逆转录病毒(HERVs)源于古代逆转录病毒对生殖细胞的整合,占人类基因组约8%,长期被视为“垃圾DNA”,在生理条件下多数因累积突变和宿主表观抑制而沉默。但近年研究揭示,部分HERVs在人类发育中发挥关键功能,如合胞素-1(ERVW-1编码)和合胞素-2(ERVFRD-1编码)参与胎盘形态发生中的细胞融合,HERV-H元件可调控基因表达程序并构建新型拓扑关联结构域。同时,HERVs的异常激活与多发性硬化、肌萎缩侧索硬化等复杂疾病相关。然而,现有研究多基于家族水平分析HERVs,无法解析位点特异性的转录调控与功能,也缺乏对生理条件下人体各部位HERVs表达全景的系统刻画,这一空白限制了对HERVs在发育与疾病中作用的深入理解。本研究通过优化基于组装的检测管道,构建了位点特异性的人体各部位HERVs生理表达图谱,为解析HERVs的生物学功能与疾病关联提供了全新视角。
2. 文献综述解析
作者对领域内现有研究按功能与技术维度分类评述:第一类聚焦HERVs在发育与疾病中的功能,核心结论包括HERVs在胎盘发育、干细胞调控中的不可或缺性,以及异常激活与神经退行性疾病、自身免疫病的关联;技术方法上,早期微阵列研究证实正常组织中存在HERVs表达,但分辨率有限,基于RNA-seq的比对方法虽提升了检测效率,却无法区分位点特异性转录本,易产生假阳性。第二类关注HERVs的调控机制,现有研究表明DNA甲基化在早期发育中抑制HERVs活性,组蛋白修饰参与其异常激活,但生理条件下的调控机制仍不清晰。
通过对比现有研究的局限性,本研究的创新价值凸显:首次采用基于转录组装的方法实现位点特异性HERVs转录本的准确鉴定,系统分析了42个人体部位的HERVs表达模式,结合遗传与表观组学数据解析其调控机制,并通过GWAS关联揭示了生理表达HERVs与复杂疾病的潜在联系,弥补了家族水平分析的不足,为HERVs的功能研究提供了高分辨率的全景图谱。
3. 研究思路总结与详细解析
本研究的核心目标是构建人体各部位生理表达的HERVs位点特异性图谱,解析其表达模式、遗传与表观调控机制及疾病关联;核心科学问题是生理条件下位点特异性HERVs的表达规律、调控网络及与复杂疾病的因果关联;技术路线遵循“方法优化→图谱构建→模式分析→调控解析→功能验证→疾病关联”的闭环逻辑。
3.1 位点特异性HERVs检测管道优化与实验验证
实验目的是开发并验证准确的位点特异性HERVs转录本鉴定方法。研究团队首先优化了基于转录组装的检测管道,先在1000 Genomes Project和GTEx项目的EBV转化淋巴细胞数据中测试,随后在人皮肤成纤维细胞(HSFs)中鉴定HERVs转录本,选取5个HERVs通过逆转录PCR(RT-PCR)结合桑格测序验证全长序列,另外5个通过实时定量逆转录PCR(RT-qPCR)验证表达水平。结果显示,管道鉴定的HERVs在不同数据集中表达一致性高,RT-PCR成功扩增出目标HERVs的全长序列,RT-qPCR结果与RNA-seq检测的表达水平高度吻合,证明该管道具备可靠的位点特异性HERVs检测能力。实验所用关键产品:Vazyme的FastPure® Cell/Tissue Total RNA Isolation Kit V2、HiScript® III 1st Strand cDNA Synthesis Kit (+ gDNA wiper)、Green Taq Mix、ChamQ Universal SYBR qPCR Master Mix;INTERFERin® transfection reagent(Polyplus)。
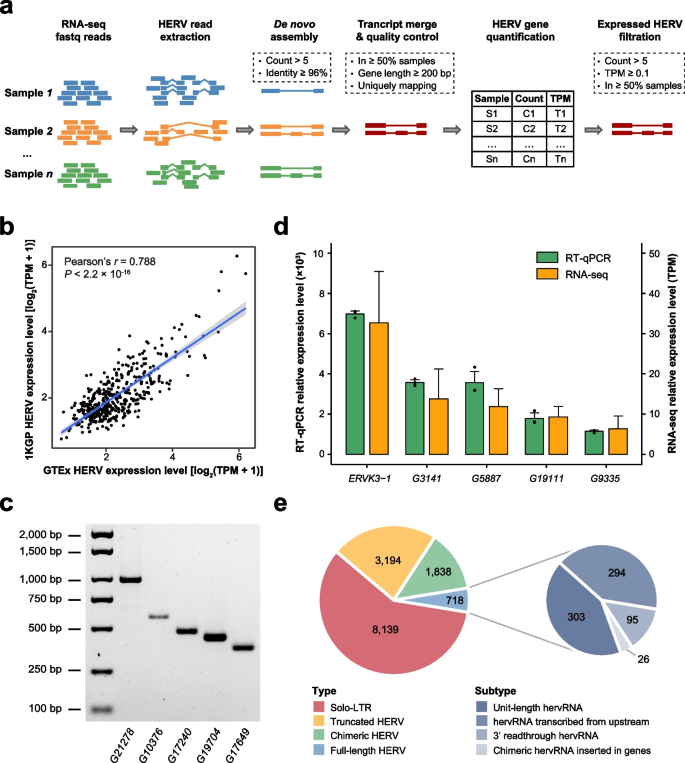
3.2 人体各部位HERVs转录组全景图谱构建
实验目的是系统鉴定人体各部位生理表达的位点特异性HERVs。研究团队分析了GTEx项目的9466个RNA-seq样本(覆盖42个人体部位、686个个体),通过优化后的管道共鉴定出13889个表达的HERVs(hervRNAs),并按基因组位置、HERVd数据库注释及编码潜能进行分类:按位置分为6681个反义转录本、4471个基因间转录本和2737个插入型转录本;按结构分为8139个单独长末端重复序列(solo-LTRs)、3194个截短型、1838个嵌合型和718个全长型,其中110个hervRNAs具备编码潜能。各部位hervRNAs数量差异显著,睾丸中最多(5035个),骨骼肌中最少(640个),小脑的表达量仅次于睾丸;hervRNAs占poly(A)尾转录本的0.19%-1.91%,中位表达水平显著高于长链非编码RNA(lncRNAs);其表达谱可准确区分不同人体部位,尤其是脑亚区的分辨率优于lncRNAs和蛋白编码基因。
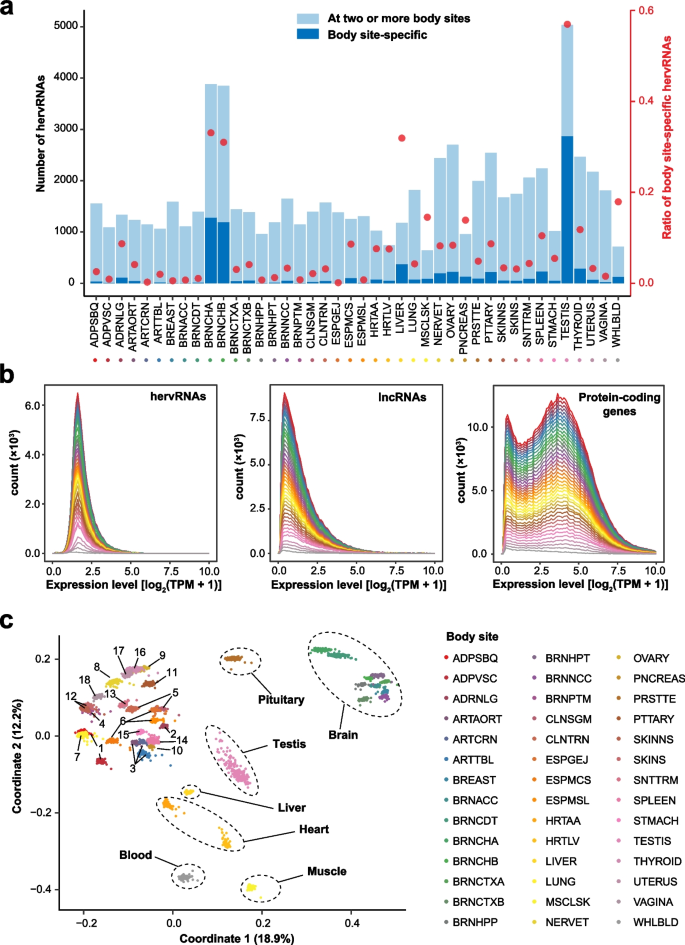
3.3 泛表达HERVs的功能验证
实验目的是探索泛表达HERVs的生物学功能。研究团队鉴定出在≥40个部位表达的127个泛表达hervRNAs,其表达水平显著高于其他hervRNAs(Wilcoxon秩和检验,FDR<0.05)。通过加权基因共表达网络分析,选取表达量最高的HERV_00001917进行敲低实验,在HSFs中转染靶向siRNA后进行RNA-seq分析。结果显示,敲低HERV_00001917后有2808个基因差异表达,这些基因显著富集于病毒应答、γ干扰素应答、NF-κB信号通路,提示该HERV在宿主免疫调控中发挥重要作用。
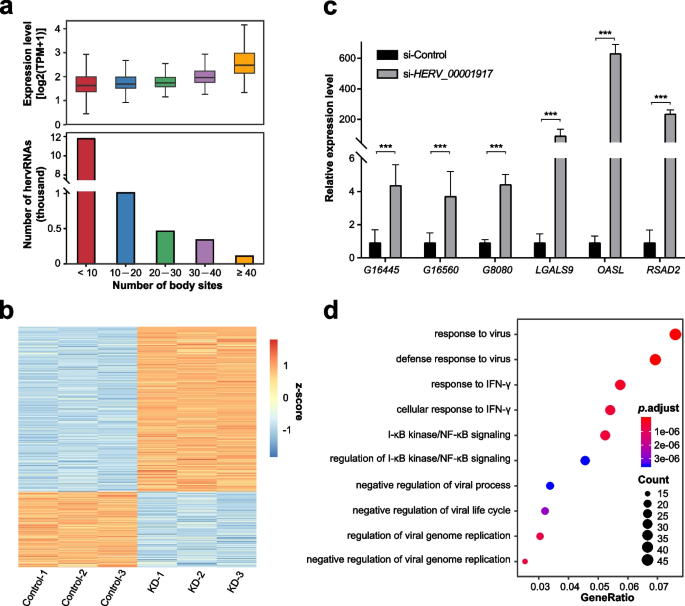
3.4 生物因素对HERVs表达的调控分析
实验目的是解析性别、种族、年龄对hervRNAs表达的影响。研究团队用DESeq2分析性别和种族差异,线性混合模型评估整体效应,皮尔逊相关分析年龄与表达的关联。结果显示,在37个非性别特异性部位鉴定到1095个性别差异hervRNAs,大部分富集于乳腺;脑特异性的HERV_00007673在男性6个脑亚区的表达显著高于女性(P<0.01)。鉴定到1604个种族差异hervRNAs,超过50%位于皮肤,其中51个属于HERV-K家族(与黑色素瘤进展相关);脑特异性的HERV_00003665在非裔美国人脑亚区的表达显著高于欧裔美国人。鉴定到3496个年龄相关hervRNAs,脑区尤其是海马体富集年龄相关下调的hervRNAs,如HERV_00001450在胶质母细胞瘤(GBM)样本中的表达显著低于正常样本(P<2.2×10^-16,n=165 vs n=5)。
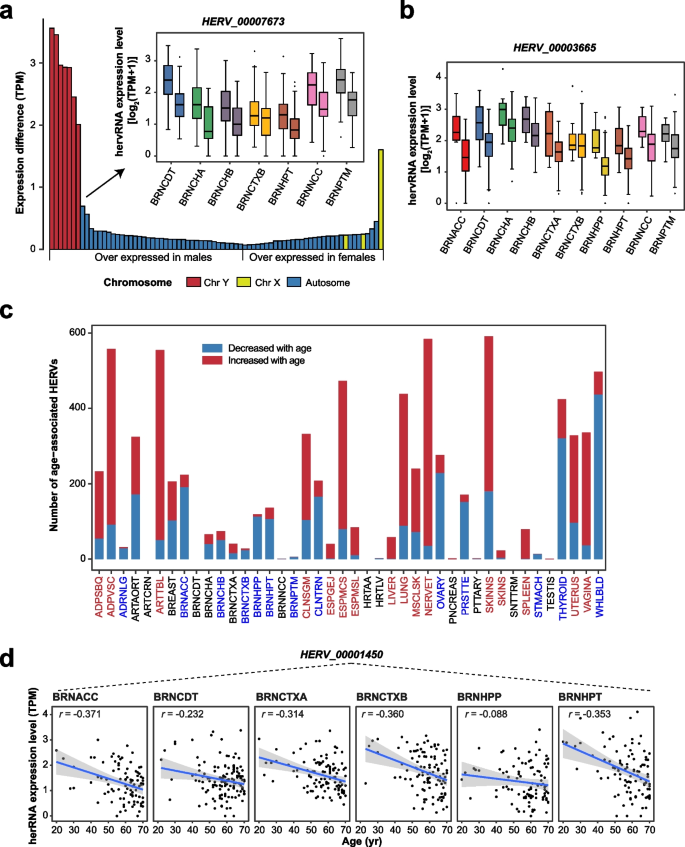
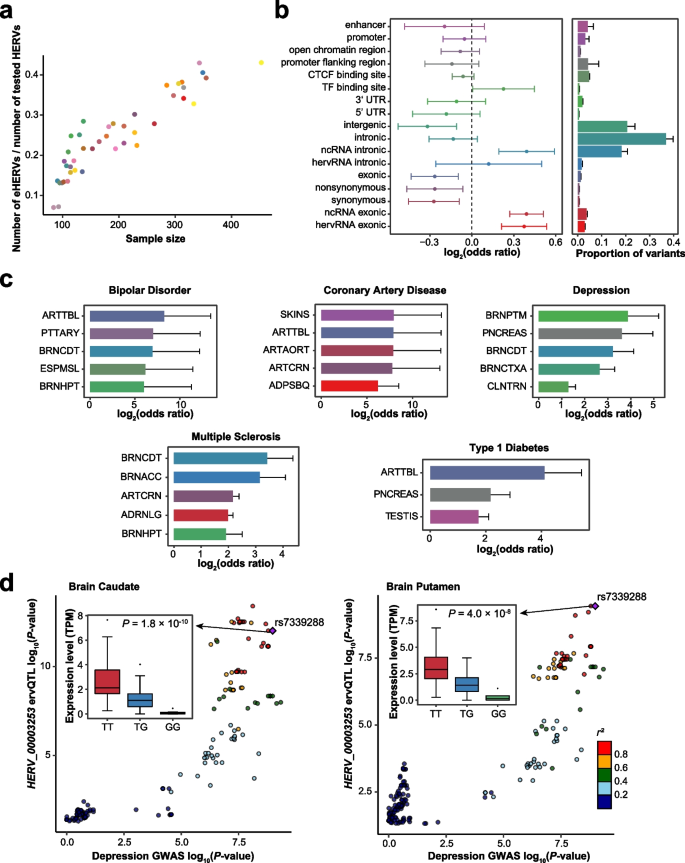
3.5 HERVs的遗传调控与疾病关联分析
实验目的是解析遗传变异对hervRNAs表达的调控及与复杂疾病的关联。研究团队对每个部位进行顺式ERV相关数量性状位点(cis-ervQTL)分析,共鉴定出451096个cis-ervQTLs,对应5435个受遗传调控的HERVs(eHERVs),且eHERVs显著富集于全长HERVs(P=0.011);功能注释显示,cis-ervQTLs主要富集于非编码RNA相关区域,而非剪接位点。结合22种复杂疾病的GWAS数据,富集分析表明hervRNAs失调与神经退行性疾病、精神疾病等密切相关,共定位分析鉴定出12个与疾病相关的位点特异性hervRNAs,如抑郁症相关的HERV_00003253仅在脑尾状核和壳核表达,与参与突触发生的B3GLCT基因呈反义方向。
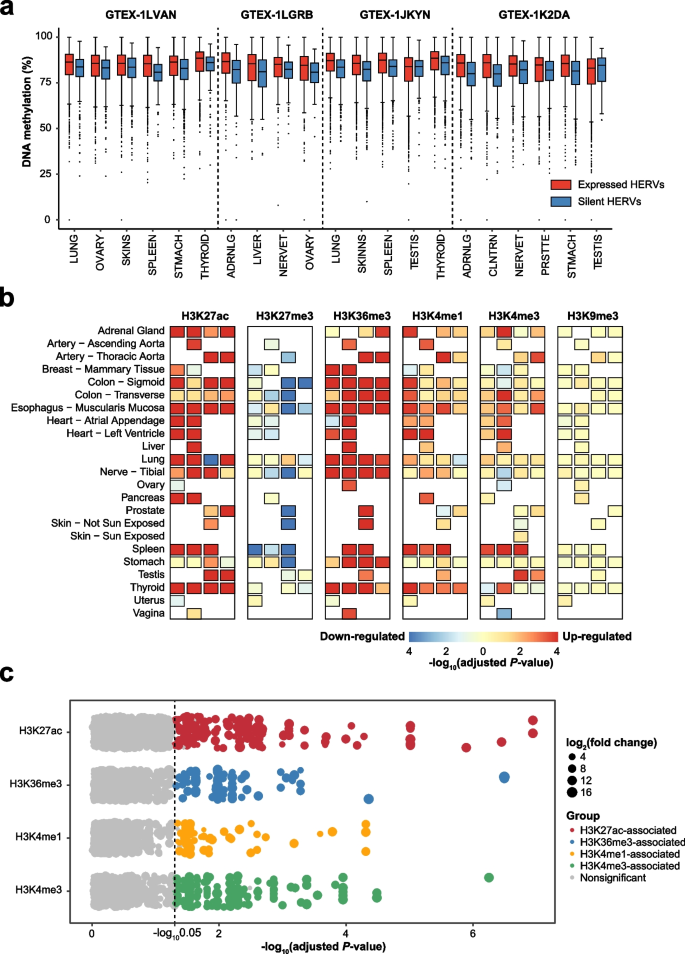
3.6 HERVs的表观调控机制解析
实验目的是探索生理条件下hervRNAs的表观调控机制。研究团队整合ENTEx项目的转录组与表观组数据,比较表达与沉默HERVs的DNA甲基化水平,分析组蛋白修饰与表达的关联。结果显示,生理表达HERVs的DNA甲基化中位水平超过80%,显著高于沉默HERVs(除睾丸外,P<0.01),提示DNA去甲基化不是生理表达的主要调控机制;而表达的HERVs与H3K27ac、H3K36me3等组蛋白修饰显著相关,334个HERVs受组蛋白修饰调控,且富集于嵌合型HERVs(P=4.2×10^-5)。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究筛选出的与复杂疾病相关的位点特异性hervRNAs,可作为潜在疾病Biomarker。筛选逻辑为:通过cis-ervQTL分析鉴定受遗传调控的HERVs,结合GWAS数据进行富集分析(P<5×10^-8)和共定位分析(后验概率PP4>0.9),锁定与疾病发病机制相关的位点特异性hervRNAs。
研究过程详述
这些Biomarker的来源为GTEx项目的正常组织转录组数据,验证方法包括GWAS富集分析、共定位分析及肿瘤样本与正常样本的表达差异验证。例如,与胶质母细胞瘤相关的HERV_00001450,在TCGA-GBM样本中的表达显著低于GTEx正常样本(P<2.2×10^-16,n=165 vs n=5);与抑郁症相关的HERV_00003253仅在脑尾状核和壳核表达,与该疾病的关键脑区高度关联,具备组织特异性。
核心成果提炼
本研究首次在位点特异性水平揭示了生理表达HERVs与复杂疾病的关联,发现多个潜在Biomarker:如HERV_00001450可作为胶质母细胞瘤的预后Biomarker,其表达下调与疾病进展相关;HERV_00003253可作为抑郁症的潜在Biomarker,参与突触发生相关的调控通路。这些Biomarker的创新性在于突破了传统家族水平分析的局限,为复杂疾病的诊断、预后评估及治疗靶点开发提供了全新的方向,其功能关联与调控机制的解析也为HERVs在疾病中的作用提供了直接证据。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。