Automated measurement of cell motility and proliferation
细胞运动性和增殖的自动化测量
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2005 | 起止号: | 2005 Apr 14;6(1):19 |
| doi: | 10.1186/1471-2121-6-19 | 研究方向: | 细胞生物学 |
文献解析
1. 领域背景与文献引入
文献英文标题:Automated measurement of cell motility and proliferation;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学-细胞运动与增殖自动化分析。
细胞的运动与增殖是生命活动的核心过程,参与免疫应答、肿瘤发生与转移、伤口愈合、组织再生及胚胎发育等众多生理病理事件,对其进行精准定量分析是揭示相关机制、开发干预策略的关键。领域共识:传统的细胞运动分析方法包括transwell实验、琼脂糖下迁移实验、伤口愈合实验等,其中时间 lapse 显微成像能直观反映细胞的动态行为,获取单个细胞的运动速度、轨迹持续性等细节信息,是细胞运动研究的金标准之一。然而,早期的时间 lapse 分析依赖手动追踪细胞轨迹,不仅耗时费力、通量极低,还易因实验人员疲劳引入主观偏差;已报道的半自动化分析方法仍需定制观测设备及手动交互步骤,限制了实验的变量数量、观察时长、重复次数及统计效能,无法满足大规模药物筛选或复杂因子组合研究的需求。当前领域的核心问题是缺乏一种全自动化、无偏差、高通量的细胞运动与增殖分析系统,能同时处理大量样本,提供稳定可靠的定量数据。
本研究针对这一空白,开发了一套全自动化的分析系统,可从384孔板中24/7自动获取图像并处理,生成高含量的细胞运动与形态学数据,旨在解决传统方法的局限性,为大规模细胞功能研究提供高效、精准的技术平台,其学术价值在于建立了细胞运动与增殖分析的新范式,推动该领域向高通量、标准化方向发展。
2. 文献综述解析
作者按细胞运动分析方法的技术类型对现有研究进行分类,涵盖传统终点法与动态成像法,重点评述了各类方法的优势、局限性及应用场景,明确了全自动化分析的必要性。
现有研究中,transwell实验因操作简便被广泛用于细胞迁移的批量检测,但其仅能提供群体细胞的迁移终点数据,无法反映单个细胞的动态运动过程;琼脂糖下迁移、软琼脂滴法、吞噬动力学轨迹实验等方法各有适用场景,但均存在通量低、操作复杂的问题;时间 lapse 显微成像虽能获取单个细胞的动态行为,但传统的手动追踪及半自动化分析存在效率低、偏差大的缺陷,且受限于定制设备,难以实现大规模样本的连续监测。已报道的半自动化系统仍需手动参与图像采集或数据处理步骤,易引入人为偏差,同时无法实现24小时不间断的实验监测,限制了实验的时间跨度与样本规模。
与现有研究相比,本研究的创新点在于首次实现了完全无需手动交互的细胞运动与增殖全自动化分析,系统可从384孔板中自动、连续地获取图像,通过自定义算法完成细胞分割、轨迹追踪及数据定量,不仅消除了人为偏差,还大幅提高了实验通量与时间跨度,能同时监测数百个样本的动态行为;此外,系统还提供了丰富的质量统计数据,可用于评估实验稳定性、过滤无效数据,为实验设计与质量控制提供依据,弥补了现有方法在数据可靠性与实验可扩展性上的不足。
3. 研究思路总结与详细解析
本研究的核心目标是开发并验证一套全自动化的细胞运动与增殖分析系统,解决传统方法的通量低、偏差大、操作复杂等问题;核心科学问题是如何实现无偏差、高通量的细胞动态行为定量分析,以及如何确保数据的准确性与可靠性;技术路线遵循“系统构建→模型验证→方法学评估→应用示范”的闭环逻辑,先搭建自动化成像与分析平台,再利用成骨细胞系验证系统的性能,通过与手动追踪比较评估方法准确性,最后应用于细胞外基质对细胞运动影响的研究,同时建立系统的质量控制体系。
3.1 细胞模型选择与培养
实验目的是选择具有成骨细胞表型的细胞系,验证自动化系统对不同细胞类型的适用性。方法细节:选用KM101人骨髓基质细胞系(具有成骨分化潜能,可分泌骨型碱性磷酸酶)与MG-63人骨肉瘤细胞系(具有成骨细胞特征,高表达1,25-(OH)₂D₃响应性碱性磷酸酶,合成骨钙素与I型胶原)作为实验模型;KM101细胞培养于含10%胎牛血清的Iscove改良Dulbecco培养基,MG-63细胞培养于含10%胎牛血清的Minimum Essential培养基,培养环境为37℃、5%CO₂的 humidified 培养箱;实验前用0.25%胰酶消化细胞,调整密度至2000个/ml,接种于384孔板,每孔加入60μl细胞悬液,初始视野内约5-15个细胞。产品关联:MG-63细胞购自ATCC,培养基、胰酶等试剂来自Gibco/Invitrogen;文献未提及具体实验抗体,领域常规使用细胞培养基础试剂、消化酶等。
3.2 细胞外基质包被处理
实验目的是通过不同细胞外基质的刺激,验证自动化系统对细胞运动响应的检测能力。方法细节:选用层粘连蛋白I、I型胶原、IV型胶原三种细胞外基质包被384孔板,对照组用无血清Iscove改良Dulbecco培养基进行模拟包被;层粘连蛋白I稀释于无血清培养基,I型胶原与IV型胶原稀释于无菌水,包被浓度为10μg/ml或100μg/ml,每孔加入10μl包被液,37℃孵育1小时;胶原包被的孔吸去液体后在超净台晾干20分钟,所有孔用培养基冲洗后接种细胞。产品关联:层粘连蛋白I与IV型胶原购自Cultrex,I型胶原购自Sigma,培养基来自Gibco/Invitrogen。
3.3 自动化成像与图像分析系统构建
实验目的是搭建全自动化的细胞成像与分析平台,实现无手动交互的图像获取与数据处理。方法细节:定制环境控制培养室,安装于Nikon TE300倒置显微镜的电动载物台(Ludl Electronics),通过反馈回路控制温度、湿度与CO₂浓度,避免玻璃窗口冷凝;采用Photometrics SenSys高分辨率CCD相机,每30分钟自动采集一次384孔板的图像;开发自定义软件,通过局部直方图均衡、各向异性滤波等步骤增强图像对比度,采用区域生长法分割细胞,利用概率匹配算法构建细胞轨迹,计算细胞运动(速度、轨迹长度、持续性等)与形态学(面积、周长、伸长率等)参数。结果解读:系统可自动识别并追踪单个细胞,生成的细胞轨迹显示,KM101细胞在层粘连蛋白包被表面的轨迹长度显著长于I型胶原、IV型胶原及对照塑料表面,表明其运动速度更快。
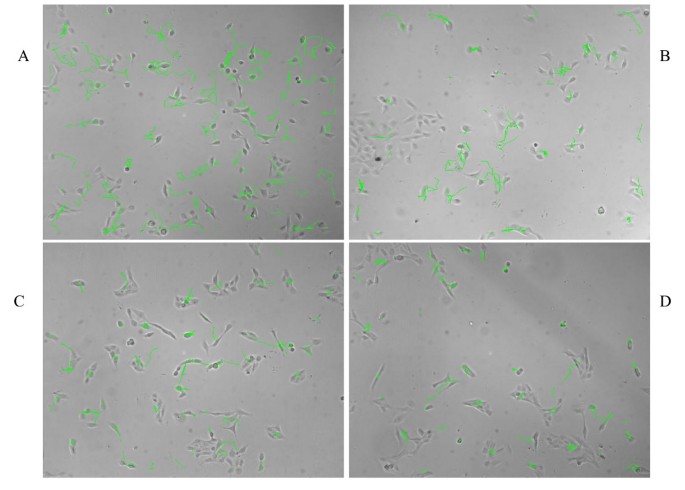
3.4 数据过滤与质量控制体系建立
实验目的是去除非细胞物体的干扰,提高数据的准确性与可靠性。方法细节:定义“fence size”为细胞在x或y方向的最大移动距离,通过手动评分确定20μm为阈值,过滤fence size≤20μm的轨迹(对应静止的非细胞物体);同时根据细胞面积过滤,仅保留面积在单个细胞范围内的物体(KM101细胞面积1200-3000平方微米,MG-63细胞面积1200-5800平方微米);当细胞汇合度超过30%时,停止速度测量以避免细胞间干扰。结果解读:过滤后的数据中,非细胞物体的占比降至10%以下,与手动追踪结果的一致性显著提高;3D轨迹可视化显示,静止物体的轨迹呈垂直直线,而活细胞轨迹呈随机游走;fence size过滤的有效性通过手动评分验证,20μm阈值可排除大部分非细胞物体,同时保留活细胞数据。
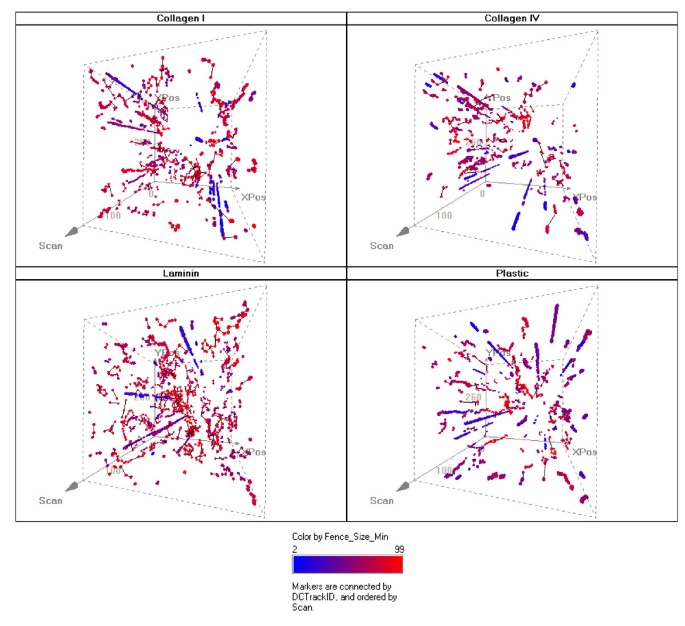
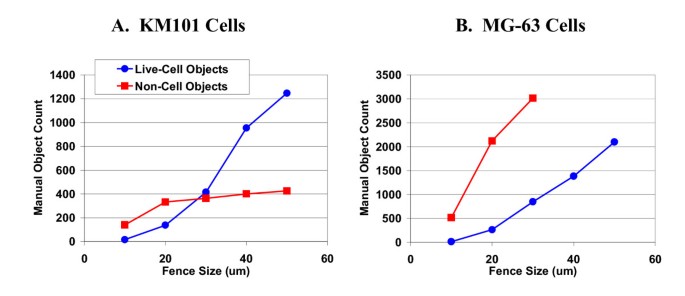
3.5 细胞运动的动力学与剂量反应分析
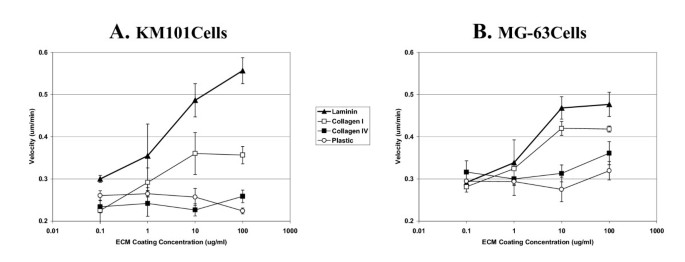
实验目的是分析细胞运动的时间动态及对细胞外基质浓度的响应。方法细节:在细胞接种后连续监测72小时,每4小时计算一次平均速度;设置不同浓度的细胞外基质包被(1μg/ml、10μg/ml、100μg/ml),分析细胞速度的剂量反应曲线。结果解读:KM101细胞在层粘连蛋白包被表面的速度随浓度增加而升高,每10倍浓度增加对应速度提升约0.1μm/min(n=3,P<0.0001);MG-63细胞在所有包被表面均呈现持续加速的趋势,而KM101细胞在对照塑料与IV型胶原表面的速度保持稳定或缓慢下降;剂量反应曲线显示,KM101细胞对层粘连蛋白的响应呈线性,对I型胶原的响应在10μg/ml时达到平台期。
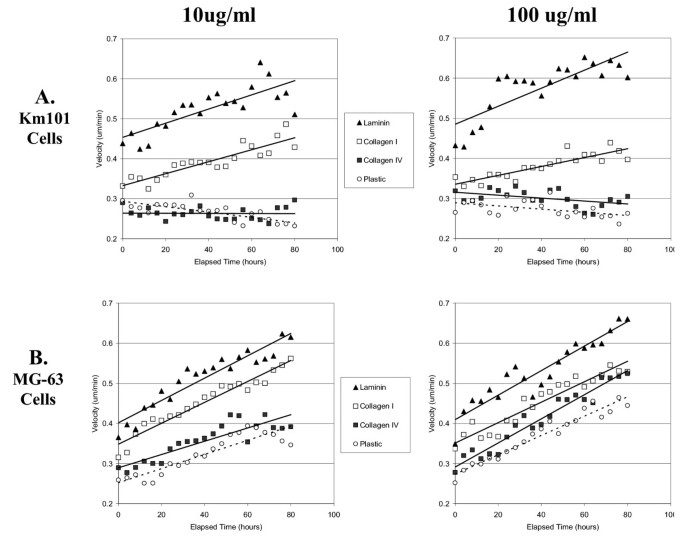
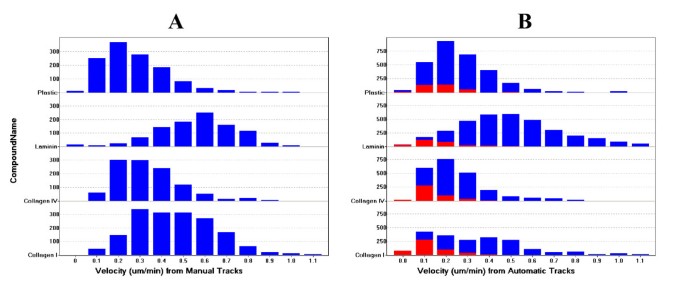
3.6 自动化与手动追踪的准确性比较
实验目的是验证自动化追踪方法的准确性与可靠性。方法细节:使用自定义程序手动追踪27个细胞的轨迹,记录细胞的x、y坐标;开发匹配算法,将自动化追踪的细胞位置与手动追踪的位置进行匹配,通过回归分析与精度计算比较两种方法的差异。结果解读:自动化追踪的速度分布与手动追踪高度相似,过滤非细胞物体后,两者的速度分布几乎完全重合;回归分析显示,自动化追踪与手动追踪的速度相关性系数r=0.81(P<0.0001),且自动化追踪的细胞位置更接近两次手动追踪的平均值,精度优于单独的手动追踪;手动追踪的精度为x方向1.91像素、y方向2.03像素,自动化追踪与手动追踪均值的精度为x方向1.87像素、y方向1.91像素,表明自动化方法的准确性不低于手动,且重复性更好。
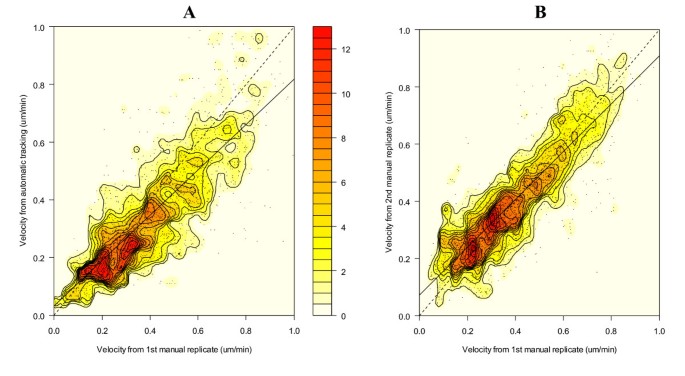
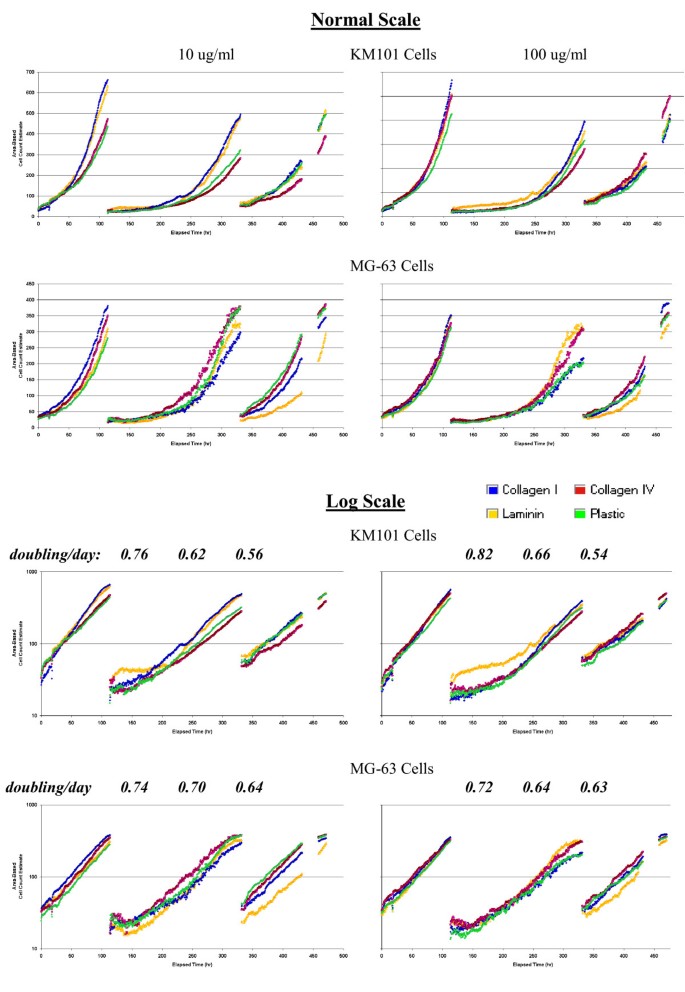
3.7 细胞增殖的自动化分析
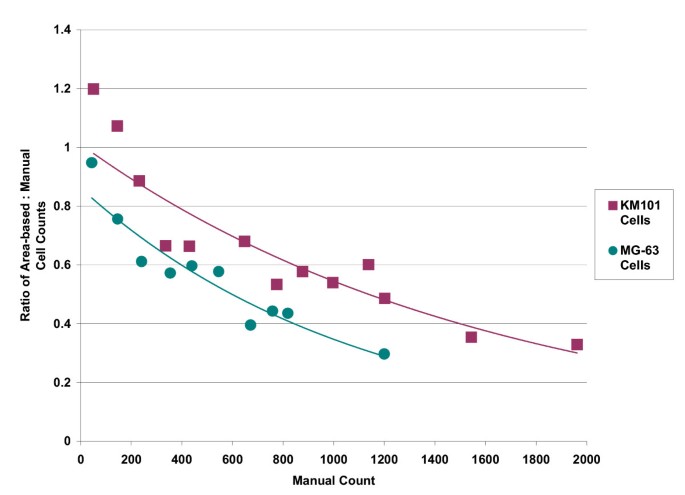
实验目的是验证自动化系统对细胞增殖的监测能力。方法细节:通过总细胞面积的变化监测细胞增殖,将总细胞面积除以单个细胞的平均面积估算细胞数;同时采用手动计数的方法,对90张不同汇合度的图像进行计数,比较自动化估算与手动计数的差异。结果解读:总细胞面积的对数增长呈线性,可用于估算细胞的倍增时间,但总细胞面积与绝对细胞数不呈线性相关,随着汇合度增加,自动化估算的细胞数逐渐低于手动计数;尽管如此,总细胞面积的变化仍能有效反映实验间的生长差异,可用于筛选可靠的追踪数据,评估实验的稳定性。
4. Biomarker研究及发现成果
本研究为方法学开发,未涉及疾病相关的传统Biomarker,但建立了细胞运动与增殖的定量功能指标,以及系统性能的质量控制Biomarker,为细胞功能研究与实验质量控制提供了标准化工具。
Biomarker定位:本研究的Biomarker分为两类,一是细胞运动与增殖的功能指标(如细胞速度、轨迹长度、总细胞面积),用于定量评估细胞的功能状态;二是系统性能的质量控制指标(如fence size、stage noise),用于评估数据的可靠性与系统的稳定性。筛选/验证逻辑:功能指标通过自动化成像与分析系统获取,通过与手动追踪比较验证准确性;质量控制指标通过数据过滤与系统性能测试确定,通过实验间的重复性验证可靠性。
研究过程详述:细胞运动功能指标来自384孔板的时间 lapse 图像,通过自动化分割与追踪算法得到单个细胞的速度(单位μm/min)、轨迹长度等参数,验证方法为手动追踪对比,特异性表现为fence size过滤后可去除90%以上的非细胞物体,敏感性可检测到0.1μm/min的速度变化;质量控制指标中,stage noise的标准偏差小于1像素(对应0.07μm/min的速度误差),fence size<20μm对应静止的非细胞物体,这些指标通过多次实验的重复性验证了可靠性。
核心成果提炼:建立了全自动化的细胞运动与增殖分析系统,可无偏差、高通量地获取细胞动态行为数据,其中KM101细胞在100μg/ml层粘连蛋白包被表面的平均速度比对照高0.2μm/min(n=3,P<0.0001),MG-63细胞在所有包被表面的速度随时间持续升高,72小时后比初始速度高0.3μm/min(n=3,P<0.0001);系统的质量控制指标可用于实验设计与质量控制,如fence size过滤可确保数据来自活细胞,stage noise评估可确保成像的稳定性;创新性在于首次实现了完全无需手动交互的384孔板细胞运动与增殖连续分析,解决了传统方法通量低、偏差大的问题,为大规模药物筛选、复杂因子组合研究提供了高效的技术平台。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。