S-nitrosothiols modulate G protein-coupled receptor signaling in a reversible and highly receptor-specific manner
S-亚硝基硫醇以可逆且高度受体特异性的方式调节G蛋白偶联受体信号传导。
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2005 | 起止号: | 2005 Apr 25;6(1):21 |
| doi: | 10.1186/1471-2121-6-21 | 研究方向: | 信号转导 |
文献解析
1. 领域背景与文献引入
文献英文标题:S-Nitrosothiols modulate G protein-coupled receptor signaling in a reversible and highly receptor-specific manner;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:G蛋白偶联受体(GPCR)信号转导调控、一氧化氮(NO)介导的蛋白质S-亚硝基化修饰。
G蛋白偶联受体(GPCR)是人体内最大的跨膜蛋白家族,参与几乎所有生理过程,是超过30%临床药物的作用靶点,其经典信号转导通路为激动剂结合后激活异源三聚体G蛋白,进而调控下游效应分子。随着研究深入,GPCR信号转导的复杂调控机制逐渐被揭示,其中活性氧物种(ROS)包括一氧化氮(NO)的翻译后修饰调控成为热点。NO的经典作用机制是激活可溶性鸟苷酸环化酶(sGC)产生环鸟苷酸(cGMP),而近年来非经典的S-亚硝基化修饰(即NO与蛋白质半胱氨酸残基的巯基结合形成S-亚硝基硫醇,RSNO)被证实可直接调控GPCR及其信号伙伴的功能。然而,此前的研究多聚焦于单个GPCR或特定细胞类型,缺乏对不同GPCR家族成员的系统性研究,核心空白在于RSNO对GPCR信号的调控是否具有受体特异性,以及其具体的分子靶点(受体本身或下游信号伙伴)和作用机制尚未明确。
针对这一研究空白,本研究系统探讨了RSNO对多种Gi/o偶联GPCR信号转导的调控作用,旨在明确其调控的受体特异性及潜在分子机制,为GPCR信号的氧化还原调控提供系统性的实验依据。
2. 文献综述解析
作者在综述部分以NO的作用机制为核心分类维度,梳理了NO经典cGMP通路与非经典S-亚硝基化通路的研究进展,同时围绕GPCR信号转导的氧化还原调控,总结了现有研究的成果与局限性。
现有研究证实NO可通过S-亚硝基化修饰GPCR或其下游信号分子(如G蛋白、调控蛋白等),影响GPCR的信号转导效率;部分研究发现RSNO可调控单个GPCR的活性,但未形成系统性的认知。此前的研究多采用细胞系异源表达系统或纯化蛋白,技术方法上的优势在于实验体系可控,但无法完全模拟GPCR在天然组织中的微环境;局限性则体现在缺乏对不同GPCR家族成员的横向比较,无法明确RSNO调控的受体特异性,同时对于RSNO的作用靶点是GPCR本身还是其天然信号伙伴的问题,尚未得到清晰解答,且具体的分子机制(如对G蛋白激活的影响)研究不足。
与现有研究相比,本研究的创新价值在于首次在天然组织和异源表达系统中系统性地研究了RSNO对多种Gi偶联GPCR的调控作用,明确了其高度受体特异性的调控模式;通过对比天然组织与异源表达系统的结果,区分了RSNO的作用靶点是GPCR本身还是下游天然信号伙伴;进一步揭示了RSNO增强M2/M4受体信号的具体分子机制,填补了该领域的系统性研究空白。
3. 研究思路总结与详细解析
本研究的整体目标是明确RSNO对Gi偶联GPCR信号转导的调控作用、受体特异性及分子机制,核心科学问题包括RSNO是否以受体特异性方式调控GPCR信号、其作用靶点是受体本身还是下游信号伙伴、以及具体的分子调控机制。技术路线遵循“筛选验证→靶点区分→机制解析”的闭环逻辑:首先利用脑冰冻切片的[³⁵S]GTPγS放射自显影筛选RSNO对不同GPCR的调控作用,随后通过膜结合实验验证结果并扩展受体类型,再通过CHO细胞异源表达系统区分作用靶点,最后通过时间响应实验和竞争结合实验解析分子机制。
3.1 脑冰冻切片中RSNO对GPCR信号的调控筛选
实验目的:系统性筛选RSNO对多种Gi偶联GPCR信号转导的调控作用,明确是否存在受体特异性,并验证调控作用的可逆性。
方法细节:选取4周龄雄性Wistar大鼠制备脑冰冻切片,采用[³⁵S]GTPγS放射自显影技术,实验分为三个步骤:20℃预孵育20min、GDP加载+RSNO(如GSNO、CysNO)处理60min、[³⁵S]GTPγS标记+受体激动剂刺激90min;同时加入二硫苏糖醇(DTT)或还原型谷胱甘肽(GSH)验证效应的可逆性,设置无RSNO处理的对照组。
结果解读:如图1所示,GSNO处理后,M2/M4毒蕈碱受体激动剂卡巴胆碱(CCh)刺激的G蛋白活性在脑干、纹状体、上丘浅层等受体富集区域显著增强,而P2Y₁₂嘌呤能受体激动剂2MeSADP和LPA₁受体激动剂LPA刺激的G蛋白活性则被显著抑制,且所有效应均可被DTT或GSH完全逆转,表明调控作用依赖于巯基修饰;图2显示GSNO的调控作用呈剂量依赖性,M2/M4受体在0.05mM GSNO时即出现响应,P2Y₁₂和LPA₁受体在0.2mM及以上浓度时被显著抑制;图3显示不同类型的RSNO(如CysNO、SNAP等)均能产生类似效应,而NO供体硝普钠(SNP)和cGMP类似物8Br-cGMP无显著作用,排除了经典cGMP通路的参与;图4显示腺苷A₁、μ阿片(MOR)、阿片相关受体(ORL1)的信号转导几乎不受GSNO影响,进一步证实了RSNO调控的高度受体特异性。
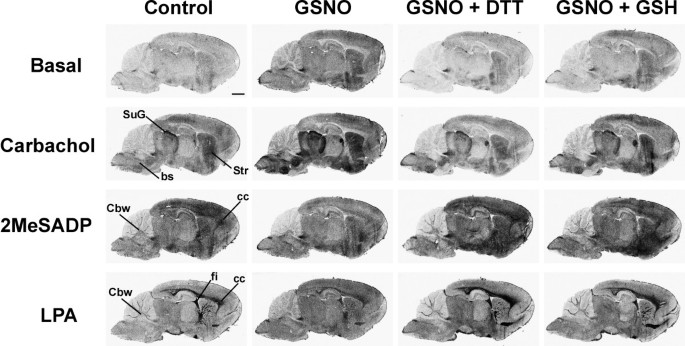
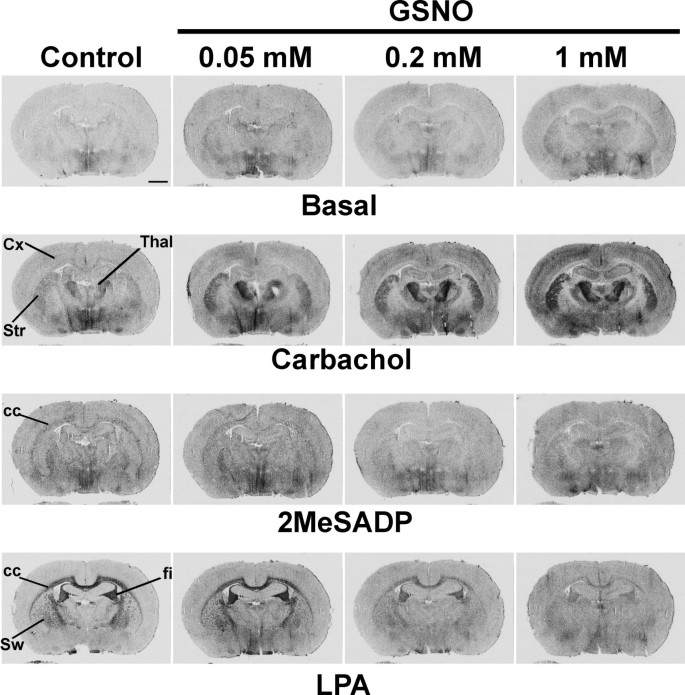
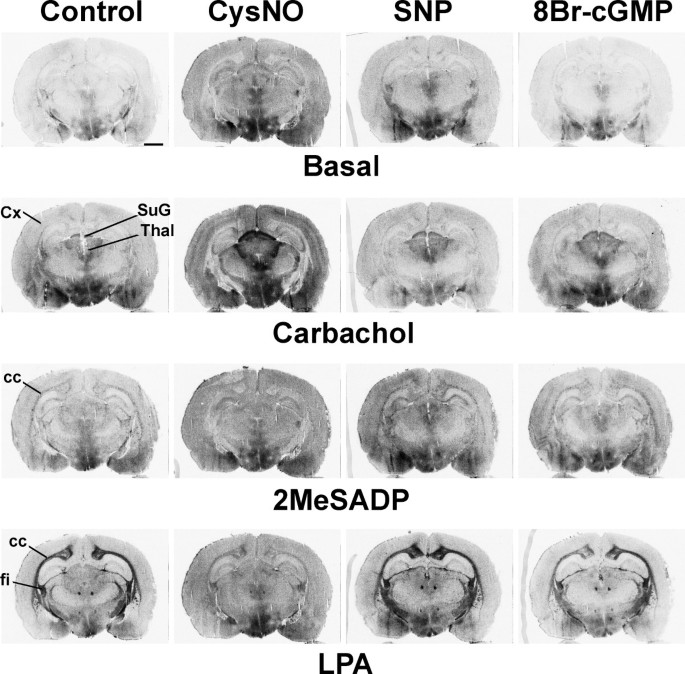
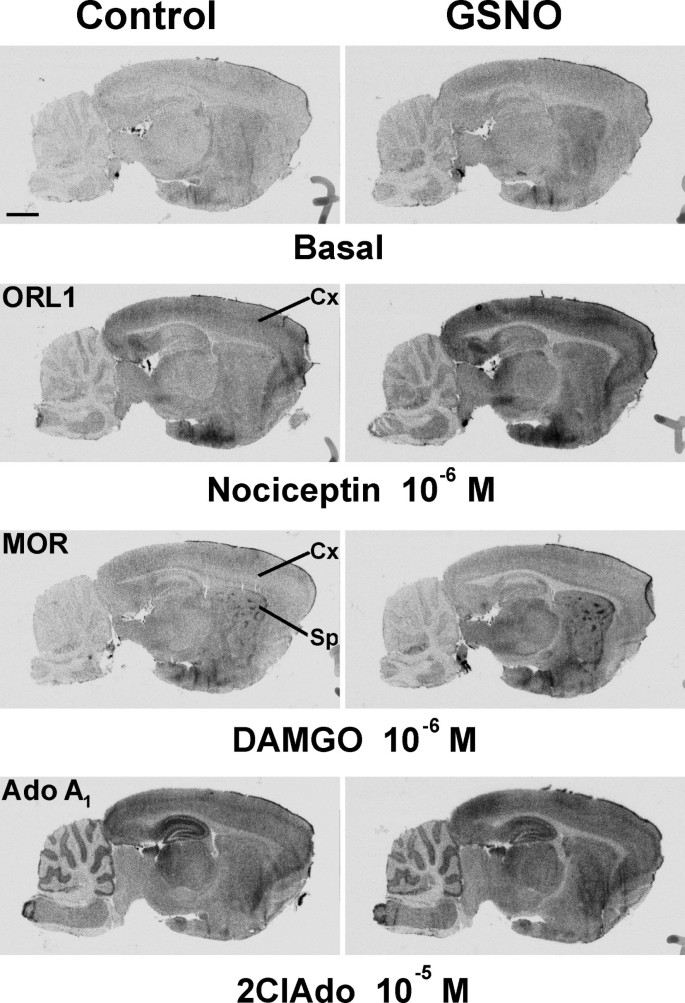
产品关联:文献未提及具体实验产品,领域常规使用放射性标记的[³⁵S]GTPγS、受体特异性激动剂/拮抗剂、组织冰冻切片制备设备、放射自显影成像系统等。
3.2 膜结合实验验证受体特异性调控
实验目的:在膜蛋白水平验证脑冰冻切片的实验结果,并扩展更多Gi偶联GPCR的研究范围,进一步明确RSNO调控的受体特异性。
方法细节:分别制备大鼠前脑膜、人血小板膜、CHO细胞裂解液,进行[³⁵S]GTPγS膜结合实验:膜样品预孵育GSNO 30min后,加入不同浓度的受体激动剂,孵育90min后通过过滤法分离结合的放射性配体,用液体闪烁计数器检测放射性强度;采用GraphPad Prism软件分析剂量响应曲线,计算激动剂的效能(Emax)和效力(EC₅₀)。
结果解读:与放射自显影结果一致,GSNO处理显著增强M2/M4毒蕈碱受体激动剂的效能和效力,而LPA₁受体和CB₁大麻素受体激动剂的效能显著降低,对腺苷A₁、MOR、ORL1受体的信号无显著影响;在人血小板膜中,GSNO抑制P2Y₁₂受体的信号转导,但显著增强α₂A肾上腺素能受体的信号;相关表格总结了不同GPCR在GSNO处理后的剂量响应参数变化,进一步量化了RSNO调控的受体特异性。
产品关联:文献未提及具体实验产品,领域常规使用膜蛋白制备试剂盒、液体闪烁计数器、数据分析软件等。
3.3 异源表达系统区分RSNO作用靶点
实验目的:明确RSNO的作用靶点是GPCR本身还是其天然细胞信号伙伴,通过对比天然组织与异源表达系统的结果进行区分。
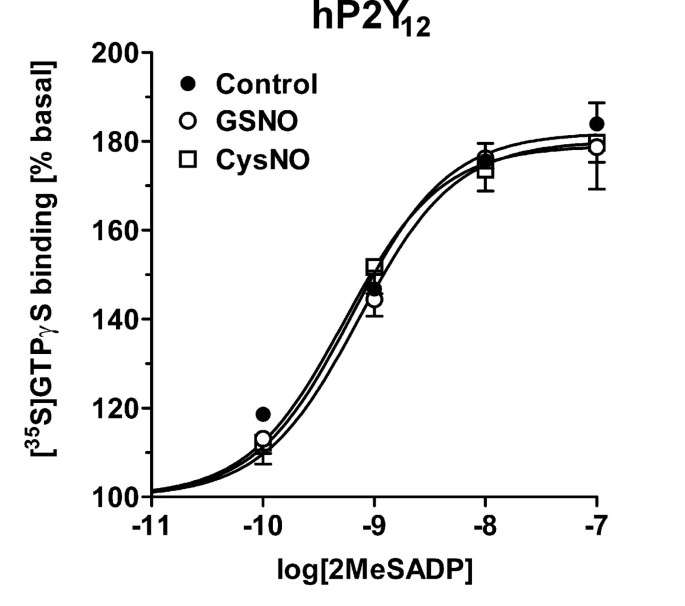
方法细节:在CHO细胞中稳定表达人P2Y₁₂受体、人M4毒蕈碱受体(野生型及C133S突变体,C133为潜在S-亚硝基化位点),制备细胞膜样品后进行[³⁵S]GTPγS膜结合实验,检测GSNO对激动剂刺激的G蛋白活性的影响,同时与天然组织(大鼠脑、人血小板)的结果进行对比。
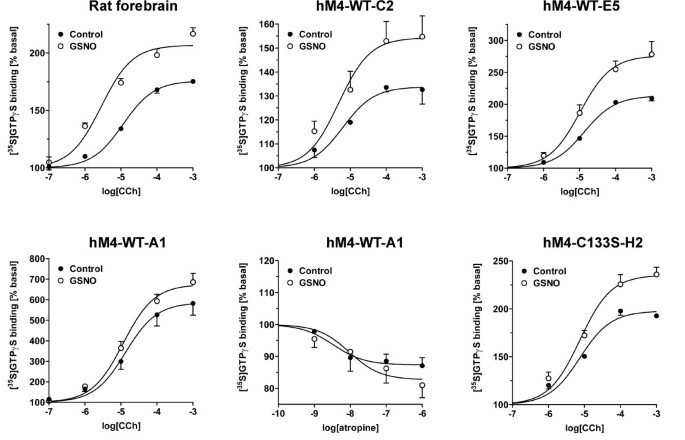
结果解读:如图5所示,GSNO对CHO细胞中异源表达的P2Y₁₂受体信号无显著影响,而在天然大鼠脑和人血小板中P2Y₁₂受体信号被显著抑制,说明RSNO的作用靶点是天然细胞中的信号伙伴而非P2Y₁₂受体本身;图8显示,GSNO处理显著增强野生型M4受体的信号效能,但在组成型激活的M4细胞系中该效应消失,且C133S突变体的信号仍能被GSNO增强,说明C133并非RSNO的作用靶点,且组成型激活的受体可能通过类似机制影响G蛋白活性。
产品关联:文献未提及具体实验产品,领域常规使用基因转染试剂、稳定细胞系筛选试剂、蛋白突变体构建试剂盒等。
3.4 RSNO调控M2/M4受体信号的机制研究
实验目的:解析RSNO增强M2/M4毒蕈碱受体信号转导的具体分子机制,明确其对G蛋白激活过程的影响。
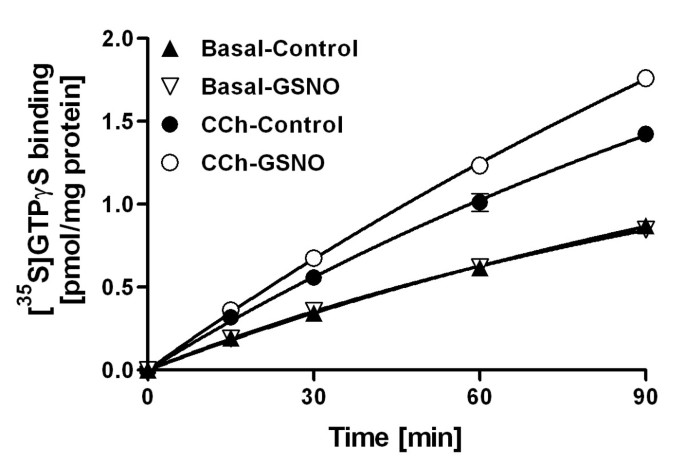
方法细节:采用大鼠前脑膜进行两个关键实验:①时间响应实验:预孵育GSNO后,检测不同时间点(15、30、60、90min)[³⁵S]GTPγS的结合量,分析G蛋白激活的动力学过程;②竞争结合实验:预孵育GSNO后,加入不同浓度的未标记GTPγS,检测[³⁵S]GTPγS的结合情况,分析高亲和力GTP结合位点的数量变化。
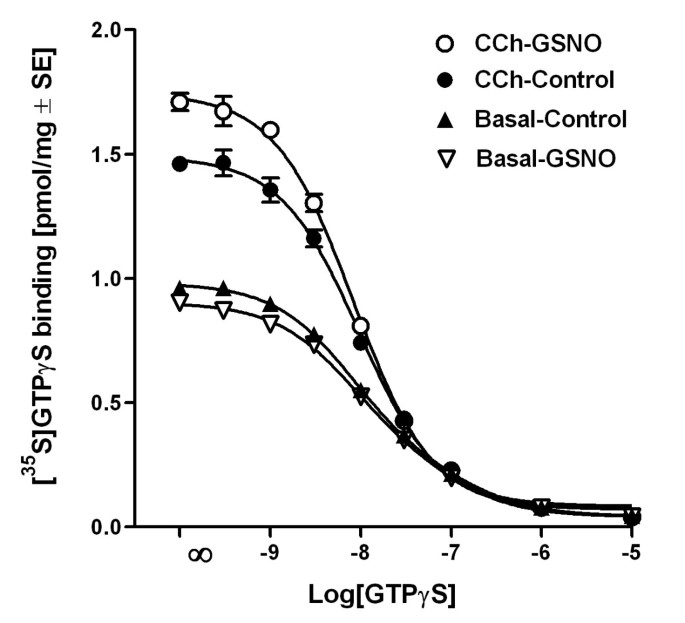
结果解读:如图6所示,GSNO处理显著加快了CCh刺激的[³⁵S]GTPγS结合速率,但对基础状态下的结合速率无影响,说明RSNO通过加快GDP/GTP交换速率增强G蛋白激活;图7显示,GSNO处理后,CCh刺激的高亲和力[³⁵S]GTPγS结合位点数量从1.49±0.02 pmol/mg蛋白增加到1.75±0.02 pmol/mg蛋白(n=3,P<0.001),而未标记GTPγS的效力(EC₅₀)无显著变化,表明RSNO增加了可被激动剂激活的G蛋白数量。
产品关联:文献未提及具体实验产品,领域常规使用放射性配体结合实验相关试剂、动力学分析软件等。
4. Biomarker研究及发现成果解析
本研究中与Biomarker相关的核心内容是RSNO调控GPCR信号的分子靶点及特异性调控模式,其筛选与验证逻辑为“天然组织系统性筛选→异源表达系统靶点区分→机制实验功能验证”,明确了RSNO对不同GPCR的特异性调控及潜在分子靶点。
Biomarker定位:本研究涉及的Biomarker为RSNO调控GPCR信号的分子靶点,包括G蛋白及其天然调控伙伴(而非GPCR本身,如P2Y₁₂受体的情况),以及M2/M4受体信号通路中参与GDP/GTP交换的关键分子;筛选逻辑为:首先通过脑冰冻切片筛选出对RSNO响应的GPCR,然后通过异源表达系统区分靶点是受体还是下游信号伙伴,最后通过机制实验明确具体的功能分子。
研究过程详述:Biomarker的来源为大鼠脑、人血小板的天然组织及CHO细胞异源表达系统;验证方法包括[³⁵S]GTPγS放射自显影、膜结合实验、突变体功能分析;特异性数据:RSNO对不同GPCR的调控具有高度特异性,如M2/M4、α₂A受体信号被增强,P2Y₁₂、LPA₁、CB₁受体信号被抑制,而腺苷A₁、MOR、ORL1受体信号不受影响;敏感性数据:GSNO在0.05mM即可显著增强M2/M4受体信号,0.2mM及以上浓度可显著抑制P2Y₁₂和LPA₁受体信号;统计学结果:如高亲和力结合位点数量变化的P<0.001(n=3),组成型激活M4细胞系中阿托品抑制率为13±3%(n=3,P<0.05)。
核心成果提炼:本研究的核心成果包括:①首次发现RSNO以可逆且高度受体特异性的方式调控Gi偶联GPCR的信号转导;②明确对于P2Y₁₂受体,RSNO的作用靶点是天然细胞信号伙伴而非受体本身;③揭示RSNO增强M2/M4受体信号的机制为加快GDP/GTP交换速率及增加高亲和力G蛋白结合位点数量;④创新性地建立了系统性研究GPCR氧化还原调控的实验体系,为后续研究提供了方法学参考。该成果的创新性在于首次系统性地揭示了RSNO对GPCR信号的受体特异性调控,填补了该领域的研究空白,为GPCR信号的氧化还原调控机制提供了新的认知。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。