The two-faced role of ATF2 on cisplatin response in gastric cancer depends on p53 context
ATF2 对胃癌顺铂治疗反应的双面作用取决于 p53 环境
| 期刊: | Cell and Bioscience | 影响因子: | 6.100 |
| 时间: | 2022 | 起止号: | 2022 May 31;12(1):77. |
| doi: | 10.1186/s13578-022-00802-w | 方法学: | FCM、IF、IHC-P |
| 靶点: | P53 | 研究方向: | 肿瘤 |
| 疾病类型: | 胃癌 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:The two-faced role of ATF2 on cisplatin response in gastric cancer depends on p53 context;发表期刊:Cell & Bioscience;影响因子:10.75(2022年);研究领域:胃癌化疗耐药机制与生物标志物研究。
胃癌是全球第五大常见恶性肿瘤,也是第三大癌症相关死亡原因,在中国其发病率和死亡率仅次于肺癌,严重威胁公众健康。领域共识:尽管手术、放化疗、靶向治疗等多模式治疗已改善胃癌患者预后,但由于化疗耐药导致的高复发率,患者5年生存率仍不足30%,解析化疗耐药的分子机制、寻找精准预测标志物是当前胃癌研究的核心方向。激活转录因子2(ATF2)作为碱性亮氨酸拉链家族成员,在不同肿瘤中呈现癌基因或抑癌基因的双重功能,但其在胃癌化疗应答中的作用机制尚未明确,现有研究也未揭示ATF2与p53状态的关联对化疗敏感性的调控作用,因此本研究旨在填补这一空白,为胃癌精准化疗提供新的分子靶点与预测指标。
2. 文献综述解析
作者对领域内现有研究的分类维度主要包括ATF2的细胞/组织特异性功能、亚细胞定位与功能的关联、p53在化疗应答中的核心作用三个层面。现有研究显示,ATF2在黑色素瘤、非小细胞肺癌中发挥癌基因功能,促进肿瘤增殖与转移;而在非黑色素瘤皮肤癌、乳腺癌中则作为抑癌基因,抑制肿瘤发生发展,其亚细胞定位是功能调控的关键因素,核定位的ATF2通常与癌基因功能相关,线粒体定位的ATF2则参与凋亡调控。同时,p53作为经典肿瘤抑制因子,在超过50%的人类癌症中存在突变,突变型p53不仅丧失抑癌功能,还会获得促癌特性,与化疗耐药密切相关,但ATF2与p53在胃癌化疗应答中的相互作用机制尚未被阐明。通过对比现有研究的未解决问题,本研究的创新价值在于首次揭示ATF2与p53的直接相互作用,明确ATF2在胃癌顺铂应答中的双面功能完全依赖于p53的功能状态,为胃癌化疗敏感性的精准预测提供了新的联合生物标志物。
3. 研究思路总结与详细解析
本研究的整体目标是明确ATF2在胃癌顺铂应答中的作用及分子机制,核心科学问题是ATF2的双面功能是否由p53状态调控,技术路线遵循临床样本分析→细胞功能验证→分子机制探究→动物实验与临床预后验证的闭环逻辑,系统解析了ATF2与p53的相互作用对顺铂敏感性的调控网络。
3.1 胃癌组织中ATF2的表达与临床意义分析
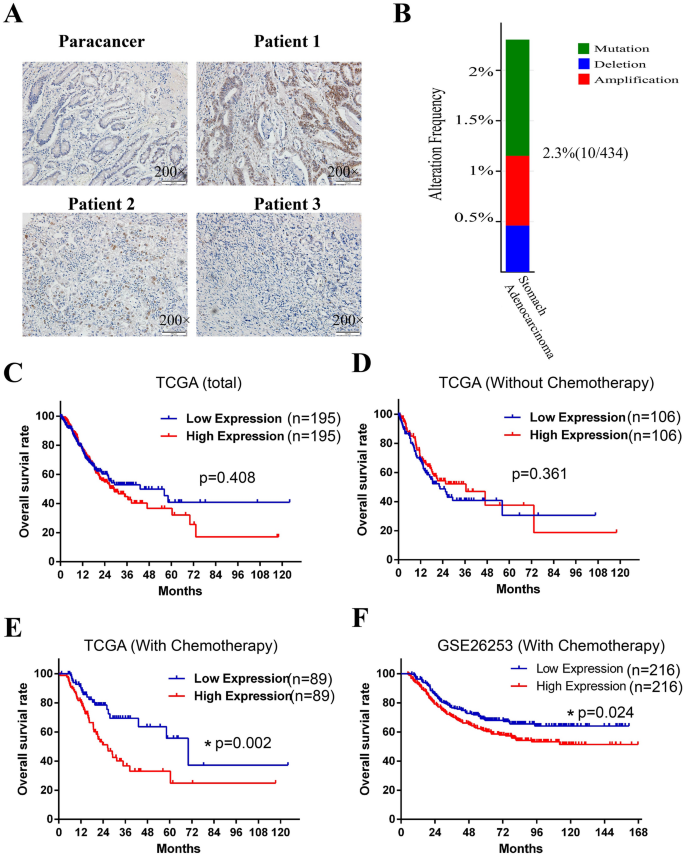
本环节的核心目标是明确ATF2在胃癌组织中的表达定位及与患者预后的关联。研究采用免疫组化检测胃癌组织中ATF2的表达与亚细胞定位,结合TCGA、GEO数据库分析不同ATF2表达水平患者的生存预后。结果显示,ATF2主要定位于胃癌细胞的细胞核,在部分患者中表达水平显著高于癌旁组织;TCGA数据库分析显示,高ATF2表达的胃癌患者总体生存率无显著差异,但接受化疗的高ATF2表达患者5年生存率显著更低(P<0.05),这一结果在GSE26253数据集中得到验证。实验所用关键产品:ATF2抗体(Santa Cruz Biotechnology)、免疫组化检测试剂盒(MaiXin.Bio)。
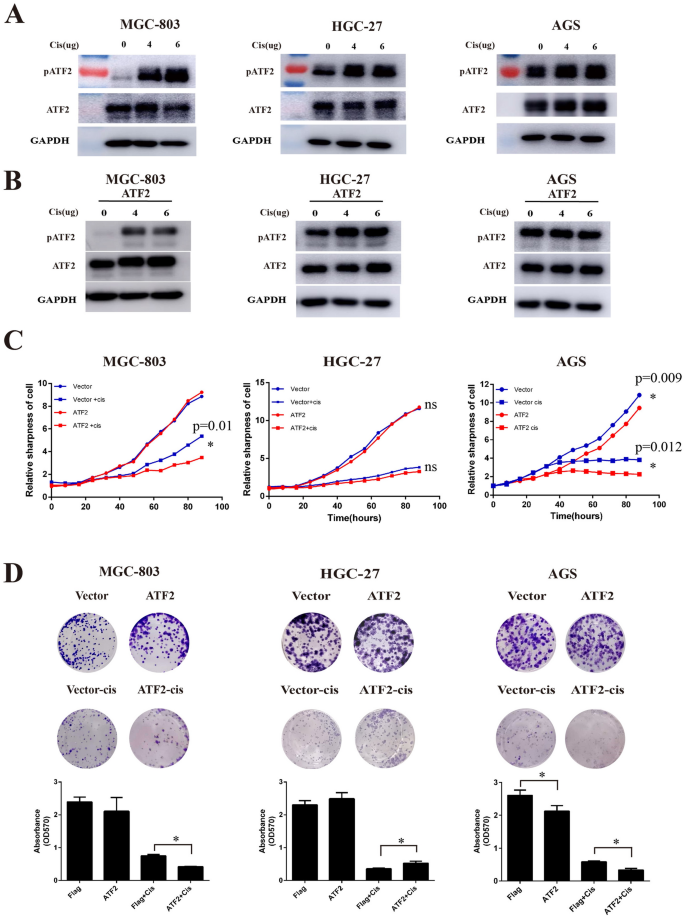
3.2 细胞水平验证ATF2对顺铂应答的影响
本环节旨在验证ATF2在不同胃癌细胞系中对顺铂敏感性的调控作用。研究首先通过Western Blot检测顺铂处理后不同胃癌细胞系中磷酸化ATF2(p-Thr71)的表达变化,随后构建ATF2稳定过表达细胞系,采用IncuCyte活细胞分析系统、克隆形成实验检测细胞增殖与顺铂敏感性。结果显示,顺铂以剂量依赖方式激活MGC-803、HGC-27细胞中的p-ATF2表达,但对AGS细胞的p-ATF2表达影响较小;ATF2过表达可增强AGS、MGC-803细胞的顺铂敏感性,促进细胞死亡,而在HGC-27细胞中则显著降低顺铂敏感性,促进细胞存活。实验所用关键产品:p-Thr71 ATF2抗体(Cell Signaling Technology)、IncuCyte®活细胞分析系统(EssenBioScience)。
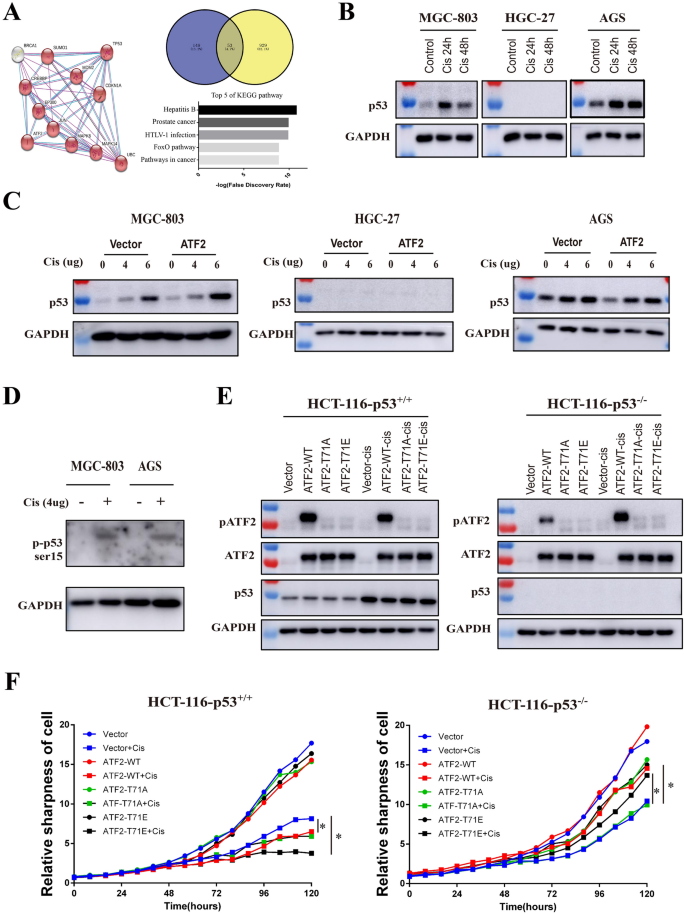
3.3 p53状态对ATF2功能的调控作用分析
本环节的核心目标是明确p53状态是否为ATF2双面功能的关键调控因素。研究利用不同p53状态的胃癌细胞系(AGS为p53野生型、MGC-803为p53点突变型、HGC-27为p53截短型)及结肠癌细胞系HCT-116(p53+/+、p53-/-),通过Western Blot检测顺铂处理后p53的表达与磷酸化水平,结合细胞增殖实验分析ATF2功能与p53状态的关联。结果显示,顺铂处理可显著上调p53野生型细胞中p53的表达与磷酸化水平,而p53缺陷细胞中无p53表达;在p53野生型细胞中,ATF2过表达增强顺铂敏感性,而在p53缺陷/突变细胞中,ATF2过表达则促进细胞存活,证实p53状态是ATF2功能的关键调控因素。文献未提及具体实验产品,领域常规使用p53抗体、细胞培养相关试剂。
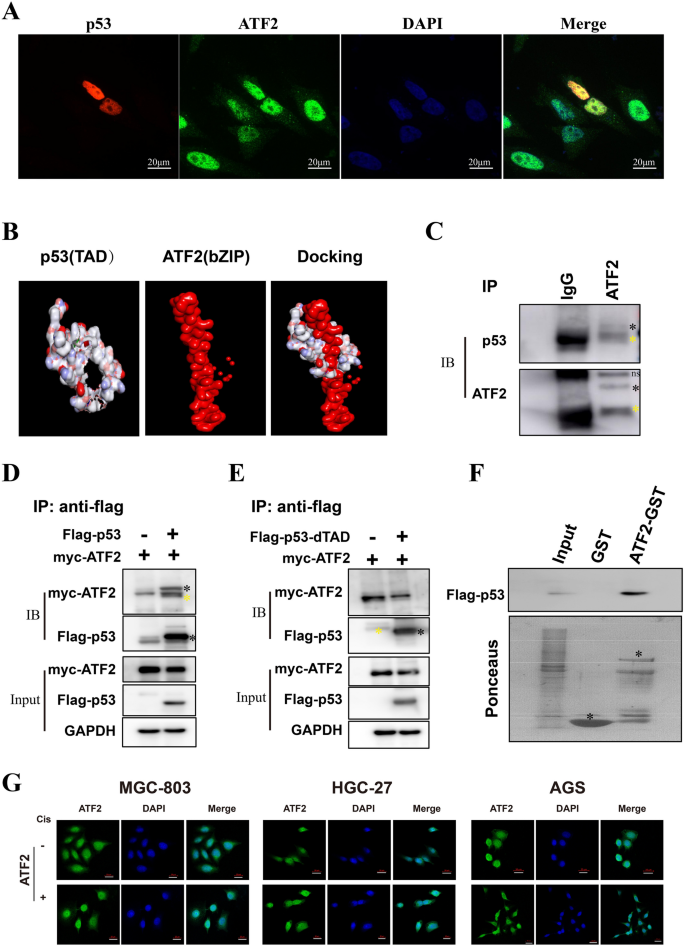
3.4 ATF2与p53的相互作用机制探究
本环节旨在明确ATF2与p53的相互作用区域及亚细胞定位变化。研究采用免疫荧光共定位观察ATF2与p53的亚细胞分布,通过分子对接预测两者的相互作用结构域,结合免疫沉淀(IP)、GST-pull down实验验证直接相互作用。结果显示,ATF2与p53均定位于细胞核,分子对接显示ATF2的bZIP结构域可与p53的反式激活结构域(TAD)结合;IP与GST-pull down实验证实两者存在直接相互作用,且当p53的TAD结构域缺失时,相互作用消失;顺铂处理后,p53野生型细胞中ATF2发生核输出,定位于细胞质,而p53突变细胞中ATF2仍主要定位于细胞核。实验所用关键产品:Flag标签抗体(Abmart)、GST-pull down试剂盒(GE Healthcare)、共聚焦显微镜。
3.5 ATF2调控ERK1/2通路的分子机制验证
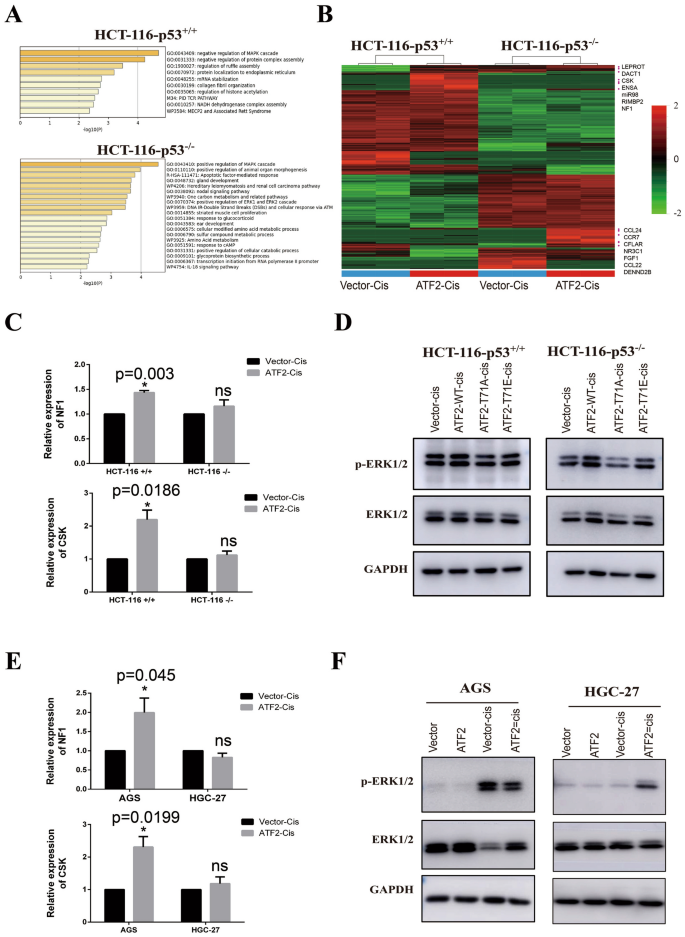
本环节的核心目标是解析ATF2依赖p53状态调控ERK1/2通路的具体机制。研究通过RNA测序分析ATF2过表达后p53野生型与缺陷细胞的差异表达基因,结合实时定量PCR、Western Blot验证关键基因的表达与ERK1/2通路的激活状态。结果显示,p53野生型细胞中ATF2过表达显著上调MAPK通路负调控因子CSK、NF1的表达,抑制ERK1/2的磷酸化激活;而在p53缺陷细胞中,ATF2过表达上调MAPK通路正调控因子,促进ERK1/2的磷酸化激活,证实ATF2通过调控ERK1/2通路介导顺铂应答的双面功能,且该调控依赖p53状态。实验所用关键产品:RNA测序服务(GENEWIZ)、TB Green定量PCR试剂盒(Takara)。
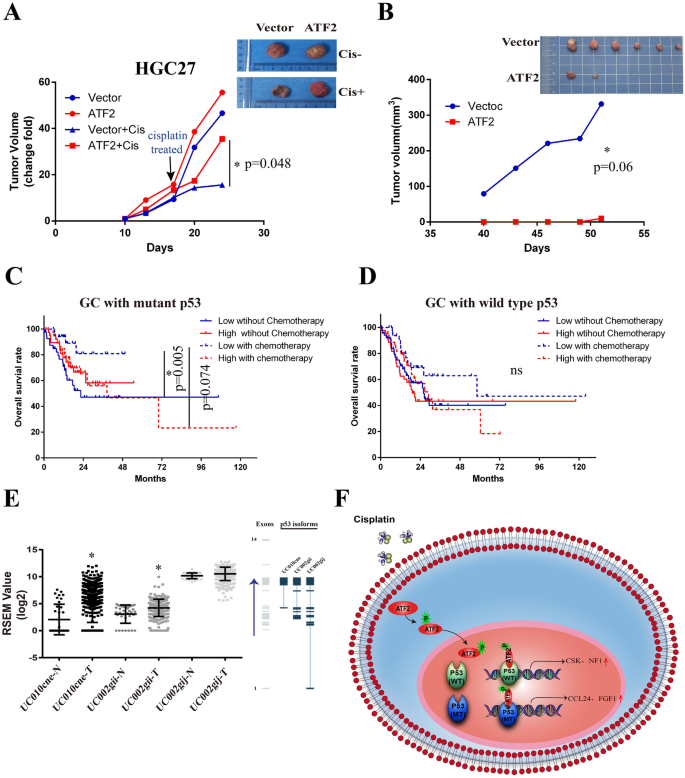
3.6 动物实验与临床预后的验证
本环节旨在体内验证ATF2的双面功能,并明确其临床预后价值。研究构建免疫缺陷叙利亚仓鼠的肿瘤异种移植模型,分别接种ATF2过表达的HGC-27(p53截短型)与AGS(p53野生型)细胞,观察顺铂处理后的肿瘤生长情况;同时结合TCGA数据库分析不同ATF2表达与p53状态患者的预后差异。结果显示,HGC-27细胞中,ATF2过表达组在顺铂处理后肿瘤体积显著大于对照组(n=5,P<0.05);AGS细胞中,ATF2过表达组即使未接受顺铂处理,肿瘤生长也被显著抑制;TCGA数据库分析显示,p53突变且ATF2低表达的化疗患者预后显著优于未化疗组(P<0.05),而p53野生型患者中不同ATF2表达组的预后无显著差异。实验所用关键产品:免疫缺陷叙利亚仓鼠、顺铂试剂。
4. Biomarker研究及发现成果
Biomarker定位
本研究确定的核心Biomarker为ATF2表达水平联合p53功能状态,其筛选与验证逻辑遵循临床样本关联分析→细胞/动物功能验证→大样本预后分析的完整链条,可作为胃癌顺铂化疗敏感性与预后的预测指标。
研究过程详述
该Biomarker的来源为胃癌临床组织样本及TCGA、GEO公共数据库的临床数据,验证方法包括免疫组化检测ATF2表达、基因测序分析p53状态、Kaplan-Meier生存分析评估预后价值。特异性与敏感性分析显示,在p53突变的胃癌患者中,低ATF2表达的化疗患者5年生存率显著高于未化疗组(Log-rank检验P<0.05),而高ATF2表达的化疗患者生存率显著更低,提示该联合Biomarker对p53突变患者的化疗预后具有较好的预测价值。
核心成果提炼
该Biomarker的功能关联在于,ATF2与p53状态的联合分析可有效区分胃癌患者的顺铂化疗敏感性,p53突变且ATF2低表达的患者更易从顺铂化疗中获益;创新性在于首次揭示ATF2通过与p53的TAD结构域相互作用,依赖p53状态调控ERK1/2通路,介导顺铂应答的双面功能。统计学结果显示,TCGA数据库中p53突变且ATF2低表达的化疗患者预后显著优于其他组(P<0.05),动物实验中HGC-27细胞ATF2过表达组顺铂处理后肿瘤体积较对照组增加约30%(n=5,P<0.05)。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。