Decreased Krüppel-like factor 4 in adenomyosis impairs decidualization by repressing autophagy in human endometrial stromal cells
子宫腺肌病中 Krüppel 样因子 4 减少通过抑制人类子宫内膜基质细胞的自噬来损害蜕膜化
| 期刊: | BMC Molecular and Cell Biology | 影响因子: | 2.400 |
| 时间: | 2022 | 起止号: | 2022 Jun 27;23(1):24. |
| doi: | 10.1186/s12860-022-00425-6 | 种属: | Human |
| 研究方向: | 信号转导、细胞生物学 | 细胞类型: | 基质细胞 |
| 信号通路: | Autophagy | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Decreased Krüppel-like factor 4 in adenomyosis impairs decidualization by repressing autophagy in human endometrial stromal cells;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:生殖医学-子宫腺肌病与子宫内膜蜕膜化调控
子宫腺肌病是导致女性不孕及辅助生殖技术(ART)周期妊娠率降低、流产率升高的关键因素之一,全球发病率约15%,ART就诊患者中发病率可达54%。领域发展关键节点显示,近年ART胚胎质量控制技术已逐步成熟,但子宫内膜功能障碍(如蜕膜化受损)成为限制妊娠成功的核心瓶颈;已知子宫内膜基质细胞蜕膜化是胚胎植入和妊娠维持的关键生理过程,涉及细胞形态转变、功能分子分泌及免疫微环境调控,其受损会直接导致胚胎植入失败;Krüppel样因子(KLF)家族作为进化保守的转录因子,已被证实参与子宫内膜生理功能调控,自噬与子宫内膜蜕膜化、胚胎植入的关联也逐渐被揭示,但子宫腺肌病中蜕膜化与自噬的具体调控机制尚未明确。
针对子宫腺肌病患者子宫内膜KLF4表达异常降低、自噬水平紊乱与蜕膜化受损的关联机制空白,本研究旨在明确KLF4调控子宫内膜基质细胞自噬及蜕膜化的分子机制,为子宫腺肌病相关不孕提供新的生物标志物与治疗靶点,具有重要的临床转化价值。
2. 文献综述解析
作者从子宫腺肌病的临床影响、子宫内膜蜕膜化的生理功能、KLF家族的调控作用、自噬与生殖的关联四个维度梳理现有研究,构建了“临床问题-生理机制-分子调控”的综述逻辑框架。
现有研究证实,子宫腺肌病对妊娠的负面影响主要源于子宫内膜功能异常,包括胚胎黏附相关因子(如HOXA10、LIF)表达异常及蜕膜化受损;蜕膜化过程中,子宫内膜基质细胞会从细长型转变为圆形分泌型,分泌蜕膜催乳素(dPRL)、胰岛素样生长因子结合蛋白1(IGFBP-1)等功能分子,同时参与免疫细胞信息传递,为胚胎植入提供免疫耐受微环境;KLF家族成员如KLF5、KLF9、KLF12已被证实参与子宫内膜蜕膜化调控,其中KLF12通过抑制NR4A1和FOXO1A表达损害蜕膜化;自噬方面,正常妊娠蜕膜组织自噬水平显著高于胚胎植入失败或早期流产患者,肥胖小鼠模型中自噬抑制会损害人工诱导的蜕膜化,子宫腺肌病患者子宫内膜处于高雌激素刺激和孕激素抵抗状态,通过mTOR通路抑制自噬,但KLF家族与自噬的关联尚未被报道。
现有研究已明确子宫腺肌病患者存在蜕膜化受损、自噬水平降低的表型,但未揭示两者的调控关联及关键分子;本研究首次发现KLF4通过转录激活自噬相关基因ATG5表达,调控子宫内膜基质细胞自噬与蜕膜化,填补了子宫腺肌病中蜕膜化调控分子机制的空白,为理解子宫腺肌病相关不孕的病理机制提供了新视角。
3. 研究思路总结与详细解析
本研究以“临床样本差异表达分析→细胞功能验证→分子机制解析→动物模型验证”为核心技术路线,研究目标是明确KLF4在子宫腺肌病患者子宫内膜中的表达模式,揭示其调控子宫内膜基质细胞自噬及蜕膜化的分子机制;核心科学问题是KLF4如何通过自噬通路调控子宫内膜基质细胞蜕膜化,以及该机制在子宫腺肌病中的病理意义。
3.1 临床样本与动物模型分子表达检测
实验目的:检测子宫腺肌病患者及模型小鼠子宫内膜中KLF4与自噬标志物的表达模式及相关性。
方法细节:收集12例子宫腺肌病不孕患者及12例 fertile 对照的子宫内膜组织,采用他莫昔芬诱导构建子宫腺肌病小鼠模型;采用免疫组化(IHC)、蛋白质免疫印迹(Western blot)检测KLF4、LC3-B/LC3-A、Beclin-1的表达水平,通过Pearson相关性分析KLF4与自噬标志物的关联。
结果解读:
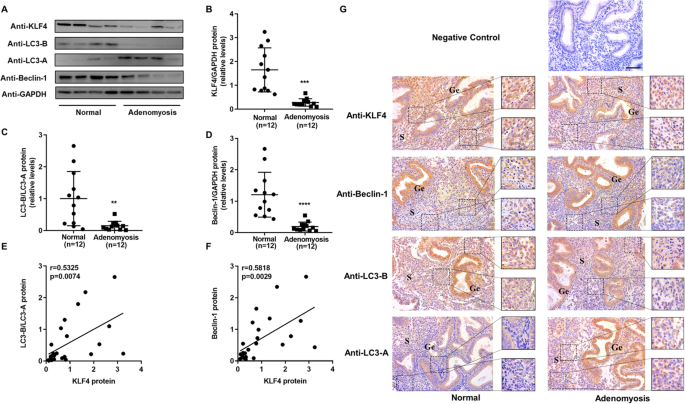
如图1所示,子宫腺肌病患者子宫内膜KLF4蛋白水平显著低于对照组(P<0.0001,n=24),自噬标志物LC3-B/LC3-A、Beclin-1表达也显著降低(P<0.01,n=24);相关性分析显示KLF4与LC3-B/LC3-A(r=0.5325,P=0.0074)、Beclin-1(r=0.5815,P=0.0029)呈中度正相关;免疫组化结果显示,KLF4与自噬标志物的降低主要发生在子宫内膜基质细胞中。
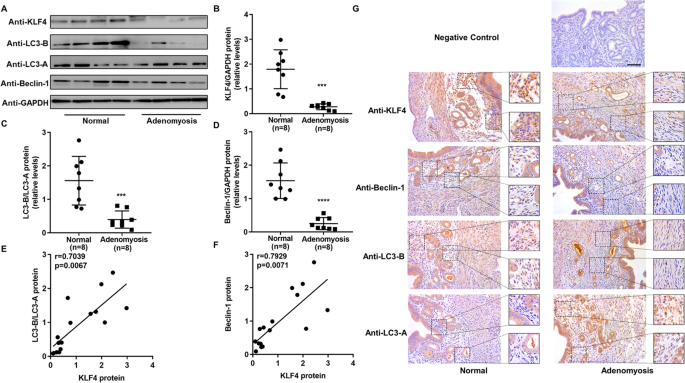
在子宫腺肌病模型小鼠中也观察到类似表达模式(图5),KLF4与自噬标志物LC3-B/LC3-A、Beclin-1表达均显著降低,且呈正相关(r=0.7039,P=0.0067;r=0.7929,P=0.0071,n=16)。
实验所用关键产品:Proteintech的KLF4抗体(货号11880-1-AP)、Beclin-1抗体(货号11306-1-AP)、LC3A抗体(货号18722-1-AP)、LC3B抗体(货号18725-1-AP),Bio-Rad的Bradford蛋白浓度测定试剂盒、Quantity-one软件等。
3.2 KLF4对子宫内膜基质细胞蜕膜化的调控作用验证
实验目的:明确KLF4对人子宫内膜基质细胞(hESCs)蜕膜化的调控功能。
方法细节:分离子宫腺肌病患者及对照的hESCs,采用KLF4过表达腺病毒(Ad-His-KLF4)和敲低siRNA(SiKLF4)干预细胞内KLF4表达;用0.5 mM 8-Br-cAMP和1 μM甲羟孕酮(MPA)诱导蜕膜化,通过实时荧光定量PCR(qRT-PCR)检测dPRL、IGFBP-1的mRNA表达,酶联荧光法(ELFA)检测dPRL分泌水平,免疫荧光染色观察F-actin形态变化。
结果解读:
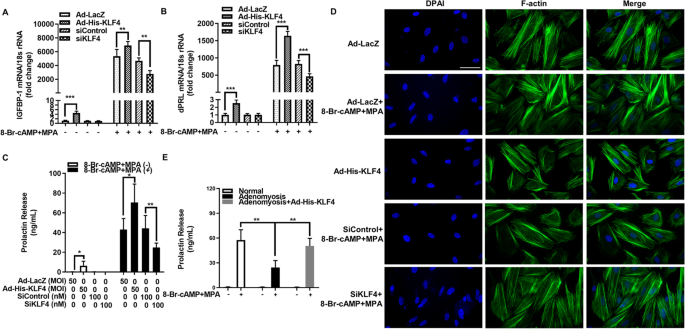
如图2所示,过表达KLF4显著上调蜕膜化诱导后hESCs的dPRL、IGFBP-1 mRNA表达(P<0.001,n=3)及dPRL分泌水平(P<0.01,n=3),并促进细胞从细长型向圆形分泌型转变;敲低KLF4则抑制上述蜕膜化指标;在子宫腺肌病来源的hESCs中,过表达KLF4可逆转其蜕膜化受损表型,显著提升dPRL分泌水平(P<0.01,n=3)。
实验所用关键产品:RiboBio的SiKLF4 siRNA,Sigma的8-Br-cAMP、MPA,Life Technologies的Lipofectamine 3000转染试剂等。
3.3 KLF4通过自噬调控蜕膜化的功能验证
实验目的:验证KLF4调控蜕膜化的作用依赖于自噬通路。
方法细节:用Ad-His-KLF4过表达hESCs,同时用5 mM自噬抑制剂3-甲基腺嘌呤(3-MA)预处理细胞;通过Western blot检测自噬标志物LC3-B/LC3-A、Beclin-1的蛋白表达,qRT-PCR检测dPRL、IGFBP-1的mRNA表达,ELFA检测dPRL分泌水平,免疫荧光染色观察细胞形态变化。
结果解读:
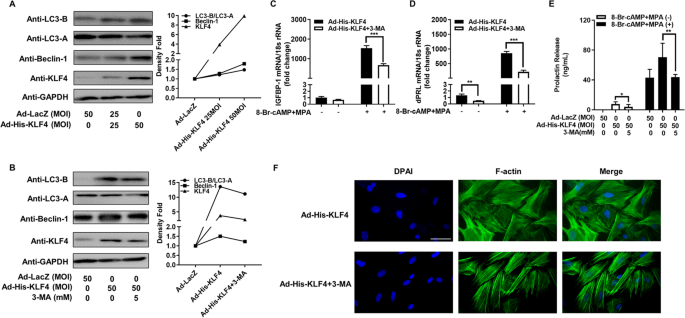
如图3所示,过表达KLF4可显著上调hESCs的LC3-B/LC3-A、Beclin-1表达水平(P<0.01,n=3);3-MA预处理可逆转KLF4对自噬标志物的上调作用,同时抑制KLF4诱导的dPRL、IGFBP-1表达及dPRL分泌(P<0.01,n=3),并阻断细胞形态的蜕膜化转变,证实KLF4通过促进自噬调控蜕膜化。
实验所用关键产品:MedChemExpress的3-MA,Proteintech的自噬标志物抗体等。
3.4 KLF4调控自噬的分子机制解析
实验目的:明确KLF4调控自噬的下游靶基因及转录调控机制。
方法细节:通过qRT-PCR、Western blot检测KLF4过表达后自噬相关基因ATG5的mRNA及蛋白表达;构建含ATG5启动子KLF4结合位点的荧光素酶报告质粒(ATG5-Luc-WT)及缺失结合位点的质粒(ATG5-Luc-DEL),进行荧光素酶报告实验;采用染色质免疫沉淀(ChIP)-PCR、亲和素-生物素偶联DNA沉淀(ABCD)实验验证KLF4与ATG5启动子的直接结合。
结果解读:
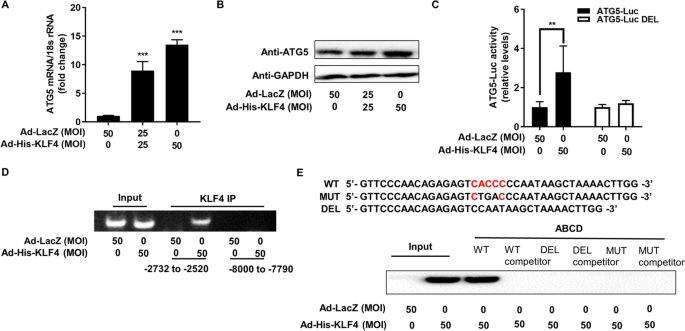
如图4所示,过表达KLF4显著上调ATG5的mRNA及蛋白表达(mRNA水平上调约3倍,P<0.001,n=3);荧光素酶报告实验显示KLF4可激活ATG5-Luc-WT的荧光素酶活性(P<0.01,n=3),但对ATG5-Luc-DEL无显著影响;ChIP-PCR证实KLF4可富集ATG5启动子的特定片段,ABCD实验显示KLF4仅与野生型ATG5启动子寡核苷酸结合,缺失或突变结合位点后结合消失,证实KLF4通过直接结合ATG5启动子转录激活其表达。
实验所用关键产品:Promega的双荧光素酶分析系统,Sigma的链霉亲和素琼脂糖珠等。
4. Biomarker研究及发现成果解析
本研究中涉及的Biomarker为KLF4及自噬相关分子ATG5,筛选逻辑为“临床样本差异表达分析→细胞功能验证→分子机制解析→动物模型验证”,形成了完整的“临床-细胞-分子-动物”验证链条。
Biomarker来源为子宫腺肌病患者及对照的子宫内膜组织、hESCs及子宫腺肌病模型小鼠子宫组织;验证方法包括免疫组化、Western blot、qRT-PCR检测表达水平,ChIP-PCR、ABCD实验验证KLF4与ATG5的调控关系;特异性与敏感性数据显示,KLF4在子宫腺肌病患者子宫内膜基质细胞中表达显著降低(Western blot统计显示蛋白水平降低约60%,P<0.0001,n=24),与自噬标志物LC3-B/LC3-A、Beclin-1呈中度正相关;ATG5作为KLF4的下游靶基因,其表达随KLF4过表达显著上调(mRNA水平上调约3倍,P<0.001,n=3)。
核心成果提炼显示,KLF4可作为子宫腺肌病相关蜕膜化受损的潜在诊断生物标志物,其功能关联为通过转录激活ATG5表达促进自噬,进而维持子宫内膜基质细胞蜕膜化;本研究首次揭示KLF4-ATG5-自噬轴在子宫腺肌病蜕膜化调控中的作用,为子宫腺肌病相关不孕的治疗提供了新靶点;统计学结果显示,KLF4与自噬标志物的相关性、KLF4对ATG5及蜕膜化指标的调控作用均具有显著统计学意义(P<0.01),所有细胞实验均重复至少3次,样本量n=3,数据可靠性较高。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。