Induction of chronic asthma up regulated the transcription of senile factors in male rats
慢性哮喘的诱发上调了雄性大鼠衰老因子的转录
| 期刊: | BMC Molecular and Cell Biology | 影响因子: | 2.400 |
| 时间: | 2024 | 起止号: | 2024 Oct 18;25(1):23. |
| doi: | 10.1186/s12860-024-00518-4 | 靶点: | IL1B |
| 研究方向: | 发育与干细胞 | 疾病类型: | 哮喘 |
| 信号通路: | Senescence | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Induction of chronic asthma up regulated the transcription of senile factors in male rats;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:哮喘与细胞衰老机制。
哮喘是全球最常见的慢性呼吸道疾病之一,以慢性炎症和肺结构重塑为核心特征,2019年全球患者达2.62亿,导致45.5万例死亡。其核心发病机制为Th2型辅助淋巴细胞介导的炎症反应,淋巴细胞分泌IL-4、IL-5、IL-13等细胞因子,诱导炎症细胞浸润和气道重塑,但哮喘病理的分子机制仍存在未明确环节。领域共识:慢性炎症与细胞衰老密切相关,细胞衰老以不可逆周期停滞和衰老相关分泌表型(SASP)为特征,已被证实参与慢性阻塞性肺疾病、肺纤维化等慢性肺病的病理过程,但哮喘是否直接诱导肺组织细胞衰老的研究证据不足,这一空白限制了对哮喘慢性病理损伤机制的全面理解。因此,本研究旨在通过慢性哮喘大鼠模型,系统性检测炎症因子与衰老相关基因的表达,明确哮喘与肺组织细胞衰老的关联,为哮喘的病理机制研究提供新的分子证据。
2. 文献综述解析
本文综述部分以“慢性炎症-细胞衰老-慢性肺病”的关联逻辑为核心,将现有研究分为哮喘炎症机制、细胞衰老分子特征、慢性肺病与细胞衰老关联三类。
哮喘炎症机制方面,现有研究已明确Th2细胞介导的细胞因子分泌是哮喘炎症的核心驱动因素,该机制在动物模型和临床样本中均得到验证,但针对炎症下游分子事件的研究仍不充分;细胞衰老分子特征方面,现有研究已确定β-半乳糖苷酶为经典衰老阳性标志物,Klotho、Sox2为调控衰老的关键负向调控基因,这些标志物在多种衰老相关疾病中得到验证,但在哮喘中的应用尚未见系统性报道;慢性肺病与细胞衰老关联方面,现有研究已证实慢性阻塞性肺疾病、肺纤维化会诱导肺组织细胞衰老,但哮喘作为高发性慢性呼吸道疾病,其与细胞衰老的直接关联研究较少,缺乏在动物模型中对多个衰老标志物的同步检测。本文的创新价值在于,首次在卵清蛋白诱导的慢性哮喘大鼠模型中,同时检测炎症因子和三类核心衰老相关基因的表达,填补了哮喘与细胞衰老关联研究的空白,为理解哮喘的慢性病理损伤机制提供了新的分子视角。
3. 研究思路总结与详细解析
本文的研究目标是明确慢性哮喘是否诱导大鼠肺组织细胞衰老,核心科学问题为哮喘的慢性炎症是否通过调控衰老相关基因的表达加速肺组织衰老,技术路线遵循“模型构建-病理验证-分子检测-结论推导”的闭环逻辑,通过组织病理、炎症因子检测和分子生物学实验的多维度验证,确保研究结论的可靠性。
3.1 慢性哮喘大鼠模型构建与伦理审批
实验目的是构建稳定的慢性哮喘动物模型,为后续研究提供标准化实验对象。方法细节为选取16只体重200±20g的雄性Wistar大鼠,适应性饲养1周后随机分为对照组和哮喘组,每组8只;哮喘组在实验第1、7天腹腔注射1mg卵清蛋白与200mg氢氧化铝的混合液致敏,第14天至第70天每日给予1%卵清蛋白雾化吸入30分钟,对照组全程给予生理盐水处理;实验方案经Tabriz医科大学伦理委员会批准(IR.TBZMED.AEC.1401.023),符合动物实验伦理规范。结果解读为后续组织病理检测显示哮喘组出现典型的哮喘病理改变,证实模型构建成功。文献未提及具体实验产品,领域常规使用卵清蛋白、氢氧化铝等致敏试剂。
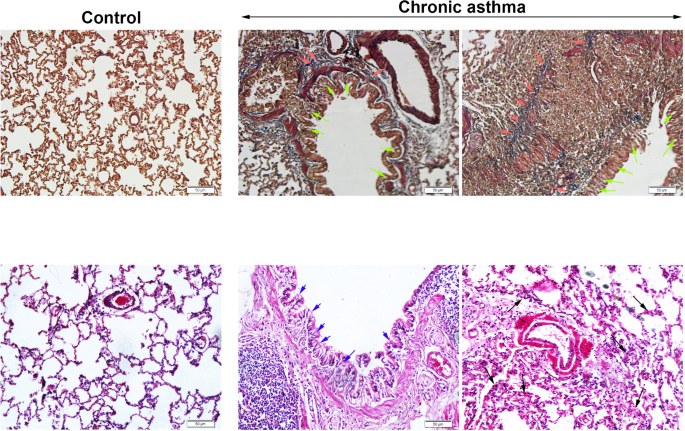
3.2 肺组织病理学检测
实验目的是验证慢性哮喘诱导的肺组织病理损伤,确认模型的病理有效性。方法细节为大鼠处死后取肺组织,立即置于4%多聚甲醛中固定24小时,经脱水、透明、包埋后制作5μm厚的石蜡切片,分别进行苏木精-伊红(H&E)染色和Masson三色染色,采用Olympus BX41光学显微镜在高倍视野下观察,每组至少观察4个视野。结果解读为哮喘组肺组织出现充血、间质性肺炎、纤维蛋白凝块、胸膜炎症细胞浸润等典型哮喘病理改变,与对照组的正常肺组织形成显著差异,进一步证实了慢性哮喘模型的成功构建。
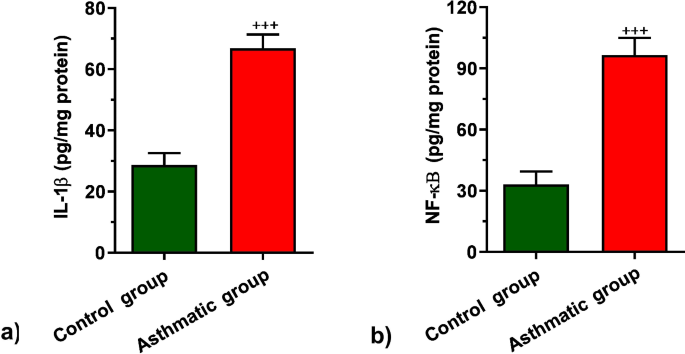
3.3 炎症因子ELISA检测
实验目的是检测慢性哮喘大鼠肺组织中炎症因子的表达水平,明确炎症激活状态。方法细节为取肺组织在冰上机械研磨,采用Potter-Elvehjem匀浆器(Kinematica,加拿大)制备组织匀浆,3500g、4℃离心10分钟后取上清;使用Abcam的IL-1β ELISA试剂盒(货号ab100768)和Zellbio的NF-κB ELISA试剂盒(货号RK08775),按照试剂盒说明书进行操作,在450nm波长下读取吸光度值。结果解读为哮喘组肺组织中IL-1β和NF-κB的蛋白水平显著高于对照组(n=3,P<0.001),证实慢性哮喘模型中存在显著的炎症激活,为后续细胞衰老的研究提供了炎症背景依据。
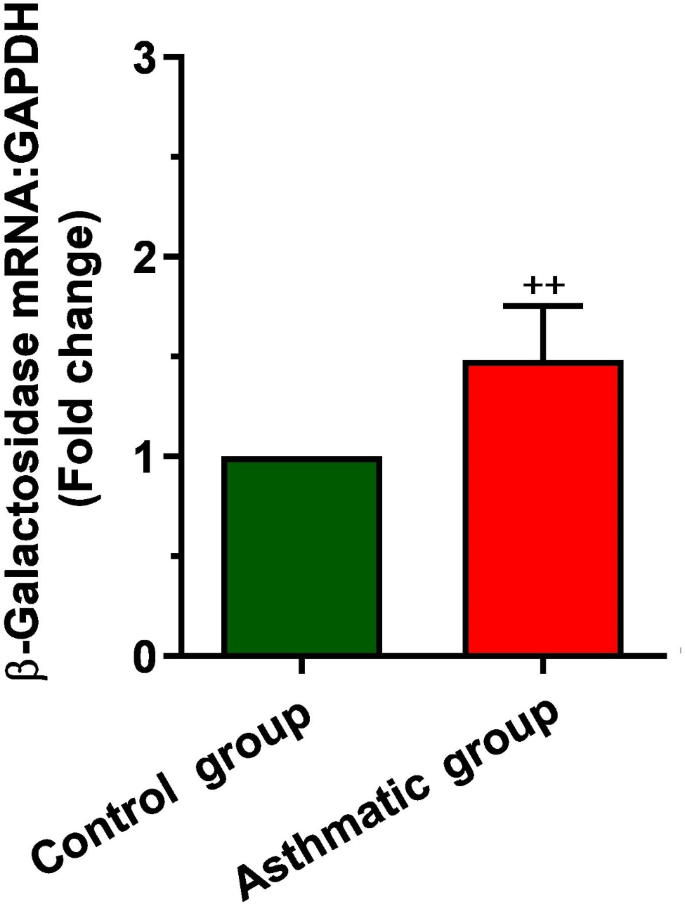
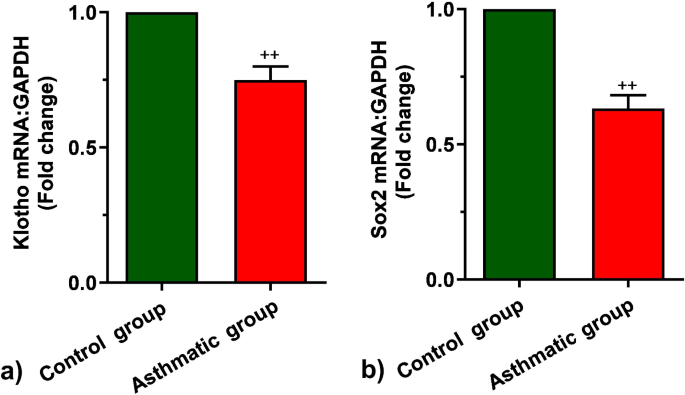
3.4 衰老相关基因表达检测
实验目的是检测慢性哮喘大鼠肺组织中衰老相关基因的表达水平,明确哮喘对细胞衰老的调控作用。方法细节为取大鼠肺组织立即冻存于-80℃,经液氮研磨后采用YektaTajhiz(伊朗)的RNA提取试剂盒提取总RNA,通过NanoDrop 1000分光光度计检测RNA浓度和纯度;取1μg RNA采用YektaTajhiz的cDNA合成试剂盒反转录为cDNA,以GAPDH为内参基因,使用SYBR Green qPCR试剂盒(YektaTajhiz)进行实时荧光定量PCR,反应条件为95℃预变性5分钟,40个循环的95℃10秒、59℃60秒,采用2^-ΔΔCt法分析基因相对表达量。结果解读为哮喘组β-半乳糖苷酶基因表达显著上调(n=8,P<0.01),Klotho和Sox2基因表达显著下调(n=8,P<0.01),提示慢性哮喘通过调控衰老相关基因的表达,加速了肺组织细胞的衰老进程。
4. Biomarker研究及发现成果
本文聚焦于细胞衰老相关生物标志物的检测与验证,通过在慢性哮喘大鼠模型中对三类经典衰老标志物的基因表达分析,明确了哮喘诱导肺组织细胞衰老的分子证据,为哮喘的病理机制研究提供了新的生物标志物组合。
Biomarker定位:本文涉及的细胞衰老生物标志物包括β-半乳糖苷酶(衰老阳性标志物,高表达提示细胞衰老)、Klotho和Sox2(衰老阴性标志物,低表达提示细胞衰老),筛选逻辑基于领域内已证实的经典细胞衰老标志物,验证逻辑为结合组织病理结果、炎症因子水平与基因表达数据,多维度验证标志物与哮喘诱导细胞衰老的关联。研究过程详述:标志物来源为慢性哮喘模型大鼠的肺组织,验证方法为实时荧光定量PCR(qPCR),检测结果显示哮喘组β-半乳糖苷酶基因表达显著上调(n=8,P<0.01),Klotho和Sox2基因表达显著下调(n=8,P<0.01),三类标志物的表达变化趋势一致,共同提示哮喘诱导的肺组织细胞衰老。核心成果提炼:本研究首次在慢性哮喘大鼠模型中证实,哮喘的慢性炎症状态会通过调控细胞衰老相关基因的表达,加速肺组织细胞衰老;该发现为哮喘的慢性病理损伤机制提供了新的分子视角,提示细胞衰老可能是哮喘气道重塑的潜在驱动因素,β-半乳糖苷酶、Klotho和Sox2可作为哮喘病理进程中细胞衰老状态的检测标志物,为哮喘的早期诊断和治疗靶点筛选提供了新的方向。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。