随着机体衰老,细胞每年会自然累积数十种基因突变。波士顿儿童医院的研究人员发表的最新研究表明,脑内的固有免疫细胞——小胶质细胞(microglia)会在特定癌症驱动基因上累积突变,但并不会诱发癌症,反而可能驱动阿尔茨海默病(Alzheimer’s disease, AD)的发生。
该研究团队由波士顿儿童医院遗传与基因组学部主任、霍华德·休斯医学研究所研究员克里斯托弗·沃尔什(Christopher Walsh)医学博士/哲学博士牵头,合作者包括同属遗传与基因组学部的爱丽丝·恩贞·李(Alice Eunjung Lee)哲学博士与黄岳(August Yue Huang)哲学博士,三人同时为哈佛医学院教授、麻省理工学院与哈佛大学博德研究所副成员。团队表示,该研究结果有望为阿尔茨海默病的新型诊断与治疗方案提供思路。
沃尔什指出:“我们发现,阿尔茨海默病在一定程度上与癌症类似,由驱动淋巴瘤、白血病等血液癌症的同种突变驱动。这一发现极具应用价值,因为目前已有大量抗肿瘤药物,其中部分或可用于阿尔茨海默病的治疗。”
研究人员的相关成果发表于《细胞》(Cell)期刊,论文题为《阿尔茨海默病类小胶质细胞中富集的体细胞癌症变异可驱动炎症与增殖表型》。
小胶质细胞是脑内的固有免疫细胞,发挥“清道夫”功能,可吞噬细胞碎片、受感染细胞或濒死细胞。作者在论文中提到:“大规模遗传关联研究已证实小胶质细胞在阿尔茨海默病发病机制中的重要作用,这类研究在越来越多的小胶质细胞相关基因中发现了阿尔茨海默病风险变异。一旦小胶质细胞在阿尔茨海默病中出现异常活化,就会促进突触与神经元丢失,同时加剧tau蛋白病变。”
此前学界普遍认为,与全身血液循环中循环的其他免疫细胞不同,小胶质细胞无法穿越血脑屏障。在这项最新发表的研究中,研究团队对190例阿尔茨海默病患者捐献的脑组织样本与121例健康脑样本的149个癌症驱动基因进行了测序。结果显示,阿尔茨海默病样本的DNA单碱基突变数量多于健康组织,且突变频率最高的位点集中在5个相同的癌症驱动基因中,提示小胶质细胞在特定基因上存在突变累积。团队表示:“对311例脑样本的深度(>1000×)靶向测序显示,阿尔茨海默病脑组织的癌症驱动基因中体细胞单核苷酸变异(somatic single-nucleotide variants, sSNVs)富集,尤其是与克隆性造血(clonal hematopoiesis, CH)相关的基因。”
研究人员在小胶质细胞中发现的这些癌症基因突变,在血液癌症中十分常见。基于这一特征,团队检测了阿尔茨海默病患者血液样本中是否存在同样的突变,此前研究团队并不认为血液中会存在这类突变。但最终沃尔什团队发现,同一批阿尔茨海默病患者的血细胞中同样携带这些癌症突变。
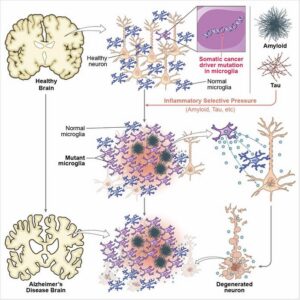
研究人员指出:“这些体细胞单核苷酸变异与克隆扩增相关,同时存在于多个脑区的类小胶质脑巨噬细胞(microglia-like brain macrophages, MLBMs)以及配对的血液样本中,提示其可能起源于造血系统。”黄岳表示:“这确实是一项非常出人意料的发现,揭示了阿尔茨海默病发病的全新机制。该结果表明,携带癌症突变的血液免疫细胞很可能进入脑内,参与了疾病的发生发展。”
研究人员提出的假说为:血脑屏障会随着衰老或损伤发生通透性升高,使血液免疫细胞得以进入脑内,这些新进入的细胞随后转化为类小胶质细胞。同时,脑内的蛋白聚集体累积会激活小胶质细胞增殖并行使免疫功能,具有选择优势的细胞(如携带癌症突变的类小胶质细胞)会成为优势群体。但与健康小胶质细胞相比,这些突变的小胶质细胞会营造出炎症水平更高、更具细胞毒性的微环境,导致周围的无辜神经元死亡,最终诱发阿尔茨海默病。研究人员强调:“这些发现表明,类小胶质脑巨噬细胞中的体细胞驱动克隆变异在阿尔茨海默病患者中富集,可能促进神经炎症与神经退行性变。体细胞癌症驱动变异在阿尔茨海默病发病机制中的潜在作用,为阿尔茨海默病治疗开辟了全新方向,可与目前靶向淀粉样蛋白和tau的治疗方案形成互补。”
李补充道:“由于很难获取活患者的脑组织,未来可开发基于血液样本的基因筛查方案,检测个体是否携带这些突变,评估其阿尔茨海默病的发病风险。”李与黄岳开展了一项后续研究,目前已作为预印本发表于bioRxiv平台(https://doi.org/10.1101/2025.05.19.654981)。研究结果显示,患者血液样本中检测到的癌症驱动突变可增加阿尔茨海默病的发病风险,且该效应独立于已明确的遗传风险因子载脂蛋白E4(APOE4)。
专业注释
- 克隆性造血:造血干细胞突变后克隆性扩增的生理/病理现象
- 体细胞单核苷酸变异:非生殖细胞发生的单碱基突变,不遗传给后代
