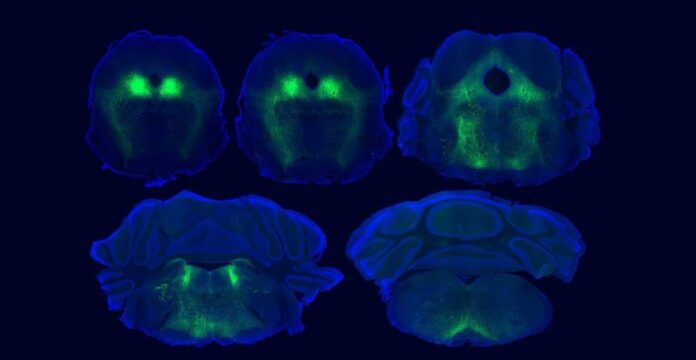
图注:参与小鼠安慰剂镇痛的关键脑回路荧光成像图。位于腹外侧导水管周围灰质(ventrolateral periaqueductal gray, vlPAG)的疼痛调控神经元被标记为绿色,其胞体呈绿色点状,线状轴突延伸至脑干以抑制疼痛。[图源:Janie Chang-Weinberg]
尽管安慰剂效应是一种已被充分证实的现象,但其背后的神经机制尚未被完全阐明。目前,由加州大学圣地亚哥分校(UCSD)团队牵头、多家机构合作的科学家团队已在小鼠体内定位到了他们认为介导安慰剂镇痛的脑回路。相关研究结果发表于《神经元》(Neuron)期刊的最新论文中,研究人员在文中描述了介导安慰剂效应的脑区,同时明确了内源性阿片神经肽发送信号、调控安慰剂镇痛的关键位点。
该论文题为《下行疼痛调制系统的自上而下调控驱动多模态安慰剂镇痛》(Top-down control of the descending pain modulatory system drives multimodal placebo analgesia)。据研究团队介绍,这是首个通过调整适用于人类的研究方案、在小鼠模型中明确安慰剂作用机制的研究。加州大学圣地亚哥分校团队与宾夕法尼亚大学、加州大学欧文分校等多个实验室合作,检测到小鼠脑中与既往人类研究中提示的同源脑区存在活动。此外,通过精准绘制小鼠的神经通路与脑活动图谱,研究团队明确了安慰剂镇痛过程中,连接大脑皮层、脑干与脊髓的神经回路发挥的核心作用。
研究人员还发现,训练小鼠针对某一类疼痛产生安慰剂效应后,该效应可缓解包括损伤性疼痛在内的多种不同类型疼痛。加州大学圣地亚哥分校神经生物学系副教授、该研究的主要作者Matthew Banghart博士解释道,这一发现意义尤为重大,因为它“直接提示了人类的安慰剂训练可用于提升个体对未来损伤性疼痛的耐受能力”。他还指出,该研究结果也为“预期驱动型”安慰剂效应替代成瘾性镇痛药物提供了新思路,即有望通过安慰剂条件化训练,帮助患者预先建立疼痛耐受能力。
论文中详细列出了研究结果与所用方法。研究团队表示,他们采用了传感器技术与Banghart实验室开发的光激活药物,研究脑内天然存在的阿片肽的作用。具体而言,在安慰剂试验过程中,研究人员使用传感器检测疼痛信号的已知中枢——腹外侧导水管周围灰质(vlPAG)区域的阿片肽信号;随后使用名为光激活纳洛酮(photoactivatable naloxone, PhNX)的光激活药物,证实这些阿片肽确实以与吗啡等药物类似的方式介导镇痛效应。光调控使研究人员可以精准控制阿片信号干扰的时机。借助PhNX,研究人员证实吗啡诱导的镇痛与安慰剂镇痛均利用了脑内vlPAG区域的同一套阿片信号通路。
该研究的第一作者之一、加州大学圣地亚哥分校生物科学研究生院博士生Janie Chang-Weinberg表示:“本质上,我们训练小鼠大脑按需自行产生广谱镇痛物质,且这些物质仅在需要镇痛的部位发挥作用,不会产生阿片类镇痛药物的脱靶效应。”
研究团队计划后续进一步探索安慰剂学习在脑内的发生机制,并在小鼠中评估不同的安慰剂训练策略,以期开发可直接转化应用的方案,帮助慢性疼痛患者建立安慰剂介导的疼痛耐受能力。
专业注释
- 腹外侧导水管周围灰质(vlPAG):脑干内调控疼痛信号传导的核心核团
- 光激活纳洛酮(PhNX):可通过光照精准调控作用时机的阿片受体拮抗剂
- 安慰剂条件化:通过关联训练使个体建立预期、产生安慰剂效应的干预方式
