Characterization of regeneration initiating cells during Xenopus laevis tail regeneration
非洲爪蟾尾部再生过程中再生起始细胞的表征
| 期刊: | Genome Biology | 影响因子: | 10.100 |
| 时间: | 2024 | 起止号: | 2024 Oct 1;25(1):251. |
| doi: | 10.1186/s13059-024-03396-3 | 种属: | Xenopus |
| 研究方向: | 细胞生物学 | 细胞类型: | 其它细胞 |
文献解析
1. 领域背景与文献引入
文献英文标题:Characterization of regeneration initiating cells during Xenopus laevis tail regeneration;发表期刊:Genome Biology;影响因子:未公开;研究领域:两栖动物再生生物学。
再生是组织通过增殖和分化完全恢复缺失结构与功能的过程,区别于伴随瘢痕形成的修复。两栖动物(如非洲爪蟾)在胚胎期具有近乎完美的尾部再生能力,但发育至“refractory阶段”(胚胎第46期)后再生能力丧失,为研究再生调控提供了理想模型。现有研究揭示,再生依赖于胚基(blastema)形成、ECM重塑和免疫调控,但多集中在损伤后1天及以后的时间点,损伤后数小时内启动再生的关键细胞类型及机制尚未明确——这一空白直接限制了对再生启动的核心逻辑的理解。
非洲爪蟾尾部再生的早期(0.5-12小时)事件,如早期基因表达爆发、氧化应激和细胞状态转变,可能决定了再生的“开关”。本研究针对这一空白,整合多组学技术解析早期细胞动态,识别启动再生的关键细胞群(再生起始细胞,RICs),并验证其功能,为理解再生启动机制提供了全新视角。
2. 文献综述解析
文献综述按“再生基本概念→动物模型的再生能力→再生关键步骤→现有技术局限”的逻辑展开,核心评述如下:
现有研究的核心结论与局限
- 再生的关键机制:再生依赖胚基(增殖性祖细胞群)的形成,ECM重塑(MMPs降解ECM)和温和免疫反应促进再生,而成体强烈免疫反应导致瘢痕。
- 技术进展与局限:单细胞RNA-Seq揭示了再生相关细胞群(如ROCs),但研究集中在损伤后1天及以后,忽略了早期启动事件;空间转录组技术虽能解析细胞定位,但未应用于早期阶段;缺乏“refractory阶段”早期细胞变化的对比,无法解释再生能力的丧失。
本研究的创新价值
- 首次聚焦早期事件:针对损伤后0.5小时至12小时的细胞动态,识别出全新的再生起始细胞(RICs)。
- 多组学整合:通过bulk RNA-Seq(时间动态)、单细胞RNA-Seq(细胞异质性)和空间转录组(空间定位),从三维维度解析RICs特征。
- 功能验证:通过再生芽移除、MO抑制实验,明确RICs是再生启动的必要条件,揭示其通过ECM重塑促进胚基形成的机制。
3. 研究思路总结与详细解析
整体框架
研究目标:识别非洲爪蟾尾部再生早期的关键细胞群(RICs)并解析其功能;核心科学问题:再生启动阶段的关键细胞如何调控ECM重塑和胚基形成?;技术路线:“bulk RNA-Seq(时间动态)→单细胞RNA-Seq(细胞类型)→空间转录组(空间定位)→功能实验(验证必要性)”。
3.1 bulk RNA-Seq解析基因表达时间动态
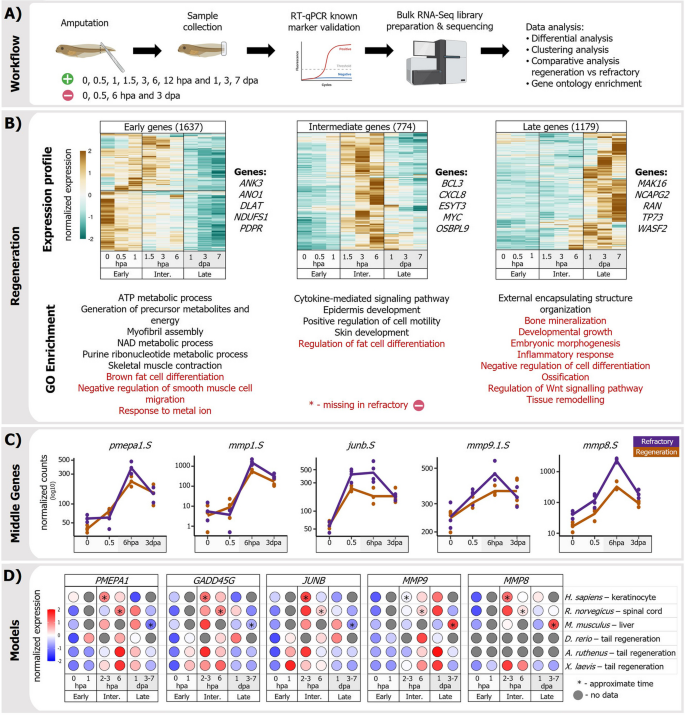
实验目的:识别再生和refractory阶段的差异表达基因(DEGs),划分再生的时间阶段。
方法细节:选取再生(第40期)和refractory(第46期)胚胎,损伤后0、0.5、1.5、3、6小时及1、3、7天收集尾部组织,提取总RNA进行bulk RNA-Seq(3-4个生物学重复)。通过DESeq2分析DEGs,按表达峰值分为早期(0.5-1.5 hpa)、中间(1.5-6 hpa)和晚期(1 dpa+)阶段。
结果解读:共鉴定4358个DEGs。早期DEGs包括早期反应基因(fos、jun)和代谢基因(氧化磷酸化相关ndufa);中间DEGs与ECM重塑(mmp1/8/9)、细胞迁移(epcam)和发育调控(sox11)相关;晚期DEGs涉及Wnt/TGFβ通路。对比再生与refractory阶段,中间DEGs在refractory阶段显著下调,提示其是再生启动的关键。
产品关联:文献未提及具体实验产品,领域常规使用RNA提取试剂盒(如Trizol)、bulk RNA-Seq文库制备试剂盒(如Lexogen SENSE)等。
3.2 单细胞RNA-Seq识别RICs细胞群
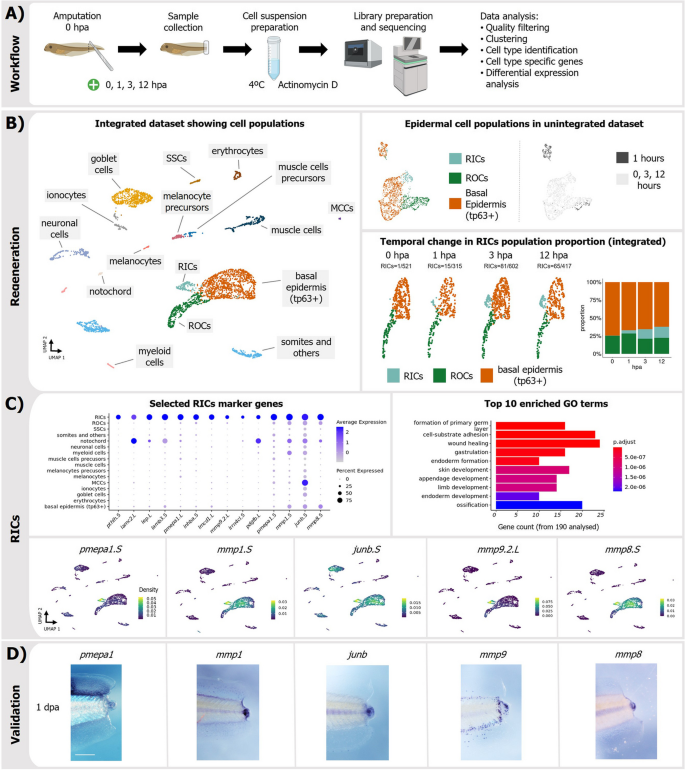
实验目的:解析再生早期的细胞异质性,识别启动再生的关键细胞群。
方法细节:选取再生胚胎损伤后0、1、3、12小时的尾部组织,解离为单细胞悬液(木瓜蛋白酶+蛋白酶,4℃操作),进行10x Genomics单细胞RNA-Seq(每个时间点约1000细胞,平均每个细胞覆盖~6000基因)。通过Seurat聚类、CellRank轨迹分析和scvelo velocity分析,注释细胞类型并识别RICs。
结果解读:基底表皮细胞(tp63+)在早期发生状态转变,形成RICs——仅在再生早期(1-12 hpa)出现,占基底表皮细胞的10%(12 hpa时)。RICs的标记基因包括mmp8、mmp9、pmepa1,其转录调控网络富集FOSL1、JUNB等再生相关转录因子。细胞通讯分析显示,RICs在3 hpa和12 hpa时与脊索细胞、基底表皮细胞的信号交流最活跃,涉及胶原蛋白、层粘连蛋白通路。
产品关联:文献未提及具体实验产品,领域常规使用单细胞解离试剂盒(如Miltenyi gentleMACS)、10x Genomics Chromium文库制备试剂盒等。
3.3 空间转录组解析RICs的空间定位
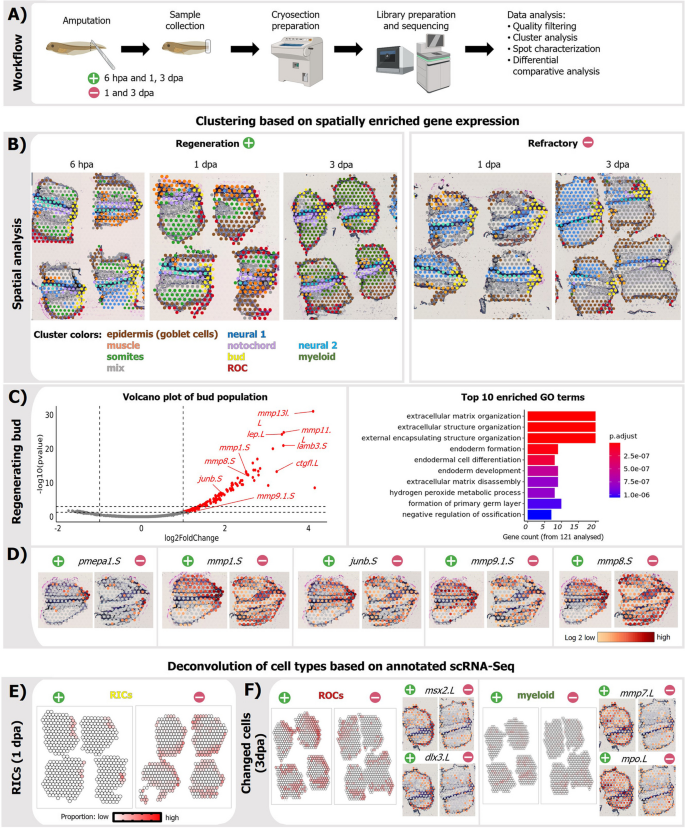
实验目的:确定RICs在再生组织中的空间分布,对比再生与refractory阶段的差异。
方法细节:选取再生和refractory胚胎损伤后6小时、1天、3天的尾部组织,进行10x Visium空间转录组测序(H&E染色成像,结合单细胞数据deconvolution)。
结果解读:RICs特异性富集在再生阶段的“再生芽”区域(损伤部位的增殖区),而refractory阶段RICs分散于尾部表面,未形成集中的再生芽。再生芽的基因表达与RICs标记基因(mmp8/9、pmepa1)高度重叠,且这些基因在再生芽中的表达比refractory阶段高5倍以上(空间转录组数据)。
产品关联:文献未提及具体实验产品,领域常规使用10x Visium空间转录组试剂盒、H&E染色试剂等。
3.4 功能实验验证RICs的必要性
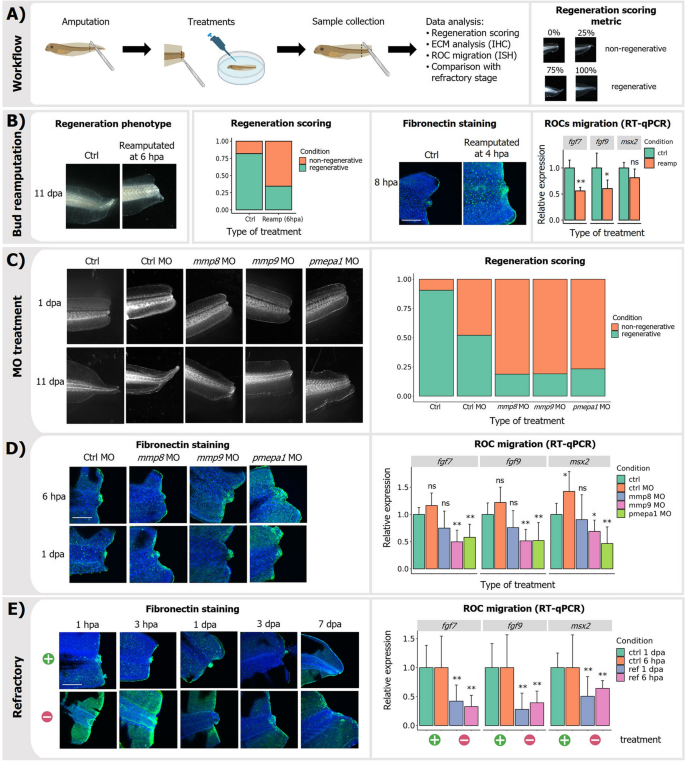
实验目的:验证RICs在再生启动中的作用,解析其机制。
方法细节:1)再生芽移除:损伤后6小时手动移除再生芽(富含RICs);2)MO抑制:用250 nM Vivo-MOs抑制mmp8、mmp9或pmepa1;3)表型分析:通过尾部形态评分(0-1分)、纤维连接蛋白免疫组化(纤维化程度)、RT-qPCR(ROCs标记基因msx2/dlx3)评估结果。
结果解读:1)再生芽移除后,胚胎失去再生能力(评分从0.75降至0.2),纤维连接蛋白沉积增加(荧光强度从100增至300),ROCs标记基因表达降低50%(n=100,P<0.01);2)抑制mmp8/9/pmepa1后,再生效率显著下降(评分<0.25),纤维化增加,ROCs迁移障碍。这些结果证明,RICs通过ECM重塑促进ROCs迁移和再生芽形成,是再生启动的必要条件。
产品关联:文献未提及具体实验产品,领域常规使用Gene Tools Vivo-MOs、抗纤维连接蛋白抗体(如Sigma F3648)、RT-qPCR试剂盒等。
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
本研究的Biomarker是RICs的分子标记(mmp8、mmp9、pmepa1),属于“细胞型Biomarker”(特定细胞群的分子特征)。筛选逻辑:
1. bulk RNA-Seq:识别中间阶段(1.5-6 hpa)上调的基因;
2. 单细胞RNA-Seq:筛选RICs特异性表达的基因(fold change>2x,Padj<0.05);
3. 空间转录组:验证基因在再生芽中的富集;
4. 功能实验:验证基因抑制后再生失败。
研究过程与核心成果
Biomarker来源:非洲爪蟾尾部再生早期的RICs细胞群(来自基底表皮细胞)。
验证方法与数据:
- 特异性:单细胞RNA-Seq显示,mmp8、mmp9、pmepa1在RICs中的表达比其他细胞群高2-5倍;
- 敏感性:bulk RNA-Seq显示,这些基因在再生阶段的3-6 hpa表达比损伤前高3-10倍;
- 与再生能力的相关性:空间转录组显示,refractory阶段这些基因的表达比再生阶段低50%以上。
核心成果:
1. Biomarker功能:mmp8/9通过降解ECM促进细胞迁移,pmepa1通过调控TGFβ信号抑制纤维化;
2. 再生预测价值:这些Biomarker的表达水平与再生能力正相关(再生阶段高表达,refractory阶段低表达);
3. 统计学验证:抑制mmp8后,再生评分从0.75±0.1降至0.2±0.05(n=100,P<0.01);纤维连接蛋白荧光强度从100±10增至300±20(n=5,P<0.01);ROCs标记基因msx2表达从1.0±0.1降至0.3±0.05(n=3,P<0.05)。
本研究通过多组学整合和功能验证,首次识别出再生启动的关键细胞RICs及其Biomarker,为理解再生启动机制提供了全新的细胞和分子靶点,也为再生医学的转化研究(如促进成体组织再生)提供了理论基础。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。