1. 领域背景与文献
文献英文标题:Clinical characteristics, prognostic factors, and management strategies of immune checkpoint inhibitor-related pneumonitis across diverse malignancies;发表期刊:Cancer Immunology, Immunotherapy;影响因子:未公开;研究领域:肿瘤免疫治疗不良反应(免疫检查点抑制剂相关肺炎)
领域共识:肿瘤免疫治疗是近10年肿瘤学领域的核心突破,2011年首个免疫检查点抑制剂(ICI)获批上市后,以PD-1/PD-L1抑制剂为代表的ICIs通过阻断免疫抑制通路重新激活抗肿瘤免疫,显著改善了多种晚期恶性肿瘤患者的生存预后。随着ICIs的广泛应用,免疫相关不良反应(irAEs)成为临床管理的核心挑战,其中ICI相关肺炎是最严重的irAEs之一,报道发生率为3%-5%,占ICI相关死亡病例的约35%。当前临床指南推荐≥2级肺炎需停用ICI,3-4级肺炎需永久停药,但这可能中断有效的抗肿瘤治疗;同时,现有研究多集中于肺癌患者,缺乏跨多种恶性肿瘤的ICI肺炎特征对比数据,也未明确不同肿瘤类型中ICI继续治疗的安全性及预后预测因素,这些空白限制了ICI肺炎的个体化管理。
本研究针对上述核心问题,通过大样本回顾性队列分析,系统对比了肺癌与非肺癌患者中ICI肺炎的临床特征,筛选出致命性肺炎的预后因素,并探索了ICI继续治疗的可行性及预测因素,为跨肿瘤类型的ICI肺炎管理提供了循证依据。
2. 文献综述解析
原文综述部分以“ICIs疗效-irAEs挑战-ICI肺炎的特殊性-现有研究局限”为核心逻辑展开评述,首先按“疗效突破-不良反应风险”的维度梳理了ICIs的临床应用现状,明确ICIs在多种肿瘤中的生存获益,同时指出irAEs是其广泛应用的主要障碍;随后聚焦ICI肺炎这一细分领域,按“发生率-死亡率-现有指南推荐”的维度总结了当前认知,强调ICI肺炎的高致死性及现有指南中停药推荐的局限性;最后提出研究空白:现有研究多基于肺癌人群,不同恶性肿瘤中ICI肺炎的临床特征是否具有一致性尚未明确,ICI继续治疗的安全性及预测因素缺乏跨肿瘤类型的验证数据。
现有研究的关键结论包括:ICI肺炎的发生率约3%-5%,致死率高;现有指南推荐基于肺炎分级决定ICI停药策略;部分小样本研究提示ICI重新挑战可能改善生存,但肺炎的复发率高于其他irAEs。现有研究的技术方法优势在于多采用回顾性队列设计,能反映真实世界临床实践;局限性则体现在研究人群多集中于肺癌,样本量较小,缺乏跨肿瘤类型的对比分析,且关于ICI继续治疗的预测因素数据不足。
本研究的创新价值在于首次基于1320例跨多种恶性肿瘤的大样本队列,系统对比了肺癌与非肺癌患者中ICI肺炎的临床特征,验证了ICI肺炎的临床特征及预后因素在不同肿瘤类型中的一致性,同时明确了ICI继续治疗的可行性及潜在预测因素,填补了跨肿瘤类型ICI肺炎管理的研究空白,为临床个体化决策提供了更全面的循证依据。
3. 研究思路总结与详细解析
整体研究框架:本研究的核心目标是明确不同恶性肿瘤患者中ICI肺炎的临床特征、致命性肺炎的预后因素,以及ICI继续治疗的可行性及预测因素;核心科学问题为ICI肺炎的临床特征是否跨肿瘤类型一致,哪些临床、影像及实验室指标可预测致命性肺炎,哪些因素支持安全继续ICI治疗;技术路线采用“回顾性队列构建-分组对比分析-单因素回归筛选预后因素”的逻辑闭环,通过大样本队列数据验证研究假设。
3.1 研究队列构建与数据收集
实验目的:构建符合研究要求的回顾性队列,系统收集患者临床、治疗及结局数据。
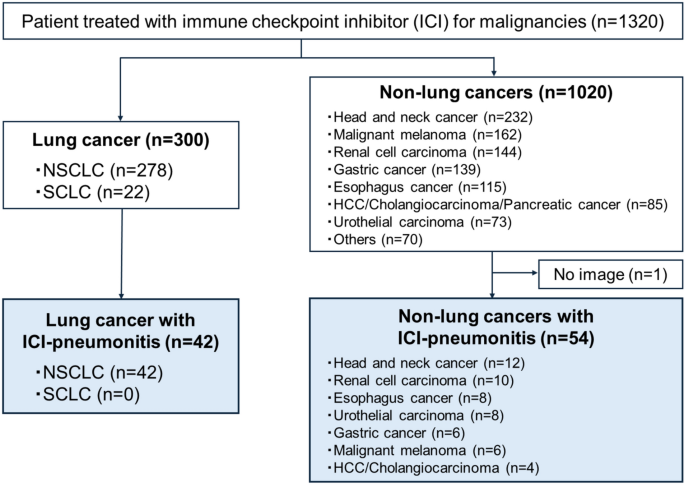
方法细节:回顾性纳入日本九州大学医院2014年9月至2023年3月期间接受ICI治疗的1320例晚期恶性肿瘤患者,按肿瘤类型分为肺癌组(300例)和非肺癌组(1020例),通过电子病历系统收集患者人口统计学特征、治疗细节、实验室检查、影像学结果及生存结局数据,临床随访截止至2025年7月31日。
结果解读:最终从1320例患者中筛选出96例发生ICI肺炎的患者,其中肺癌组发生率为14.0%(42/300),非肺癌组为5.3%(54/1020);非肺癌患者中尿路上皮癌的ICI肺炎发生率最高(11.0%),其次为食管癌(7.0%)。
产品关联:文献未提及具体实验产品,领域常规使用电子病历系统、医学影像存档与通信系统(PACS)等。
3.2 临床评估与诊断标准制定
实验目的:统一ICI肺炎的诊断、分级及影像学评估标准,确保研究数据的一致性。
方法细节:基线胸部计算机断层扫描(CT)用于评估背景肺异常,肺气肿、间质性肺异常(ILA)、间质性肺疾病(ILD)均采用国际公认的影像学诊断标准;ICI肺炎的诊断由多学科团队(肿瘤学、呼吸病学、放射学专家及护理、药学人员)结合临床症状、实验室检查及影像学结果确诊,排除感染、肿瘤进展等其他病因;肺炎严重程度采用不良事件通用术语标准(CTCAE)5.0版分级,致命性肺炎定义为诊断后30天内因肺炎导致的呼吸衰竭死亡,且无快速肿瘤进展证据。
结果解读:两名独立呼吸科医师对影像学模式的分类一致性较高(Cohen’s κ=0.782,95%CI 0.727-0.834),确保了影像学评估的可靠性。
产品关联:文献未提及具体实验产品,领域常规使用胸部CT扫描仪、CTCAE分级系统等。
3.3 ICI肺炎临床特征跨肿瘤类型对比分析
实验目的:对比肺癌与非肺癌患者中ICI肺炎的临床特征,验证其跨肿瘤类型的一致性。
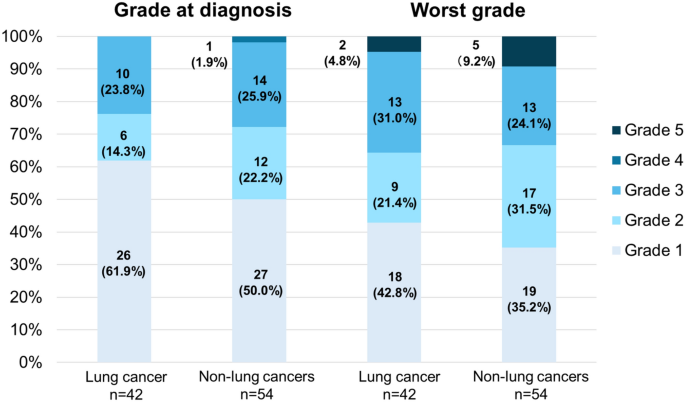
方法细节:从基线特征、肺炎发病时间、影像学模式、肺炎分级、治疗策略及结局等维度,对肺癌组与非肺癌组ICI肺炎患者进行对比分析,采用Student’s t检验、Mann-Whitney U检验、卡方检验或Fisher精确检验进行统计学分析。
结果解读:两组患者在肺炎发病时间、实验室指标(CRP、KL-6)、肺炎分级分布、治疗策略及结局方面无显著差异;影像学模式方面,肺癌组中机化性肺炎(OP)模式占比更高(78.6% vs 59.3%),非肺癌组中非特异性间质性肺炎(NSIP)模式占比更高(22.2% vs 7.1%),但整体分布无统计学差异(P=0.085)。
产品关联:文献未提及具体实验产品,领域常规使用临床实验室检测设备(如CRP、KL-6检测试剂盒)等。
3.4 致命性ICI肺炎预后因素分析
实验目的:筛选出预测致命性ICI肺炎的临床、影像及实验室因素,为风险分层提供依据。
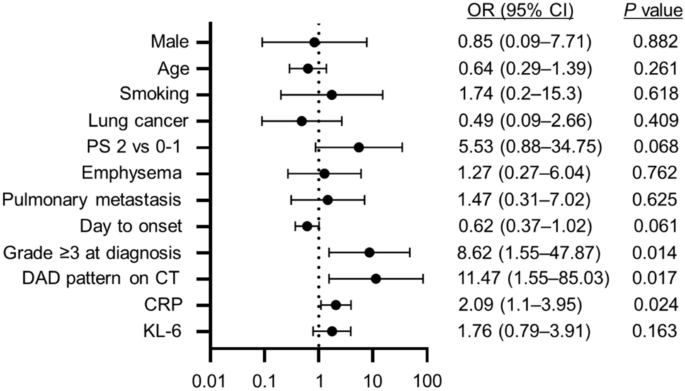
方法细节:采用单因素logistic回归分析,对96例ICI肺炎患者的基线特征、肺炎诊断时的临床指标与致命性肺炎结局进行关联分析,计算比值比(OR)及95%置信区间(CI)。
结果解读:弥漫性肺泡损伤(DAD)影像学模式(OR=11.47,95%CI 1.55-85.03,P=0.017)、诊断时≥3级肺炎(OR=8.62,95%CI 1.55-47.87,P=0.014)、诊断时CRP水平升高(OR=2.09,95%CI 1.10-3.95,P=0.024)是致命性肺炎的独立预测因素;ECOG体能状态≥2(OR=5.53,95%CI 0.88-34.75,P=0.068)及肺炎发病时间更短(OR=0.62,95%CI 0.37-1.02,P=0.061)显示出风险升高的趋势,但未达统计学显著性。
产品关联:文献未提及具体实验产品,领域常规使用统计学分析软件(如R语言)等。
3.5 ICI继续治疗可行性及预测因素分析
实验目的:评估ICI肺炎患者继续ICI治疗的可行性,并筛选出预测成功继续治疗的因素。
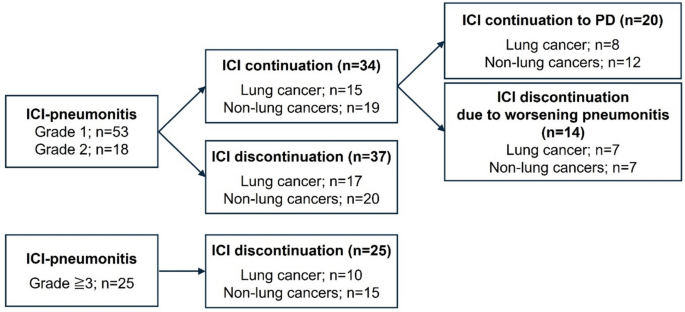
方法细节:首先分析ICI肺炎患者后续治疗策略的分布,随后对尝试继续ICI治疗的34例患者进行随访,对比成功维持治疗至疾病进展与因肺炎恶化停药患者的基线特征,采用单因素logistic回归分析筛选预测因素。
结果解读:35.7%的肺癌患者和35.2%的非肺癌患者在肺炎后尝试继续ICI治疗,其中58.8%(20/34)成功维持治疗至疾病进展,中位维持时间为114天;基线正常肺实质(无ILA或ILD)与成功继续治疗呈趋势性关联(OR=0.13,95%CI 0.01-1.34,P=0.087),提示无基线间质性肺异常的患者可能更适合继续ICI治疗。
产品关联:文献未提及具体实验产品,领域常规使用临床随访系统、统计学分析软件等。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究涉及两类Biomarker:一类是致命性ICI肺炎的预测Biomarker,包括弥漫性肺泡损伤(DAD)影像学模式、诊断时≥3级肺炎、C反应蛋白(CRP)升高;另一类是ICI继续治疗成功的潜在预测Biomarker,即基线正常肺实质(无ILA/ILD)。筛选与验证逻辑为:基于大样本回顾性队列,通过单因素logistic回归分析,从临床、影像、实验室指标中筛选与结局显著相关的因素,其中致命性肺炎的Biomarker通过96例ICI肺炎患者的结局数据验证,ICI继续治疗的Biomarker通过34例尝试继续治疗患者的随访数据验证。
研究过程详述
致命性ICI肺炎的Biomarker来源为患者的胸部CT影像(DAD模式)、肺炎严重程度分级、实验室检测结果(CRP);验证方法为单因素logistic回归分析,具体数据包括:DAD模式的OR=11.47(95%CI 1.55-85.03,P=0.017),诊断时≥3级肺炎的OR=8.62(95%CI 1.55-47.87,P=0.014),CRP水平升高的OR=2.09(95%CI 1.10-3.95,P=0.024)。ICI继续治疗成功的Biomarker来源为患者的基线胸部CT影像(正常肺实质);验证方法为单因素logistic回归分析,数据为OR=0.13(95%CI 0.01-1.34,P=0.087),虽未达统计学显著性,但显示出趋势性关联。
核心成果提炼
致命性ICI肺炎的Biomarker具有明确的预后价值,DAD模式、≥3级肺炎、高CRP水平提示患者致命风险显著升高,临床需强化治疗及监测;基线正常肺实质作为潜在Biomarker,提示无基线间质性肺异常的患者尝试继续ICI治疗的风险较低,可为个体化治疗决策提供参考。本研究的创新性在于首次在跨多种恶性肿瘤的大样本队列中验证了这些Biomarker的价值,打破了现有研究局限于肺癌人群的限制,为ICI肺炎的跨肿瘤类型管理提供了循证依据。其中,致命性肺炎Biomarker的统计学结果均具有显著性(P<0.05),ICI继续治疗Biomarker的结果显示趋势性关联(P=0.087),样本量分别为n=96(致命性肺炎分析)和n=34(ICI继续治疗分析)。