1. 领域背景与文献
文献英文标题:Multi-omics profiling reveals an immunosuppressive plasma cell subset within tertiary lymphoid structures in cervical cancer;发表期刊:Cancer Immunology, Immunotherapy;影响因子:未公开;研究领域:肿瘤免疫学(宫颈癌肿瘤免疫微环境调控)。
领域共识:宫颈癌是全球女性第四大常见恶性肿瘤,也是癌症相关死亡的第六位原因,尽管筛查和治疗手段不断进步,晚期宫颈癌患者仍因复发和转移面临较差的预后,深入解析肿瘤免疫微环境的调控机制是发现新型生物标志物和治疗靶点的核心方向。既往肿瘤免疫研究多聚焦于T细胞的抗肿瘤作用,B细胞在肿瘤微环境中的功能异质性尚未被充分解析,尤其是宫颈癌中B细胞及浆细胞亚群的分类、功能表型及临床意义尚不明确。近年研究显示三级淋巴结构(TLS)是肿瘤微环境中免疫细胞相互作用的重要场所,通常与患者良好预后相关,但部分三级淋巴结构可呈现免疫抑制表型,其内在的细胞组成及调控机制尚未阐明。本研究针对宫颈癌中B细胞功能研究不足的领域空白,通过多组学整合分析解析B细胞异质性,鉴定功能异常的浆细胞亚群及其免疫调控机制,为宫颈癌的预后评估和免疫治疗新靶点开发提供理论依据。
2. 文献综述解析
作者在综述部分按照免疫细胞类型、B细胞亚群功能、三级淋巴结构免疫调控作用三个维度梳理现有研究进展,系统对比了不同研究的结论差异与技术局限性,为本次研究的创新设计提供了立论基础。
现有研究已证实T细胞是抗肿瘤免疫的核心效应细胞,其功能状态直接决定了免疫治疗的响应率,而B细胞可通过分泌肿瘤特异性抗体、呈递抗原等方式参与免疫调控,其中浆细胞作为抗体分泌细胞,是体液免疫的核心组成部分。在技术层面,单细胞RNA测序(scRNA-seq)、空间转录组等多组学技术的发展,为在单细胞分辨率和空间层面解析免疫细胞的异质性及细胞间互作提供了可靠工具,已被广泛应用于多种肿瘤的免疫微环境研究。但现有研究仍存在明显局限性:一是宫颈癌中B细胞的亚群分类及功能表型尚未被系统解析,尤其是浆细胞的异质性及功能差异缺乏研究证据;二是三级淋巴结构中的B细胞亚群组成及其与其他免疫细胞的空间互作机制尚不明确,无法解释部分三级淋巴结构的免疫抑制表型;三是缺乏可用于宫颈癌预后评估和治疗响应预测的B细胞相关生物标志物。本研究的创新价值在于首次在宫颈癌中系统鉴定出功能相反的两群浆细胞亚群,明确了HSPA1B阳性浆细胞在三级淋巴结构中的免疫抑制作用,揭示了其与调节性T细胞(Treg)、辅助性T细胞17(Th17)的空间共定位及互作机制,填补了领域内宫颈癌B细胞异质性及三级淋巴结构免疫抑制亚型的研究空白,为后续的免疫治疗靶点开发提供了新方向。
3. 研究思路总结与详细解析
本研究的核心目标是系统解析宫颈癌肿瘤微环境中B细胞的异质性,明确不同浆细胞亚群的功能特征、临床意义及免疫调控机制,整体技术路线遵循“多组学数据整合→细胞亚群鉴定→功能验证→预后关联→空间互作解析→机制推导”的闭环逻辑,核心科学问题为宫颈癌中不同浆细胞亚群的功能差异是什么,以及免疫抑制性浆细胞如何参与三级淋巴结构的免疫抑制微环境形成。
3.1 样本收集与单细胞测序数据预处理
实验目的为获取高质量的宫颈癌及正常宫颈组织B细胞单细胞转录组数据,排除低质量细胞和批次效应对后续分析的干扰,为B细胞异质性解析提供可靠的基础数据集。方法细节:研究共纳入65例样本,分为发现队列和验证队列,其中发现队列包含17例样本(12例宫颈癌组织、5例正常宫颈组织),其中3例为新纳入的HPV阳性宫颈癌患者临床样本,其余5735个B细胞来自已发表的宫颈癌及正常宫颈组织公开数据集;验证队列包含48例未接受治疗的宫颈癌样本,来自GEO等公共数据库。临床样本处理阶段,采用流式细胞术分选CD45+CD19+的活B细胞,分选前使用BioLegend的CD19、CD45单克隆抗体4℃孵育15分钟,7-AAD染色标记死细胞,通过BD FACSAria III细胞分选仪完成细胞分离。测序数据预处理采用Seurat(版本4.9.9)软件进行降维与无监督聚类,DoubletFinder(版本2.0.3)去除双细胞,质控标准为每个细胞检测基因数介于450~4500、UMI数≤40000、线粒体基因占比≤20%,使用LogNormalize方法(缩放因子10000)对表达矩阵进行归一化,采用Harmony算法去除不同数据集的批次效应。结果解读:经质控后共获得15876个高质量细胞,其中发现队列包含7903个B细胞,验证队列包含7973个细胞,无低质量数据干扰,可用于后续细胞亚群分类分析。实验所用关键产品:BioLegend的CD19(克隆号HIB19)、CD45(克隆号2D1)小鼠抗人单克隆抗体,eBioscience的7-AAD活性染色液,BD FACSAria III细胞分选仪。
3.2 B细胞亚群分类与特征分析
实验目的为基于单细胞转录组数据解析宫颈癌中B细胞的异质性,鉴定具有不同分子特征的B细胞亚群,为后续浆细胞功能研究提供分类基础。方法细节:采用均匀流形近似与投影(UMAP)进行降维可视化,通过Seurat的“Find All Markers”函数识别每个细胞亚群的特征基因,基于B细胞谱系特异性标记基因的表达模式进行细胞类型注释。结果解读:共鉴定出9个B细胞亚群,包括4个非浆细胞B细胞亚群和5个浆细胞亚群,其中非浆细胞亚群分别为CD37+记忆B细胞、GPR34+记忆B细胞、IFIT3+记忆B细胞、TTN+初始B细胞,浆细胞亚群为IGKC+浆细胞、HSPA1B+浆细胞(HSPA1B_PC)、MANF+浆细胞(MANF_PC)、IGHA1+浆细胞、IGLC2+浆细胞。初始B细胞高表达MS4A1、低表达CD27,符合初始B细胞的分子特征;记忆B细胞共表达CD27和MS4A1,符合记忆B细胞的标记特征。对应的分析结果通过UMAP图和标记基因气泡图呈现(图1)。
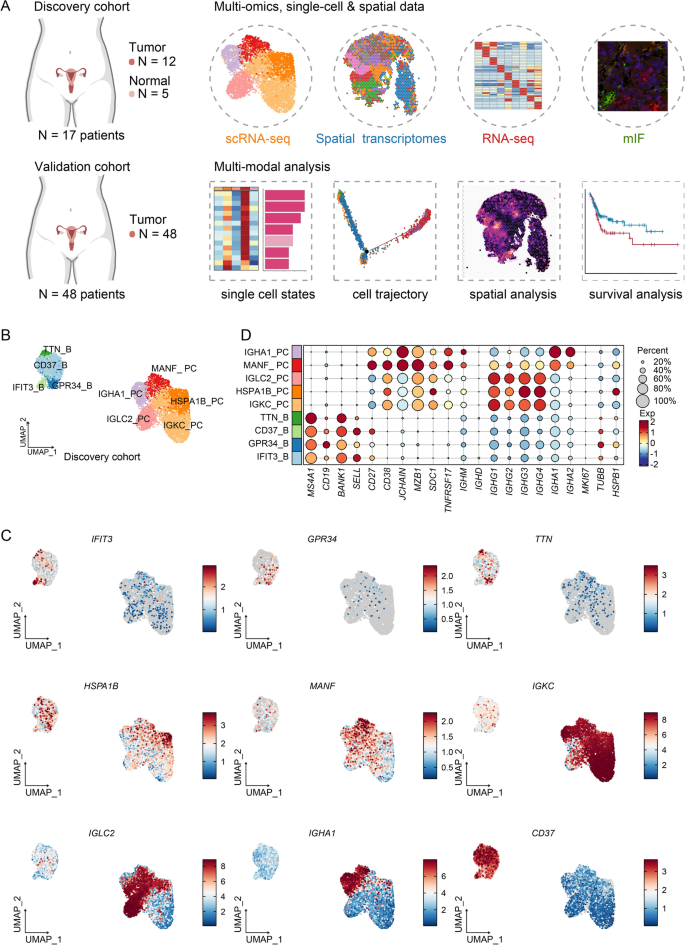
。文献未提及额外实验产品,领域常规使用Seurat、Harmony等R包完成单细胞数据的聚类与注释分析。
3.3 IgA与IgG型浆细胞的功能差异分析
实验目的为比较IgA+和IgG+浆细胞在正常宫颈和宫颈癌组织中的比例差异,解析两类浆细胞的功能特征差异,明确其在肿瘤微环境中的不同作用。方法细节:统计正常组织和肿瘤组织中各B细胞亚群的占比,采用秩和检验比较组间比例差异,通过基因本体(GO)富集分析解析两类浆细胞的功能通路差异,分别比较其在正常组织和肿瘤组织中的通路激活特征。结果解读:记忆B细胞和初始B细胞的比例在正常和肿瘤组织中无显著差异(n=17,P>0.05);肿瘤组织中IgA+浆细胞的比例显著降低,IgG+浆细胞的比例显著升高(n=17,P<0.05)。功能富集分析显示,IgA+浆细胞富集于内质网应激反应、蛋白折叠、B细胞活化等通路,提示其处于抗体合成活跃的功能状态;IgG+浆细胞富集于氧化应激反应、凋亡信号调控通路,提示其处于应激状态。在肿瘤微环境中,IgA+浆细胞上调免疫激活相关通路,包括B细胞活化正调控、免疫球蛋白介导的免疫反应、抗病毒防御反应等;IgG+浆细胞上调免疫抑制和凋亡相关通路,包括免疫反应负调控、半胱氨酸型内肽酶活性正调控等。对应的分析结果通过细胞比例箱线图、GO富集分析图呈现(图2)。
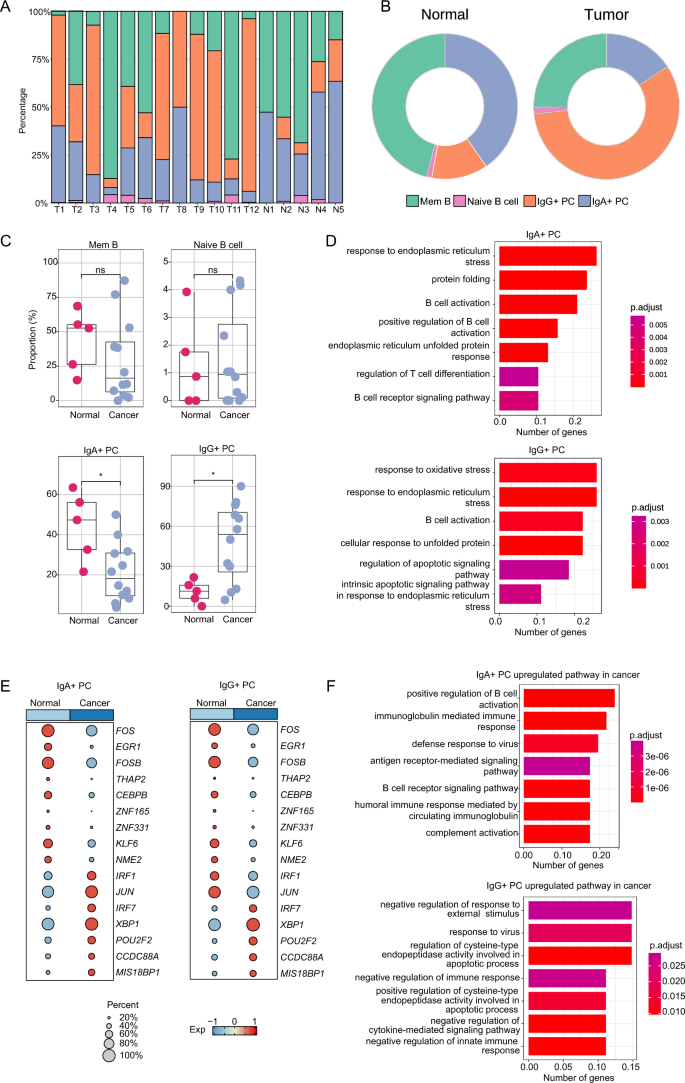
。实验所用分析工具为ClusterProfiler(版本4.6.2)R包。
3.4 浆细胞亚群的精细鉴定与验证
实验目的为进一步解析5个浆细胞亚群的分子特征和组织分布差异,在组织水平和独立队列中验证HSPA1B_PC亚群的存在,确保亚群鉴定的可靠性。方法细节:对5个浆细胞亚群的特征基因进行表达谱聚类分析,统计各亚群在正常和肿瘤组织中的比例差异;采用多重免疫荧光(mIF)技术在宫颈癌组织切片中标记HSPA1B_PC,标记物为HSP70(HSPA1B的蛋白产物)、IGHG1、CD38,以DAPI进行核染色,通过酪酰胺信号放大法增强染色信号,使用PerkinElmer的Mantra系统进行切片扫描与图像分析;同时结合验证队列的单细胞转录组数据和空间转录组数据,交叉验证HSPA1B_PC亚群的存在。结果解读:IGKC_PC、HSPA1B_PC、IGLC2_PC在肿瘤组织中显著富集,MANF_PC在正常组织中显著富集(n=17,P<0.05);HSPA1B_PC高表达HSP70家族蛋白和IGHG系列基因,符合IgG型浆细胞的分子特征;多重免疫荧光结果显示宫颈癌组织中存在CD38+IGHG1+HSP70+的三阳性细胞,证实了HSPA1B_PC在组织水平的存在;验证队列的单细胞数据和空间转录组数据中均检测到该亚群的特征基因表达,进一步验证了亚群鉴定的准确性。对应的分析结果通过比例统计箱线图、特征基因热图、多重免疫荧光图呈现(图3)。
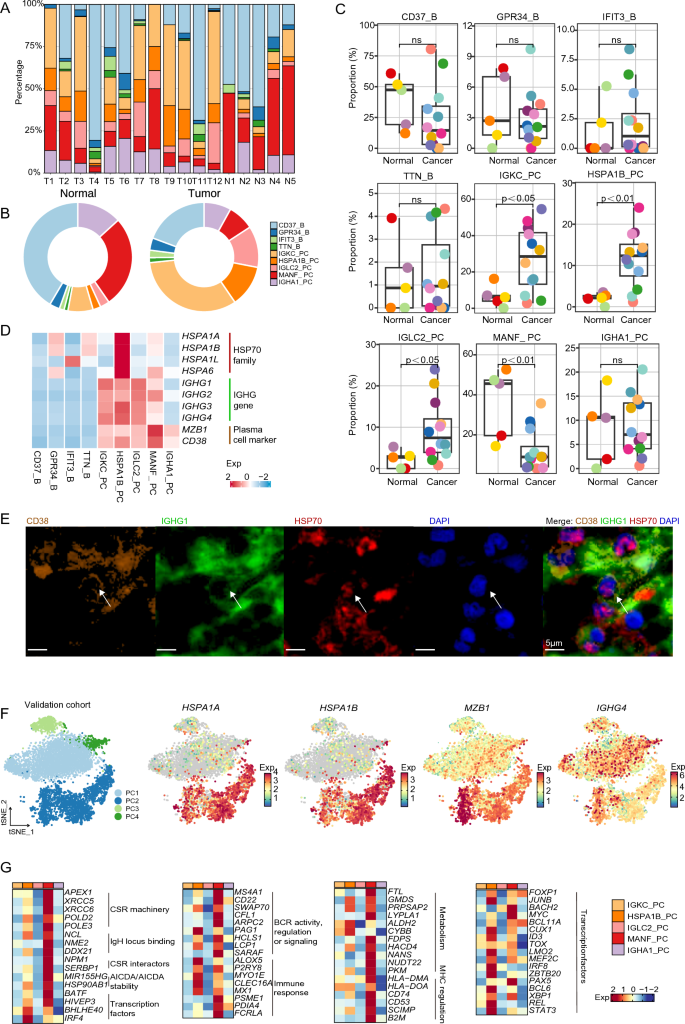
。实验所用关键产品:Abcam的HSP70抗体(货号ab181606)、Invitrogen的IGHG1抗体(货号PA5-75428)、Invitrogen的CD38抗体(货号PA5-95840),PerkinElmer的Mantra扫描系统。
3.5 MANF_PC的功能与预后价值分析
实验目的为明确MANF_PC的分化状态、功能特征及其与宫颈癌患者放疗预后的关联,评估其作为保护性生物标志物的潜力。方法细节:采用GO富集分析解析MANF_PC的功能通路特征;从TCGA数据库获取187例接受放疗的宫颈癌患者的bulk RNA测序数据和临床信息,基于单细胞数据筛选的MANF_PC前5个上调特征基因,采用单样本基因集富集分析(ssGSEA)计算每个样本的MANF_PC特征评分,通过survminer包的“surv_cutpoint”函数确定最佳截断值将患者分为高、低评分组,采用Kaplan-Meier曲线和log-rank检验比较两组的生存差异;采用monocle2(版本1.6.1)软件进行拟时序分析,解析MANF_PC的分化阶段及基因表达动态变化。结果解读:GO富集分析显示MANF_PC富集于内质网应激反应、蛋白折叠、淋巴细胞活化正调控、未折叠蛋白反应等通路,提示其处于抗体合成活跃的功能状态;拟时序分析显示MANF_PC处于B细胞分化的终末阶段,分化过程中B细胞特征基因PAX5、BACH2表达下调,抗体分泌细胞特征基因IRF4、XBP1、PRDM1表达上调,符合终末分化浆细胞的分子特征;生存分析显示,MANF_PC特征评分高的患者总体生存率显著高于评分低的患者(n=187,P=0.018),提示其与放疗良好响应相关。对应的分析结果通过GO富集图、生存曲线、拟时序分析图呈现(图4)。
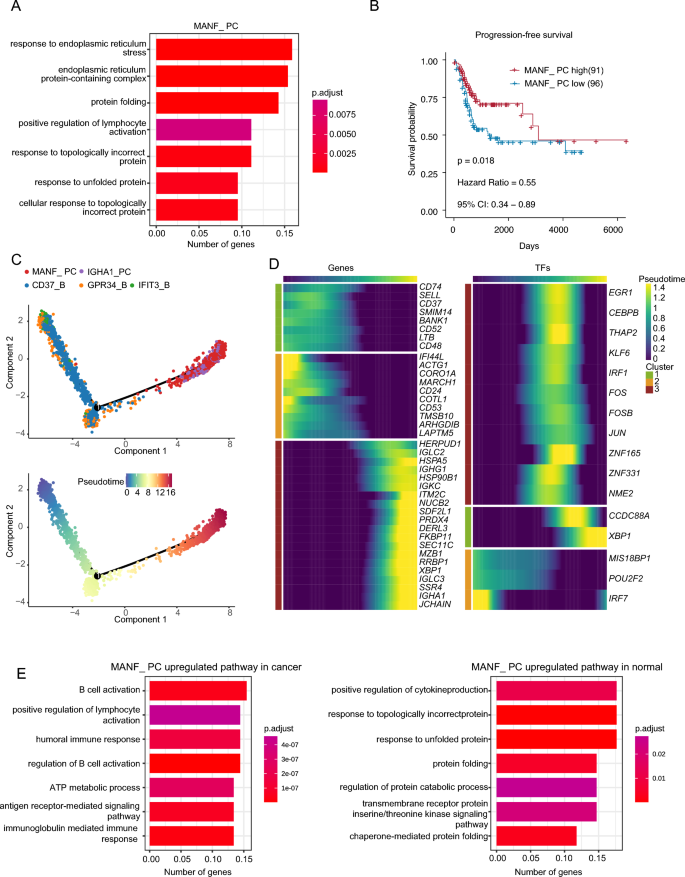
。实验所用分析工具为ClusterProfiler、ssGSEA、survminer、monocle2等R包。
3.6 HSPA1B_PC的功能与预后价值分析
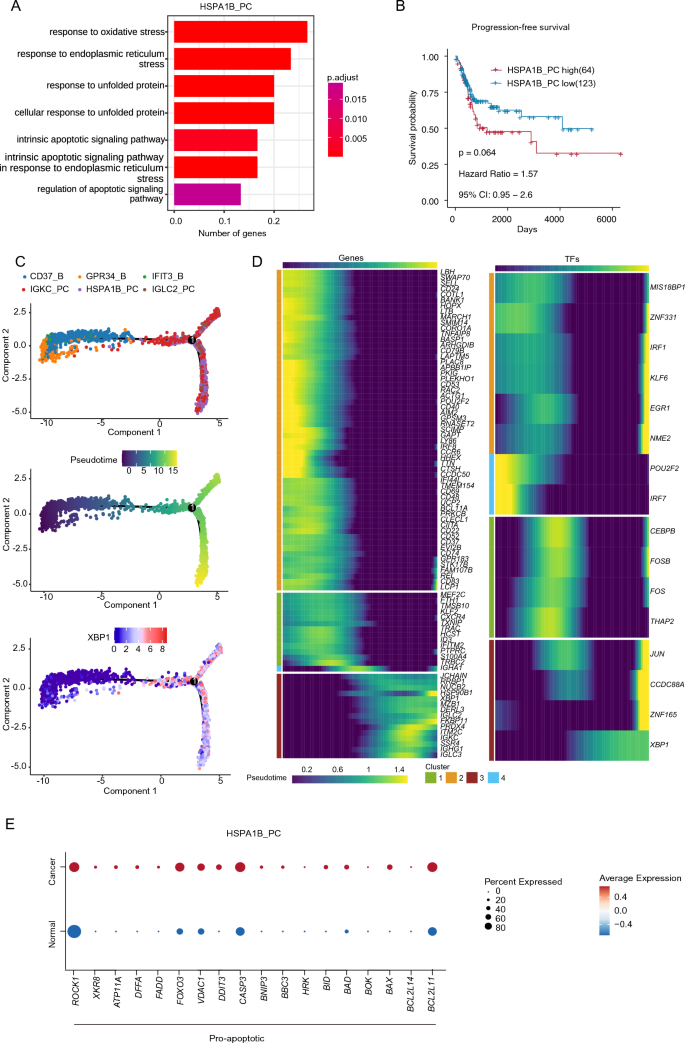
实验目的为明确HSPA1B_PC的功能特征、分化状态及其与宫颈癌患者放疗预后的关联,评估其作为不良预后生物标志物的潜力。方法细节:采用GO富集分析解析HSPA1B_PC的功能通路特征;采用与MANF_PC相同的TCGA队列分析方法,评估HSPA1B_PC特征评分与患者预后的关系;通过拟时序分析验证其分化状态,比较正常和肿瘤组织中HSPA1B_PC的促凋亡基因表达差异。结果解读:GO富集分析显示HSPA1B_PC富集于氧化应激反应、内质网应激、未折叠蛋白反应、内源性凋亡信号通路、凋亡信号调控等通路,提示其处于高应激和促凋亡状态;拟时序分析显示HSPA1B_PC也处于浆细胞的终末分化阶段,高表达XBP1等浆细胞成熟相关基因;肿瘤组织中的HSPA1B_PC高表达BCL2L11、BAX、BID、BIM等促凋亡基因,而正常组织中该亚群的促凋亡基因表达水平较低;生存分析显示,HSPA1B_PC特征评分高的患者总体生存率低于评分低的患者,差异接近统计学显著性(n=187,P=0.064),提示其与不良预后相关。对应的分析结果通过GO富集图、生存曲线、促凋亡基因表达热图呈现(图5)。
。分析工具同前序研究环节。
3.7 HSPA1B_PC与免疫抑制T细胞的空间互作分析
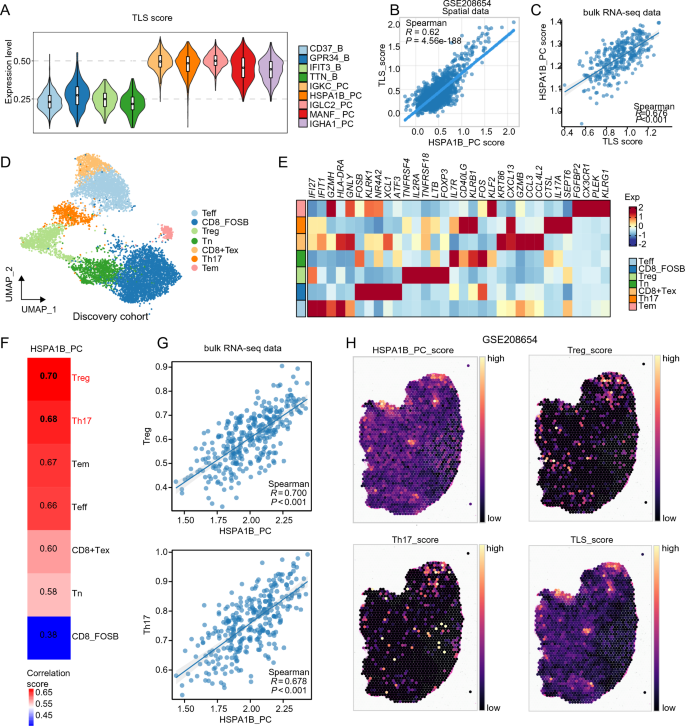
实验目的为解析HSPA1B_PC与T细胞亚群的相关性及空间共定位关系,揭示其在三级淋巴结构中的免疫调控机制,明确其参与免疫抑制微环境形成的分子基础。方法细节:对单细胞数据中的T细胞进行亚群注释,分为效应T细胞、调节性T细胞、初始T细胞、耗竭T细胞、辅助性T细胞17、效应记忆T细胞等亚群,采用斯皮尔曼相关性分析评估HSPA1B_PC丰度与各T细胞亚群比例的相关性;基于空间转录组数据计算HSPA1B_PC、Treg、Th17的特征评分及三级淋巴结构评分,分析其空间分布的共定位关系;采用配体-受体互作分析预测HSPA1B_PC与Treg、Th17细胞的潜在互作分子对。结果解读:HSPA1B_PC高表达三级淋巴结构相关标记基因,其特征评分与三级淋巴结构评分呈显著正相关(空间转录组数据r=0.62,P<0.001;bulk RNA测序数据r=0.58,P<0.001),提示其主要定位于三级淋巴结构中;T细胞亚群相关性分析显示,HSPA1B_PC的丰度与Treg、Th17细胞的比例呈显著正相关(TCGA数据中Treg相关系数r=0.51,P<0.001;Th17相关系数r=0.47,P<0.001),而与效应T细胞比例无显著相关性;空间转录组的空间特征图显示,HSPA1B_PC与Treg、Th17细胞在三级淋巴结构区域存在明显的空间共定位;配体-受体分析显示,HSPA1B_PC高表达SPP1,而Treg和Th17细胞高表达其受体CD44,SPP1-CD44是两群细胞间互作强度最高的分子对,提示该轴是HSPA1B_PC调控免疫抑制T细胞的关键机制。对应的分析结果通过相关性热图、空间特征图呈现(图6)。
。实验所用分析工具为Scanpy(版本1.8.2)、CellPhoneDB等。
4. Biomarker 研究及发现成果
本研究共鉴定出两个具有临床应用潜力的浆细胞生物标志物,分别是具有预后保护作用的MANF_PC和具有免疫抑制及不良预后提示作用的HSPA1B_PC,两类标志物的筛选和验证遵循“单细胞测序筛选→多队列验证→功能解析→临床关联→空间定位”的完整逻辑链条,为宫颈癌的预后评估和免疫治疗靶点开发提供了新的方向。
MANF_PC属于IgA型浆细胞亚群,其特征为高表达MANF、IRF4、XBP1等抗体合成相关基因,筛选逻辑为基于单细胞转录组的浆细胞亚群分类,通过功能富集和拟时序分析明确其终末分化和抗体合成的功能特征。该标志物的来源为B细胞分化终末阶段的浆细胞,在正常宫颈组织中富集,在肿瘤组织中比例降低。验证方法包括单细胞转录组的特征基因分析、拟时序分化轨迹分析、TCGA bulk队列的生存分析,其预后价值显示,高丰度MANF_PC的宫颈癌放疗患者总体生存风险降低48%,风险比HR=0.52(n=187,P=0.018,95%CI 0.31-0.87),提示其可作为放疗响应的保护性预测标志物。
HSPA1B_PC属于IgG型浆细胞亚群,是本研究首次在宫颈癌中鉴定的免疫抑制性浆细胞亚群,特征为高表达HSPA1B、IGHG1、CD38,筛选逻辑为基于浆细胞亚群的组织分布差异,重点解析肿瘤富集亚群的功能特征,通过多重免疫荧光、空间转录组等方法验证其存在和定位。该标志物主要来源于肿瘤微环境中的终末分化浆细胞,在宫颈癌组织中特异性富集。验证方法包括单细胞转录组特征分析、多重免疫荧光染色(CD38+IGHG1+HSP70+三阳性验证)、公共队列的交叉验证、空间转录组的定位分析,其预后价值显示,高丰度HSPA1B_PC的宫颈癌放疗患者总体死亡风险升高78%,风险比HR=1.78(n=187,P=0.064,95%CI 0.97-3.27),提示其为不良预后的潜在标志物。此外,该亚群的功能验证显示其高表达免疫抑制相关分子,包括TGFB3、PD-L1(CD274)、TIM-3(HAVCR2),可通过SPP1-CD44轴与Treg、Th17细胞相互作用,促进免疫抑制微环境的形成。
核心成果方面,本研究首次揭示了宫颈癌中浆细胞的功能异质性,其中MANF_PC作为保护性生物标志物,与抗体合成和免疫激活相关,可用于预测宫颈癌患者的放疗响应;HSPA1B_PC作为免疫抑制性生物标志物,是宫颈癌三级淋巴结构免疫抑制亚型的关键组成部分,其通过多重机制促进免疫抑制微环境的形成,是宫颈癌预后评估和免疫治疗的潜在新靶点。文献未明确提供两类标志物作为诊断或预后检测的敏感性、特异性及ROC曲线数据,后续需扩大临床样本量进一步验证其临床应用价值。
