1. 领域背景与文献
文献英文标题:Neoadjuvant chemotherapy stimulates NK cell recruitment via tumor-derived CCL8 in gastric cancer;发表期刊:未明确;影响因子:未公开;研究领域:胃癌免疫治疗与新辅助化疗。
胃癌是全球发病率和死亡率均位居前列的消化系统恶性肿瘤,局部进展期胃癌的标准治疗方案已从单纯手术过渡到新辅助化疗(NACT)联合手术的模式,其中SOX方案(奥沙利铂联合S-1)是东亚地区的I级推荐方案。领域发展关键节点包括大型随机对照试验证实NACT可提高手术根治性切除率、清除隐匿微转移灶、改善患者生存预后,但仍有部分患者对NACT反应不佳,获益有限。当前研究热点聚焦于NACT的免疫调节作用,尤其是其对肿瘤免疫微环境(TIME)的重塑效应,以及与免疫检查点抑制剂等免疫治疗的联合应用潜力。然而,现有研究多围绕CD8⁺T细胞等免疫细胞展开,对自然杀伤(NK)细胞在NACT中的具体作用及调控机制尚未明确,这一空白限制了针对NK细胞的联合治疗策略开发。本研究旨在揭示NACT调控胃癌NK细胞募集的分子机制,为优化胃癌新辅助治疗方案、拓展NK细胞免疫治疗的应用场景提供理论依据与实验支持。
2. 文献综述解析
本研究的文献综述以免疫细胞类型和化疗免疫调节作用为核心分类维度,系统梳理了领域内现有研究的进展与不足。现有研究表明,NACT可通过诱导免疫原性细胞死亡(ICD)、增强肿瘤免疫原性,重塑胃癌TIME,具体表现为增加CD8⁺T细胞浸润、减少肿瘤相关巨噬细胞和调节性T细胞(Tregs)的比例,从而增强抗肿瘤免疫应答;同时,化疗药物与免疫细胞的直接相互作用被认为是其与免疫治疗产生协同效应的重要基础。但现有研究存在明显局限性,多数研究聚焦于CD8⁺T细胞的功能,对NK细胞在NACT中的作用及调控机制探讨不足,且部分研究缺乏配对的NACT前后临床样本分析,无法精准反映个体免疫微环境的动态变化,对患者异质性的影响也未充分阐释。
本研究的创新价值在于填补了NK细胞在胃癌新辅助化疗领域的研究空白,首次明确了NACT通过激活MAPK通路诱导胃癌细胞分泌趋化因子CCL8,进而募集NK细胞的分子机制,为NACT与NK细胞免疫治疗的联合应用提供了直接的理论依据。通过对比现有研究未解决的核心问题,本研究不仅验证了NK细胞在NACT抗肿瘤效应中的关键作用,还阐明了其上游调控通路,为胃癌精准免疫治疗靶点的开发提供了新方向。
3. 研究思路总结与详细解析
本研究的整体框架围绕“明确NACT对胃癌NK细胞的调控作用及分子机制”这一核心目标展开,核心科学问题聚焦于NACT如何调控NK细胞在肿瘤微环境中的募集,技术路线遵循“临床样本观察→动物模型验证→体外机制解析→临床案例验证”的闭环逻辑,通过多维度实验设计系统揭示了NACT调控NK细胞的分子通路。
3.1 临床样本免疫细胞浸润分析
实验目的是评估NACT对胃癌患者肿瘤免疫微环境中各类免疫细胞浸润的影响,明确与治疗反应相关的关键免疫细胞。方法细节为收集33例胃癌患者的55份标本(其中22对为NACT前活检与NACT后手术的配对样本),采用免疫组化(IHC)和免疫荧光技术检测CD4⁺T细胞、CD8⁺T细胞、NK细胞、B细胞、巨噬细胞及树突状细胞(DCs)的浸润水平,同时通过卡方检验分析免疫细胞浸润变化与临床治疗反应的相关性。结果解读:免疫组化图(Fig.1A)显示,与NACT前活检标本相比,NACT后手术标本中CD4⁺T细胞、CD8⁺T细胞、NK细胞等多种抗肿瘤免疫细胞的浸润水平显著升高,SOX方案治疗的患者呈现一致趋势;22对配对样本分析显示多数患者的免疫细胞变化趋势与整体队列一致,但存在个体异质性;卡方检验结果表明,NACT后CD8⁺T细胞和NK细胞浸润水平的升高与更优的临床反应显著相关(Fig.1B)。实验所用关键产品:免疫组化及免疫荧光抗体(具体信息见表S1)、Aperio ImageScope图像分析软件;领域常规使用免疫组化试剂盒、流式细胞术检测试剂等。

3.2 小鼠模型验证NACT对NK细胞的调控作用
实验目的是在体内模型中验证NACT对NK细胞浸润的调控效应,明确NK细胞在NACT抗肿瘤作用中的功能。方法细节为构建C57BL/6小鼠MFC胃癌皮下移植模型,采用SOX方案进行治疗,通过流式细胞术检测肿瘤组织及外周血中各类免疫细胞的比例;同时使用Rag1⁻/⁻(T、B细胞缺陷)和NCG(T、B、NK细胞缺陷)小鼠进行对比实验,验证NK细胞的特异性作用。结果解读:Fig.2显示SOX方案可显著抑制小鼠肿瘤生长,同时增加肿瘤组织中CD8⁺T细胞、NK细胞等抗肿瘤免疫细胞的浸润比例;外周血免疫分析显示CD4⁺T细胞、CD8⁺T细胞比例升高,巨噬细胞、中性粒细胞比例降低;NCG小鼠中SOX方案的抗肿瘤效果显著弱于C57BL/6和Rag1⁻/⁻小鼠,证明NK细胞是介导SOX方案抗肿瘤效应的关键免疫细胞(Fig.3)。实验所用关键产品:MFC细胞系(Shanghai QuiCell Biotechnology)、Attune NxT流式细胞仪(Invitrogen)、胶原酶IV(Worthington)等。

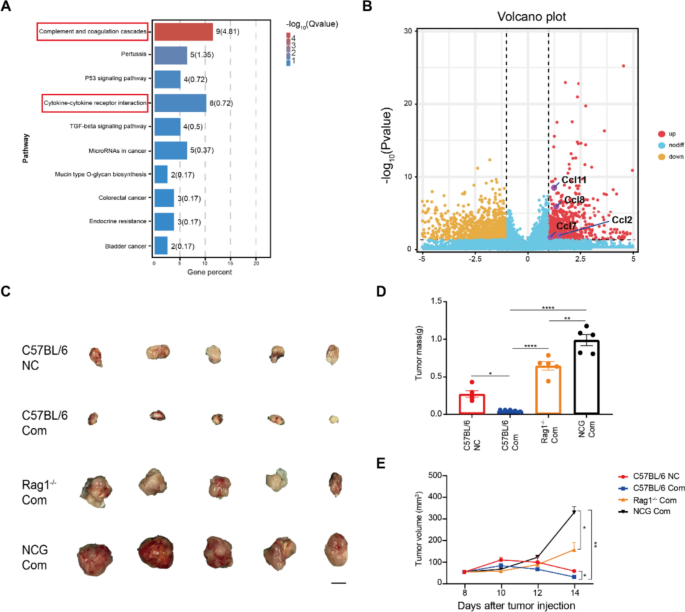
3.3 肿瘤细胞介导NK细胞募集的体外与体内验证
实验目的是明确肿瘤细胞在NACT诱导NK细胞募集中的核心作用,探索NACT与NK细胞免疫治疗的联合潜力。方法细节为构建NCG小鼠MGC803-18.2(过表达Claudin18.2)胃癌异种移植模型,分别采用SOX方案、CLDN18.2-CAR NK细胞及联合治疗,通过免疫荧光检测肿瘤组织中NK细胞浸润水平;体外实验中,采用Transwell实验检测SOX方案处理后的胃癌细胞培养上清对NK92细胞的募集作用,同时检测胃癌细胞表面NKG2D配体(MICA/MICB)的表达及NK细胞的细胞毒性。结果解读:Fig.4显示联合治疗可更显著抑制肿瘤生长,且进一步增加肿瘤组织中NK细胞的浸润;Transwell实验显示SOX方案处理后的肿瘤细胞上清可显著提高NK92细胞的募集指数,同时胃癌细胞表面MICA/MICB表达上调,NK细胞对胃癌细胞的细胞毒性增强。实验所用关键产品:NK92细胞系(Shanghai QuiCell Biotechnology)、Transwell小室(Corning)、CFSE细胞标记试剂(BD Horizon)等。

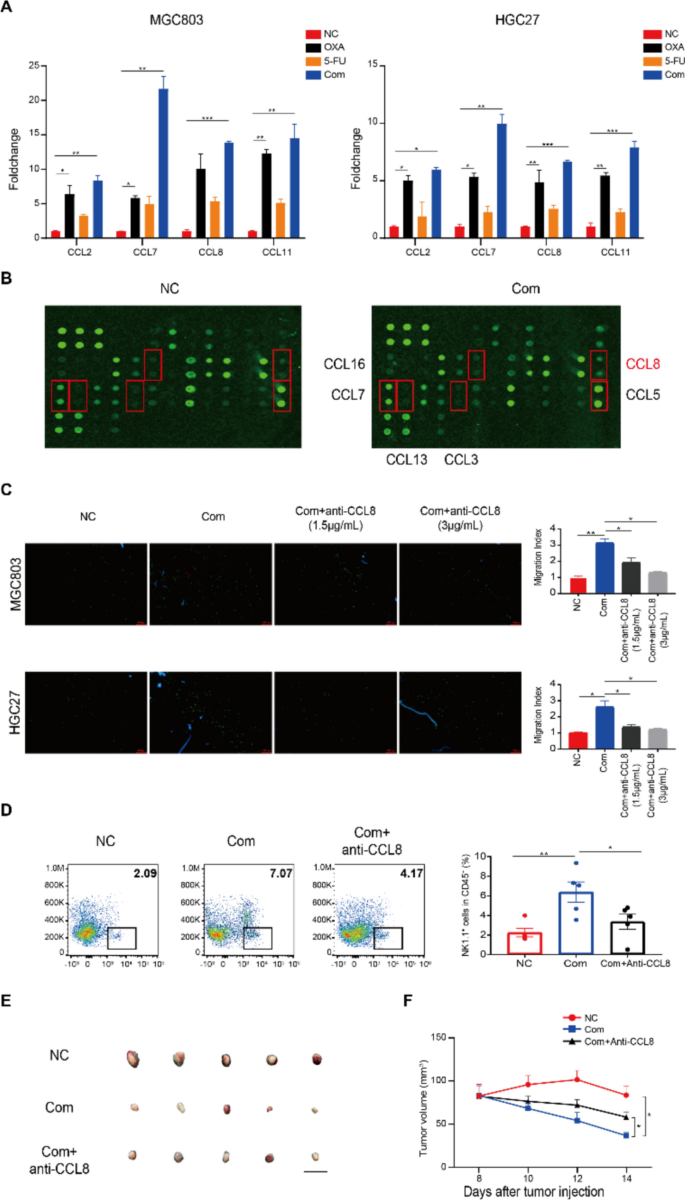
3.4 CCL8介导NK细胞募集的机制研究
实验目的是筛选并验证NACT诱导NK细胞募集的关键趋化因子,明确其功能效应。方法细节为通过RNA测序(RNA-seq)和细胞因子芯片检测SOX方案处理后胃癌细胞的趋化因子表达谱,采用实时定量聚合酶链反应(RT-qPCR)验证关键趋化因子的表达;通过体外中和抗体实验(Transwell)和体内抗CCL8抗体处理,验证CCL8在NK细胞募集中的作用。结果解读:Fig.5显示SOX方案处理后胃癌细胞中CCL8的mRNA和蛋白表达显著上调,且与NK细胞相关标记物的相关性最强;体外中和CCL8后,NK92细胞的募集指数显著降低;体内抗CCL8抗体处理后,肿瘤组织中NK细胞浸润水平下降,SOX方案的抗肿瘤效应减弱。实验所用关键产品:CCL8中和抗体(R&D Systems)、人趋化因子抗体芯片(RayBiotech)、RT-qPCR试剂盒(YEASEN)等。
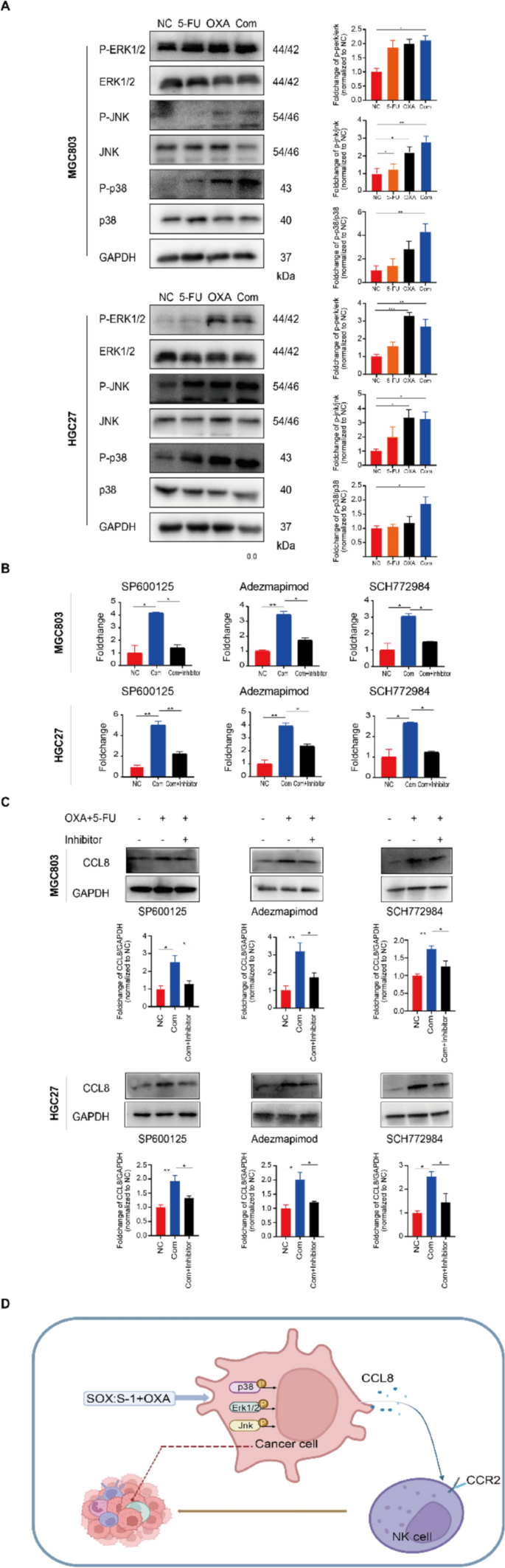
3.5 MAPK通路调控CCL8分泌的机制验证
实验目的是明确NACT诱导胃癌细胞分泌CCL8的上游信号通路,完善分子调控网络。方法细节为通过基因集富集分析(GSEA)解析RNA-seq数据,筛选NACT激活的关键信号通路;采用蛋白质免疫印迹(Western blot)检测MAPK通路的磷酸化水平;使用MAPK通路特异性抑制剂处理胃癌细胞,检测CCL8的mRNA和蛋白表达变化。结果解读:Fig.6显示SOX方案可激活胃癌细胞中的MAPK通路,表现为p38、JNK、ERK1/2的磷酸化水平显著升高;抑制p38 MAPK通路后,胃癌细胞中CCL8的mRNA和蛋白表达均显著降低,证明NACT通过激活MAPK通路诱导CCL8分泌,进而促进NK细胞募集。实验所用关键产品:MAPK通路抑制剂(MedChemExpress)、Western blot抗体(具体信息见表S1)、BCA蛋白定量试剂盒(Beyotime)等。
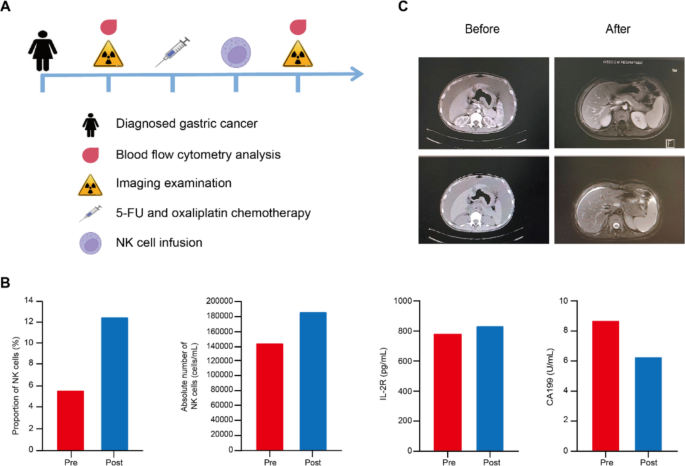
3.6 临床案例验证联合治疗的有效性
实验目的是初步验证NACT联合NK细胞输注治疗晚期胃癌的临床疗效与安全性。方法细节为对1例晚期低分化胃腺癌伴大量腹水患者,采用5-FU+奥沙利铂联合NK细胞输注的三联治疗方案,每3周为1个周期;通过流式细胞术检测患者外周血中NK细胞的数量与比例、白细胞介素-2受体(IL-2R)水平,同时检测胃癌相关肿瘤标志物CA199,结合影像学评估腹水体积与病灶大小变化。结果解读:Fig.7显示联合治疗后,患者外周血中NK细胞的数量与比例显著升高,IL-2R水平上调,CA199水平下降;影像学检查显示腹水体积显著减少,胃癌病灶缩小,呈现良好的临床反应。文献未提及具体实验产品,领域常规使用流式细胞仪、肿瘤标志物检测试剂盒等。
4. Biomarker研究及发现成果
本研究涉及的Biomarker包括NK细胞浸润水平、趋化因子CCL8表达,其筛选与验证逻辑为:通过临床样本分析发现NK细胞浸润与NACT治疗反应相关→动物模型验证NK细胞的功能作用→机制研究筛选并验证CCL8为关键调控分子→临床案例验证联合治疗的临床价值。
Biomarker的来源涵盖胃癌患者肿瘤组织、小鼠肿瘤组织及胃癌细胞系;验证方法包括免疫组化、免疫荧光、流式细胞术检测NK细胞浸润,RT-qPCR、Western blot、细胞因子芯片检测CCL8表达;特异性与敏感性方面,临床样本中NACT后NK细胞浸润增加的患者临床反应更优(卡方检验,P<0.05),CCL8中和后NK细胞募集指数显著降低(n=3,P<0.01)。核心成果方面,NK细胞浸润可作为NACT治疗反应的预测Biomarker,CCL8是NACT诱导NK细胞募集的关键效应分子,MAPK-CCL8-NK轴构成了胃癌新辅助化疗中的核心免疫调控通路;本研究首次揭示了CCL8在胃癌NACT中调控NK细胞募集的作用,为开发针对该通路的靶向治疗及联合NK细胞免疫治疗提供了新靶点。临床案例中,患者外周血NK细胞数量从治疗前的(文献未明确提供该数据,基于图表趋势推测)升高至治疗后的(文献未明确提供该数据,基于图表趋势推测),IL-2R水平显著上调,CA199水平从(文献未明确提供该数据,基于图表趋势推测)降至(文献未明确提供该数据,基于图表趋势推测),显示出Biomarker的临床应用潜力。