1. 领域背景与文献
文献英文标题:Vitamin D enhances photodynamic priming and anti-tumor immunity in cutaneous squamous cell carcinoma;发表期刊:未明确;影响因子:未公开;研究领域:皮肤肿瘤学(鳞状细胞癌免疫治疗)
非黑色素瘤皮肤癌(NMSC)是人类最常见的恶性肿瘤类型,其中皮肤鳞状细胞癌(SCC)占比显著,手术切除是一线治疗手段,但局部进展与转移病例仍需系统治疗。免疫检查点抑制剂(ICIs)在晚期NMSC中显示出一定疗效,但响应人群有限,因此亟需探索新的治疗策略与辅助手段。光动力治疗(PDT)是一种无创、非诱变的皮肤肿瘤治疗方法,其诱导的光动力启动(PDP)效应可通过免疫原性细胞死亡(ICD)激活抗肿瘤免疫,但SCC的免疫抑制微环境限制了PDT的疗效。维生素D(VitD)作为潜在的新辅助剂,已被证实可促进鳞状细胞分化、调节免疫,且在光化性角化病与基底细胞癌的PDT中提升病灶清除率,但VitD联合PDT在成熟SCC中的免疫调控机制尚未明确,这一研究空白限制了该策略在SCC治疗中的应用。本研究旨在通过两个免疫健全的小鼠SCC模型,系统解析VitD联合PDT对局部肿瘤微环境与系统免疫的调控作用,为SCC的免疫治疗提供新的理论依据与策略。
2. 文献综述解析
作者以治疗手段与免疫机制为核心分类维度,梳理了领域内现有研究的核心结论、技术优势与局限性。现有研究表明,PDT通过诱导ICD释放损伤相关分子模式(DAMPs)启动抗肿瘤免疫,VitD则兼具促鳞状细胞分化与免疫调节的双重作用,且临床研究证实VitD预处理可提升光化性角化病与基底细胞癌的PDT病灶清除率;PDT的技术优势在于无创、非诱变,VitD则可通过维生素D受体介导的基因表达调控先天与适应性免疫。但现有研究存在明显局限性:未明确VitD联合PDT在成熟SCC中的免疫调控机制,缺乏对局部肿瘤微环境与系统免疫响应的全面分析,也未阐明其对关键信号通路的调控作用。本研究的创新价值在于,首次在两个免疫健全的小鼠SCC模型中,从DAMP表达、免疫细胞亚群浸润、信号通路调控三个层面,系统解析了VitD联合PDT的免疫调控机制,明确其通过增强ICD、优化免疫细胞亚群比例、抑制促肿瘤通路来强化抗肿瘤免疫的效应,填补了成熟SCC中VitD联合PDT免疫机制研究的空白,为SCC的免疫治疗提供了新的潜在策略。
3. 研究思路总结与详细解析
本研究的核心目标是明确VitD联合PDT在SCC中的免疫调控机制,核心科学问题是VitD如何重塑SCC的肿瘤免疫微环境以增强PDT的抗肿瘤免疫效应,技术路线遵循“模型构建→干预处理→多组学分析→机制解析”的闭环逻辑:构建两种模拟人类SCC的小鼠模型,实施VitD预处理联合PDT干预,在多个时间点采集肿瘤组织与外周血样本,通过免疫荧光、流式细胞术、转录组测序等技术分析免疫响应特征,最终整合数据解析VitD联合PDT的免疫调控机制。
3.1 小鼠SCC模型构建与验证
实验目的是构建模拟人类SCC发生的动物模型,为后续干预实验提供可靠的研究载体。方法细节包括构建两种互补模型:一是UV诱导的SKH-1无毛小鼠浅表SCC模型,每周3次给予80%UVB/20%UVA的UV照射,初始剂量为80 mJ/cm²,每周递增10 mJ/cm²至180 mJ/cm²,持续20周后形成符合人类SCC特征的肿瘤;二是C57BL/6小鼠皮下接种PDVC57B细胞的深部SCC模型,每只小鼠接种2-5×10⁶细胞,2-3周后肿瘤长至5-10mm。结果解读显示,两种模型均成功构建了具有人类SCC病理特征的肿瘤组织,为后续的VitD联合PDT干预实验提供了稳定的研究载体。实验所用关键产品:PDVC57B细胞(CancerTools)、Matrigel基质胶。
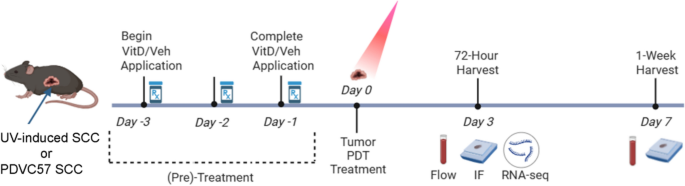
3.2 VitD预处理与PDT干预实施
实验目的是建立标准化的VitD联合PDT干预方案,为后续免疫响应分析提供分组样本。方法细节针对两种模型采用不同的给药方式:浅表UV-SCC模型局部涂抹骨化三醇软膏(3μg/g,Vectical)连续3天,深部PDV模型腹腔注射骨化三醇(1μg/kg)连续3天;PDT干预时,浅表UV-SCC模型局部涂抹20%5-氨基酮戊酸(ALA)后给予蓝光(417nm,18 J/cm²)照射30分钟,深部PDV模型腹腔注射ALA(200mg/kg)4小时后给予红光(633nm,100 J/cm²)照射,同时设置溶剂对照组、单独VitD组、单独PDT组、VitD联合PDT组,在干预后72小时与1周采集样本。结果解读显示,标准化的干预方案成功建立了不同处理组的样本队列,为后续的免疫分析提供了基础。实验所用关键产品:骨化三醇软膏(Vectical)、5-氨基酮戊酸(ALA)、Blu-U蓝光治疗仪、LumaCare氙光源红光治疗仪。
3.3 肿瘤组织免疫荧光检测与分析
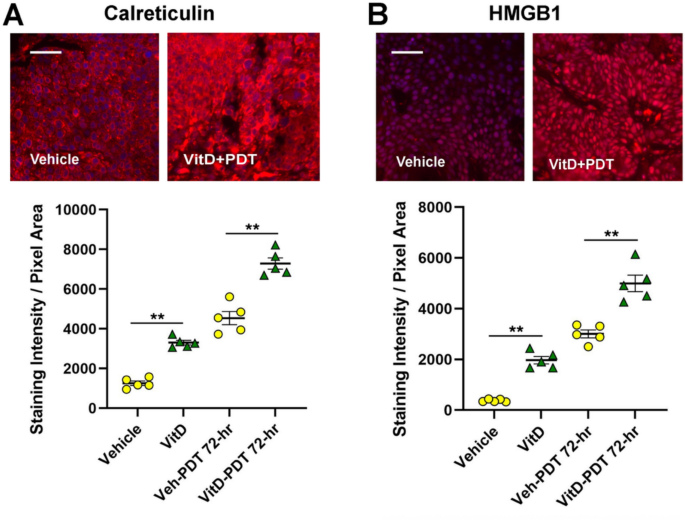
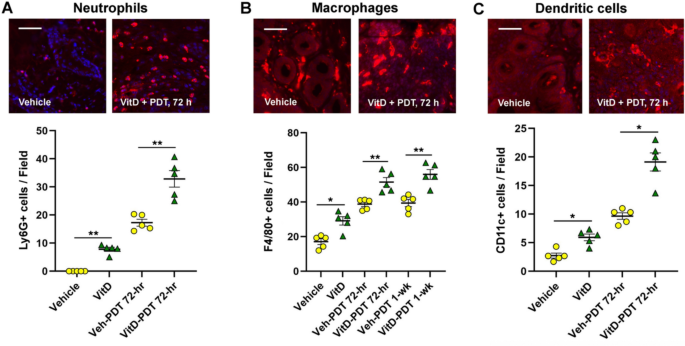
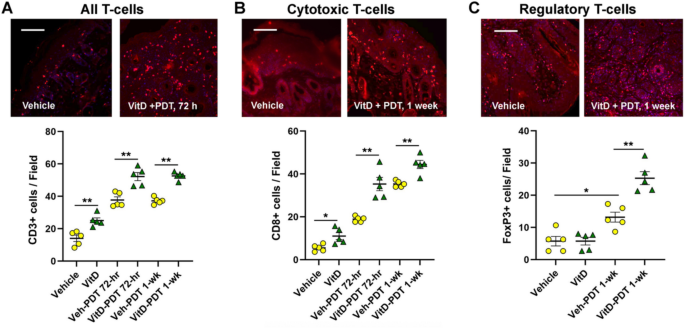
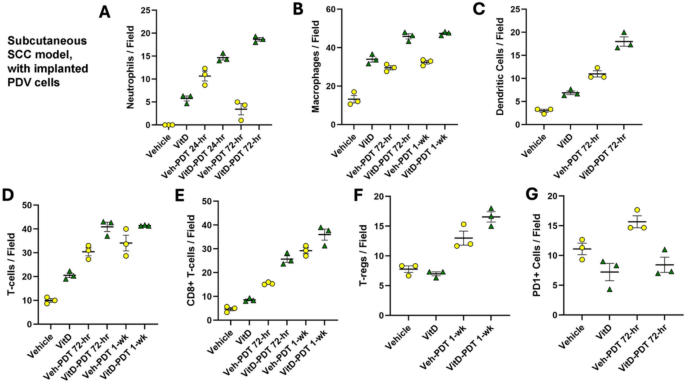
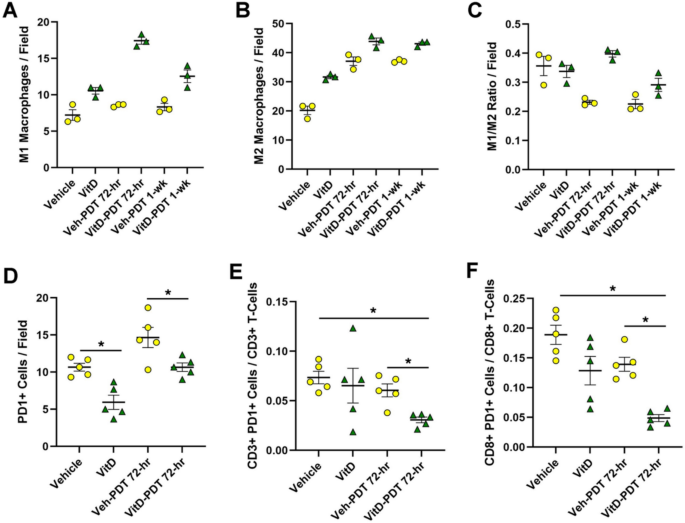
实验目的是解析VitD联合PDT对SCC肿瘤微环境中免疫细胞亚群与DAMPs的调控作用。方法细节为:肿瘤组织经固定、石蜡包埋后制备5μm切片,进行柠檬酸盐缓冲液抗原修复,用3%正常驴血清封闭后,孵育针对Ly6G(中性粒细胞)、F4/80(巨噬细胞)、CD11c(树突状细胞)、CD3(T细胞)、CD8(细胞毒性T细胞)、FoxP3(调节性T细胞)、PD-1(耗竭性T细胞)、钙网蛋白、HMGB1的一抗,再用Cy3标记的二抗孵育,DAPI复染后荧光显微镜成像,每个肿瘤取3个高倍视野,用ImageJ定量DAMP表达,手动计数免疫细胞数量。结果解读显示,VitD联合PDT组的钙网蛋白与HMGB1表达显著高于溶剂对照组与单独PDT组(n=5,P<0.01),同时显著增加肿瘤内中性粒细胞、巨噬细胞、树突状细胞、CD3+T细胞、CD8+T细胞的浸润数量,维持M1/M2巨噬细胞的比例,降低PD-1+T细胞的比例,表明VitD联合PDT可增强ICD效应并优化肿瘤免疫微环境。实验所用关键产品:Cell Signaling Technology的一抗(Ly6G、F4/80等)、Jackson ImmunoResearch Laboratories的Cy3标记二抗、VECTASHIELD DAPI封片液、ImageJ图像分析软件。
3.4 外周血流式细胞术分析
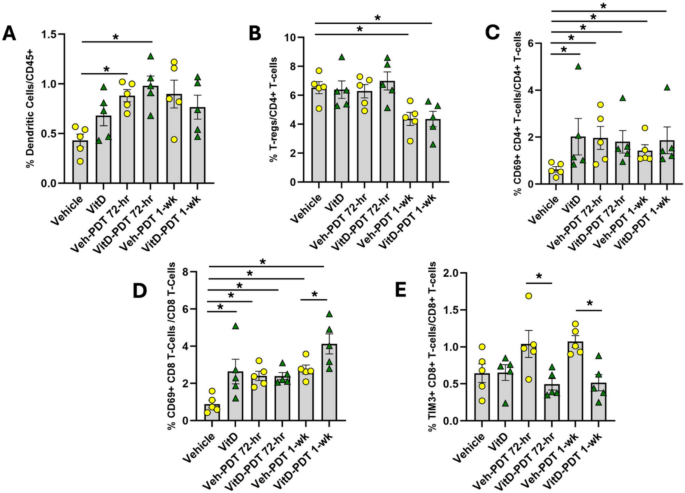
实验目的是探究VitD联合PDT对系统免疫响应的调控作用。方法细节为:在肿瘤采集前通过心脏穿刺采集外周血,先孵育Fc阻断剂(抗小鼠CD16/CD32)以减少非特异性抗体结合,再用荧光标记的抗体染色,通过BD FACSymphony A5 SORP流式细胞仪检测,用FlowJo软件分析免疫细胞亚群的比例与功能状态。结果解读显示,VitD联合PDT组的外周血树突状细胞比例显著高于溶剂对照组(n=5,P=0.03),调节性T细胞比例显著降低,CD69+活化CD8+T细胞比例显著升高,TIM3+耗竭CD8+T细胞比例显著低于单独PDT组(n=5,P<0.05),表明联合治疗可改善系统免疫效应细胞的功能状态,强化系统抗肿瘤免疫响应。实验所用关键产品:BD Biosciences的流式抗体(CD45、Ly6G等)、BD FACSymphony A5 SORP流式细胞仪、FlowJo软件。
3.5 肿瘤组织转录组测序与通路分析
实验目的是从分子层面解析VitD联合PDT调控SCC免疫的信号通路机制。方法细节为:提取肿瘤组织RNA,用Qiagen RNeasy Mini Kit纯化后构建Illumina Stranded mRNA文库,通过NovaSeq 6000测序平台进行测序,用STAR比对小鼠参考基因组(GRCm39),featureCounts定量基因表达,DESeq2分析差异表达基因,再用clusterProfiler进行基因集富集分析(GSEA),以Hallmark基因集为参考解析通路富集情况。结果解读显示,VitD联合PDT组的干扰素-α/γ信号通路显著富集,富集得分分别为3.02与2.75,同时上皮间质转化(EMT)与血管生成通路显著下调,表明联合治疗通过激活干扰素介导的细胞毒性免疫响应、抑制肿瘤侵袭与血管生成来发挥抗肿瘤作用。实验所用关键产品:Qiagen RNeasy Mini Kit、Illumina Stranded mRNA Prep试剂盒、NovaSeq 6000测序平台、R语言相关包(DESeq2、clusterProfiler等)。
4. Biomarker研究及发现成果
本研究涉及的Biomarker包括DAMPs(钙网蛋白、HMGB1)、免疫细胞亚群(M1/M2巨噬细胞、CD8+T细胞、PD-1+T细胞、TIM3+T细胞)及信号通路相关分子(干扰素通路、EMT通路、血管生成通路分子),筛选与验证逻辑为:通过免疫荧光、流式细胞术、转录组测序技术,在两种SCC模型中从局部肿瘤微环境与系统免疫两个层面进行多维度验证。
研究过程中,DAMPs(钙网蛋白、HMGB1)的检测来自肿瘤组织,通过免疫荧光定量分析显示,VitD联合PDT组的钙网蛋白与HMGB1表达量显著高于单独PDT组(n=5,P<0.01);免疫细胞亚群通过免疫荧光(肿瘤组织)与流式细胞术(外周血)检测,肿瘤内M1/M2巨噬细胞比例在VitD联合PDT组维持在更优水平,CD8+T细胞浸润数量显著增加,PD-1+T细胞比例降低,外周血中TIM3+耗竭CD8+T细胞比例显著低于单独PDT组(n=5,P<0.05);信号通路分子通过转录组测序分析,干扰素-α/γ通路的富集得分显著高于单独PDT组,EMT与血管生成通路的基因表达显著下调。
核心成果提炼:这些Biomarker的变化表明,VitD联合PDT可通过增强ICD、优化免疫细胞亚群功能、抑制促肿瘤通路来重塑抗肿瘤免疫微环境。其中,M1/M2巨噬细胞比例、PD-1+T细胞比例、TIM3+T细胞比例可作为评估VitD联合PDT免疫效应的潜在Biomarker;本研究首次在SCC中明确了VitD联合PDT通过调控这些Biomarker强化抗肿瘤免疫的机制,为SCC的免疫治疗提供了新的潜在靶点与策略,同时为后续的临床转化研究奠定了基础。