1. 领域背景与文献引入
文献英文标题:Safety and efficacy of nivolumab plus cabozantinib versus pembrolizumab plus lenvatinib for metastatic renal cell carcinoma: a multicenter retrospective study;发表期刊:Journal of Cancer Research and Clinical Oncology;影响因子:未公开;研究领域:泌尿生殖系统肿瘤(转移性肾细胞癌免疫治疗)。
领域共识:转移性肾细胞癌(mRCC)是泌尿系统常见的恶性肿瘤,传统治疗以酪氨酸激酶抑制剂(TKI)单药为主,但疗效有限。2015年以来,免疫检查点抑制剂(ICI)的获批开启了mRCC治疗的新时代,随后ICI+ICI、ICI+TKI联合方案相继通过CheckMate 214、CheckMate 9ER、CLEAR等随机对照试验(RCT)证实疗效优于传统TKI,成为一线治疗的标准方案。当前研究热点聚焦于不同联合方案的头对头比较、真实世界疗效与毒性验证、毒性管理策略以及疗效预测生物标志物的探索。领域内未解决的核心问题包括:缺乏直接头对头RCT比较主流ICI+TKI方案的安全性与疗效,RCT的严格入组标准可能无法反映真实世界人群的治疗结局,临床治疗选择依赖医生经验,缺乏真实世界的直接比较证据。
针对上述研究空白,本研究开展了一项多中心回顾性研究,纳入185例真实世界mRCC患者,采用倾向评分匹配(PSM)平衡基线特征,直接比较纳武利尤单抗联合卡博替尼(Nivo+Cabo)与帕博利珠单抗联合仑伐替尼(Pem+Len)两种一线方案的安全性与疗效,为临床治疗决策提供真实世界依据,填补了直接头对头比较的证据空白。
2. 文献综述解析
作者在引言部分按研究类型(RCT、网络荟萃分析NMA、真实世界研究)梳理了mRCC免疫联合治疗的研究现状,明确了现有研究的结论、优势与局限性,进而引出本研究的必要性。
现有RCT证实,ICI+TKI联合方案的疗效显著优于传统TKI单药,其中CheckMate 9ER试验显示Nivo+Cabo的总生存期(OS)、无进展生存期(PFS)、客观缓解率(ORR)均优于舒尼替尼,CLEAR试验显示Pem+Len的PFS、ORR优于舒尼替尼和帕博利珠单抗联合伊匹木单抗;RCT的优势在于严格的试验设计和控制混杂因素,能明确方案的疗效差异,但局限性在于入组患者通常排除合并症多、年龄较大的人群,无法完全代表真实世界患者。现有NMA的间接比较结果显示,ICI+TKI方案的疗效优于ICI+ICI方案,且Nivo+Cabo的OS更优,Pem+Len的PFS和ORR更优,安全性相当;NMA的优势在于能整合多个RCT数据进行间接比较,局限性在于依赖RCT的入组人群和研究设计,存在间接比较的偏倚。现有真实世界研究多聚焦于单一ICI+TKI方案的疗效与毒性,缺乏直接的头对头比较,无法明确两种主流方案在真实世界中的差异。
与现有研究相比,本研究的创新点在于首次在真实世界大样本中采用倾向评分匹配(PSM)直接比较两种主流ICI+TKI方案的安全性与疗效,纳入了RCT中常排除的老年、合并症患者,更贴近临床实际;通过PSM平衡基线特征,减少了混杂因素的影响,结果更可靠;填补了直接头对头真实世界比较的空白,为临床治疗选择提供了更具实用性的证据。
3. 研究思路总结与详细解析
本研究的整体研究目标是比较Nivo+Cabo与Pem+Len作为mRCC一线治疗的安全性与疗效,核心科学问题是两种方案在真实世界人群中的毒性差异是否显著,以及疗效是否一致;技术路线遵循“多中心回顾性入组→基线特征分析→安全性结局评估→倾向评分匹配平衡基线→匹配后疗效结局分析→后续治疗探索→结论”的闭环逻辑,通过回顾性研究设计结合统计方法控制偏倚,确保结果的真实性。
3.1 患者入组与基线特征分析
实验目的:确定符合研究标准的真实世界mRCC患者群体,明确两组患者的基线特征差异,为后续安全性与疗效分析提供基础。
方法细节:回顾性收集日本8家大学医院和15家附属医院2018年1月至2025年6月期间接受ICI+TKI联合治疗的mRCC患者,纳入标准为经组织学或细胞学确诊的转移性肾细胞癌,接受Nivo+Cabo或Pem+Len作为一线治疗;排除标准为随访时间不足3个月、临床数据缺失、无远处转移(包括肿瘤栓塞)的患者。最终入组185例患者,其中Nivo+Cabo组81例,Pem+Len组104例,收集患者的年龄、国际转移性肾细胞癌数据库联盟(IMDC)风险分层、既往肾切除术史、转移部位等基线数据。
结果解读:Nivo+Cabo组患者的中位年龄为72岁,显著高于Pem+Len组的68岁(标准化均数差SMD=0.23);Nivo+Cabo组既往接受肾切除术的比例为70%(n=57),高于Pem+Len组的56%(n=58,SMD=0.3);IMDC不良风险患者比例在Nivo+Cabo组为16%(n=13),低于Pem+Len组的23%(n=24,SMD=0.22),两组基线存在一定差异。
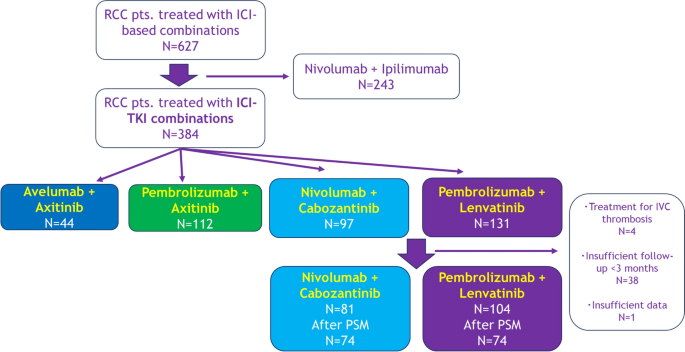
产品关联:文献未提及具体实验产品,领域常规使用电子病历系统、计算机断层扫描(CT)等影像学设备进行患者入组与基线数据收集。
3.2 安全性结局评估
实验目的:比较两组患者的治疗相关不良事件(TrAEs)发生率、严重程度,以及因TrAEs导致的TKI剂量降低和治疗停药情况,明确两种方案的毒性差异。
方法细节:采用美国国立癌症研究所不良事件通用术语标准(CTCAE)5.0版,由各参与机构的研究者评估患者的TrAEs,统计任何级别、3级及以上严重TrAEs的发生率,同时记录TKI剂量降低和因TrAEs停药的患者比例。
结果解读:任何级别TrAEs的发生率在Nivo+Cabo组为90%(n=72,p=0.6),Pem+Len组为92%(n=96,p=0.6),两组无显著差异;但3级及以上严重TrAEs的发生率在Pem+Len组为44%(n=46,p=0.048),显著高于Nivo+Cabo组的30%(n=24,p=0.048)。常见的任何级别TrAEs(发生率>10%)包括高血压(Nivo+Cabo组19% vs Pem+Len组28%)、腹泻或结肠炎(15% vs 12%)、手足综合征(PPE,32% vs 14%)、皮疹(12% vs 17%)、肝功能损伤(33% vs 19%)、甲状腺功能减退(19% vs 25%),其中Pem+Len组的高血压、恶心或食欲下降(13%)、蛋白尿(19%)发生率更高。严重TrAEs中,肝功能损伤在两组的发生率均超过10%(17% vs 12%),Pem+Len组的严重高血压(8.7%)、腹泻或结肠炎(5.8%)、皮疹(4.8%)、蛋白尿(4.8%)发生率更高。尽管TrAEs谱存在差异,但两组的TKI剂量降低率(70% vs 76%,p=0.4)和因TrAEs停药率(21% vs 24%,p=0.7)无显著差异。
产品关联:文献未提及具体实验产品,领域常规使用CTCAE 5.0评估量表、临床不良事件记录系统进行毒性评估。
3.3 倾向评分匹配(PSM)与匹配后基线平衡
实验目的:通过统计方法平衡两组患者的基线特征,减少混杂因素对疗效结局分析的影响,确保疗效比较的可靠性。
方法细节:采用单变量逻辑回归模型计算倾向评分,纳入的协变量包括IMDC风险分层、年龄、病理亚型、既往肾切除术史、转移部位;按照1:1的比例对两组患者进行匹配,匹配容差设置为logit转换倾向评分标准差的0.2倍,以保证匹配质量。
结果解读:匹配后每组纳入74例患者,所有基线特征的标准化均数差(SMD)均小于0.2,提示两组基线特征达到良好平衡,混杂因素的影响被有效控制。
产品关联:文献未提及具体实验产品,领域常规使用R软件(Version 4.2.3)进行倾向评分匹配与统计分析。
3.4 疗效结局评估(匹配后)
实验目的:在基线平衡的基础上,比较两组患者的无进展生存期(PFS)、癌症特异性生存期(CSS)、总生存期(OS)和客观缓解率(ORR),明确两种方案的疗效差异。
方法细节:采用实体瘤疗效评价标准(RECIST)1.1版评估患者的最佳客观缓解,包括完全缓解(CR)、部分缓解(PR)、稳定疾病(SD)、疾病进展(PD);采用Kaplan-Meier法绘制PFS、CSS、OS的生存曲线,通过log-rank检验比较两组的生存差异;计算1年PFS率、2年CSS率、2年OS率及相应的95%置信区间(CI)。
结果解读:中位随访时间在Nivo+Cabo组为17.0个月(四分位距IQR:9.42-24.3),Pem+Len组为16.8个月(IQR:9.24-26.6)。两组的1年PFS率分别为76.3%(95% CI:64.1-84.9,n=74,p=0.4)和70.9%(95% CI:58.1-80.5,n=74,p=0.4),无显著差异;中位CSS在Nivo+Cabo组为44个月(95% CI:27.7-未达到,n=74,p=0.9),Pem+Len组未达到(95% CI:43-未达到,n=74,p=0.9),两组无显著差异,2年CSS率分别为70.2%(95% CI:54.2-81.6)和78.3%(95% CI:64.4-87.4);中位OS在两组间也无显著差异(p=0.5),2年OS率分别为66.6%(95% CI:51.1-78.1)和78.3%(95% CI:64.4-87.4)。客观缓解率(ORR)在Nivo+Cabo组为66%(n=49,p=0.6),Pem+Len组为71%(n=52,p=0.6),无显著差异;完全缓解(CR)率分别为6.8%(n=5,p=0.4)和11%(n=8,p=0.4),也无显著差异。
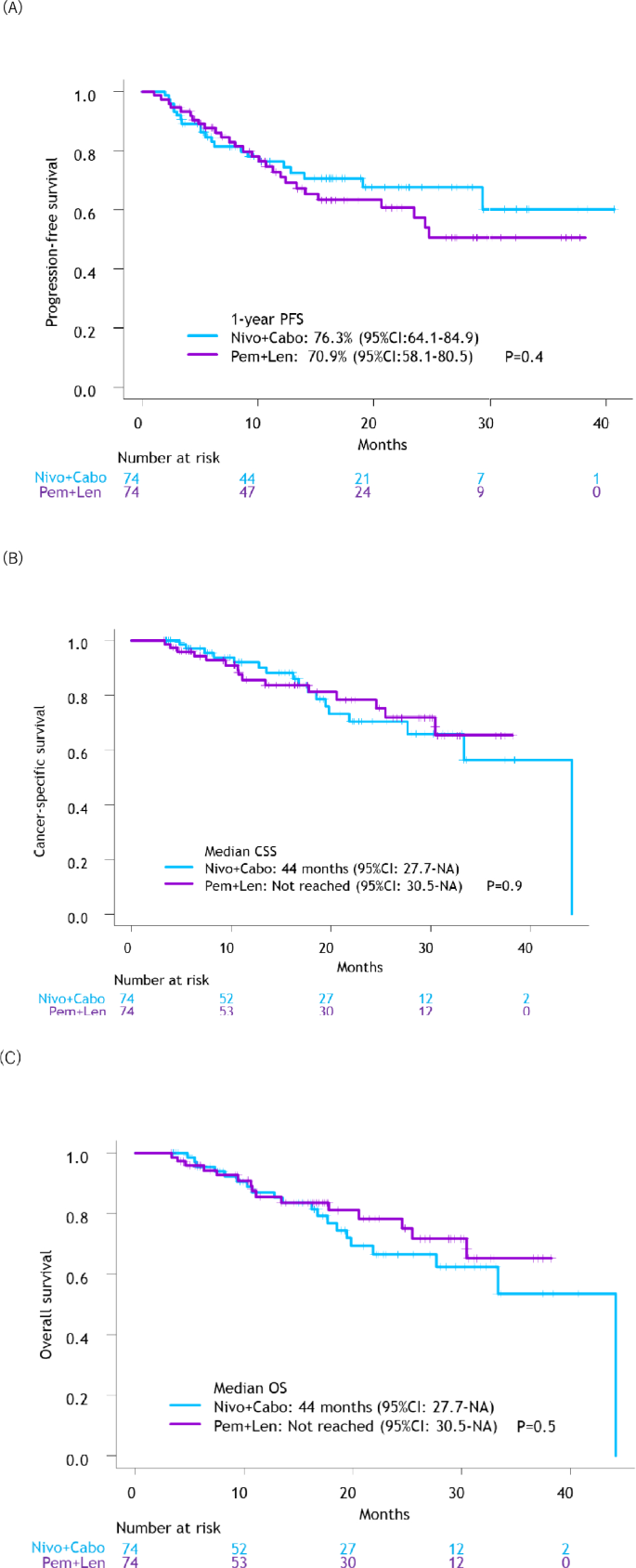
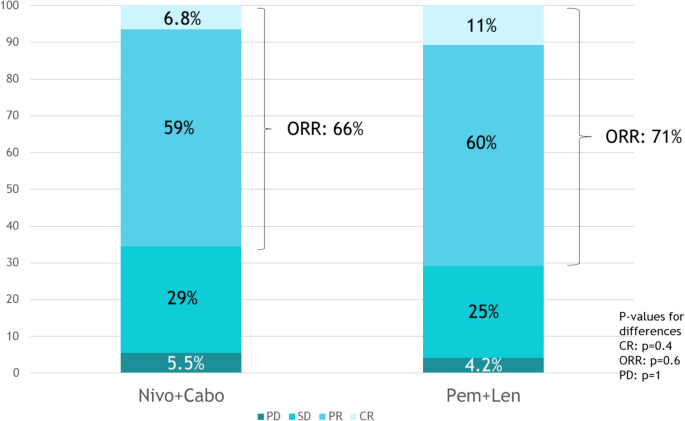
产品关联:文献未提及具体实验产品,领域常规使用RECIST 1.1评估量表、Kaplan-Meier生存分析软件进行疗效评价。
3.5 后续治疗分析
实验目的:探索两组患者疾病进展后的后续治疗模式及疗效,为治疗线序选择提供参考。
方法细节:收集患者疾病进展后的治疗方案,统计后续治疗的患者比例,对接受二线治疗的患者采用Kaplan-Meier法分析后续PFS,并通过log-rank检验比较差异。
结果解读:Nivo+Cabo组有15%(n=11)的患者接受后续治疗,所有患者均接受阿昔替尼单药治疗;Pem+Len组有30%(n=22)的患者接受后续治疗,最常用的方案为卡博替尼(77%,n=17),其次为阿昔替尼(9%,n=2)、纳武利尤单抗(9%,n=2)、依维莫司(5%,n=1)。在疾病进展后接受二线治疗的患者中,阿昔替尼组的1年PFS率为35.7%(95% CI:5.2-69.9,n=7,p=0.3),卡博替尼组为55.0%(95% CI:18.2-81.1,n=12,p=0.3),两组无显著差异。
产品关联:文献未提及具体实验产品,领域常规使用阿昔替尼、卡博替尼等临床获批的抗肿瘤药物进行后续治疗。
4. Biomarker研究及发现成果解析
本研究未开展针对性的生物标志物(Biomarker)筛选或验证实验,仅在讨论部分指出了Biomarker在mRCC精准治疗中的重要性,为后续研究指明方向。
Biomarker定位:本研究未涉及具体Biomarker的筛选与验证,作者在讨论中提出,未来需探索可预测ICI+TKI方案疗效或毒性的Biomarker,如肿瘤突变负荷(TMB)、基因表达谱等,以实现mRCC的精准治疗,其潜在筛选逻辑为基于基因组学或转录组学数据,通过回顾性分析或前瞻性研究验证Biomarker与疗效/毒性的关联,进而用于患者分层。
研究过程详述:本研究无相关Biomarker实验数据,未开展Biomarker的来源收集、验证方法及特异性敏感性分析。
核心成果提炼:本研究未发现新的Biomarker,仅强调了Biomarker在mRCC治疗中的重要性,指出当前缺乏可用于临床的疗效预测Biomarker,未来需开展相关研究以填补空白,为精准治疗提供依据。