1. 领域背景与文献
文献英文标题:Dynamic circulating biomarkers-based prediction model for moderate-to-severe adverse events in PRaG therapy for advanced solid tumors;发表期刊:Cancer Immunology, Immunotherapy;影响因子:未公开;研究领域:肿瘤免疫治疗(放疗联合免疫治疗细分领域)
肿瘤免疫治疗领域自2014年PD-1抑制剂首次获批以来,已成为晚期实体瘤的核心治疗策略之一,其中放疗联合免疫治疗因可通过放疗诱导肿瘤抗原释放、增强免疫细胞浸润,进一步提升疗效,成为研究热点。PRaG疗法(PD-1/PD-L1抑制剂联合放疗与粒细胞-巨噬细胞集落刺激因子GM-CSF)是中国国家卫生健康委员会推广的新型联合治疗方案,为多线治疗失败的晚期难治性实体瘤患者提供了新选择。当前领域内的研究热点聚焦于联合治疗的疗效优化、耐药机制探索,以及安全性管理,其中未解决的核心问题包括:PRaG疗法的真实世界安全性数据仍不充分,现有免疫治疗不良事件预测多依赖静态基线指标,无法捕捉治疗过程中免疫系统的动态变化;同时多数研究仅采用单一类型生物标志物,难以全面反映免疫失衡的多维度特征,导致预测模型的敏感性与特异性不足。
基于上述领域现状,本研究针对PRaG疗法的安全性评估需求及现有不良事件预测的局限性,旨在系统解析PRaG疗法的不良事件谱,并构建基于动态循环生物标志物的多模态预测模型,为临床安全应用提供精准的风险预警工具,填补了放疗联合免疫治疗领域动态不良事件预测的研究空白。
2. 文献综述解析
作者在综述部分按现有研究的局限性维度分类评述,一是静态基线指标的预测缺陷,二是单一生物标志物的应用局限,进而引出本研究的动态多模态预测模型的创新性。
现有研究的核心结论显示,循环生物标志物(如淋巴细胞亚群、细胞因子)可用于免疫治疗不良事件的风险预测,其技术方法优势在于外周血样本易获取、检测可重复性高,为非侵入性预测提供了可能。但现有研究存在显著局限性:多数分析仅依赖治疗前的静态基线指标,无法反映治疗过程中免疫系统的动态激活与失衡状态,而免疫治疗的不良事件是免疫动态变化的结果,静态指标的预测效能有限;同时大量研究仅探索单一类型甚至单个标志物的预测价值,而免疫调控是涉及多种细胞、分子的复杂网络,单一标志物难以全面捕捉免疫平衡的细微变化,导致预测模型的敏感性与特异性不足,无法满足临床精准预警的需求。
对比现有研究的未解决问题,本研究的创新价值体现在三个方面:首次针对PRaG这一特定联合治疗方案开展不良事件的动态预测研究;首次整合事件前一周期的动态循环指标(而非仅基线指标)进行模型构建;首次结合机器学习算法构建多模态联合预测模型,整合血常规、细胞因子、精细T细胞亚群等多类型生物标志物,显著提升了预测效能,为放疗联合免疫治疗的不良事件预测提供了新的技术范式。
3. 研究思路总结与详细解析
本研究的整体框架为:以明确PRaG疗法的不良事件谱、构建中重度不良事件的精准预测模型为研究目标,核心科学问题是动态循环生物标志物能否有效区分中重度与轻度不良事件,以及多模态模型的临床应用价值;技术路线遵循“队列构建→数据收集→标志物筛选→模型构建→独立验证”的闭环逻辑,确保研究结果的可靠性与可重复性。
3.1 患者入组与治疗方案
实验目的:建立PRaG治疗晚期实体瘤的前瞻性研究队列,明确治疗方案的标准化流程,为后续安全性与预测研究奠定基础。
方法细节:本研究共入组203例接受PRaG治疗的晚期实体瘤患者,分为生物标志物发现/模型构建集(165例,来自3项前瞻性临床研究)和独立内部验证集(38例,来自2项独立前瞻性研究);所有患者均签署知情同意书,治疗方案包括三部分:大分割放疗,连续3天给药(剂量为8Gy/3次或5Gy/3次),放疗部位与野区由两名放射肿瘤科医师确定;GM-CSF皮下注射,剂量200μg,自放疗当日或次日开始,至少连续给药5天;PD-1/PD-L1抑制剂,在放疗完成后1周内开始给药,每3周为1个周期重复。
结果解读:队列基线特征分析显示,165例模型构建集中,58.2%的患者ECOG体力状况评分≥2,提示患者整体身体状态较差;按不良事件严重程度分层后,中重度不良事件组(≥2级)与轻度不良事件组(≤1级)在年龄、性别、ECOG评分、肿瘤类型方面无统计学差异(p>0.05),但肝转移状态存在显著差异(p=0.010)。
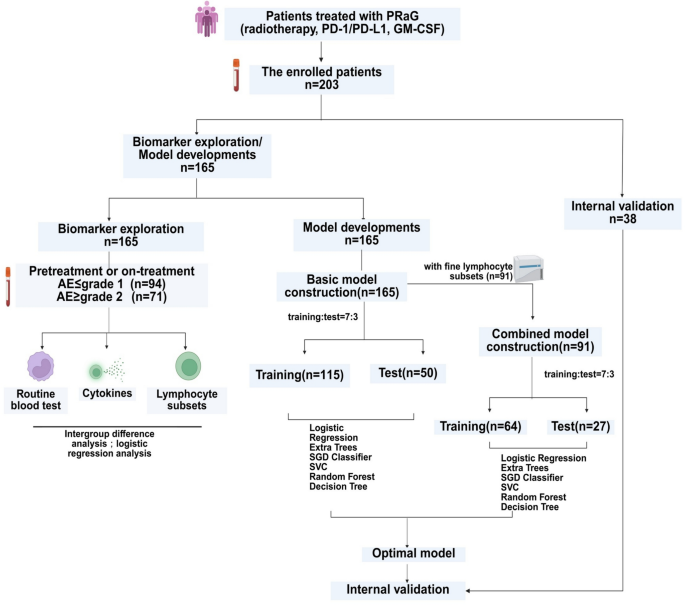
文献未提及具体实验产品,领域常规使用放疗设备、GM-CSF制剂、PD-1/PD-L1抑制剂等临床治疗产品。
3.2 数据收集与不良事件评估
实验目的:系统收集患者的临床特征、疗效、生存及不良事件数据,明确不良事件的发生规律与临床意义。
方法细节:收集患者的基线特征(性别、年龄、ECOG评分、肿瘤类型、肝转移状态)、疗效评估数据(按实体瘤疗效评价标准RECIST 1.1由两名独立肿瘤医师评估)、生存数据(无进展生存期PFS定义为治疗开始至疾病进展或任何原因死亡的时间,总生存期OS定义为治疗开始至任何原因死亡的时间);不良事件按不良事件通用术语标准CTCAE 5.0由两名盲法评估的肿瘤医师分级,评估周期至少为治疗开始后3个月;同时收集基线及不良事件发生前一周期的外周血指标,包括血常规、生化指标、细胞因子、基础淋巴细胞亚群、精细循环T细胞亚群分型,所有样本均在治疗周期开始前采集并由专业技术人员检测。
结果解读:165例患者中,中重度不良事件(≥2级)发生率为43%,其中重度不良事件(≥3级)发生率为7.3%;不良事件发生时间分析显示,发热、皮疹、疲劳、呕吐等急性不良事件的中位发生时间在10天内,而甲状腺功能减退、肺炎、心肌炎、肝功能异常等迟发性不良事件的中位发生时间超过15天;疗效与生存分析显示,中重度不良事件组的客观缓解率ORR为13.9%,显著高于轻度不良事件组的8.8%;中位OS在中重度不良事件组为15.80个月,显著长于轻度组的9.47个月(n=165,p=0.007);中位PFS在中重度不良事件组为4.63个月,显著长于轻度组的3.53个月(n=165,p=0.0069),提示中重度不良事件的发生与更好的生存结局相关。
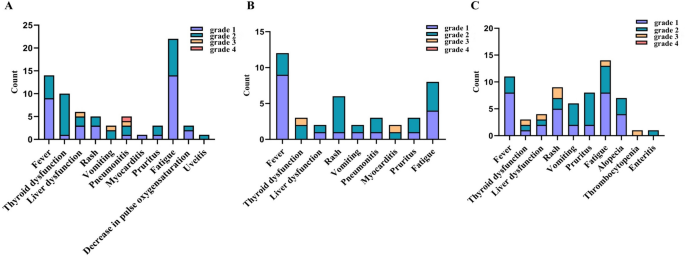

文献未提及具体实验产品,领域常规使用流式细胞仪检测淋巴细胞亚群、酶联免疫吸附试验ELISA检测细胞因子、全自动生化分析仪检测血常规与生化指标等。
3.3 循环生物标志物的筛选与分析
实验目的:对比基线与不良事件前一周期循环指标的预测价值,筛选可独立预测中重度不良事件的生物标志物。
方法细节:对基线及不良事件前一周期的外周血指标分别进行单因素与多因素logistic回归分析,筛选具有预测价值的指标;同时进行组间差异分析,比较中重度与轻度不良事件组的指标水平差异。
结果解读:基线指标的单因素logistic回归分析显示,红细胞计数、IL-2、IL-4、初始CD4+T细胞、CD4+效应记忆T细胞(Tem)5项指标具有显著预测价值(p<0.05),但多因素分析后无指标被确定为独立预测因子;不良事件前一周期指标的单因素分析显示,IL-2、IL-10、初始CD4+T细胞、调节性T细胞Treg、CD4+Tem、CD8+Tem、CD4+Tem/CD8+Tem比值、CD4+Tem/CD4+中央记忆T细胞Tcm比值9项指标具有预测价值(p<0.05),多因素分析后确定血小板计数(p=0.028)、IL-2(p=0.004)、CD4+Tem(p<0.001)、CD8+Tem(p=0.012)、CD4+Tem/CD8+Tem比值(p<0.001)为中重度不良事件的独立预测因子;组间差异分析显示,不良事件前一周期的血小板计数降低(n=165,p=0.013)、IL-2升高(n=165,p=0.004)、IL-10升高(n=165,p=0.040)、初始CD4+T细胞升高(n=165,p=0.023)、CD4+Tem升高(n=165,p<0.001)、CD8+Tem降低(n=165,p<0.001)与中重度不良事件的发生显著相关,证实动态指标的预测效能显著优于静态基线指标。
文献未提及具体实验产品,领域常规使用流式细胞仪进行T细胞亚群精细分型、ELISA定量检测细胞因子、血常规分析仪检测血小板计数等。
3.4 动态预测模型的构建与验证
实验目的:构建并验证基于动态循环生物标志物的中重度不良事件预测模型,评估模型的性能与临床应用价值。
方法细节:构建两种预测模型,基础模型包含患者基线特征与不良事件前一周期的血常规、细胞因子、基础淋巴细胞亚群指标;联合模型在基础模型的基础上增加精细循环T细胞亚群指标;采用6种机器学习算法(逻辑回归LR、极端随机树、支持向量分类器SVC、决策树、随机森林、随机梯度下降分类器SGD Classifier)分别训练模型,以受试者工作特征曲线下面积AUC为主要评估指标,同时比较准确率、精确率、F1值;在模型构建集中按7:3比例随机分为训练集与测试集,评估模型性能后,选择最优模型在独立内部验证集(38例)中进行验证。
结果解读:基础模型中,逻辑回归算法的预测性能最优,测试集AUC为0.685;联合模型中,逻辑回归算法仍为最优,测试集AUC提升至0.867,显著高于基础模型,证实精细T细胞亚群指标可显著提升预测效能;特征重要性分析显示,CD4+Tem是模型中最重要的预测特征;独立内部验证集的结果显示,联合模型的AUC为0.913(n=38),验证了模型的可靠性与泛化能力。
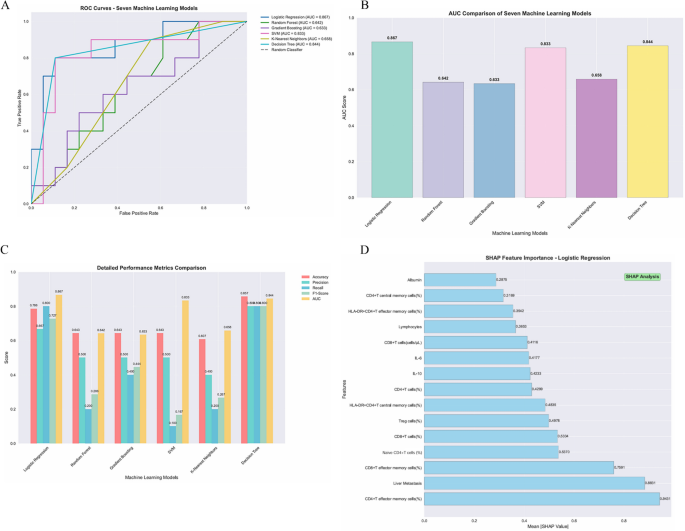
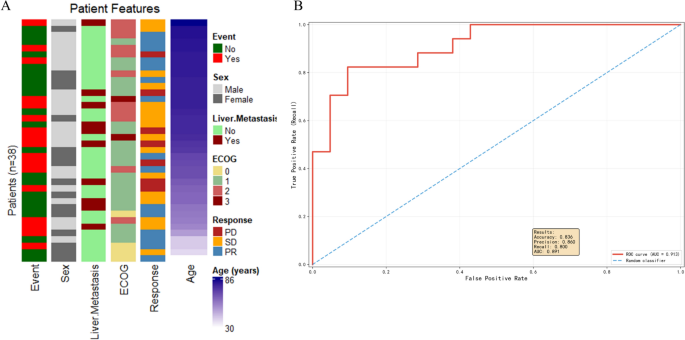
文献未提及具体实验产品,领域常规使用SPSS软件进行统计分析、Python语言进行机器学习建模。
4. Biomarker研究及发现成果解析
本研究涉及的Biomarker类型包括细胞因子(IL-2)、血小板计数、精细T细胞亚群(CD4+效应记忆T细胞、CD8+效应记忆T细胞、调节性T细胞),筛选与验证逻辑为“单因素多因素回归分析筛选→组间差异验证→模型整合验证→独立队列验证”,形成完整的证据链。
研究过程详述:Biomarker来源于患者的外周血样本,验证方法包括流式细胞术检测T细胞亚群的百分比与绝对计数、ELISA定量检测细胞因子水平、血常规分析仪检测血小板计数;特异性与敏感性数据显示,联合模型在测试集的AUC为0.867,独立验证集的AUC为0.913,提示模型具有良好的整体判别能力;其中CD4+Tem的升高与中重度不良事件的发生显著正相关(n=165,p<0.001),CD8+Tem的降低与中重度不良事件显著正相关(n=165,p<0.001),IL-2的升高与中重度不良事件显著正相关(n=165,p=0.004)。
核心成果提炼:该Biomarker的功能关联体现在,中重度不良事件的发生与患者的生存结局显著相关,中重度不良事件组的死亡风险比HR=0.6543(n=165,p=0.0101),提示不良事件的发生反映了免疫系统的有效激活,可作为预后良好的潜在标志物;创新性在于首次在放疗联合免疫治疗领域构建基于动态循环生物标志物的多模态预测模型,突破了现有静态、单一标志物的局限,实现了中重度不良事件的精准预警;统计学结果显示,CD4+Tem、CD8+Tem、IL-2等指标的预测价值具有显著统计学意义,为临床风险分层提供了量化依据。