1. 领域背景与文献
文献英文标题:CD28/CTLA4 ratio (ccRatio) as a continuous indicator for T cell transition from activation to exhaustion and the regulatory role of VDR;发表期刊:未明确;影响因子:未公开;研究领域:肿瘤免疫治疗与T细胞耗竭分子机制研究。
领域共识:T细胞耗竭是肿瘤细胞免疫逃逸和慢性感染持续存在的核心机制之一,传统分类将其分为祖细胞耗竭T细胞和终末耗竭T细胞,依赖PD-1、TIM3等标志物,但这些标志物无法捕捉T细胞从激活到耗竭的连续分化过程,导致免疫治疗的临床指导价值有限,仅约20%-50%的肿瘤患者能从PD-1抑制剂治疗中获益。当前领域的核心未解决问题包括缺乏能连续追踪T细胞耗竭进程的精准标志物,以及T细胞耗竭的关键调控机制尚未明确。针对这一空白,本研究构建CD28/CTLA4比率(ccRatio)作为连续表征指标,旨在填补传统标志物的不足,同时筛选并验证调控该进程的关键转录因子,为免疫治疗的患者分层和靶点开发提供新依据。
2. 文献综述解析
作者以T细胞耗竭标志物的临床局限性、现有分类体系的缺陷为核心评述逻辑,对领域内现有研究进行分类梳理。
现有研究的关键结论包括:PD-1、TIM3等单标志物被广泛用于T细胞耗竭的鉴定,但PD-1在活化T细胞中也存在表达,导致特异性不足;祖细胞/终末耗竭T细胞的分类体系虽能部分区分T细胞状态,但无法反映耗竭进程的连续性,使得免疫治疗的患者分层精度有限,肿瘤患者5年生存率仅从20%提升至40%-50%。现有技术方法的优势在于通过单细胞RNA测序、免疫组化(IHC)等手段能实现标志物的高通量检测,但局限性体现在多数研究样本量较小,且仅能进行离散状态的分析,无法动态追踪T细胞的分化过程。
通过对比现有研究的未解决问题,本研究的创新价值凸显:首次将CD28与CTLA4的比率作为连续指标,动态表征T细胞从激活到耗竭的完整进程,突破了传统离散分类的局限;同时,本研究首次发现维生素D受体(VDR)作为调控ccRatio的关键转录因子,参与T细胞耗竭的分化过程,为T细胞耗竭的机制研究和免疫治疗靶点开发提供了新方向,这些创新点均有文献原文的实验数据支持。
3. 研究思路总结与详细解析
本研究的整体框架为“假设提出→多组学数据验证→临床与感染模型验证→功能机制解析→体外实验验证”的闭环逻辑,研究目标是构建并验证ccRatio作为T细胞耗竭的连续表征指标,明确其与T细胞功能、免疫治疗响应及患者预后的关联,同时筛选并验证调控该进程的关键转录因子;核心科学问题包括ccRatio的动态变化是否与T细胞耗竭进程直接相关,以及哪些转录因子参与调控ccRatio介导的T细胞分化过程。
3.1 多组学数据验证ccRatio与T细胞耗竭进程的关联
实验目的是验证ccRatio是否随T细胞耗竭的进展呈现连续降低的趋势,同时明确其与肿瘤发生、患者预后的关联。研究人员首先采用Beltra团队定义的4种T细胞耗竭状态数据集(GSE149879),分析CD28、CTLA4的表达及ccRatio的变化,每组样本量为3;随后使用Miller团队的单细胞RNA测序数据(GSE122713)、慢性与急性病毒感染的bulk RNA-seq数据(GSE132028)、TCGA数据库的肿瘤与正常配对样本数据进行验证。结果显示,ccRatio从祖细胞1到终末耗竭状态持续降低(Jonckheere-Terpstra检验,P<0.05);慢性病毒感染组的ccRatio显著低于急性感染组(慢性n=5,急性n=4,双侧t检验,P<0.05);肿瘤样本的ccRatio显著低于配对正常样本(n=681,双侧t检验,P<0.05);高ccRatio组的肿瘤患者无进展生存期显著长于低ccRatio组(n=9602,Log-rank检验,P<0.05)。
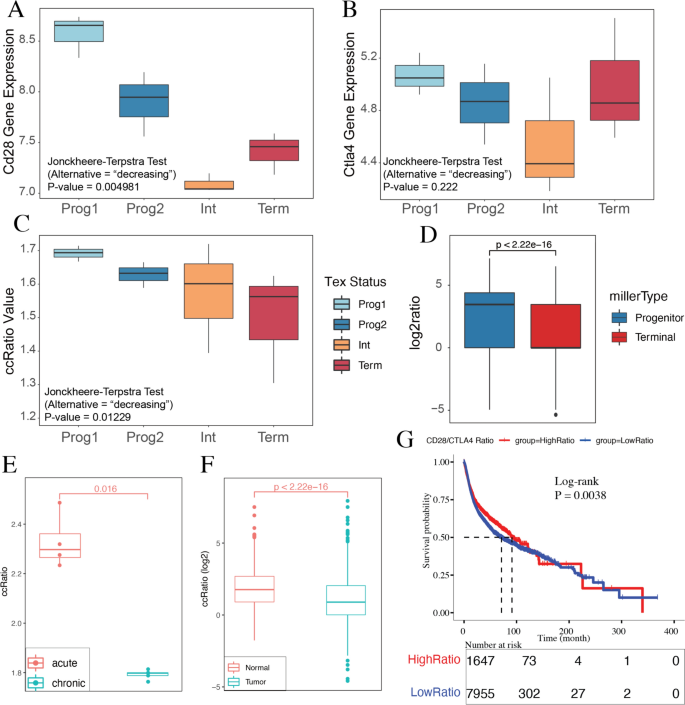
产品关联:文献未提及具体实验产品,领域常规使用RNA-seq测序平台、Seurat、GSVA等生物信息学分析软件。
3.2 ccRatio与免疫检查点阻断治疗响应的关联分析
实验目的是验证ccRatio是否可作为免疫检查点阻断(ICB)治疗响应的预测指标。研究人员采用多个公共ICB治疗数据集,包括GSE115821、GSE118201、E-MTAB-12733及Chen P.L.团队的数据集,对比响应组与非响应组的ccRatio差异。结果显示,抗CTLA4治疗的响应组ccRatio显著高于非响应组(响应n=8,非响应n=45,双侧t检验,P<0.05);其他ICB治疗数据集虽部分未达到统计学显著性,但均呈现响应组ccRatio更高的一致趋势;此外,ICB治疗后恢复活性的T细胞ccRatio显著高于对照组(恢复n=3,对照n=2,双侧t检验,P<0.05)。

产品关联:文献未提及具体实验产品,领域常规使用免疫治疗响应评估标准(RECIST标准)、生物信息学分析工具进行数据挖掘。
3.3 ccRatio与T细胞耗竭特征及功能的关联验证
实验目的是明确ccRatio与T细胞耗竭的分子特征及核心功能的关联。研究人员收集15种癌症类型的单细胞RNA-seq数据,按Beltra的分类标准定义T细胞的耗竭状态,进行单细胞基因集富集分析(GSEA)及功能富集分析。结果显示,ccRatio随T细胞耗竭进程持续降低(祖细胞1 n=5786,终末耗竭n=15776,双侧t检验,P<0.05);TCF7阴性、CXCR5阴性的T细胞组ccRatio显著更低;高ccRatio组的祖细胞耗竭基因集富集评分显著更高,终末耗竭基因集评分显著更低;功能富集分析显示,“T细胞活化”功能在14种癌症类型中显著富集,多数与ccRatio相关的基因参与T细胞活化通路。
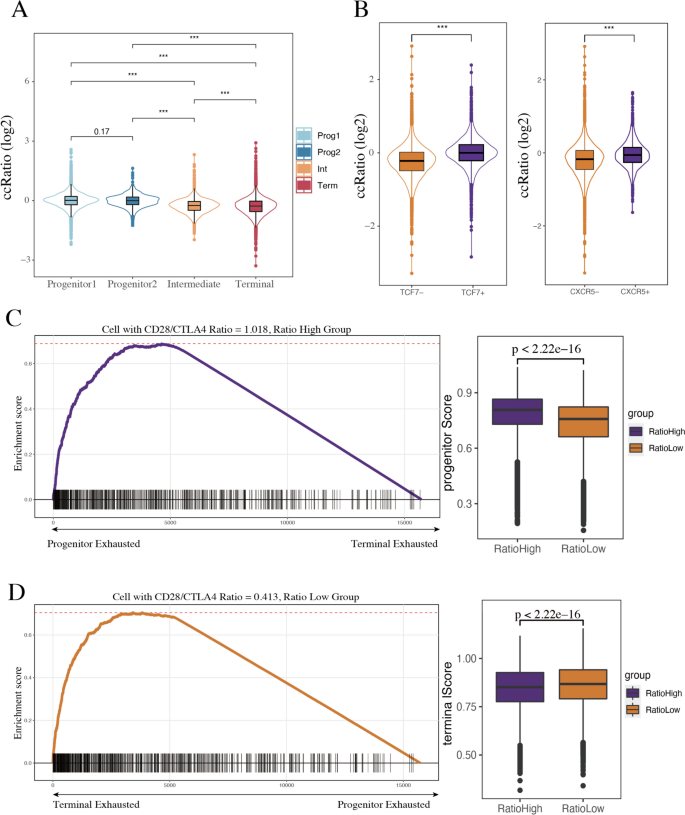
产品关联:文献未提及具体实验产品,领域常规使用单细胞RNA测序平台、clusterProfiler等功能富集软件进行分析。
3.4 病毒感染模型验证ccRatio与T细胞功能的关联
实验目的是在病毒感染模型中验证ccRatio与T细胞功能的关联,确保结论的通用性。研究人员采用COVID-19感染的外周血单个核细胞(PBMC)样本(GSE239799),共纳入4748个CD3+CD28+CTLA4+T细胞,进行与肿瘤样本一致的功能富集和相关性分析。结果显示,肿瘤数据中88%的显著富集功能在该病毒感染模型中重现,“T细胞活化”功能在急性感染、感染后恢复等4种样本条件中均显著富集;52%-76%的肿瘤中与ccRatio相关的基因,在病毒感染模型中保持显著相关性,证实ccRatio与T细胞功能的关联具有跨疾病的通用性。
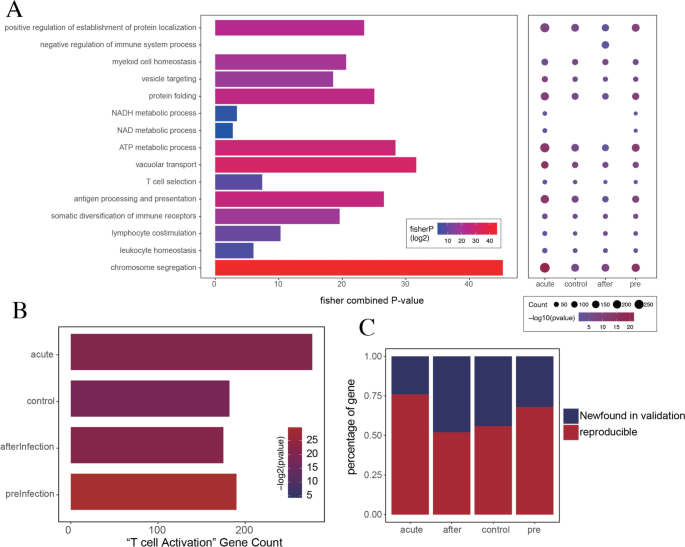
产品关联:文献未提及具体实验产品,领域常规使用PBMC分离试剂盒、流式细胞仪等进行样本处理和检测。
3.5 ccRatio调控因子的筛选与体外功能验证
实验目的是筛选并验证调控ccRatio及T细胞耗竭进程的关键转录因子。研究人员通过相关性分析筛选与ccRatio在多种癌症中相关的转录因子,发现BATF、PRDM1、VDR是跨癌症类型相关性最高的3个转录因子;随后通过体外T细胞培养实验,用CD3刺激诱导T细胞耗竭,分别加入VDR激动剂(骨化三醇)和抑制剂(骨化二醇),检测ccRatio的变化。结果显示,VDR激动剂处理组的ccRatio在第12天较第8天显著降低(Mann-Whitney U检验,P=0.02857),而VDR抑制剂处理组的ccRatio下降趋势被显著抑制(Mann-Whitney U检验,P=0.3429),证实VDR参与调控T细胞从激活到耗竭的分化过程。
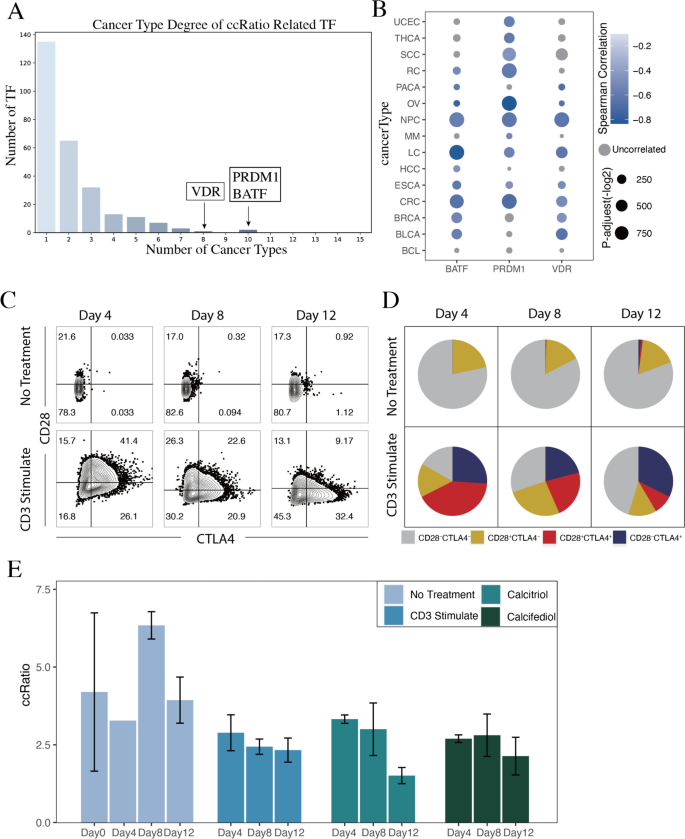
产品关联:实验所用关键产品:EasySep™人T细胞分离试剂盒(Steam Cell,#17951)、T-Activator CD3/CD28 Dynabeads®(Life Technologies,11131D)、BD LSRFortessa™ X-20流式细胞仪。
4. Biomarker研究及发现成果
本研究鉴定的Biomarker为CD28/CTLA4比率(ccRatio),属于细胞表面分子比率类Biomarker,其筛选与验证逻辑为“机制假设→多组学数据验证→临床样本与感染模型验证→体外实验验证”的完整链条。
该Biomarker的来源包括肿瘤组织样本、慢性/急性病毒感染样本、健康人及COVID-19患者的PBMC样本;验证方法涵盖单细胞RNA测序、bulk RNA测序、流式细胞术检测等;特异性与敏感性方面,ccRatio能有效区分T细胞的不同耗竭状态,在慢性感染组与急性感染组、肿瘤样本与正常样本中均呈现显著差异(P<0.05),但文献未明确提供ROC曲线的AUC值等敏感性、特异性量化数据。
核心成果方面,ccRatio作为T细胞耗竭的连续表征标志物,与肿瘤患者的无进展生存期显著相关,高ccRatio组患者的无进展生存期更长(n=9602,Log-rank检验,P<0.05);同时,ccRatio可作为抗CTLA4免疫治疗的响应预测指标,响应组ccRatio显著高于非响应组(n=53,双侧t检验,P<0.05);此外,本研究首次发现VDR作为调控ccRatio的关键转录因子,参与T细胞从激活到耗竭的分化过程,为T细胞耗竭的机制研究提供了新靶点。这些成果的创新性在于突破了传统离散标志物的局限,实现了T细胞耗竭进程的连续追踪,同时为免疫治疗的患者分层和靶点开发提供了新的依据。