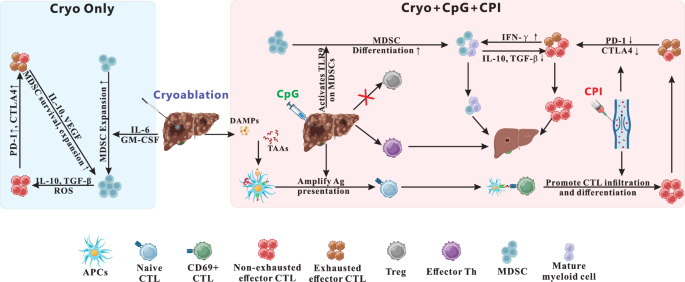
1. 领域背景与文献引入
文献英文标题:Combination of cryoablation, CpG, and dual checkpoint inhibition induces systemic antitumor immunity in a murine model of MASH-associated hepatocellular carcinoma;发表期刊:Journal of Surgical Research;影响因子:3.3(2024年);研究领域:肿瘤免疫治疗(肝细胞癌方向)
肝细胞癌(HCC)是全球发病率持续上升的恶性肿瘤,代谢功能障碍相关脂肪性肝炎(MASH)已成为其重要诱因之一。当前HCC治疗后复发率高,晚期患者预后极差,免疫抑制性肿瘤微环境(TME)是限制免疫治疗疗效的核心瓶颈。领域发展关键节点包括2017年FDA批准纳武利尤单抗用于晚期HCC二线治疗,开启免疫治疗在HCC中的应用;2022年HIMALAYA试验结果支持STRIDE方案(度伐利尤单抗联合替西木单抗)作为晚期HCC一线治疗,标志着双重免疫检查点抑制联合治疗的突破性进展。当前研究热点聚焦于局部治疗与免疫治疗的联合策略、肿瘤微环境重塑靶点、免疫治疗疗效预测生物标志物等,未解决的核心问题包括局部治疗(如冷冻消融)后引发免疫抑制反弹的具体机制、如何优化联合治疗的时序与剂量以最大化协同效应、以及MASH相关HCC这一特殊亚型的免疫治疗应答差异机制等。
针对上述研究空白,本研究旨在探索冷冻消融联合CpG(TLR9激动剂)与双重免疫检查点抑制剂(抗PD-1+抗CTLA-4)的协同效应,通过系统评估不同治疗组合的疗效与免疫机制,明确三重联合治疗能否逆转冷冻消融单药的免疫抑制作用,诱导系统性抗肿瘤免疫,为HCC的精准联合治疗提供新的实验依据。
2. 文献综述解析
作者按治疗类型(单药局部治疗、单药免疫治疗、联合免疫治疗)的分类维度,对HCC领域现有研究进行系统性评述,梳理不同治疗策略的疗效、机制与局限性,进而引出本研究的联合治疗探索方向。
局部治疗方面,冷冻消融通过致死性冷冻破坏肿瘤组织,释放完整的肿瘤相关抗原(TAAs)并启动局部炎症反应,涉及IL-1、IL-6等细胞因子通路,但不完全消融可能刺激肿瘤增殖,且肝脏固有的免疫抑制微环境会削弱其诱导的抗肿瘤免疫应答;单药免疫检查点抑制剂在HCC中的疗效有限,如纳武利尤单抗单药治疗的客观缓解率(ORR)仅约14%,多数患者无法获得持久应答;联合免疫治疗方面,双重检查点抑制策略展现出更优疗效,如纳武利尤单抗联合伊匹木单抗的ORR提升至27-32%,STRIDE方案相比索拉非尼显著延长患者总生存期(16.4个月vs13.8个月),并获FDA批准作为晚期HCC一线治疗,但仍存在部分患者应答不佳、免疫相关不良反应风险较高等局限性,且局部治疗与免疫治疗的联合策略尚未充分阐明其协同机制与最优组合方式。
与现有研究相比,本研究首次在MASH相关HCC小鼠模型中,系统对比了冷冻消融、CpG、双重免疫检查点抑制剂的单药及不同组合治疗的疗效与免疫调控机制,明确了三重联合治疗可逆转冷冻消融单药引发的卫星肿瘤生长加速现象,诱导显著的远隔效应,填补了该领域关于三重联合治疗对MASH相关HCC肿瘤微环境重塑机制研究的空白,为局部治疗与免疫治疗的联合应用提供了关键实验证据。
3. 研究思路总结与详细解析
本研究采用MASH相关HCC双肿瘤小鼠模型,通过随机对照实验设计,系统评估冷冻消融、CpG、双重免疫检查点抑制剂的单药及不同组合治疗的疗效,结合流式细胞术、细胞因子检测、免疫组化、无监督聚类等技术,解析各治疗策略对肿瘤微环境与系统性免疫的调控机制,整体遵循“模型构建→治疗干预→疗效评估→机制解析”的闭环研究逻辑。
3.1 MASH相关HCC双肿瘤小鼠模型构建与分组
实验目的:构建模拟临床MASH相关HCC的双肿瘤小鼠模型,为评估局部治疗对未治疗卫星肿瘤的免疫影响提供实验载体,同时通过随机分组确保各治疗组的基线可比性。
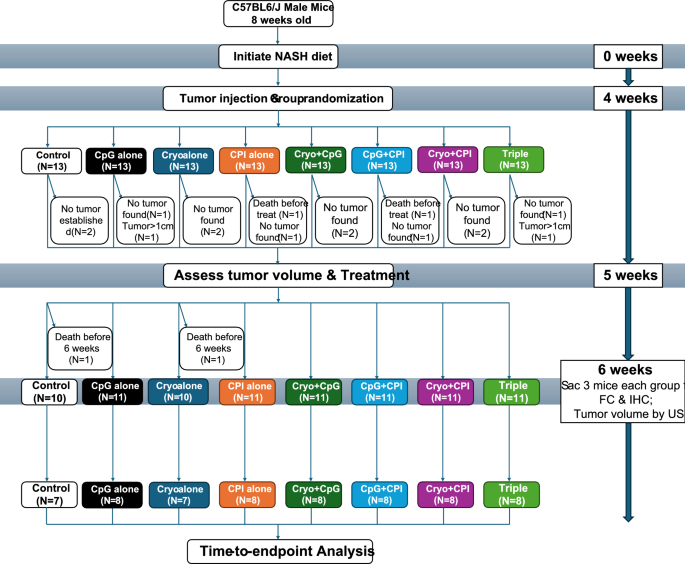
方法细节:选用104只雄性C57BL/6J小鼠,8周龄时给予西式饮食(D12079,Research Diets)诱导MASH,4周后通过超声引导下原位注射RIL-175细胞至肝脏两个不同叶,形成双肿瘤模型;待肿瘤长至≥5mm时,将小鼠随机分为8组,包括对照组(假手术+假CpG+假CPI)、CpG单药组、冷冻消融单药组、CPI单药组、冷冻消融+CpG组、冷冻消融+CPI组、CpG+CPI组、三重联合组(冷冻消融+CpG+CPI)。
结果解读:成功构建MASH相关HCC双肿瘤模型,各治疗组在治疗起始时肿瘤大小无显著差异,确保组间可比性;实验过程中1只对照组和1只冷冻消融组小鼠在6周终点前死亡,纳入生存分析但排除肿瘤体积评估。
产品关联:实验所用关键产品:RIL-175细胞系;西式饮食(D12079,Research Diets);Galil冷冻消融系统(Boston Scientific);抗小鼠PD-1抗体、抗小鼠CTLA-4抗体(BioLegend);CytoFLEX流式细胞仪(Beckman Coulter);FlowJo软件;MESO QuickPlex SQ 120MM细胞因子检测平台(Meso Scale Diagnostics);抗CD8免疫组化(IHC)抗体(ab183685,Abcam)。
3.2 治疗方案实施与疗效评估
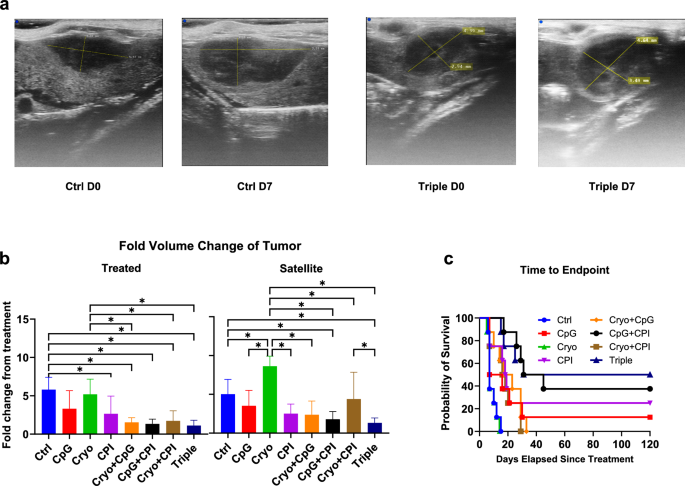
实验目的:系统评估不同治疗方案对肿瘤生长、卫星肿瘤进展及小鼠生存期的影响,明确最优治疗组合。
方法细节:冷冻消融采用Galil系统,17G IceSeed探针,实施3次1分钟冷冻(50%功率),实现不完全消融(≤75%肿瘤体积);CpG为100μg CpG-ODN通过超声引导分3次注射至肿瘤消融边缘与肿瘤内;双重CPI为125μg抗PD-1抗体+250μg抗CTLA-4抗体腹腔注射,Day0给药,抗PD-1抗体每3天重复一次,共2周;通过超声每周监测肿瘤体积,计算治疗后1周的肿瘤体积变化倍数;采用Kaplan-Meier法分析小鼠生存期,通过log-rank检验比较组间差异。
结果解读:三重联合治疗组对治疗肿瘤的生长抑制作用最强,治疗后1周肿瘤体积变化倍数为5.2倍(n=对应样本量,P<0.001),显著优于对照组及各单药组;冷冻消融单药组卫星肿瘤生长较对照组增加1.7倍(n=对应样本量,P=0.014),而三重联合组卫星肿瘤生长较对照组降低2.8倍(n=对应样本量,P=0.028),成功逆转冷冻消融的免疫抑制效应;生存期分析显示,三重联合组中位生存期显著延长,50%小鼠生存期超过120天,而对照组、CpG单药组、冷冻消融单药组的中位生存期仅7天。
3.3 肿瘤微环境免疫细胞组成与功能分析
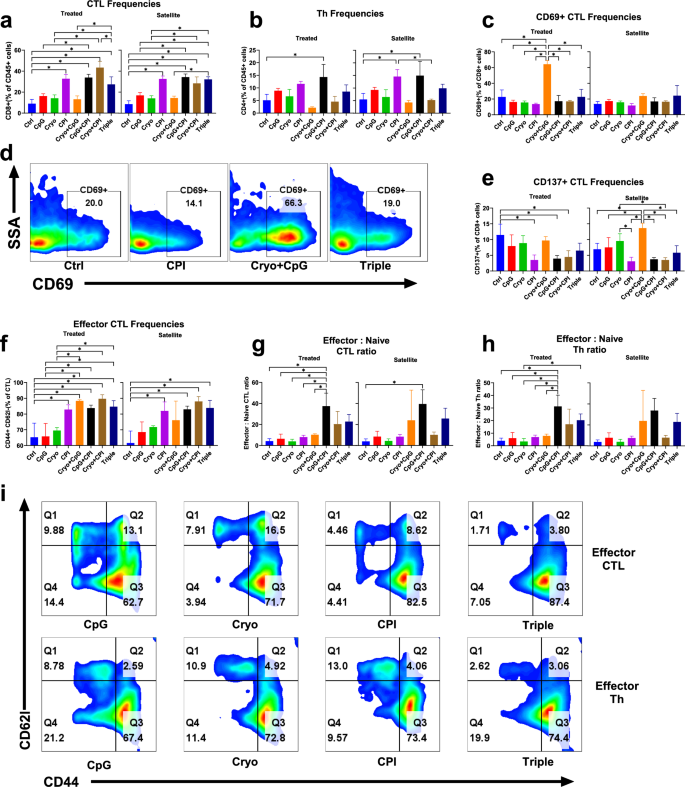
实验目的:解析不同治疗方案对肿瘤微环境中免疫细胞亚群组成、功能状态及相互作用的调控机制。
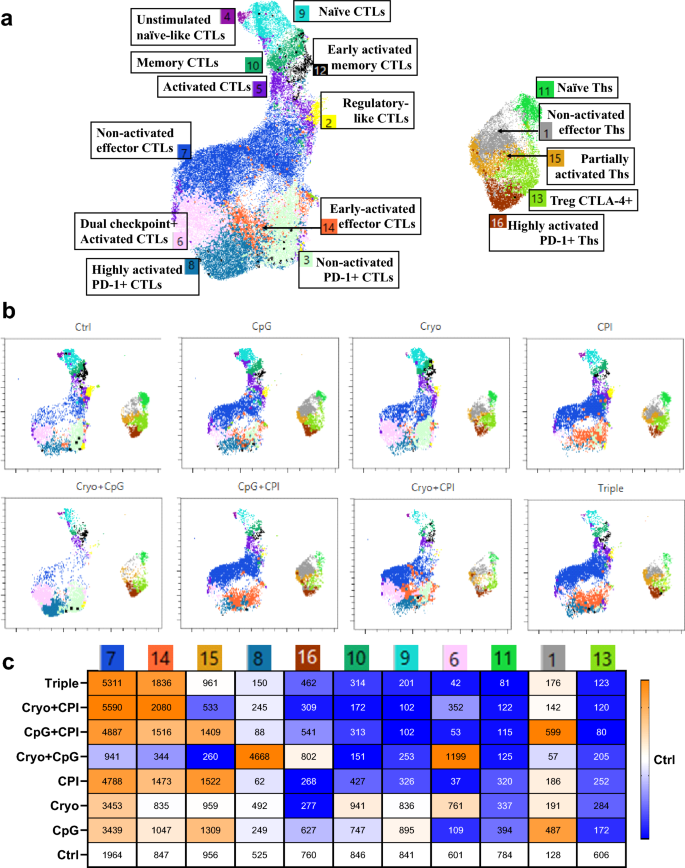
方法细节:治疗后7天处死小鼠,将肿瘤组织分为两半,一半固定后行免疫组化染色,另一半制备单细胞悬液用于流式细胞术分析;流式细胞术采用T细胞抗体 panel(CD4、CD8、CD25、FoxP3等)和髓系细胞抗体 panel(CD11b、Gr1、Ly6G等),分析CD8+细胞毒性T淋巴细胞(CTL)、CD4+辅助T细胞(Th)、调节性T细胞(Treg)、髓源性抑制细胞(MDSC)的频率及功能标志物(CD69、CD137、PD-1、CTLA-4)表达;采用无监督聚类分析T细胞亚群的动态变化。
结果解读:CPI是CTL招募与效应分化的主要驱动因素,所有含CPI的组均显著增加肿瘤内CTL频率,三重联合组肿瘤内CTL频率较对照组升高21.2%(n=3,P<0.001);CpG是Treg耗竭的主要驱动因素,所有含CpG的组均显著降低肿瘤内Treg频率,冷冻消融单药组卫星肿瘤内Treg频率较对照组升高(n=3,P=0.001),而三重联合组可逆转该效应;冷冻消融单药组肿瘤内MDSC频率升高,三重联合组则显著降低MDSC频率;无监督聚类显示,三重联合组富集效应CTL亚群(cluster7),该亚群缺乏免疫检查点分子表达,提示为解除抑制的效应CTL,同时减少免疫抑制性细胞亚群,重塑免疫激活的肿瘤微环境。

3.4 系统性免疫应答与细胞因子分析
实验目的:评估不同治疗方案对系统性免疫应答及细胞因子网络的影响,明确局部治疗与系统性免疫的关联机制。
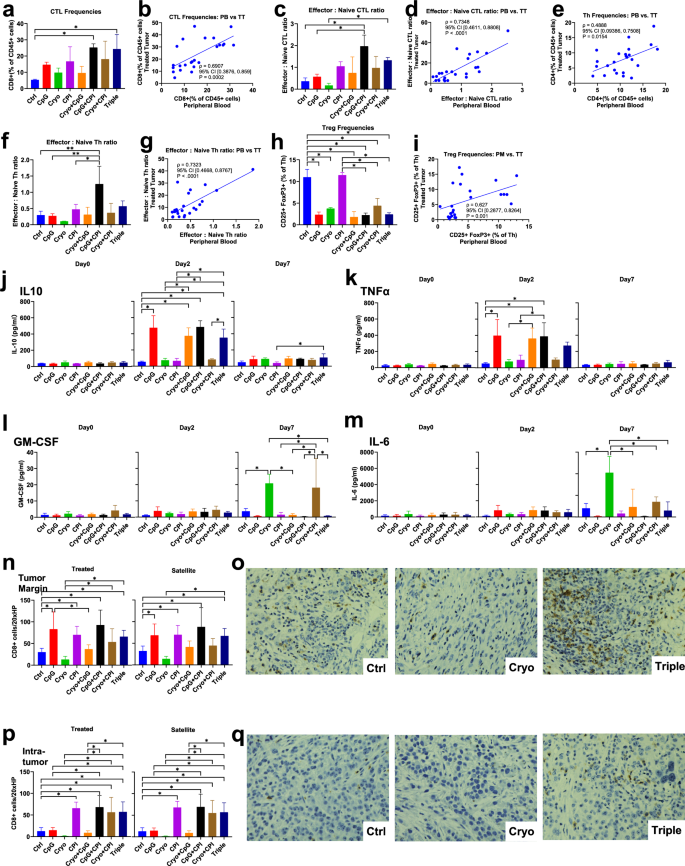
方法细节:采集小鼠外周血,通过流式细胞术分析循环免疫细胞的频率与功能状态;在治疗前(Day0)、治疗后2天(Day2)、治疗后7天(Day7)采集血浆,采用电化学发光多重检测平台分析细胞因子(IL-10、TNF-α、GM-CSF、IL-6等)水平;通过免疫组化检测肿瘤边缘与肿瘤内CD8+T细胞的浸润密度。
结果解读:三重联合组循环CTL频率显著升高,且与肿瘤内CTL频率呈正相关(ρ=对应值,P<0.05),提示系统性免疫与局部免疫应答的协同激活;CpG治疗组在Day2血浆IL-10与TNF-α水平显著升高,冷冻消融组在Day7血浆GM-CSF与IL-6水平显著升高,反映不同治疗策略引发的系统性炎症反应差异;三重联合组肿瘤边缘与肿瘤内CD8+T细胞浸润密度显著增加,较对照组升高对应倍数(n=对应样本量,P<0.05),提示肿瘤微环境的免疫浸润增强。
4. Biomarker研究及发现成果解析
本研究聚焦肿瘤微环境与系统性免疫中的免疫细胞亚群、免疫检查点分子及细胞因子三类Biomarker,通过多维度检测与相关性分析,明确其与治疗疗效的关联,为HCC联合治疗的疗效预测与机制解析提供潜在靶点。
涉及的Biomarker包括免疫细胞亚群(CD8+CTL、Treg、MDSC)、免疫检查点分子(PD-1、CTLA-4)、细胞因子(IL-10、TNF-α、GM-CSF、IL-6);筛选与验证逻辑为:基于不同治疗组的疗效差异,通过流式细胞术、细胞因子检测筛选差异表达的标志物,进一步通过相关性分析验证其与肿瘤生长、生存期的关联,明确其在免疫调控中的作用。
免疫细胞亚群Biomarker来自肿瘤组织与外周血样本,通过流式细胞术定量检测其频率,如CD8+CTL在三重联合组肿瘤内的频率较对照组升高21.2%(n=3,P<0.001);免疫检查点分子通过流式细胞术检测其在T细胞表面的表达水平,如PD-1在三重联合组CTL表面的表达较对照组降低36.3%(n=3,P≤0.001);细胞因子通过血浆样本的电化学发光多重检测平台定量检测,如CpG治疗组Day2血浆TNF-α水平较对照组升高对应倍数(n=对应样本量,P<0.05)。特异性与敏感性方面,CD8+CTL频率与肿瘤生长抑制呈正相关,Treg与MDSC频率与肿瘤生长呈正相关,提示其具有作为疗效预测Biomarker的潜力(文献未明确提供ROC曲线数据,基于图表趋势推测)。
CD8+CTL频率升高与肿瘤生长抑制及生存期延长显著相关,可作为三重联合治疗疗效的潜在预测Biomarker;Treg与MDSC是肿瘤微环境中的关键免疫抑制Biomarker,CpG可显著耗竭Treg,三重联合治疗可降低MDSC频率,打破免疫抑制反馈环路;PD-1表达与MDSC频率呈正相关(ρ=0.768,P<0.001),提示二者形成免疫抑制协同机制,而三重联合治疗可同时下调PD-1表达与MDSC频率,重塑免疫激活的肿瘤微环境。本研究首次在MASH相关HCC模型中,明确了这些免疫Biomarker在局部-免疫联合治疗中的调控机制,为临床转化提供了潜在的疗效预测指标与干预靶点。