1. 领域背景与文献
文献英文标题:Metformin enhances γδ T cell-mediated antitumor immunity in triple-negative breast cancer through immunometabolic reprogramming;发表期刊:未公开;影响因子:未公开;研究领域:三阴性乳腺癌免疫治疗
领域共识:三阴性乳腺癌(TNBC)是一类缺乏雌激素受体、孕激素受体及人表皮生长因子受体2(HER2)表达的乳腺癌亚型,约占所有乳腺癌病例的12%-20%,具有恶性程度高、早期复发转移风险大、预后差的特点,传统化疗是目前的标准治疗方案,但存在耐药性问题,患者长期生存获益有限。免疫治疗为TNBC带来了新的突破,PD-1/PD-L1抑制剂等免疫检查点抑制剂在部分患者中显示出抗肿瘤活性,KEYNOTE-522临床试验进一步确立了帕博利珠单抗联合化疗用于早期TNBC的治疗地位;过继细胞治疗如肿瘤浸润淋巴细胞(TIL)转移也在转移性乳腺癌的初步研究中显示出客观应答潜力。γδ T细胞作为一类独特的淋巴细胞亚群,无需主要组织相容性复合体(MHC)分子即可直接识别肿瘤相关配体(如MICA/B、BTN3A1等),具有强大的直接细胞毒作用和免疫调节功能,其中外周血中占主导的Vγ9Vδ2亚型可通过体外高效扩增,成为过继细胞免疫治疗的潜在候选细胞。然而,γδ T细胞在肿瘤微环境中易出现功能耗竭和免疫抑制,其抗肿瘤活性受到限制,如何增强γδ T细胞在TNBC中的抗肿瘤效应是当前研究的空白。二甲双胍作为一线口服降糖药物,已被证实具有抗肿瘤作用,可通过激活AMPK通路抑制肿瘤细胞增殖,同时还能调节免疫细胞功能,如增强效应T细胞活性、抑制调节性T细胞的免疫抑制作用,与免疫检查点抑制剂具有协同效应,但关于二甲双胍对γδ T细胞的调控作用及其在TNBC中的联合应用尚未得到系统研究,因此本研究旨在探讨二甲双胍是否能通过免疫代谢重编程增强γδ T细胞介导的TNBC抗肿瘤免疫,为TNBC的免疫治疗提供新的联合策略。
2. 文献综述解析
作者从TNBC治疗现状、γδ T细胞的抗肿瘤特性及应用潜力、二甲双胍的抗肿瘤与免疫调节作用三个维度对领域内现有研究进行了系统梳理,明确了当前研究的进展与不足。
现有研究中,TNBC治疗方面,传统化疗是基石,但存在耐药性高、特异性差等局限性;免疫治疗领域,免疫检查点抑制剂虽在部分患者中有效,但整体响应率仍较低,且缺乏有效的预测生物标志物;过继细胞治疗如TILs显示出潜力,但细胞制备流程复杂、成本高,限制了其广泛应用。γδ T细胞的研究显示,其具有无需MHC限制识别肿瘤、可体外高效扩增、抗肿瘤活性强等优势,临床研究已证实其在部分恶性肿瘤中可降低肿瘤负荷、延长患者生存,但在TNBC中的应用及功能调控机制尚未充分阐明,尤其是肿瘤微环境中γδ T细胞的耗竭机制及逆转策略仍不明确。二甲双胍的相关研究表明,其可通过AMPK通路抑制肿瘤细胞的代谢和增殖,同时还能调节免疫系统,增强效应T细胞的功能,与免疫检查点抑制剂具有协同效应,但关于其对γδ T细胞的直接调控作用及在TNBC中的联合应用尚未见报道。
本研究的创新价值在于首次系统揭示了二甲双胍通过免疫代谢重编程同时调控γδ T细胞和TNBC细胞的代谢及免疫功能,实现协同抗肿瘤效应:一方面,二甲双胍增强γδ T细胞的增殖能力、效应分子分泌,并恢复耗竭γδ T细胞的功能;另一方面,二甲双胍抑制TNBC细胞的代谢,同时上调其表面的免疫配体,增强γδ T细胞的识别和杀伤能力;此外,本研究还在化疗耐药TNBC模型中验证了这一协同效应,并结合临床数据库分析证实了AMPK激活与γδ T细胞浸润联合对TNBC患者预后的预测价值,填补了二甲双胍与γδ T细胞联合用于TNBC治疗的研究空白,为TNBC的免疫治疗提供了新的思路。
3. 研究思路总结与详细解析
本研究的整体研究目标是明确二甲双胍是否能增强γδ T细胞介导的TNBC抗肿瘤免疫,并阐明其背后的免疫代谢调控机制;核心科学问题是二甲双胍如何通过差异化调控γδ T细胞和TNBC细胞的代谢状态,进而调节两者的免疫功能,实现协同抗肿瘤作用;技术路线遵循“假设提出→体外实验验证→体内实验验证→机制阐明→临床相关性验证”的闭环逻辑,从细胞、动物、分子及临床多个层面系统验证研究假设。
3.1 γδ T细胞体外扩增与TNBC细胞模型构建
该环节的核心目标是获取高纯度的功能正常的γδ T细胞及TNBC细胞模型(包括亲本株和化疗耐药株),为后续实验提供可靠的研究工具。方法细节上,从健康供者外周血中分离外周血单个核细胞(PBMCs),采用Ficoll密度梯度离心法分离后,用唑来膦酸和人重组IL-2刺激培养9-12天,实现γδ T细胞的高效扩增;使用MDA-MB-231、MDA-MB-468两种TNBC细胞系作为亲本株,通过逐步增加紫杉醇浓度的方法构建紫杉醇耐药的MDA-MB-231/PTX和MDA-MB-468/PTX细胞系,并通过慢病毒转染构建荧光素酶标记的细胞系,用于后续细胞毒活性的定量检测;动物实验采用4-6周龄的BALB/c-nu裸鼠,经全身照射(200 cGy)后,皮下接种MDA-MB-231细胞与Matrigel的混合物,构建TNBC异种移植模型。结果解读显示,扩增后的γδ T细胞纯度高,CD4+和CD8+ T细胞污染极少;成功构建的紫杉醇耐药TNBC细胞系的紫杉醇IC50显著高于亲本细胞,证实耐药性构建成功;异种移植模型中肿瘤生长稳定,可用于体内抗肿瘤效应的评估。实验所用关键产品:Ficoll-Paque PLUS(Cytiva,货号17144002)、RPMI-1640完全培养基(Gibco,货号C11875500BT)、胎牛血清(Procell,货号164210)、唑来膦酸(Abmole,货号ab-M2329)、人重组IL-2(Prosperich,货号CSBSJ-IL-2)、TNBC细胞系(Procell,货号CL-0150、CL-0290)、荧光素酶标记细胞系(Ubigene,货号YC-D005-Luc-P、YC-D009-Luc-P)、Matrigel(Corning,货号354234)。
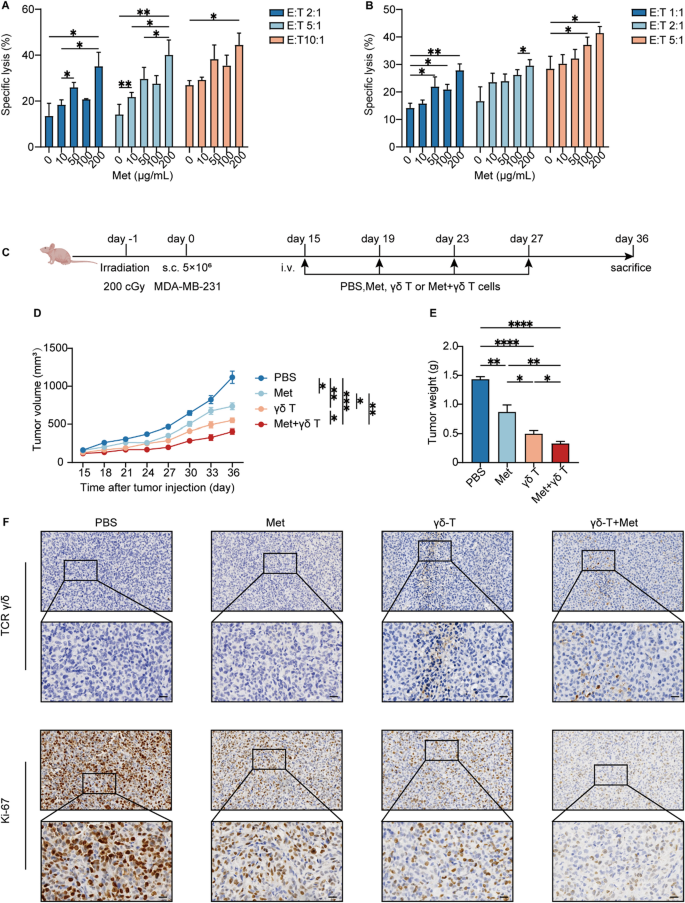
3.2 二甲双胍与γδ T细胞协同抗肿瘤效应的体外与体内验证
该环节的核心目标是验证二甲双胍是否能增强γδ T细胞介导的TNBC抗肿瘤效应。方法细节上,体外实验将γδ T细胞与TNBC细胞(包括亲本株和耐药株)按不同效靶比共培养,同时加入不同浓度的二甲双胍,采用荧光素酶法检测γδ T细胞的细胞毒活性;体内实验中,当裸鼠皮下肿瘤体积达到100-150 mm³时,将小鼠随机分为对照组、γδ T细胞组、二甲双胍组、二甲双胍+γδ T细胞组,二甲双胍采用腹腔注射,γδ T细胞采用尾静脉注射,每3天测量肿瘤体积,每6天测量小鼠体重,实验终点(肿瘤移植后36天)处死小鼠,取肿瘤组织进行免疫组化分析。结果解读显示,体外实验中,二甲双胍以剂量依赖的方式显著增强γδ T细胞对TNBC细胞的细胞毒活性,效靶比越高,增强效应越明显(n=3,P<0.05);体内实验中,单独γδ T细胞治疗可一定程度抑制肿瘤生长,而二甲双胍预处理后,γδ T细胞的抗肿瘤活性进一步增强,肿瘤体积和重量均显著低于其他组(n=6,P<0.001),免疫组化结果显示二甲双胍+γδ T细胞组的肿瘤组织中γδ T细胞浸润显著增加,Ki-67表达显著降低,提示肿瘤细胞增殖受抑。实验所用关键产品:Steady-Glo®荧光素酶检测试剂盒(Promega,货号E2510)、Ki-67抗体(Abcam,货号ab15580)、TCR γ/δ抗体(Thermo Fisher,货号TCR1061)。

3.3 二甲双胍对γδ T细胞增殖、效应功能及耗竭状态的调控
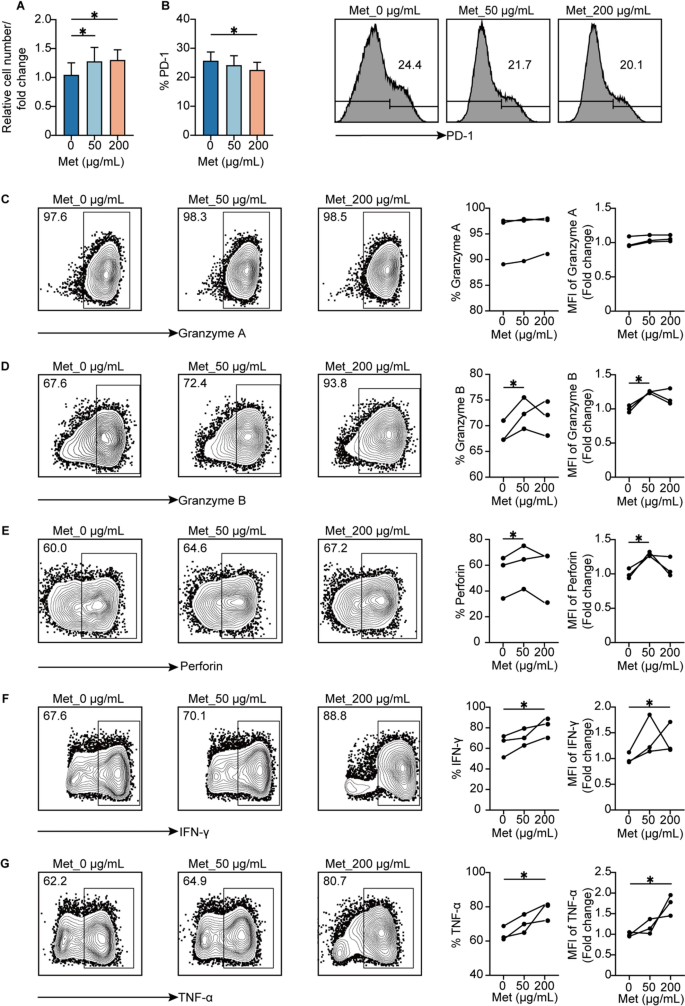
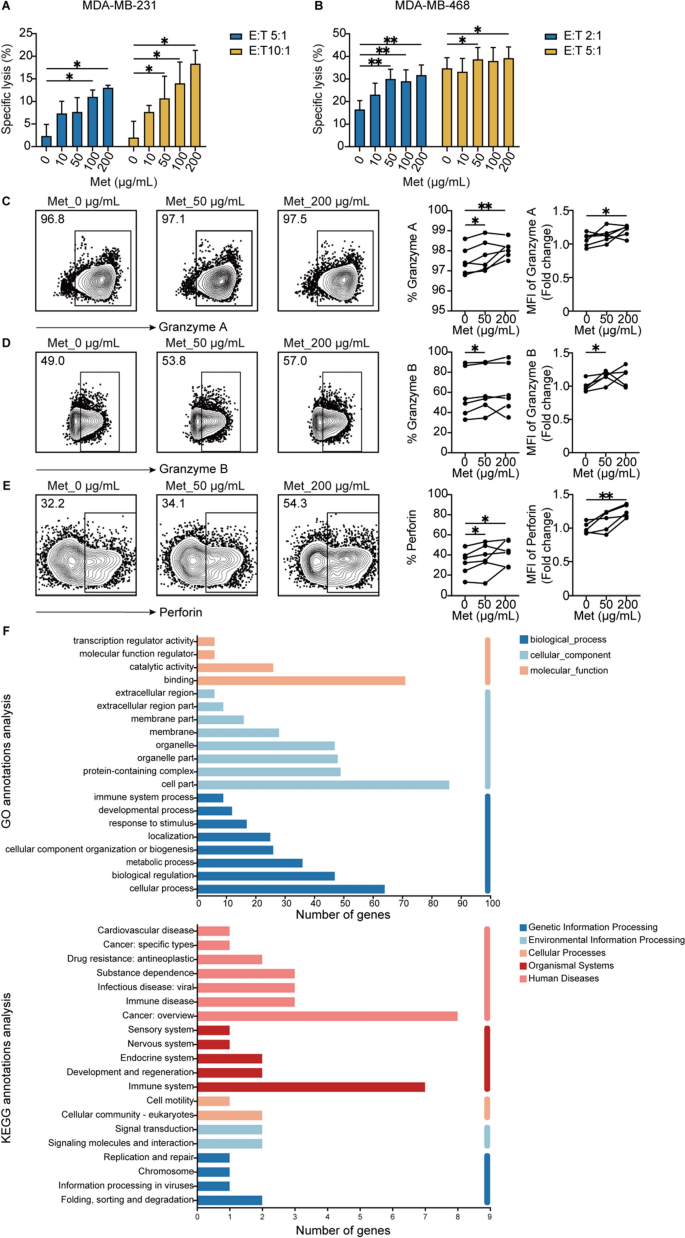
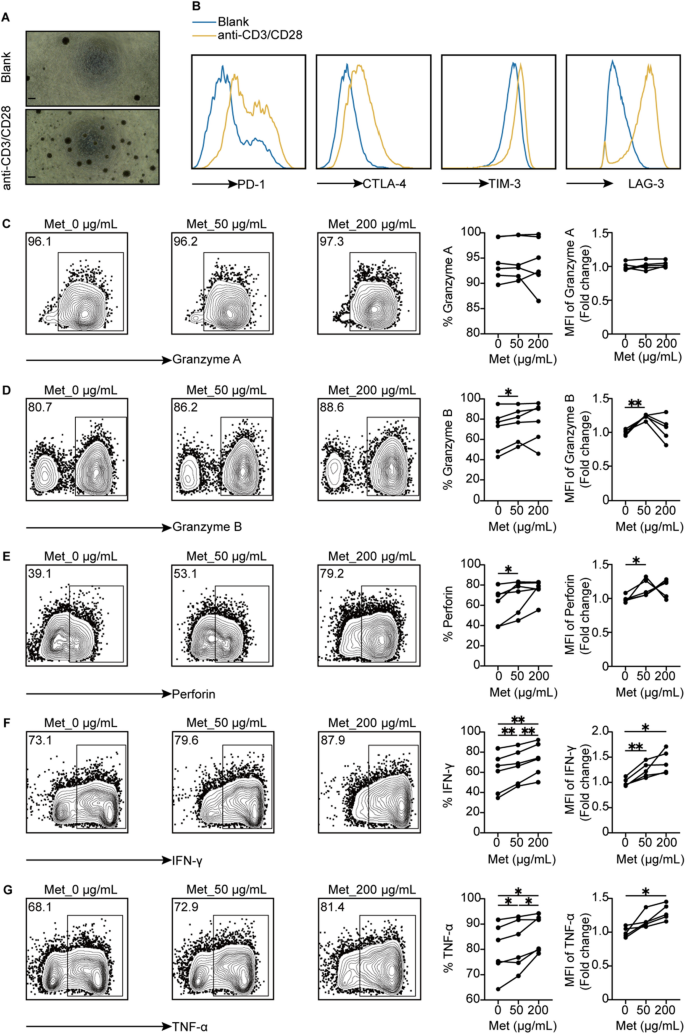
该环节的核心目标是明确二甲双胍对γδ T细胞自身功能的直接调控作用。方法细节上,用不同浓度的二甲双胍处理γδ T细胞72小时后,采用CCK-8法检测细胞增殖能力;流式细胞术检测PD-1等耗竭标志物的表达,以及颗粒酶A、颗粒酶B、穿孔素、干扰素-γ(IFN-γ)、肿瘤坏死因子-α(TNF-α)等效应分子的表达;通过T Cell TransAct™重刺激构建γδ T细胞耗竭模型,检测二甲双胍对耗竭γδ T细胞功能的恢复作用;对二甲双胍处理48小时后的γδ T细胞进行RNA-seq分析,筛选差异表达基因并进行基因本体(GO)和京都基因与基因组百科全书(KEGG)富集分析。结果解读显示,二甲双胍显著增强γδ T细胞的增殖能力(n=3,P<0.05),同时降低PD-1的表达;效应分子方面,低浓度二甲双胍可增加颗粒酶B和穿孔素的表达,高浓度二甲双胍则显著促进IFN-γ和TNF-α的分泌(n=3,P<0.05);当二甲双胍预处理的γδ T细胞与TNBC细胞共培养时,颗粒酶A、颗粒酶B和穿孔素的表达进一步增强,提示效应功能被激活;RNA-seq分析显示,二甲双胍处理后γδ T细胞中差异表达的基因主要富集在免疫调节、肿瘤通路等相关功能,其中CXCR5、SIX4等基因显著上调,CXCR5可促进免疫细胞归巢至淋巴组织,SIX4可激活干扰素基因刺激因子(STING)通路增强免疫应答;在耗竭γδ T细胞模型中,二甲双胍处理可显著增加颗粒酶B、穿孔素、IFN-γ、TNF-α的表达,恢复其抗肿瘤功能(n=3,P<0.05)。实验所用关键产品:CCK-8试剂盒(Dojindo,货号CK04)、流式细胞术抗体(Biolegend,如抗CD3货号300318、抗PD-1货号329906、抗颗粒酶B货号515408等)、T Cell TransAct™(Miltenyi Biotec,货号130-111-160)、Trizol试剂(Invitrogen,货号10296028)。
3.4 二甲双胍对γδ T细胞和TNBC细胞代谢的差异调控机制
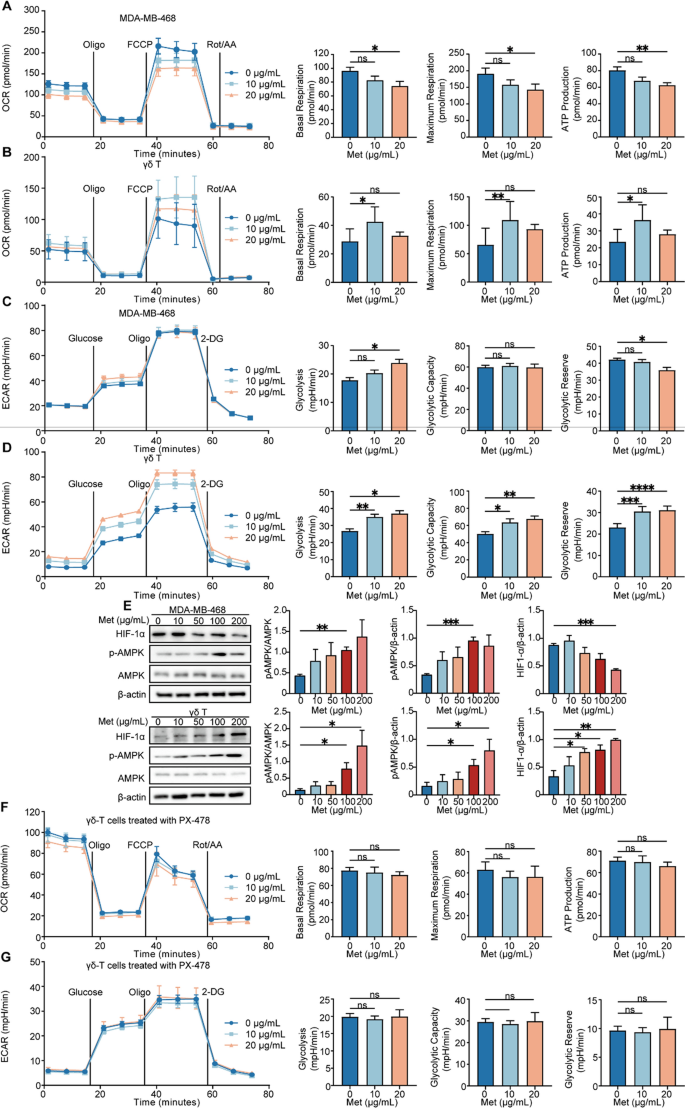
该环节的核心目标是阐明二甲双胍对γδ T细胞和TNBC细胞代谢的差异化调控机制。方法细节上,采用Seahorse XF96细胞外通量分析仪检测二甲双胍处理24小时后,两种细胞的氧消耗率(OCR,用于反映氧化磷酸化(OXPHOS)水平)和细胞外酸化率(ECAR,用于反映糖酵解水平);免疫印迹法检测二甲双胍处理4小时后,两种细胞中AMPK磷酸化水平及缺氧诱导因子-1α(HIF-1α)的表达;使用HIF-1α抑制剂PX-478和激活剂DMOG,验证HIF-1α在二甲双胍调控代谢中的作用;采用实时荧光定量PCR(qPCR)检测DMOG处理后γδ T细胞中CXCR5和SIX4的转录水平。结果解读显示,二甲双胍显著抑制TNBC细胞的氧化磷酸化,表现为基础呼吸、最大呼吸及ATP生成均降低(n=3,P<0.05),同时糖酵解水平增加但糖酵解储备降低;而γδ T细胞在二甲双胍处理后,氧化磷酸化和糖酵解水平均显著增强(n=3,P<0.01);免疫印迹结果显示,二甲双胍可激活两种细胞的AMPK通路,但TNBC细胞中HIF-1α的表达降低,γδ T细胞中HIF-1α的表达升高;PX-478可完全阻断二甲双胍对γδ T细胞代谢的调控作用,提示HIF-1α是关键调控分子;DMOG激活HIF-1α可显著上调CXCR5和SIX4的转录水平,提示HIF-1α介导了二甲双胍对γδ T细胞的免疫调控。实验所用关键产品:Seahorse XF96细胞外通量分析仪(Agilent)、免疫印迹抗体(CST,如抗磷酸化AMPKα货号2535T、抗HIF-1α货号2178S等)、HIF-1α抑制剂PX-478、激活剂DMOG(MCE)、qPCR试剂盒(Vazyme,如HiScript IV RT SuperMix货号R423-01、SupRealQ Ultra Hunter SYBR qPCR Master Mix货号Q713-02)。
3.5 二甲双胍对TNBC细胞表面免疫配体的调控作用
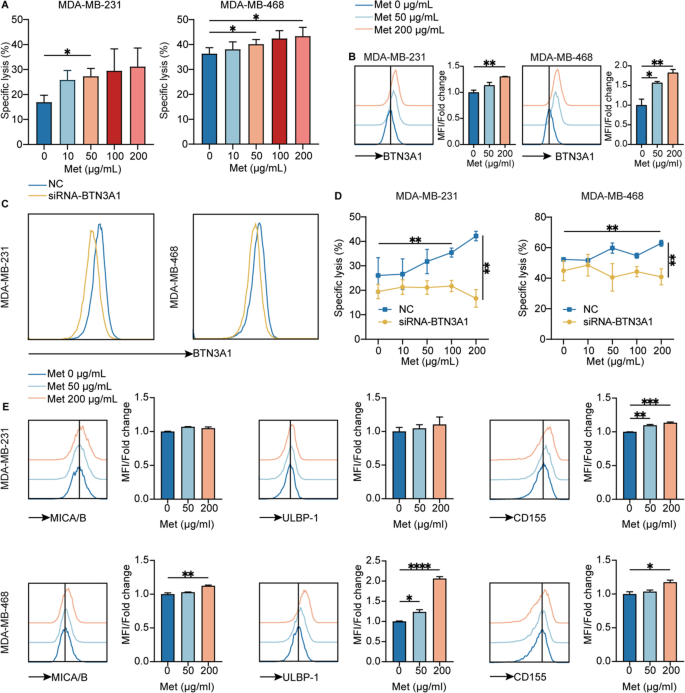
该环节的核心目标是明确二甲双胍是否通过上调TNBC细胞表面的免疫配体增强γδ T细胞的识别和杀伤能力。方法细节上,用不同浓度的二甲双胍处理TNBC细胞(包括亲本株和耐药株)24小时后,流式细胞术检测BTN3A1、MICA/B、ULBP-1、CD155等免疫配体的表达;采用siRNA敲低TNBC细胞中的BTN3A1,检测二甲双胍对γδ T细胞细胞毒活性的影响。结果解读显示,二甲双胍以剂量依赖的方式显著上调TNBC细胞表面BTN3A1的表达(n=3,P<0.001);siRNA敲低BTN3A1后,二甲双胍增强γδ T细胞细胞毒活性的作用被显著抑制(n=3,P<0.01),证实BTN3A1是关键的功能配体;此外,二甲双胍还可上调MICA/B、ULBP-1、CD155等配体的表达,且具有细胞系特异性,如MDA-MB-231细胞中主要上调CD155,而MDA-MB-468细胞中MICA/B、ULBP-1、CD155均显著上调;在紫杉醇耐药的TNBC细胞系中,二甲双胍同样可上调BTN3A1及相关免疫配体的表达,提示该调控作用在耐药株中也存在。实验所用关键产品:流式细胞术抗体(Miltenyi Biotec抗BTN3A1货号130-124-880、BD Biosciences抗MICA/B货号742322等)、BTN3A1 siRNA(MCE,货号HY-RS01673)、Lipofectamine RNAiMAX(Thermo Fisher,货号13778075)。
3.6 临床数据库分析AMPK激活与γδ T细胞浸润对TNBC患者预后的影响
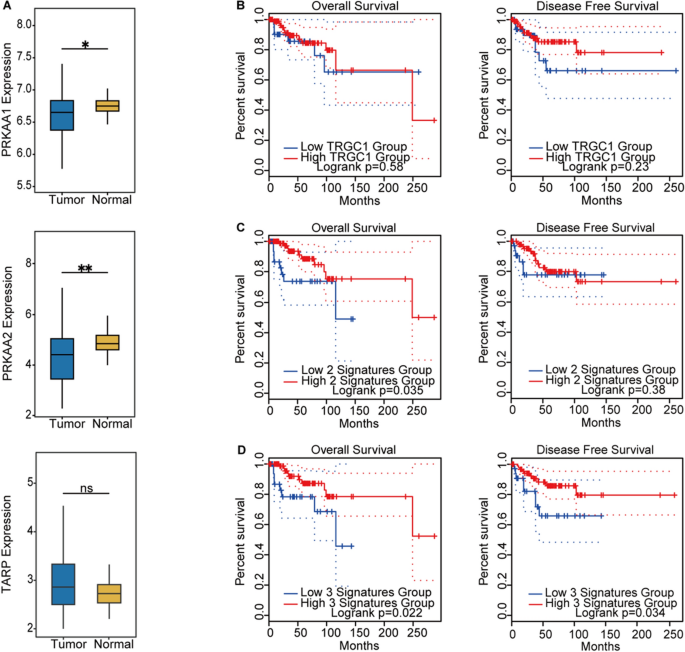
该环节的核心目标是验证研究结果的临床相关性,明确AMPK激活与γδ T细胞浸润对TNBC患者预后的影响。方法细节上,利用基因表达综合数据库(GEO,GSE76250)分析165例TNBC组织与33例正常乳腺组织中PRKAA1、PRKAA2(AMPKα亚基,代表AMPK通路激活)和TRAP(γδ T细胞浸润标记)的表达差异;利用基因表达谱交互式分析数据库(GEPIA)分析TRGC1(γδ T细胞标记)、PRKAA1+PRKAA2(AMPK激活标记)及两者联合对TNBC患者总生存期(OS)和无病生存期(DFS)的影响。结果解读显示,TNBC组织中PRKAA1和PRKAA2的表达显著低于正常组织(n=165 vs 33,P<0.05),而γδ T细胞浸润水平在TNBC与正常组织中无显著差异;单独高γδ T细胞浸润对患者OS和DFS无显著影响,单独AMPK激活与患者更好的OS相关(n=134,P<0.05),而AMPK激活联合高γδ T细胞浸润则与患者更好的OS和DFS均相关(n=134,P<0.05)。文献未提及具体实验产品,领域常规使用GEO、GEPIA等在线数据库分析工具。
4. Biomarker研究及发现成果
本研究涉及的Biomarker包括γδ T细胞浸润标记(TRGC1、TRAP)、AMPK通路激活标记(PRKAA1、PRKAA2)、TNBC细胞表面免疫配体(BTN3A1、MICA/B、ULBP-1、CD155),其筛选与验证逻辑清晰,涵盖了临床预后预测与功能验证两个层面。
γδ T细胞浸润标记(TRGC1、TRAP)和AMPK通路激活标记(PRKAA1、PRKAA2)来源于TNBC患者组织样本的转录组数据,通过GEO、GEPIA等临床数据库进行筛选与预后验证;TNBC细胞表面免疫配体则通过体外实验筛选,检测二甲双胍处理后的表达变化,并通过siRNA敲低验证其功能相关性。具体而言,γδ T细胞浸润标记的验证方法为数据库生存分析,结果显示AMPK激活联合高γδ T细胞浸润的患者OS和DFS显著长于低表达组(n=134,P<0.05);AMPK通路激活标记的验证显示,TNBC组织中PRKAA1和PRKAA2的表达显著低于正常组织(n=165 vs 33,P<0.05),高表达与患者更好的OS相关;TNBC细胞表面免疫配体方面,流式细胞术结果显示二甲双胍处理后BTN3A1表达显著上调(n=3,P<0.001),siRNA敲低BTN3A1可阻断二甲双胍对γδ T细胞细胞毒活性的增强作用(n=3,P<0.01),MICA/B、ULBP-1、CD155也呈剂量依赖上调,且在化疗耐药株中同样存在。
本研究的核心成果在于,首次确立了AMPK激活联合γδ T细胞浸润作为TNBC患者的预后Biomarker,该联合标记可有效预测患者的OS和DFS,为TNBC患者的预后评估提供了新的指标;同时明确了TNBC细胞表面的BTN3A1是二甲双胍增强γδ T细胞抗肿瘤活性的关键功能性Biomarker,为TNBC的免疫治疗提供了潜在的靶点;此外,HIF-1α作为代谢调控Biomarker,介导了二甲双胍对γδ T细胞和TNBC细胞的差异代谢调控,进而影响免疫功能,为免疫代谢调控提供了新的机制。目前研究未提供该联合Biomarker的风险比(HR)具体数值,但生存分析的统计学结果证实了其预后预测价值(P<0.05)。