1. 领域背景与文献引入
文献英文标题:TLR8 agonists optimally remodel the tumor immune microenvironment through PF4-dependent and independent mechanisms;发表期刊:未公开;影响因子:未公开;研究领域:肿瘤免疫治疗(模式识别受体调控肿瘤免疫微环境方向)
模式识别受体(PRR)作为先天免疫的关键传感器,可识别病原体相关分子模式(PAMPs)和损伤相关分子模式(DAMPs),其在肿瘤免疫中的调控作用是当前肿瘤免疫治疗的研究热点。领域发展关键节点包括:早期PRR激动剂如TLR9的CpG寡核苷酸、TLR3的poly(I:C)被开发为疫苗佐剂,通过增强树突状细胞(DC)的抗原提呈能力放大适应性免疫反应;近年来PRR激动剂逐渐向直接抗肿瘤治疗方向拓展,但其临床转化仍受限于对肿瘤免疫微环境(TIME)调控的不完全性。当前研究热点聚焦于不同PRR亚型激动剂的功效比较、PRR调控TIME的关键下游效应分子不明确;血小板因子4(PF4/CXCL4)在肿瘤中呈现双重作用,其促肿瘤与抗肿瘤功能的上下文依赖机制尚未阐明,限制了其作为治疗靶点的应用。
针对上述研究空白,本研究系统比较了多种PRR激动剂重塑TIME的功效,筛选出最优的TLR8激动剂,并深入解析其通过PF4依赖与非依赖机制调控TIME的分子通路,明确了PF4在局部肿瘤微环境中的抗肿瘤作用与系统表达时的促肿瘤作用的上下文依赖差异,为PRR激动剂的肿瘤免疫治疗应用提供了新的靶点与策略。
2. 文献综述解析
作者以PRR的功能分类与PF4的双重作用为核心维度,系统综述了PRR调控肿瘤免疫的研究现状与PF4在肿瘤中的矛盾功能,明确了当前研究的局限性与本研究的创新方向。
现有研究表明,PRR激活可双向调控肿瘤免疫,一方面可通过激活先天免疫细胞、促进DC成熟与抗原提呈,诱导适应性抗肿瘤免疫,抑制肿瘤生长;另一方面,慢性或失调的PRR信号可通过招募调节性T细胞(Treg)、髓源性抑制细胞(MDSC),形成免疫抑制性TIME,促进肿瘤进展。在技术方法上,部分PRR激动剂如TLR9、TLR3激动剂已进入临床前或早期临床研究,作为疫苗佐剂展现出增强抗肿瘤免疫的潜力,但作为单药治疗的功效有限。关于PF4的研究显示,其具有双重肿瘤调控功能:一方面可通过抗血管生成作用、干扰促肿瘤趋化发挥抗肿瘤活性;另一方面可通过促进血小板生成、MDSC浸润、Treg分化与增殖发挥促肿瘤作用,但现有研究多集中于系统表达的PF4,局部肿瘤微环境中PF4的功能与调控机制尚未明确。
与现有研究相比,本研究的核心创新点在于首次系统比较了7种不同PRR激动剂(涵盖TLR、NLR、STING家族)重塑TIME的功效,明确TLR8激动剂是唯一可同时增强先天免疫细胞功能与适应性效应T细胞浸润、降低免疫抑制细胞比例的最优激动剂;首次揭示TLR8通过NF-κB通路诱导局部肿瘤微环境中的巨噬细胞、cDC2、CD8+T细胞表达PF4,进而通过CXCR3通路招募常规CD4+T细胞(cCD4+T)的分子机制;首次明确PF4的上下文依赖双重作用,局部肿瘤微环境中诱导的PF4发挥抗肿瘤作用,而系统表达的PF4则呈现促肿瘤效应,解决了PF4在肿瘤中功能矛盾的关键问题;此外,本研究还发现TLR8激动剂与抗PD-1治疗具有显著协同作用,为临床联合治疗提供了实验依据。
3. 研究思路总结与详细解析
本研究以“系统筛选最优PRR激动剂→验证抗肿瘤活性→解析分子机制→验证关键效应分子→探索联合治疗”为闭环技术路线,明确研究目标为筛选可有效重塑TIME的PRR激动剂并解析其调控机制,核心科学问题聚焦于TLR8激动剂如何通过PF4依赖与非依赖机制重塑TIME,以及PF4上下文依赖功能的分子基础。
3.1 PRR激动剂筛选与TIME重塑功效比较
实验目的:系统比较不同PRR激动剂对TIME中免疫细胞亚群的调控效果,筛选出可诱导促免疫原性TIME的最优激动剂。方法细节:采用皮下AKR食管癌细胞肿瘤模型,当肿瘤体积达到约200 mm³时,瘤内注射7种PRR激动剂(TLR3的poly(I:C)、TLR7的咪喹莫特、TLR8的TL8-506、TLR9的CpG ODN 2395、STING的ADU-S100、NOD1的Tri-DAP、NOD2的murabutide),48小时后通过流式细胞术分析肿瘤组织中免疫细胞亚群的比例与功能。结果解读:流式细胞术结果显示,仅TLR8和NOD2激动剂显著增加CD45+白细胞在总细胞中的比例;TLR8和NOD1激动剂提升了cDC在CD45+细胞中的比例;除TLR7激动剂外,所有激动剂均增强了cDC对肿瘤抗原(ZsGreen)的吞噬能力;TLR8和NOD2激动剂增加了巨噬细胞在CD45+细胞中的比例,且仅TLR8激动剂显著促进抗原负载巨噬细胞向引流淋巴结迁移;尤为关键的是,TLR8激动剂是唯一同时上调CD8+T细胞和cCD4+T细胞比例、降低Treg细胞比例的激动剂,显著提升了cCD4+T/Treg与CD8+T/Treg的比值(n=8,P<0.05至P<0.0001),表明其可全面重塑TIME为促免疫原性状态。
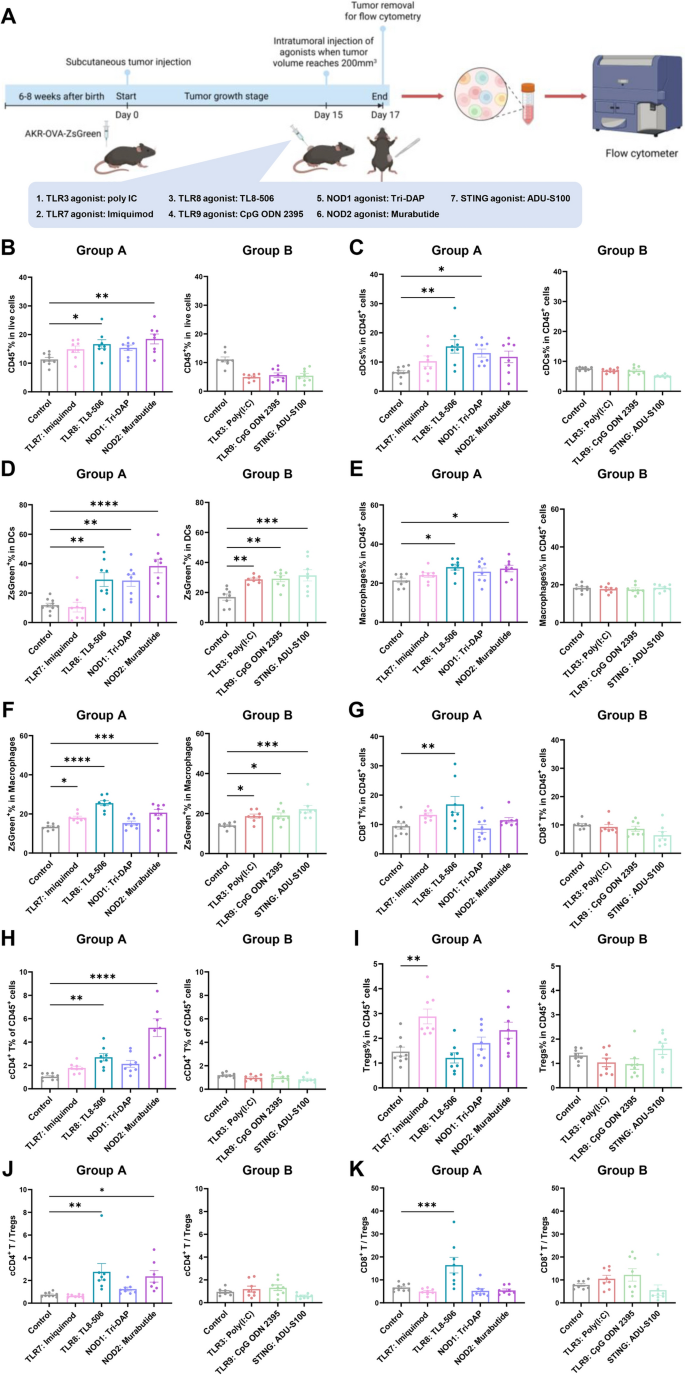
产品关联:实验所用关键产品:TLR3激动剂poly(I:C)(Sigma-Aldrich,#42424–50-0)、TLR7激动剂咪喹莫特盐酸盐(MedChemExpress,#HY-B0180A)、TLR8激动剂TL8-506(InvivoGen,#tlrl-tl8506)、TLR9激动剂CpG ODN 2395(InvivoGen,#tlrl-2395–1)、STING激动剂ADU-S100铵盐(MedChemExpress,#HY-12885B)、NOD1激动剂Tri-DAP(InvivoGen,#tlrl-tdap)、NOD2激动剂murabutide(InvivoGen,#tlrl-mbt),流式细胞术抗体来自eBioscience、BioLegend、BD Biosciences等品牌。
3.2 TLR8激动剂抗肿瘤活性的跨模型验证
实验目的:验证TLR8激动剂的抗肿瘤活性是否依赖适应性免疫,明确其对先天与适应性免疫的调控作用。方法细节:选用两种TLR8激动剂(TL8-506与临床阶段的motolimod),在免疫健全的C57BL/6小鼠与T细胞缺陷的裸鼠中构建AKR食管癌细胞与MC38结肠癌细胞肿瘤模型,瘤内注射激动剂,每3天一次,监测肿瘤生长与小鼠体重,通过流式细胞术分析TIME免疫细胞亚群,体外实验检测巨噬细胞对CFSE标记肿瘤细胞的吞噬能力。结果解读:两种TLR8激动剂在免疫健全小鼠中均显著抑制AKR与MC38肿瘤生长(n=5,P<0.001至P<0.0001),且不影响小鼠体重;在裸鼠中,TLR8激动剂仍可抑制肿瘤生长,但效果弱于免疫健全小鼠,表明其抗肿瘤活性依赖先天与适应性免疫的协同作用;流式细胞术结果显示,TLR8激动剂显著增加MC38肿瘤中CD45+白细胞比例,提升cDC与巨噬细胞的比例及抗原吞噬能力,上调CD8+T与cCD4+T细胞比例,降低Treg细胞比例,提升效应T细胞/Treg比值(n=6,P<0.05至P<0.0001);体外实验中,motolimod显著促进小鼠巨噬细胞与人THP-1来源巨噬细胞对CFSE标记肿瘤细胞的吞噬能力(n=5,P<0.01至P<0.0001)。
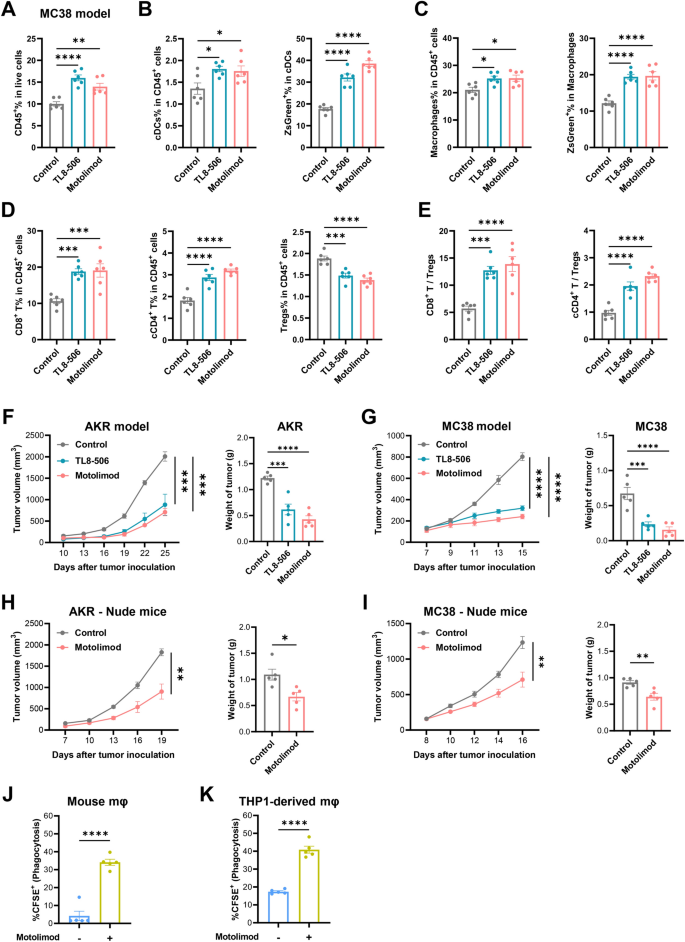
产品关联:实验所用关键产品:TLR8激动剂motolimod(MedChemExpress,#HY-13773),CFSE(Thermo Fisher,#C34554),抗PD-1抗体(Bio X Cell,clone RMP1-14)。
3.3 基于单细胞RNA测序的细胞互作与机制解析
实验目的:解析TLR8激动剂调控TIME的细胞间信号通路,识别关键下游效应分子。方法细节:对AKR肿瘤模型中motolimod处理组与对照组的肿瘤浸润免疫细胞进行单细胞RNA测序(scRNA-seq),通过Seurat进行细胞聚类与注释,利用CellChat分析细胞间配体-受体互作网络,筛选TLR8激动剂调控的关键信号通路。结果解读:scRNA-seq共分析15745个细胞,注释出多种免疫细胞亚群;TLR8(Tlr8)mRNA主要表达在CD8+T细胞、cDC2、巨噬细胞与中性粒细胞中,这些细胞是TLR8激动剂的直接响应细胞;motolimod处理后,这些细胞的促炎细胞因子(Il1b、Tnf、Ifng)、杀肿瘤分子(Nos2、Camp、Lyz2)、细胞毒性蛋白(Gzmb)表达显著上调,免疫抑制因子(Il10、Tgfb1、Pdcd1)表达下调;CellChat分析显示,TLR8激动剂显著激活了巨噬细胞、cDC2、CD8+T细胞与cCD4+T细胞之间的Pf4/Cxcl4-Cxcr3趋化通路,Pf4 mRNA在上述三种细胞中显著上调,cCD4+T细胞中Cxcr3表达显著增加(P<0.01),表明该通路是TLR8激动剂招募cCD4+T细胞的关键机制。
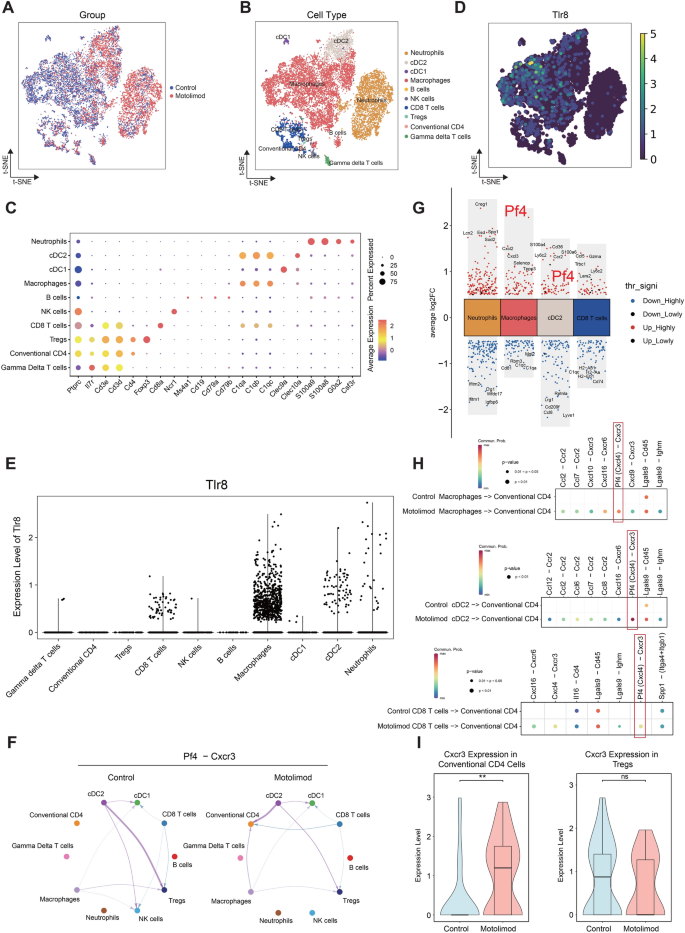
产品关联:实验所用关键产品:10× Genomics Chromium Single Cell 5′ Kit,测序平台Illumina NovaSeq 6000,生物信息学分析工具包括Seurat、CellChat、ggplot2等。
3.4 TLR8诱导PF4表达的信号通路验证
实验目的:验证TLR8激动剂是否通过NF-κB通路调控PF4的表达。方法细节:用motolimod处理小鼠腹腔巨噬细胞与人THP-1来源巨噬细胞,通过qRT-PCR检测Pf4/PF4 mRNA表达,双荧光素酶报告基因检测NF-κB通路激活;利用shRNA慢病毒敲低小鼠巨噬细胞的Rela与人巨噬细胞的RELA,检测motolimod处理后PF4的表达变化;通过Western blot检测NF-κB p65蛋白水平,ELISA检测细胞上清中PF4的分泌量。结果解读:motolimod处理显著上调小鼠与人巨噬细胞的Pf4/PF4 mRNA表达(n=3,P<0.001至P<0.0001),并激活NF-κB通路(n=3,P<0.01至P<0.0001);敲低Rela/RELA后,motolimod无法诱导Pf4/PF4的表达与分泌,Western blot结果显示敲低Rela/RELA显著降低了p65蛋白水平,表明TLR8通过NF-κB通路调控PF4的表达。
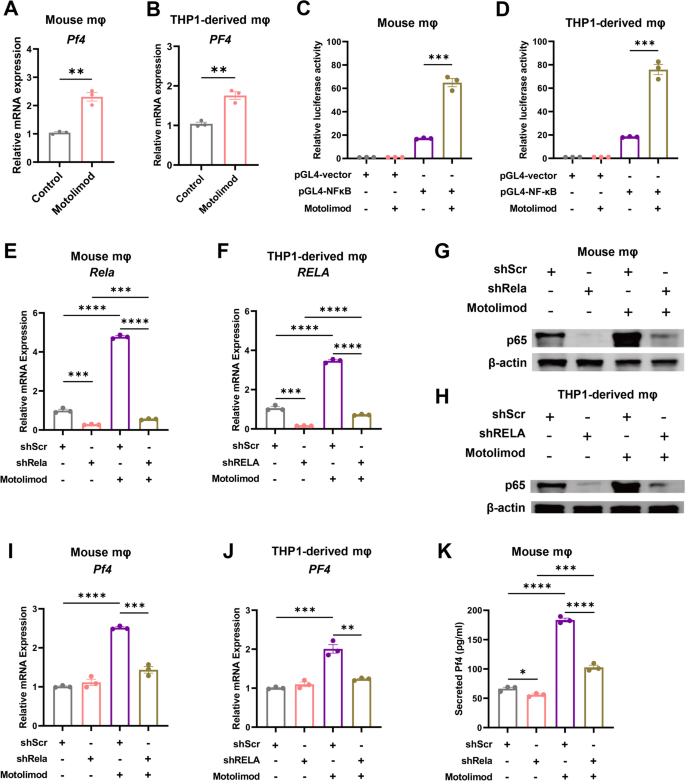
产品关联:实验所用关键产品:qRT-PCR试剂(Qiagen RNeasy Mini Kit、Takara PrimeScript RT Kit与TB Green Premix Ex Taq II),双荧光素酶报告基因试剂盒(Promega,#E1910),shRNA慢病毒(Genewiz),Western blot抗体(Cell Signaling Technology的NF-κB p65抗体、Proteintech的β-actin抗体),ELISA试剂盒(Elabscience Mouse PF4 ELISA Kit)。
3.5 PF4的功能验证与TLR8非依赖机制分析
实验目的:验证PF4在TLR8激动剂调控TIME中的关键作用,解析TLR8的PF4非依赖抗肿瘤机制。方法细节:构建稳定过表达Pf4的AKR与MC38细胞系,在C57BL/6小鼠中构建肿瘤模型,检测肿瘤生长与TIME免疫细胞亚群;通过Transwell迁移实验验证PF4对T细胞的招募作用;分析TLR8激动剂诱导的IFN-γ对Treg的调控作用。结果解读:PF4过表达显著抑制AKR与MC38肿瘤生长(n=6,P<0.01至P<0.0001),并增强motolimod的抗肿瘤效果;流式细胞术结果显示,PF4过表达增加肿瘤中CD45+、CD8+、cCD4+T细胞比例,提升cCD4+T/Treg与CD8+T/Treg比值(n=6,P<0.05至P<0.0001),但同时轻度增加Treg比例,而TLR8激动剂可降低Treg比例,提示TLR8存在PF4非依赖的Treg抑制机制;Transwell实验显示,motolimod处理的巨噬细胞可促进T细胞迁移,该作用可被抗PF4抗体阻断;结合scRNA-seq结果,TLR8激动剂诱导的IFN-γ可抑制Treg分化,是其PF4非依赖机制之一;免疫荧光染色结果显示,PF4过表达显著增加MC38肿瘤中CD8+T细胞浸润(n=6,P<0.0001)。
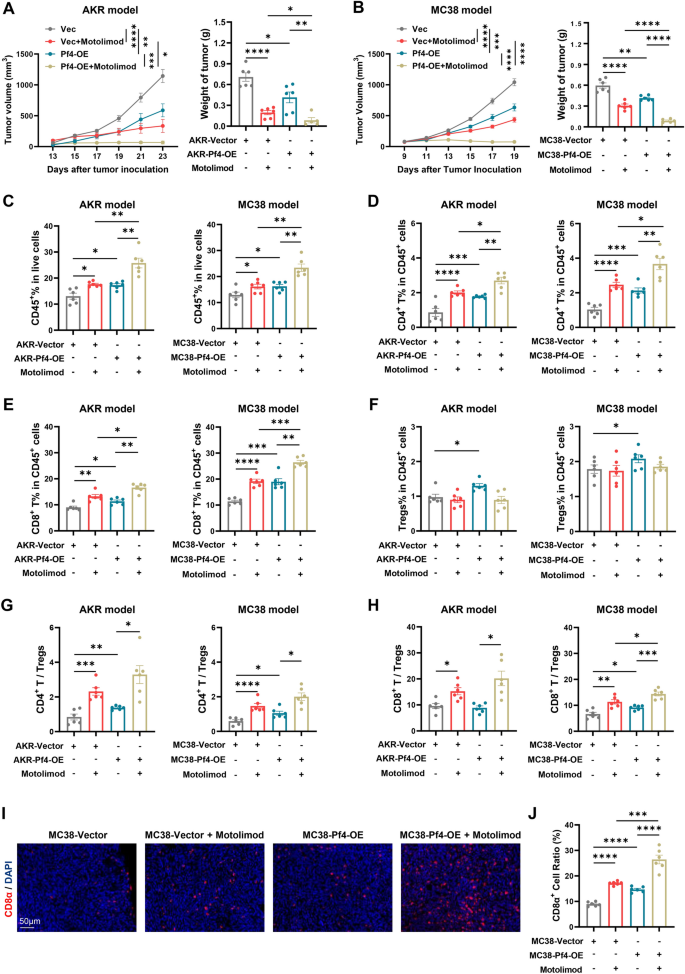
产品关联:实验所用关键产品:抗PF4抗体(R&D Systems,#AF595),Transwell小室(Corning,#3422),免疫荧光抗体(Cell Signaling Technology的CD8α抗体),DAPI(Sigma,#D8417)。
3.6 TLR8激动剂与抗PD-1的联合治疗验证
实验目的:验证TLR8激动剂与抗PD-1治疗的协同抗肿瘤效果。方法细节:在AKR与MC38肿瘤模型中,分别给予瘤内注射motolimod、腹腔注射抗PD-1抗体,或联合治疗,监测肿瘤生长与小鼠生存时间。结果解读:联合治疗显著抑制AKR与MC38肿瘤生长(n=7,P<0.0001),并显著延长小鼠生存时间(log-rank检验,P<0.0001),显示出显著的协同抗肿瘤作用,表明TLR8激动剂可重塑TIME,增强肿瘤对抗PD-1治疗的敏感性。
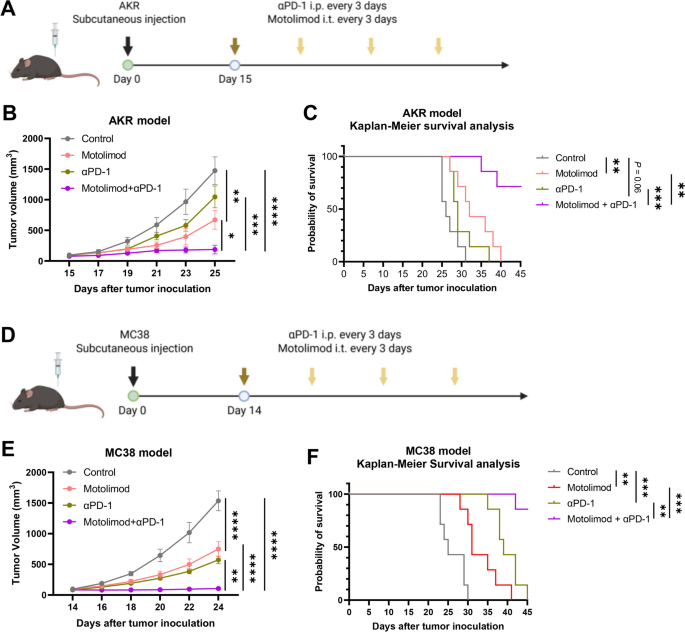
产品关联:实验所用关键产品:抗PD-1抗体(Bio X Cell,clone RMP1-14)。
4. Biomarker研究及发现成果解析
本研究识别出PF4作为TLR8激动剂调控TIME的关键功能性Biomarker,明确了其筛选与验证逻辑,系统解析了其在局部肿瘤微环境中的抗肿瘤功能与临床意义。
Biomarker定位:本研究中的Biomarker为血小板因子4(PF4/CXCL4),属于细胞因子/趋化因子类Biomarker。其筛选逻辑为:通过单细胞RNA-seq分析TLR8激动剂处理后肿瘤浸润免疫细胞的基因表达变化,结合CellChat细胞间配体-受体互作分析,筛选出显著激活的Pf4-Cxcr3通路;随后通过细胞水平、动物模型、临床数据库的多维度验证,明确了PF4作为TLR8下游关键效应分子的功能。
研究过程详述:PF4的来源为肿瘤浸润的巨噬细胞、cDC2与CD8+T细胞,在TLR8激动剂的诱导下分泌至局部肿瘤微环境。验证方法包括:细胞水平通过qRT-PCR、ELISA检测PF4的表达与分泌,Western blot与双荧光素酶报告基因验证TLR8-NF-κB-PF4的调控通路;动物模型通过构建PF4过表达肿瘤细胞系,检测其对肿瘤生长与TIME的调控作用,Transwell实验验证PF4对T细胞的招募作用;临床数据库通过Kaplan-Meier生存分析,验证PF4表达与患者生存的相关性。特异性与敏感性方面,临床数据库分析显示,PF4高表达与乳腺癌、结肠癌、肝癌患者的更好生存相关(文献未明确提供ROC曲线AUC、敏感性与特异性数据,基于图表趋势推测)。
核心成果提炼:该Biomarker的功能关联为:PF4通过与cCD4+T细胞表面的CXCR3结合,招募cCD4+T细胞浸润至肿瘤组织,同时促进CD8+T细胞浸润,提升效应T细胞/Treg比值,重塑促免疫原性TIME,发挥抗肿瘤作用;其创新性在于首次明确了PF4的上下文依赖功能,局部肿瘤微环境中诱导的PF4具有显著抗肿瘤作用,与系统表达时的促肿瘤作用形成鲜明对比,解决了PF4在肿瘤中功能矛盾的关键问题;统计学结果显示,PF4过表达显著抑制肿瘤生长(n=6,P<0.01至P<0.0001),提升CD8+T细胞浸润比例(n=6,P<0.0001),临床数据库中PF4高表达患者的生存时间显著长于低表达患者(log-rank检验,P<0.05,文献未明确具体HR值与置信区间)。