1. 领域背景与文献引入
文献英文标题:Development of TAP, a non-invasive test for qualitative and quantitative measurements of biomarkers from the skin surface;发表期刊:Biomarker Research;影响因子:未公开;研究领域:皮肤生物标志物非侵入性检测。
皮肤是人体最大的器官,由角质形成细胞、成纤维细胞、免疫细胞等多种细胞组成,可分泌细胞因子(如IL-1α、IL-1RA)、抗菌肽(如hBD-1)、趋化因子(如CXCL-1/2)等生物标志物,这些标志物能反映皮肤屏障功能、炎症状态及疾病进展(如银屑病、特应性皮炎)。传统皮肤生物标志物检测主要依赖侵入性活检,虽准确但患者依从性差;近年发展的非侵入性方法(如皮肤灌洗、胶带剥离)虽避免了创伤,但存在灵敏度低(皮肤灌洗需大量缓冲液稀释标志物)、操作复杂(胶带剥离需结合质谱)等局限。因此,开发非侵入、高灵敏度、定量的皮肤生物标志物检测工具成为领域未解决的核心问题。本研究针对这一需求,设计了Transdermal Analyses Patch(TAP)——一种基于抗体微阵列的非侵入性贴片,旨在实现皮肤表面生物标志物的定性与定量检测。
2. 文献综述解析
作者对现有非侵入性皮肤生物标志物检测方法的分类逻辑为“提取方式-技术原理-性能局限”:
1. 皮肤灌洗法:通过硅环固定在皮肤表面,用PBS提取标志物,优势是能检测亲水 cytokines(如IL-1α、TNF-α),但需大量缓冲液(导致标志物浓度低),灵敏度有限;
2. 胶带剥离法:用D-Squame胶带收集角质细胞,结合质谱分析,优势是能检测角质细胞 turnover 相关蛋白,但操作繁琐、定量困难。
作者指出,现有方法的核心局限是“灵敏度与操作简便性难以兼顾”。本研究的创新点在于:① 采用抗体微阵列直接从皮肤表面捕获标志物,避免缓冲液稀释,提高灵敏度;② 设计一体化贴片结构(粘性 plaster+膨胀层+抗体微阵列),操作简便(仅需贴敷皮肤20-30分钟),且能确保微阵列与皮肤紧密接触;③ 结合spot-ELISA定量检测,兼容临床常规实验室流程。
3. 研究思路总结与详细解析
本研究的整体思路为“TAP结构设计→抗体微阵列优化→检测 protocol 优化→人体皮肤验证→重复性与对比实验”,形成“设计-优化-验证”的闭环逻辑。
3.1 TAP结构设计与功能验证
实验目的:设计非侵入、易操作且能稳定捕获皮肤生物标志物的贴片结构。
方法细节:TAP由三部分组成(图1):① 粘性 plaster(固定贴片);② 硝酸纤维素核心(负载捕获抗体微阵列,清晰可见于贴片中央);③ 中间膨胀层(接触液体后膨胀,用于储存提取缓冲液并确保微阵列与皮肤紧密接触)。通过人体皮肤贴敷试验验证结构稳定性与皮肤相容性。
结果解读:TAP能稳定固定在皮肤表面(图1B下),膨胀层接触缓冲液后膨胀(图1B上),确保微阵列与皮肤紧密接触;贴敷后无皮肤发红、瘙痒等刺激反应,证明其安全性。
产品关联:实验所用硝酸纤维素膜为Whatman Protran BA 85(0.45μm孔隙);粘性 plaster 为定制医用级材料(文献未提及具体品牌)。

3.2 捕获抗体微阵列的制备优化
实验目的:优化微阵列的稳定性(抗体 retention)与重复性( spot 间变异)。
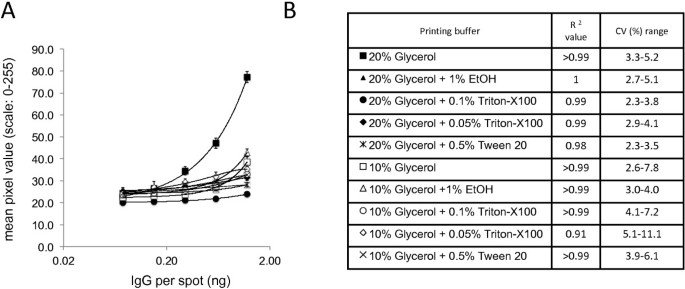
方法细节:① 测试打印缓冲液:用不同配方(PBS+10%/20%甘油,加0.1% Triton X-100、0.5% Tween-20等添加剂)打印人IgG(0.075-1.2ng/spot),用spot-ELISA检测信号强度与变异系数(CV);② 测试硝酸纤维素膜:对比Whatman Protran BA 85(0.1/0.2/0.45μm孔隙)与Amersham Hybond C-Extra(0.45μm)的打印效果。
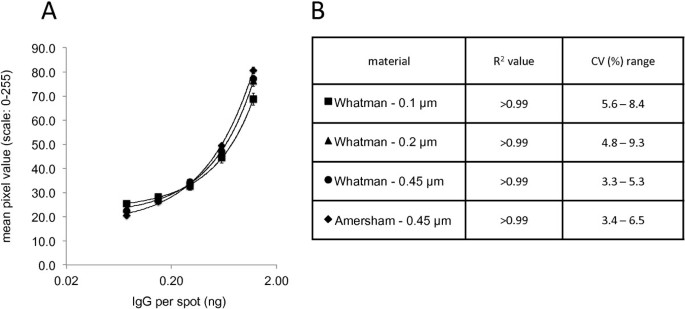
结果解读:① 打印缓冲液中,PBS+20%甘油的信号强度最高(图2A),且CV<10%(图2B);② 硝酸纤维素膜中,Whatman Protran BA 85(0.45μm)的CV最低(3.3%-5.3%,图3B),且信号与打印量的相关性最好(R²>0.99,图3A)。因此选择该组合制备微阵列。
产品关联:实验所用打印机为BioDot AD3400(非接触式 dispenser);硝酸纤维素膜为Whatman Protran BA 85。
3.3 蛋白捕获与检测 protocol 优化
实验目的:优化TAP的检测灵敏度与动态范围。
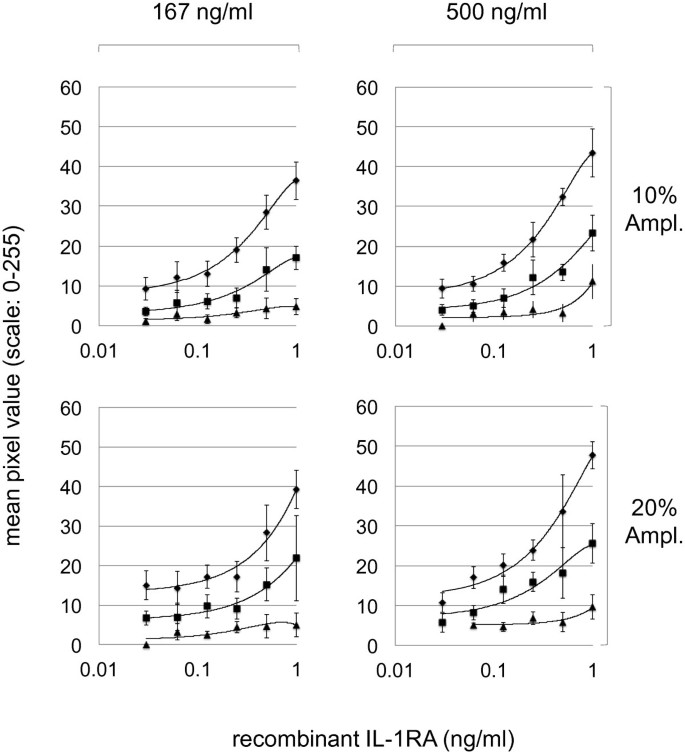
方法细节:选择IL-1α、IL-1RA、CXCL-1/2、hBD-1(文献报道的皮肤相关生物标志物)作为模型分析物,测试:① 捕获抗体量(0.75/1.5/2.25ng/spot);② 检测抗体浓度(500/166.67ng/ml);③ 信号放大试剂(Dako CSA系统,10%/20%稀释)对检测性能的影响。
结果解读:2.25ng/spot捕获抗体+166.67ng/ml检测抗体+10% CSA试剂的组合性能最优:以IL-1RA为例,标准曲线的R²>0.99(图4),动态范围覆盖0.1-10ng/ml(符合皮肤表面标志物的生理浓度)。
产品关联:实验所用检测抗体来自PeproTech ELISA开发试剂盒(如IL-1RA试剂盒Cat.No:900-K474);信号放大系统为Dako Catalysed Signal Amplification(CSA)System(K-1500)。
3.4 人体皮肤生物标志物检测验证
实验目的:验证TAP对健康人皮肤表面生物标志物的捕获能力。
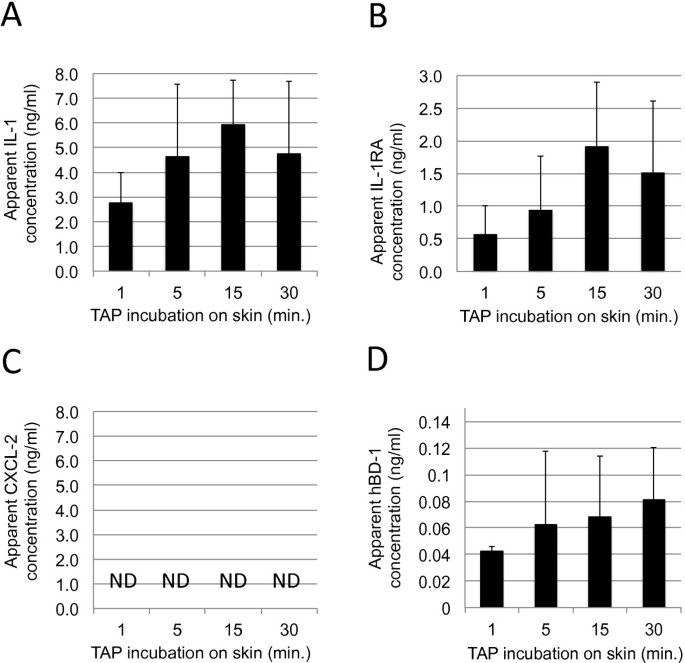
方法细节:招募3名健康志愿者,在小臂内侧皮肤贴敷TAP 1、5、15、30分钟,用spot-ELISA检测IL-1α、IL-1RA、hBD-1、CXCL-1/2的浓度(通过标准曲线定量)。
结果解读:① IL-1α、IL-1RA、hBD-1能被有效检测(图5A、B、D),CXCL-1/2未检测到(正常皮肤表达极低);② 15分钟孵育的信号强度最高(但5、15、30分钟无统计学差异),因此选择20-30分钟作为最优孵育时间。
产品关联:实验所用提取缓冲液为PBS+0.05% Tween-20+1% BSA(领域常规试剂)。
3.5 TAP检测重复性验证
实验目的:验证TAP检测的日内与部位间重复性。
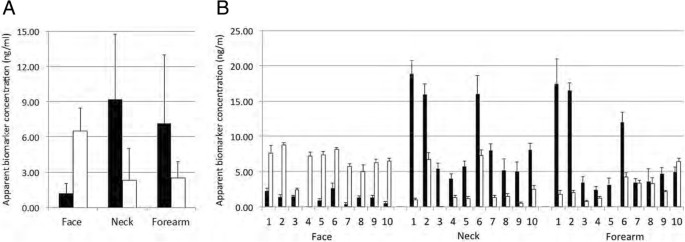
方法细节:招募10名健康志愿者,连续5天在面部(脸颊)、颈部(锁骨)、小臂内侧贴敷TAP 20分钟,检测IL-1α与IL-1RA的浓度。
结果解读:① 日内重复性:IL-1α的CV为21.1%,IL-1RA为18.4%(图6B),远低于领域可接受的CV阈值(<30%);② 部位间差异:面部皮肤的IL-1RA浓度显著高于小臂内侧(图6A),符合文献报道的“日光暴露皮肤IL-1RA表达更高”的结论。
产品关联:实验所用TAP微阵列的捕获抗体量为IL-1α 0.3ng/spot、IL-1RA 1.125ng/spot(优化后参数)。
3.6 与皮肤灌洗法的 benchmark 对比
实验目的:验证TAP的灵敏度优于现有皮肤灌洗法。
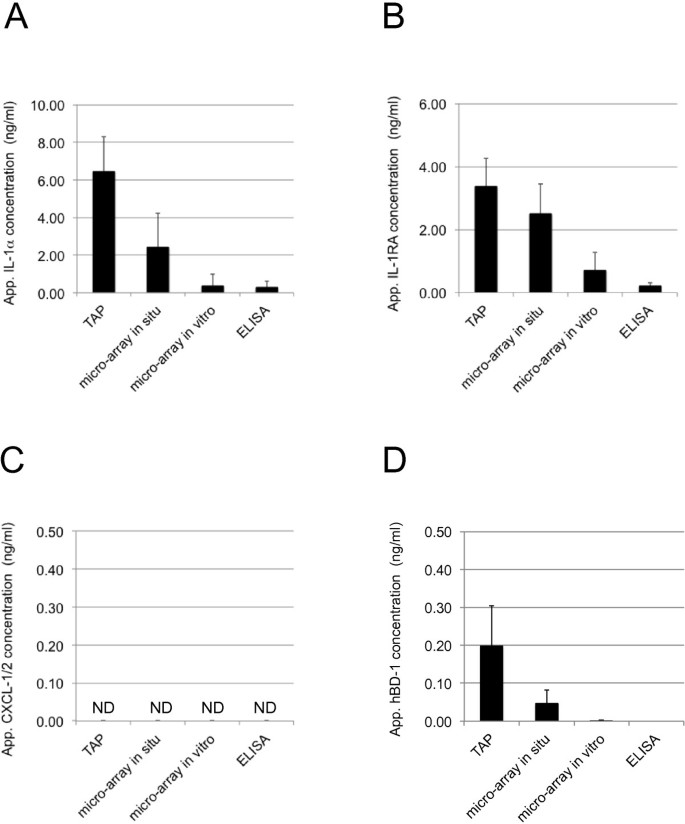
方法细节:招募10名健康志愿者,同时用TAP与三种皮肤灌洗法(① 硅环灌洗+ELISA;② 灌洗液加TAP;③ 原位TAP)检测IL-1α、IL-1RA、hBD-1、CXCL-1/2。
结果解读:TAP的灵敏度显著高于皮肤灌洗法:IL-1α的检测浓度是皮肤灌洗的20倍(图7A),IL-1RA是15倍(图7B);hBD-1的检测信号也更强(图7D);CXCL-1/2均未检测到(正常皮肤表达低)。
产品关联:实验所用硅环为Greiner Bio-One产品,ELISA板为Greiner BioOne高结合板。
4. Biomarker 研究及发现成果解析
4.1 Biomarker 定位与筛选逻辑
本研究涉及的Biomarker为皮肤分泌型蛋白:IL-1α(炎症反应标志物)、IL-1RA(IL-1α的拮抗因子,皮肤屏障功能标志物)、hBD-1(抗菌肽,皮肤免疫标志物)、CXCL-1/2(趋化因子, neutrophil 招募标志物)。
筛选逻辑:基于文献报道——这些标志物在皮肤炎症(如银屑病)、屏障损伤(如紫外线照射)中存在表达差异;验证逻辑:“体外优化→人体皮肤验证→重复性→对比实验”,确保标志物检测的可靠性。
4.2 研究过程详述
- Biomarker 来源:健康志愿者皮肤表面(小臂内侧、面部、颈部);
- 验证方法:spot-ELISA(斑点酶联免疫吸附试验)——通过捕获抗体微阵列捕获标志物,生物素化检测抗体结合,CSA系统信号放大,最后用底物显色定量;
- 特异性与敏感性:① 特异性:实验验证无交叉反应(如抗IL-1RA抗体不结合IL-1α);② 敏感性:TAP对IL-1α的检测限为0.1ng/ml(皮肤灌洗法为2ng/ml),灵敏度高20倍;对IL-1RA的检测限为0.075ng/ml(皮肤灌洗法为1.125ng/ml),灵敏度高15倍(图7)。
4.3 核心成果提炼
- 功能关联:TAP检测的IL-1α/IL-1RA比值能反映皮肤部位差异(面部IL-1RA更高),与文献报道一致;
- 创新性:首次用抗体微阵列+一体化贴片实现皮肤表面生物标志物的非侵入定量检测,解决了现有方法“灵敏度低、操作复杂”的问题;
- 临床价值:TAP检测的重复性好(CV<22%)、无皮肤刺激,可用于临床皮肤疾病(如银屑病、特应性皮炎)的 biomarker 监测。
本研究通过系统优化TAP的结构与检测 protocol,验证了其作为非侵入性皮肤生物标志物检测工具的可行性,为皮肤疾病的精准诊断与治疗监测提供了新的技术范式。
