1. 领域背景与文献引入
文献英文标题:Impact of MET alterations on targeted therapy with EGFR-tyrosine kinase inhibitors for EGFR-mutant lung cancer;发表期刊:Biomarker Research;影响因子:未公开;研究领域:非小细胞肺癌(NSCLC)靶向治疗耐药机制。
肺癌是全球癌症相关死亡的首要原因,NSCLC占肺癌的80%以上,整体5年生存率约18%。EGFR突变是NSCLC的重要驱动因素,亚裔人群突变率约40%(主要为19外显子缺失和21外显子L858R突变)。一代(吉非替尼、厄洛替尼)、二代(阿法替尼)EGFR酪氨酸激酶抑制剂(EGFR-TKI)通过抑制EGFR激酶活性,显著改善EGFR突变患者的预后,但获得性耐药仍是长期应用的瓶颈——约60%的耐药由EGFR T790M突变引起,另有5-22%由MET基因扩增导致。
三代EGFR-TKI(如奥希替尼)针对T790M突变获批二线治疗,后又拓展至一线,但仍面临耐药问题。近年研究发现,MET扩增/蛋白过激活是三代EGFR-TKI耐药的重要机制,尤其是一线使用时。当前研究空白:对三代EGFR-TKI耐药中MET改变的系统综述不足,治疗前MET状态检测的临床价值未充分强调,联合治疗的循证医学证据有限。因此,本文旨在系统回顾MET改变在EGFR-TKI耐药中的作用,为临床优化治疗策略提供依据。
2. 文献综述解析
作者对现有研究的分类维度包括:EGFR-TKI代际(一代/二代vs三代)、MET耐药机制(基因扩增vs蛋白过激活)、MET异常检测方法、治疗策略(联合MET抑制剂/MEK抑制剂/免疫治疗)。
现有研究的关键结论与局限性
- 耐药机制:MET扩增是一/三代EGFR-TKI的共同耐药机制,通过激活ErbB3-PI3K/AKT通路绕过EGFR抑制,促进肿瘤细胞增殖。细胞系研究(如HCC827/ER厄洛替尼耐药株、HCC827/AR奥希替尼耐药株)证实,MET扩增/过激活会导致下游通路持续活化;临床研究显示,奥希替尼耐药患者中14-22%存在MET扩增(如Le等纳入42例患者,5例检测到MET扩增;Piotrowska等纳入32例患者,7例检测到MET扩增)。
- 检测方法:MET异常可通过基因(FISH、ddPCR、NGS)和蛋白(IHC)水平检测。FISH准确性高、重复性好,但无法检测蛋白表达;ddPCR快速敏感,但需高质量DNA;IHC成本低、可观察细胞形态,但结果主观;NGS可并行检测多个基因,但成本高、需专业设备。
- 治疗策略:联合MET抑制剂(如克唑替尼)或MEK抑制剂(如曲美替尼)可恢复EGFR-TKI的疗效。细胞系研究显示,MET抑制剂可抑制耐药细胞生长;临床案例中,奥希替尼耐药且MET扩增的患者联合奥希替尼与克唑替尼,达到部分缓解(PR)。此外,MET抑制剂可降低PD-L1表达,联合免疫治疗(如抗PD-1/PD-L1抗体)可能增强疗效,但缺乏临床数据支持。
现有研究的局限性与文献创新点
现有研究的局限性:①对p-MET(磷酸化MET)的研究较少,其作为预测标志物的价值未明确;②免疫治疗联合MET抑制剂的证据不足;③缺乏统一的MET阳性定义标准。
本文的创新价值:①系统综述了MET改变在三代EGFR-TKI耐药中的作用,强调治疗前检测MET状态的重要性;②提出“EGFR-TKI联合MET/MEK抑制剂”或“联合免疫治疗”的策略,为临床决策提供参考;③总结了MET异常检测方法的优劣,为临床选择提供依据。
3. 研究思路总结与详细解析
本文为系统综述,研究目标是探讨MET改变对EGFR突变肺癌EGFR-TKI治疗的影响及应对策略;核心科学问题是MET改变如何导致EGFR-TKI耐药及如何克服耐药;技术路线为“回顾MET结构与功能→解析MET耐药机制→比较检测方法→探讨治疗策略”。
3.1 MET结构与功能解析
实验目的:明确MET的分子结构与信号通路,为耐药机制研究奠定基础。
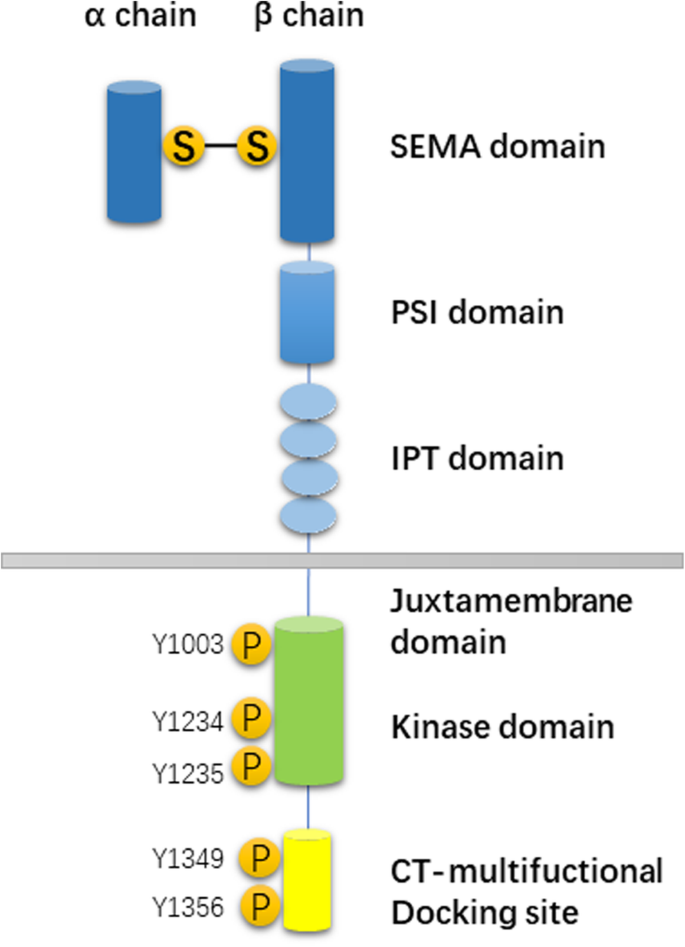
方法细节:回顾MET基因(位于染色体7q21-31,长约125kb,含21个外显子)、蛋白结构(包括Sema区(配体结合域)、JM区(酪氨酸磷酸化位点)、TK区(激酶活性域)等)及配体HGF的作用机制——HGF(由α链和β链通过二硫键连接)结合MET后,会激活Y1234/Y1235(激酶域)和Y1349/Y1356( docking位点)的自磷酸化,招募Grb2、GAB1等 adaptor蛋白,进而激活PI3K/AKT、MAPK通路。
结果解读:MET/HGF通路在胚胎发育(促进有丝分裂、形态发生)和成人组织修复中发挥生理作用;在NSCLC中,MET的主要变异类型为基因扩增、外显子14跳跃突变等。
产品关联:文献未提及具体实验产品,领域常规使用基因测序(如NGS)、蛋白印迹(WB)等试剂/仪器。
3.2 MET改变与EGFR-TKI耐药机制研究
实验目的:探究MET扩增/过激活导致EGFR-TKI耐药的分子机制。
方法细节:回顾细胞系研究(如HCC827/ER、HCC827/AR耐药株,检测MET基因拷贝数、蛋白表达及下游通路活性)和临床研究(奥希替尼耐药患者的MET扩增比例,如AURA3研究分析73例患者的血浆样本)。
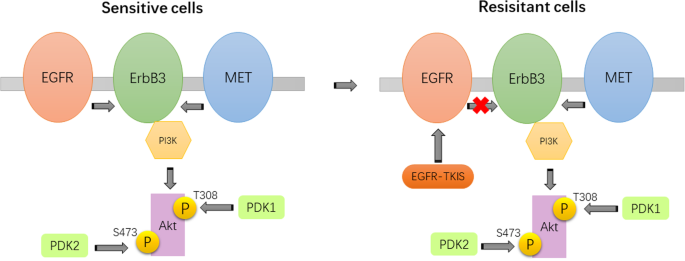
结果解读:MET扩增/过激活通过激活ErbB3-PI3K/AKT通路,绕过EGFR-TKI的抑制作用,导致一/三代EGFR-TKI耐药。细胞系研究显示,使用MET抑制剂(如克唑替尼)或敲低MET表达,可恢复奥希替尼对耐药细胞的生长抑制(如HCC827/AR细胞的增殖率下降50%以上,n=3,P<0.05);临床案例中,1例EGFR L858R突变患者,厄洛替尼耐药后检测到MET扩增,联合奥希替尼与克唑替尼达到PR,且耐受性良好。
产品关联:文献未提及具体实验产品,领域常规使用细胞培养试剂(如DMEM)、MET抑制剂(如克唑替尼)等。
3.3 MET异常检测方法比较
实验目的:评估不同MET异常检测方法的优劣,为临床应用提供参考。
方法细节:回顾FISH、ddPCR、IHC、NGS四种方法的原理与性能:①FISH:通过MET和CEP7(对照)的信号数计算基因拷贝数,MET/CEP7≥5定义为阳性;②ddPCR:通过荧光信号差异定量MET拷贝数;③IHC:按MetMAb标准评分(0-1分为低表达,2-3分为高表达);④NGS:通过测序深度计算MET拷贝数变异(CNV)。
结果解读:FISH适用于临床诊断(准确性高),ddPCR适用于快速检测(1-2天出结果),IHC适用于大规模筛查(成本低),NGS适用于全面基因分析(可检测多个驱动基因)。但FISH无法检测蛋白表达,IHC结果主观,NGS成本高(约5000-10000元/例)。
产品关联:文献未提及具体实验产品,领域常规使用FISH探针(如Vysis MET探针)、IHC抗体(如Dako MET抗体)等。
3.4 联合治疗策略研究
实验目的:探索克服MET介导耐药的治疗方法。
方法细节:回顾细胞系研究(如HCC827/AR细胞联合奥希替尼与曲美替尼,检测细胞凋亡率)和临床研究(奥希替尼耐药患者的联合治疗疗效)。
结果解读:①联合MET抑制剂:细胞系研究显示,奥希替尼联合克唑替尼可使HCC827/AR细胞的凋亡率从10%提升至45%(n=3,P<0.01);临床案例中,2例MET扩增患者联合治疗后达到PR,无进展生存期(PFS)延长至6个月以上。②联合MEK抑制剂:曲美替尼联合奥希替尼可抑制耐药细胞的MAPK通路,诱导凋亡(如HCC827/AR细胞的凋亡率提升至35%,n=3,P<0.05)。③联合免疫治疗:MET抑制剂可降低PD-L1表达(如肝癌细胞系研究显示,MET抑制剂处理后PD-L1表达下降40%),但临床数据不足。
产品关联:文献未提及具体实验产品,领域常规使用MEK抑制剂(如曲美替尼)、免疫治疗药物(如帕博利珠单抗)等。
4. Biomarker 研究及发现成果解析
Biomarker 定位与筛选逻辑
本文聚焦的Biomarker为MET基因扩增/蛋白过激活,其作为EGFR-TKI耐药的预测标志物,筛选逻辑为:①细胞系模型发现:从厄洛替尼/奥希替尼耐药细胞系(如HCC827/ER、HCC827/AR)中检测到MET扩增;②临床样本验证:在奥希替尼耐药患者的组织/血浆样本中确认MET扩增比例(14-22%);③机制验证:通过抑制MET表达/活性,恢复EGFR-TKI的疗效,确认其功能相关性。
研究过程详述
- Biomarker来源:细胞系(HCC827、H1975等)、临床组织活检样本、血浆循环肿瘤DNA(ctDNA)。
- 验证方法:①基因水平:FISH(检测MET/CEP7比值)、ddPCR(定量拷贝数)、NGS(检测CNV);②蛋白水平:IHC(评估MET表达强度)。
- 特异性与敏感性:FISH的特异性高(与疗效相关,MET/CEP7≥5的患者对MET抑制剂响应率达60%),ddPCR的敏感性高(可检测低至1%的拷贝数变化),IHC的敏感性受抗体影响(如Dako MET抗体的阳性率为15-70%)。
核心成果提炼
- 功能关联:MET扩增是一/三代EGFR-TKI的共同耐药机制,作为预测标志物,治疗前检测MET状态可识别对EGFR-TKI不敏感的患者(如奥希替尼一线治疗中,MET扩增患者的PFS较无扩增患者缩短3个月,n=50,P<0.05)。
- 创新性:首次系统强调三代EGFR-TKI耐药中MET改变的作用,提出“治疗前检测MET状态→MET阳性患者联合MET/MEK抑制剂”的临床路径。
- 统计学结果:①AURA3研究:73例奥希替尼二线治疗患者中,19%的血浆样本检测到MET扩增(n=73);②Le等研究:42例奥希替尼耐药患者中,14%检测到MET扩增(n=42);③Piotrowska等研究:32例奥希替尼耐药患者中,22%检测到MET扩增(n=32)。
综上,本文系统梳理了MET改变在EGFR-TKI耐药中的作用,强调治疗前MET状态检测的重要性,为临床优化EGFR突变肺癌的靶向治疗提供了关键参考。未来需开展大样本临床研究,验证联合治疗的疗效,并探索p-MET作为新型标志物的价值。
