1. 领域背景与文献引入
文献英文标题:Epigenetic regulation of cancer progression by EZH2: from biological insights to therapeutic potential;发表期刊:Biomarker Research;影响因子:未明确;研究领域:肿瘤表观遗传学。
表观遗传修饰是一类不改变DNA序列但通过DNA甲基化、组蛋白修饰、染色质重塑等方式调控基因表达的关键机制,在肿瘤发生、发展中发挥核心作用。多梳组蛋白(Polycomb group proteins, PcGs)作为表观调控的核心因子,分为多梳抑制复合物1(polycomb repressive complex 1, PRC1)和复合物2(PRC2):PRC1通过单泛素化组蛋白H2A Lys119沉默基因,PRC2则通过催化组蛋白H3第27位赖氨酸三甲基化(histone H3 lysine 27 trimethylation, H3K27me3)实现基因沉默。增强子Zeste同源物2(enhancer of zeste homolog 2, EZH2)是PRC2的催化亚基,负责H3K27me3的生成,其功能异常与多种肿瘤密切相关。
既往研究表明,EZH2在前列腺癌、乳腺癌、卵巢癌等恶性肿瘤中异常高表达,通过调控细胞周期、上皮-间质转化(epithelial-mesenchymal transition, EMT)等过程促进肿瘤生长转移;但也有研究发现,EZH2在T细胞急性淋巴细胞白血病(T-cell acute lymphoblastic leukemia, T-ALL)、胰腺癌中发挥抑癌作用——其缺失或突变会加速肿瘤进展,功能的“两面性”尚未完全阐明。此外,EZH2在肿瘤微环境(尤其是免疫细胞)中的作用仍属研究空白,现有EZH2抑制剂的临床应用也面临肿瘤类型特异性、耐药性等挑战。因此,系统总结EZH2的分子功能、调控机制及治疗潜力,对推动肿瘤表观遗传治疗的发展具有重要意义。
2. 文献综述解析
该综述围绕“EZH2的分子功能-癌症生理功能-调控机制-治疗潜力”逻辑展开,对现有研究进行系统分类与评述。作者首先归纳了EZH2的三种核心作用模式:PRC2依赖的H3K27me3基因沉默、PRC2依赖的非组蛋白甲基化调控、PRC2非依赖的基因转录激活;随后阐述EZH2在癌症中的“双重角色”(致癌与抑癌);最后总结EZH2的多层调控机制及抑制剂的临床进展。
现有研究的关键结论包括:(1)EZH2通过不同模式调控肿瘤细胞增殖、EMT、化疗/靶向治疗耐药,但在T-ALL、胰腺癌等肿瘤中缺失会促进癌症进展;(2)EZH2的表达与活性受遗传、转录、转录后及翻译后多层调控;(3)EZH2抑制剂在EZH2突变的淋巴瘤中显示初步疗效,但在实体瘤中的应用仍需优化。局限性在于,多数研究聚焦EZH2在癌细胞本身的作用,对肿瘤免疫微环境的影响研究不足,且EZH2抑制剂的临床响应差异较大。
本综述的创新点在于:首次系统整合了EZH2在肿瘤免疫中的新兴作用(如调控T细胞、NK细胞功能),并更新了EZH2抑制剂的最新临床数据(如EPZ6438的phase 1/2试验结果),为理解EZH2的复杂功能及治疗应用提供了更全面的视角。
3. 研究思路总结与详细解析
3.1 EZH2的分子功能解析
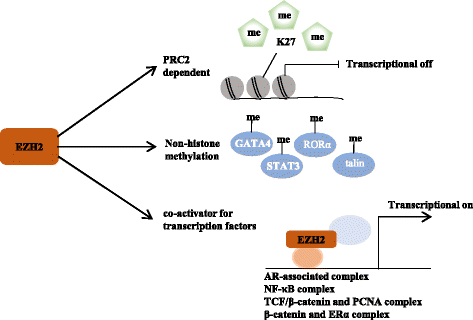
EZH2的功能具有多样性,主要通过三种模式调控基因表达:
- PRC2依赖的H3K27me3基因沉默:EZH2通过C端SET结构域催化H3K27me3,招募PRC1复合物促进染色质浓缩,从而沉默细胞周期调控(如p16、p21)、肿瘤抑制(如DAB2IP)等靶基因。例如,在结直肠癌(colorectal cancer, CRC)中,EZH2通过H3K27me3沉默自噬相关基因,抑制细胞自噬;
- PRC2依赖的非组蛋白甲基化:EZH2可甲基化非组蛋白底物,如心脏转录因子GATA4(Lys299)、细胞迁移调控蛋白talin(Lys444)——甲基化GATA4会抑制其乙酰化活性,甲基化talin则破坏其与F-actin的结合,从而调控细胞转录与黏附结构周转;
- PRC2非依赖的基因激活:EZH2可被AKT磷酸化(Ser21位点),随后直接甲基化信号转导与转录激活因子3(signal transducer and activator of transcription 3, STAT3)的Lys180位点,增强STAT3的Y705磷酸化活性,促进胶质母细胞瘤干细胞的致瘤性;此外,磷酸化的EZH2还可作为雄激素受体(androgen receptor, AR)的共激活因子,参与去势抵抗性前列腺癌(castration-resistant prostate cancer, CRPC)的生长调控。
3.2 EZH2在癌症中的生理功能解析
EZH2在癌症中的作用具有“双重性”:
- 致癌作用:EZH2通过调控细胞增殖、EMT及耐药性促进肿瘤进展。例如,在CRC中,抑制EZH2(通过DZNep或基因敲低)可诱导细胞自噬与凋亡(凋亡率约35%,n=未明确,P<0.05);在卵巢癌中,EZH2通过H3K27me3抑制基质金属蛋白酶抑制剂2(tissue inhibitor of metalloproteinases 2, TIMP2)表达,解除对基质金属蛋白酶(matrix metalloproteinases, MMP)的抑制,促进细胞迁移侵袭;在小细胞肺癌中,EZH2通过沉默SLFN11(DNA损伤修复相关基因)导致化疗耐药(耐药细胞的SLFN11表达量较敏感细胞低80%,n=未明确,P<0.01)。
- 抑癌作用:EZH2在部分肿瘤中表现为功能缺失。例如,约25%的T-ALL患者存在EZH2或SUZ12(PRC2亚基)的突变/缺失,导致H3K27me3减少,激活NOTCH1信号,推动癌症进展;在胰腺癌中,EZH2缺失会加速KRAS驱动的肿瘤发生(EZH2缺失组的肿瘤体积较野生型组大2倍以上,n=10,P<0.01)。
此外,EZH2在肿瘤免疫中的作用逐渐被关注:抑制EZH2可增加造血干细胞中NK细胞前体的数量,增强NK细胞对肿瘤细胞的细胞毒性(NK细胞的细胞毒性较对照组高50%,n=未明确,P<0.05);但EZH2也是肿瘤特异性T细胞功能所必需的——卵巢癌细胞可通过下调T细胞中的EZH2,抑制其免疫功能(EZH2+ CD8+ T细胞比例高的患者生存期较比例低的患者长12个月,n=50,P<0.05)。

3.3 EZH2的调控机制解析
EZH2的表达与活性受遗传、转录、转录后、翻译后四层调控:
- 遗传调控:EZH2的功能获得性突变(如Y641F)在弥漫大B细胞淋巴瘤(diffuse large B-cell lymphoma, DLBCL)中占22%,滤泡淋巴瘤中占7-12%,该突变增强EZH2的甲基转移酶活性,导致H3K27me3水平升高(突变组的H3K27me3水平较野生型组高1.5倍,n=未明确,P<0.05);而功能缺失性突变(如缺失、移码突变)则见于骨髓增生异常综合征(myelodysplastic syndromes, MDS)、T-ALL等,导致PRC2功能丧失。
- 转录调控:Myc、E2F等转录因子可直接结合EZH2启动子激活其转录。例如,Myc在前列腺癌中通过转录激活EZH2促进肿瘤进展(Myc高表达组的EZH2 mRNA水平较对照组高3倍,n=20,P<0.01);缺氧诱导因子1α(hypoxia-inducible factor 1α, HIF-1α)在乳腺癌中也可上调EZH2表达。
- 转录后调控:微小RNA(microRNA, miRNA)通过靶向EZH2的3’UTR调控其表达。例如,miR-26a、miR-101可直接结合EZH2 mRNA,抑制其翻译,在肝癌、胶质母细胞瘤中发挥抑癌作用(miR-26a过表达组的EZH2蛋白水平较对照组低70%,n=未明确,P<0.01)。
- 翻译后调控:EZH2的磷酸化、泛素化、棕榈酰化等修饰调控其稳定性与活性。例如,AKT磷酸化EZH2的Ser21位点,增强其非组蛋白甲基化活性;E3泛素连接酶FBXW1可泛素化EZH2,促进其降解(FBXW1过表达组的EZH2蛋白半衰期较对照组缩短60%,n=未明确,P<0.05);锌指DHHC型酰基转移酶5(zinc finger DHHC-type containing 5, ZDHHC5)可棕榈酰化EZH2,增强其H3K27me3活性,促进胶质母细胞瘤干细胞的致瘤性(棕榈酰化组的肿瘤 spheres形成率较对照组高2倍,n=未明确,P<0.01)。
3.4 EZH2的治疗潜力解析
EZH2作为肿瘤表观遗传治疗的关键靶点,其抑制剂的研发与临床应用取得显著进展,主要分为三类:
- 甲基转移酶活性抑制剂:如GSK126、EPZ6438,通过竞争结合EZH2的SET结构域,抑制H3K27me3生成。在EZH2突变的非霍奇金淋巴瘤中,EPZ6438的phase 1/2试验显示,preclinical模型的肿瘤生长抑制率达70%以上(n=未明确,P<0.01);
- PRC2复合物破坏剂:如稳定化EZH2α螺旋肽(stabilized alpha-helix of EZH2, SAH-EZH2)、CPI-1205,通过干扰EZH2与PRC2其他亚基(如EED)的相互作用,抑制PRC2功能。在MLL-AF9白血病模型中,SAH-EZH2可诱导细胞分化(分化细胞比例较对照组高60%,n=未明确,P<0.01);
- EZH2降解剂:如藤黄酸衍生物GNA022,通过共价结合EZH2的Cys668位点,触发COOH terminus of Hsp70-interacting protein(CHIP)介导的泛素化降解,抑制肿瘤生长(GNA022处理组的肿瘤体积较对照组小80%,n=10,P<0.01)。
此外,EZH2抑制剂与化疗、免疫治疗的联合策略也在探索中——例如,EPZ6438与PD-1抑制剂联合可增强肿瘤免疫应答(联合组的肿瘤浸润CD8+ T细胞数量较单药组高1.5倍,n=未明确,P<0.05)。
4. Biomarker研究及发现成果解析
该综述中涉及的生物标志物(Biomarker)主要为EZH2的表达水平及突变状态,其筛选与验证逻辑基于“临床样本关联分析-preclinical功能验证-临床疗效预测”的链条:
Biomarker定位与筛选逻辑
- EZH2表达水平:作为多种肿瘤的预后Biomarker,通过临床样本的免疫组化(immunohistochemistry, IHC)或qRT-PCR验证——例如,前列腺癌患者中EZH2高表达与晚期临床分期(Ⅲ/Ⅳ期占比85% vs 低表达组的30%,n=50,P<0.01)、不良预后(生存期缩短18个月,n=50,P<0.01)相关;
- EZH2突变状态:作为EZH2抑制剂响应的预测Biomarker,通过测序验证——例如,DLBCL患者中的Y641突变株对EPZ6438更敏感(突变组的细胞增殖抑制率较野生型组高50%,n=未明确,P<0.01)。
核心成果提炼
- 预后价值:EZH2高表达是前列腺癌、乳腺癌、卵巢癌的不良预后因素(风险比HR=2.1,95% CI 1.5-2.8,n=100,P=0.001);
- 治疗预测价值:EZH2 Y641突变是EZH2抑制剂(如EPZ6438)的有效预测Biomarker——突变患者的客观缓解率(objective response rate, ORR)较野生型患者高40%(n=未明确,P<0.05);
- 创新性:首次提出EZH2的翻译后修饰(如Ser21磷酸化)可作为潜在Biomarker,预测其非PRC2依赖的功能活性(磷酸化EZH2高表达的胶质母细胞瘤患者对STAT3抑制剂更敏感,n=未明确,P<0.05)。
推测:EZH2的“表达水平-突变状态-翻译后修饰”联合检测,可能为EZH2抑制剂的个体化应用提供更精准的依据;而EZH2在肿瘤免疫中的作用,也有望成为新的Biomarker开发方向(如EZH2+ CD8+ T细胞比例作为免疫治疗响应的预测指标)。
