1. 领域背景与文献引入
文献英文标题:Successful treatment of acute B lymphoblastic leukemia relapse in the skin and testicle by anti-CD19 CAR-T with IL-6 knocking down: a case report;发表期刊:Biomarker Research;影响因子:未公开;研究领域:急性淋巴细胞白血病的CAR-T免疫治疗
急性淋巴细胞白血病(ALL)是起源于淋巴造血系统的恶性克隆性疾病,传统治疗以化疗、放疗及异基因造血干细胞移植(allo-HSCT)为主,但髓外复发是导致治疗失败的核心原因之一。领域共识:ALL髓外复发常见于中枢神经系统,约占所有髓外复发的三分之一,而皮肤、睾丸等部位的孤立性髓外复发较为罕见,目前缺乏标准化治疗方案,患者预后极差。近年来,嵌合抗原受体修饰T细胞(CAR-T)治疗在复发难治性B细胞急性淋巴细胞白血病(r/r B-ALL)中展现出突破性疗效,可通过靶向B细胞表面的CD19抗原特异性清除肿瘤细胞,但针对皮肤、睾丸等罕见髓外复发部位的CAR-T治疗研究十分有限。同时,传统CAR-T治疗常伴随严重的细胞因子释放综合征(CRS)及细胞因子释放脑病综合征(CRES),主要由CAR-T细胞激活后大量释放白细胞介素6(IL-6)等细胞因子介导,现有抗IL-6受体单抗无法穿透血脑屏障,难以有效防治CRES。在此背景下,本研究旨在探索敲低IL-6的抗CD19 CAR-T(ssCAR-T-19)治疗皮肤及睾丸髓外复发B-ALL的有效性与安全性,为这类罕见病例提供新的治疗选择。
2. 文献综述解析
本文综述部分以ALL髓外复发的部位为核心分类维度,系统梳理了不同部位髓外复发的治疗现状与研究进展,重点对比了传统治疗与CAR-T治疗的疗效及局限性,明确了罕见部位髓外复发的治疗空白。
现有研究显示,ALL髓外复发的传统治疗以化疗联合放疗为主,但对于皮肤、睾丸等部位的复发,传统治疗的响应率较低,患者易再次复发。针对中枢神经系统髓外复发,已有研究证实抗CD19 CAR-T治疗可突破血脑屏障清除肿瘤细胞,展现出良好的可行性与安全性,但针对皮肤、睾丸髓外复发的CAR-T治疗报道极少,其疗效与安全性尚未明确。此外,传统CAR-T治疗的核心局限性在于易引发严重的CRS及CRES,主要由CAR-T细胞激活后大量释放IL-6等细胞因子介导,而现有针对CRS的治疗药物如抗IL-6受体单抗无法穿透血脑屏障,难以有效防治CRES。通过对比现有研究的未解决问题,本研究的创新点在于首次报道了ssCAR-T-19治疗皮肤及睾丸髓外复发B-ALL的成功病例,通过在CAR-T中整合IL-6 shRNA敲低IL-6表达,有效降低了治疗相关毒性,为罕见髓外复发的治疗提供了更安全的CAR-T方案。
3. 研究思路总结与详细解析
本研究为单病例临床研究,核心目标是验证ssCAR-T-19治疗皮肤及睾丸髓外复发B-ALL的有效性与安全性,核心科学问题是ssCAR-T-19能否穿透皮肤、睾丸组织清除肿瘤细胞且降低毒性,技术路线遵循“病例入组→CAR-T细胞制备与输注→疗效与毒性监测→长期随访”的逻辑闭环。
3.1 病例入组与临床诊断
实验目的:明确患者的疾病诊断与病情进展情况,评估传统治疗后的复发状态。方法细节:纳入一名29岁男性患者,该患者经诱导化疗(VDLP方案:长春新碱+柔红霉素+左旋门冬酰胺酶+泼尼松)后达到完全缓解,但3个周期巩固治疗后出现皮肤结节复发及睾丸肿大,通过骨髓穿刺、皮肤活检、流式细胞术、超声检查等手段进行病情评估。结果解读:骨髓穿刺检查显示骨髓未复发,皮肤活检流式细胞术检测显示93.1%的原始细胞表达CD19(90.9%)等B细胞标志物,病理活检证实为B淋巴细胞白血病浸润,超声检查显示左侧睾丸肿大,最终确诊为B-ALL伴皮肤及睾丸孤立性髓外复发。产品关联:文献未提及具体诊断试剂,领域常规使用流式细胞仪、病理切片染色试剂盒等。
3.2 ssCAR-T-19细胞制备
实验目的:构建并制备敲低IL-6的抗CD19 CAR-T细胞。方法细节:从患者外周血中通过Lymphoprep™梯度离心分离单个核细胞,使用抗CD3磁珠富集CD3+T细胞,经抗CD3/CD28单克隆抗体刺激24小时后,转染携带抗CD19单链可变片段(scFv)、4-1BB共刺激域、CD3-ζ激活域及IL-6 shRNA元件的慢病毒载体,随后在含10%自体血清、IL-2、IL-7、IL-15的AIM-V培养基中培养12天。结果解读:成功制备出符合临床输注标准的ssCAR-T-19细胞,细胞纯度与活性满足治疗要求。产品关联:实验所用关键产品:Lymphoprep™(Oriental Hua Hui, Beijing, China)、抗CD3磁珠(Miltenyi Biotec, Bergisch Gladbach, Germany)、抗CD3/CD28单克隆抗体(Miltenyi Biotec)、AIM-V培养基(Gibco, Grand Island, NY, USA)、IL-2(Peprotech, Rocky Hill, USA)、IL-7(Peprotech)、IL-15(Peprotech)。
3.3 预处理与细胞输注
实验目的:通过淋巴细胞清除性化疗为CAR-T细胞输注创造有利环境,确保细胞有效扩增与浸润。方法细节:在CAR-T细胞输注前3天,给予患者氟达拉滨(30mg/m²/天)联合环磷酰胺(250mg/m²/天)进行预处理,预处理后2天,分3天输注ssCAR-T-19细胞,总剂量为5×10^6细胞/千克(第1天10%,第2天30%,第3天60%)。结果解读:预处理未引发严重不良反应,细胞输注过程顺利,患者耐受良好。产品关联:文献未提及具体化疗药物品牌,领域常规使用氟达拉滨、环磷酰胺等淋巴细胞清除药物。
3.4 疗效与安全性监测
实验目的:评估ssCAR-T-19治疗的抗肿瘤疗效及相关毒性反应。方法细节:在细胞输注后,通过皮肤活检流式细胞术、超声检查监测肿瘤负荷变化,通过实时定量PCR(qPCR)监测外周血中ssCAR-T-19细胞的扩增水平,同时监测体温、细胞因子(IL-6、IFN-γ、hsCRP)水平及血液生化指标,评估CRS及CRES发生情况。结果解读:输注后1周,患者皮肤结节完全消失,超声显示睾丸体积缩小,皮肤活检流式细胞术未检测到白血病细胞;外周血中ssCAR-T-19细胞在输注后第6天达到扩增峰值,并维持高水平数天;细胞因子水平短暂升高后1周内恢复至基线,患者仅出现1级CRS(仅发热相关不适),未发生CRES,血液学毒性仅表现为粒细胞减少,输注后第8天粒细胞恢复正常。截至随访2年1个月,患者维持完全缓解状态,无骨髓、皮肤及睾丸复发迹象。
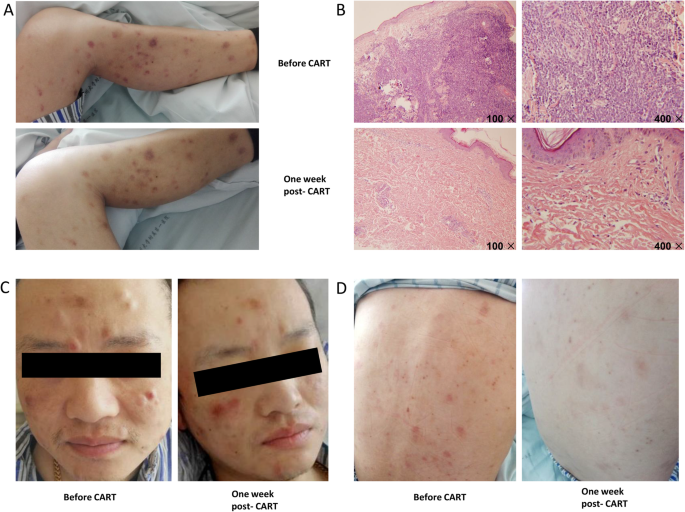
图1 患者ssCAR-T-19输注前后皮肤变化:a、c、d为输注前皮肤结节,输注后结节消失仅留色素沉着;b为皮肤活检病理染色证实白血病细胞浸润
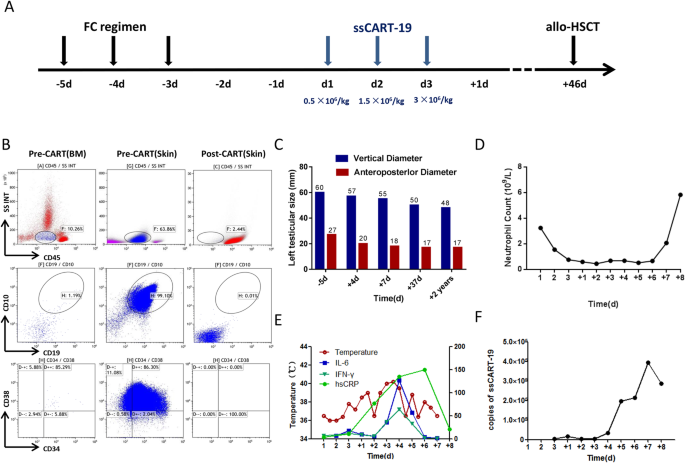
图2 ssCAR-T-19治疗相关的用药方案、临床及实验室参数:a为淋巴细胞清除化疗及细胞输注方案;b为治疗前后皮肤原始细胞比例变化;c为治疗前后睾丸体积超声测量结果;d为血液学毒性监测;e为体温及细胞因子水平变化;f为外周血ssCAR-T-19细胞扩增水平
产品关联:文献未提及具体监测试剂,领域常规使用qPCR试剂盒、细胞因子检测ELISA试剂盒等。
4. Biomarker研究及发现成果
本研究中涉及的Biomarker包括B细胞表面抗原CD19及治疗相关细胞因子(IL-6、IFN-γ),其中CD19为核心治疗靶点Biomarker,细胞因子为毒性监测Biomarker,筛选与验证逻辑基于B-ALL细胞的生物学特性及治疗毒性的发生机制。
CD19 Biomarker来源于患者的皮肤活检临床样本,验证方法为流式细胞术,检测结果显示皮肤活检样本中90.9%的原始细胞表达CD19,表明CD19在该患者的髓外复发肿瘤细胞中稳定高表达。由于本研究为单病例报告,未进行大样本的特异性与敏感性统计分析,无ROC曲线、风险比等数据。核心成果为CD19作为靶向Biomarker,介导ssCAR-T-19特异性清除了皮肤及睾丸部位的白血病细胞,实现了患者的完全缓解,且通过敲低IL-6降低了治疗相关毒性,首次证实了CD19靶向CAR-T治疗皮肤及睾丸髓外复发B-ALL的有效性与安全性。
此外,IL-6、IFN-γ等细胞因子作为治疗相关毒性的Biomarker,其水平变化与CRS的发生及严重程度相关,在本病例中IL-6水平短暂升高后迅速回落,与1级CRS的临床表现一致,可用于实时监测CAR-T治疗的毒性反应,为临床干预提供依据。
