1. 领域背景与文献引入
文献英文标题:GDF15 propeptide promotes bone metastasis of castration-resistant prostate cancer by augmenting the bone microenvironment;发表期刊:Biomarker Research;影响因子:未公开;研究领域:前列腺癌骨转移、肿瘤生物标志物。
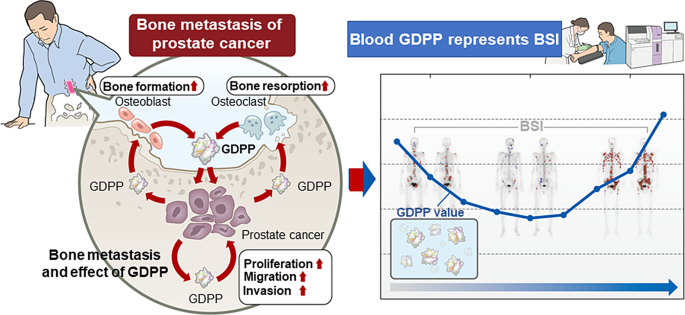
前列腺癌是全球男性发病率最高的恶性肿瘤之一,每年新发约140万例,是男性癌症相关死亡的第二大原因。雄激素剥夺治疗是转移性激素敏感性前列腺癌(mHSPC)的一线治疗方案,但几乎所有患者最终都会进展为去势抵抗性前列腺癌(CRPC)。CRPC患者的骨转移发生率高达90%,骨转移会引发骨痛、病理性骨折等骨骼相关事件,严重降低患者生活质量并缩短生存期。目前CRPC骨转移的诊断主要依赖骨扫描,但该方法存在辐射暴露、成本高、无法频繁监测等局限性;前列腺特异性抗原(PSA)是前列腺癌的常规生物标志物,但在约20%的CRPC患者中会出现神经内分泌转化,此时PSA水平无法反映疾病进展,导致临床监测困境。领域共识:现有骨代谢标志物如碱性磷酸酶(ALP)、抗酒石酸酸性磷酸酶5b(TRACP 5b)等特异性不足,难以精准诊断CRPC骨转移。因此,寻找高特异性、高敏感性的血液生物标志物,同时阐明CRPC骨转移的分子机制,是当前前列腺癌领域的核心研究需求。本研究针对这一空白,通过分泌组筛选结合临床验证,首次发现GDF15前体肽(GDPP)作为CRPC骨转移的新型生物标志物,并揭示其通过调控骨微环境促进骨转移的机制。
2. 文献综述解析
本文综述部分围绕CRPC骨转移的诊断困境与GDF15家族的研究现状展开,作者以“现有生物标志物局限性-GDF15家族研究缺口”为分类维度,系统梳理了领域内的研究进展与未解决问题。
现有研究表明,PSA作为前列腺癌的经典生物标志物,在局限性前列腺癌的诊断中具有较高价值,但在CRPC尤其是神经内分泌型前列腺癌(NEPC)中,由于肿瘤细胞丧失PSA分泌能力,PSA水平无法准确反映肿瘤负荷与骨转移状态。骨代谢标志物如ALP、骨碱性磷酸酶(BAP)、TRACP 5b等可间接反映骨转移情况,但这些标志物易受骨质疏松、骨关节炎等良性骨疾病影响,特异性不足,难以区分骨转移与良性骨病变。在GDF15家族的研究中,成熟型GDF15已被证实在多种肿瘤中高表达,参与肿瘤增殖、侵袭等过程,但针对GDF15前体肽GDPP的研究几乎空白,其是否被分泌至细胞外、是否具有生物学功能、能否作为肿瘤生物标志物均未被阐明。通过对比现有研究的局限性,本研究的创新价值凸显:首次聚焦GDF15前体肽GDPP,同时完成了生物标志物的临床验证与功能机制的阐明,填补了CRPC骨转移精准诊断与机制研究的双重空白。
3. 研究思路总结与详细解析
本文整体研究思路遵循“筛选-验证-机制-体内验证”的闭环逻辑:首先通过分泌组学筛选CRPC细胞分泌的潜在生物标志物,锁定GDPP;随后通过大样本临床队列验证GDPP作为CRPC骨转移生物标志物的诊断与预后价值;接着通过细胞实验阐明GDPP对前列腺癌细胞、成骨细胞、破骨细胞的调控作用;最后通过动物实验验证GDPP促进骨转移的体内功能,并解析其调控骨微环境的分子机制。
3.1 分泌组学筛选与GDPP的鉴定
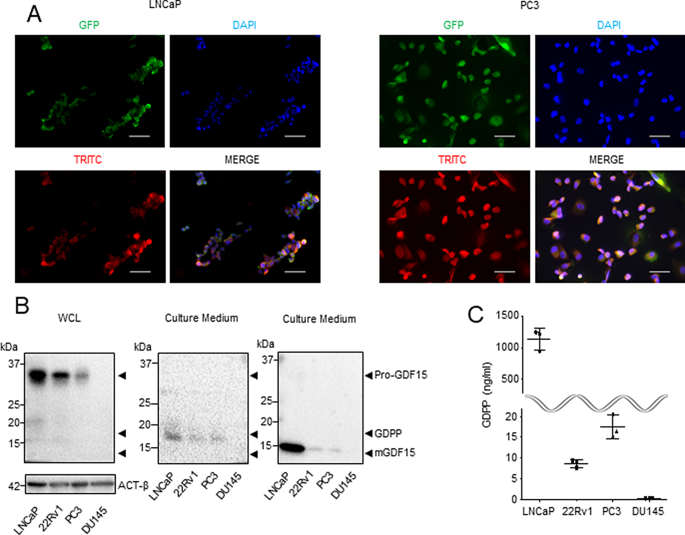
实验目的:从CRPC细胞的分泌蛋白中筛选潜在的骨转移生物标志物;方法细节:选取四种前列腺癌细胞系(LNCaP、22Rv1、PC3、DU145),培养至60%汇合度后更换无血清培养基,培养48小时后收集上清,通过Orbitrap质谱进行分泌组学分析,鉴定分泌蛋白,筛选在多种细胞系中分泌的蛋白;结果解读:共鉴定出2787种分泌蛋白,其中GDF15前体肽GDPP在LNCaP、22Rv1、PC3三种细胞系中均有分泌,进一步通过免疫荧光染色证实GDPP与成熟型GDF15在细胞内共定位,且通过furin酶切后分泌至细胞外;产品关联:实验所用关键产品:Orbitrap Velos质谱仪(Thermo Fisher Scientific)、Proteome Discoverer 2.5软件(Thermo Scientific)、兔抗GDPP多克隆抗体(Sigma‒Aldrich,货号HPA011191)等。
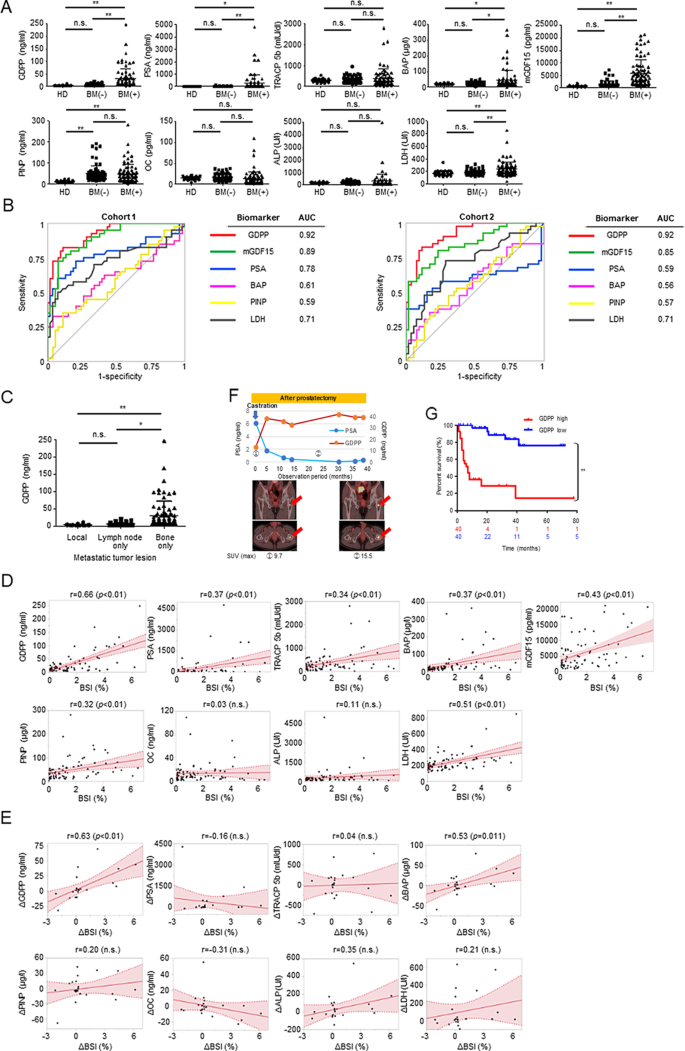
3.2 临床样本中GDPP的诊断与预后价值验证
实验目的:验证GDPP作为CRPC骨转移生物标志物的临床价值;方法细节:收集2012年12月至2022年12月期间的416例患者样本,包括30例健康对照、60例局限性前列腺癌、30例mHSPC骨转移患者、75例mCRPC无骨转移患者、80例mCRPC骨转移患者,采用自主研发的ELISA系统检测血浆GDPP水平,同时检测PSA、ALP、BAP、TRACP 5b等标志物,分析各标志物的ROC曲线、与骨扫描指数(BSI)的相关性,通过Kaplan-Meier分析评估GDPP的预后价值;结果解读:GDPP在mCRPC骨转移患者中的水平显著高于无骨转移患者及健康对照(n=80 vs n=75,P<0.01),ROC曲线显示GDPP的AUC为0.92,显著优于PSA的0.78及其他骨代谢标志物;GDPP水平与BSI的相关性系数r=0.66(n=80,P<0.01),治疗后GDPP水平的变化与BSI变化的相关性r=0.63(n=22,P<0.01);高GDPP水平的mCRPC骨转移患者总生存期显著缩短,风险比HR=11.3(95% CI 4.13-31.0,P<0.01);产品关联:实验所用关键产品:全自动化学发光酶免疫分析系统AIA-CL2400(Tosoh)、骨扫描分析软件BONENAVI等。
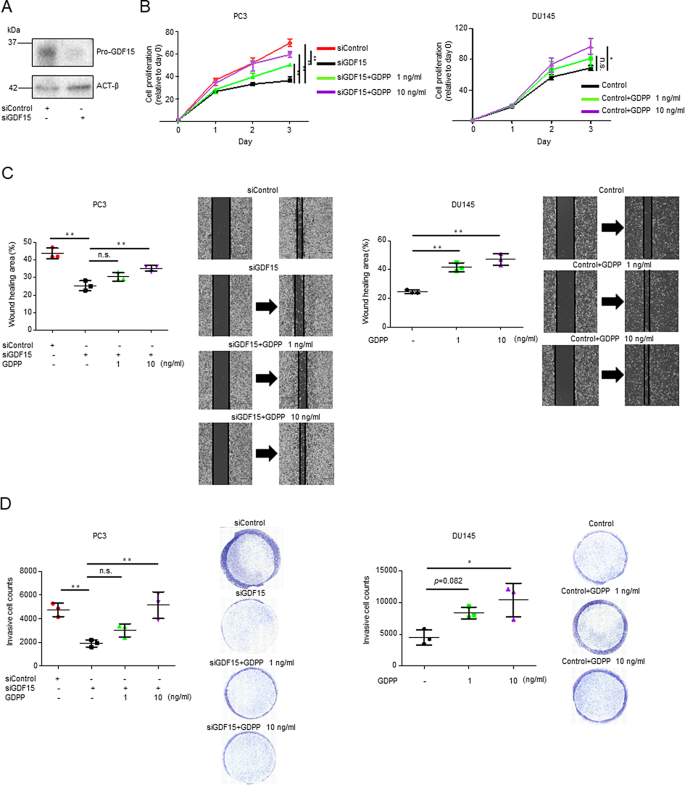
3.3 GDPP对前列腺癌细胞增殖、迁移与侵袭的调控
实验目的:验证GDPP对CRPC细胞恶性生物学行为的促进作用;方法细节:采用siRNA敲低PC3和DU145细胞中的GDF15表达,随后用重组GDPP(rGDPP)处理细胞,通过MTS实验检测细胞增殖能力,划痕实验检测细胞迁移能力,Transwell实验检测细胞侵袭能力;结果解读:敲低GDF15后,PC3和DU145细胞的增殖能力显著降低(n=3,P<0.01),而rGDPP处理可剂量依赖性地恢复细胞增殖能力;rGDPP处理还显著增强了PC3和DU145细胞的迁移与侵袭能力(n=3,P<0.01);产品关联:实验所用关键产品:siRNA(Qiagen,货号GS9518)、MT Cell Viability Substrate(Promega,货号G9712)、Matrigel侵袭小室(Corning,货号354480)等。
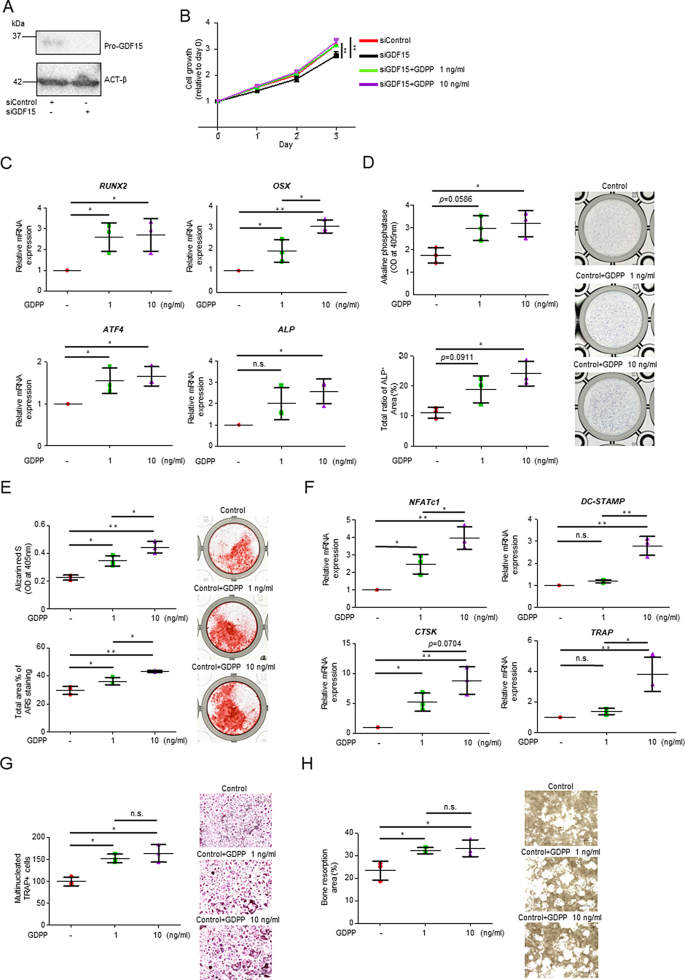
3.4 GDPP对骨微环境细胞的调控作用
实验目的:阐明GDPP对成骨细胞和破骨细胞的调控机制;方法细节:用rGDPP处理人原代成骨细胞(HOB)和破骨细胞前体(OSC15C),通过MTS实验检测增殖,qRT-PCR检测成骨/破骨分化相关基因的表达,ALP染色、茜素红染色检测成骨细胞分化与矿化,TRAP染色、骨吸收实验检测破骨细胞分化与骨吸收能力;结果解读:rGDPP促进HOB细胞增殖,上调成骨分化相关基因RUNX2、OSX、ATF4的表达(n=3,P<0.01),增强ALP活性和矿化能力;同时rGDPP促进OSC15C细胞分化为成熟破骨细胞,上调破骨分化相关基因NFATc1、DC-STAMP的表达(n=3,P<0.01),增强骨吸收能力;产品关联:实验所用关键产品:ALP染色试剂盒(Cosmo Bio,货号AK20)、茜素红S染色试剂盒(BMK,货号BMK-R009)、TRAP染色试剂盒(Cosmo Bio,货号AK04F)等。
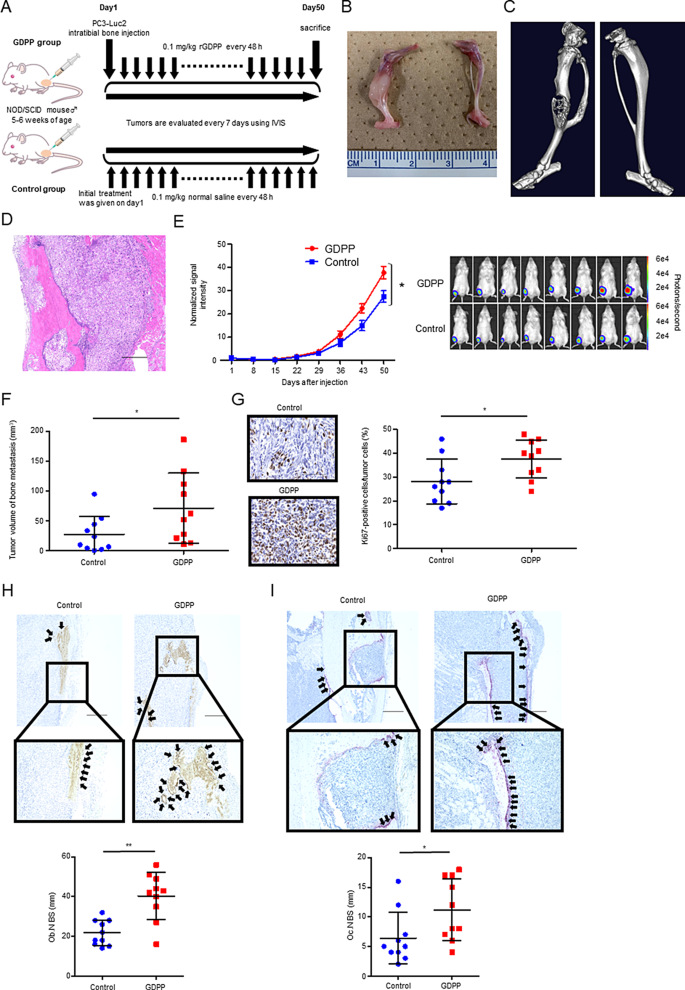
3.5 动物实验验证GDPP促进CRPC骨转移
实验目的:验证GDPP在体内促进CRPC骨转移的功能;方法细节:将PC3-Luc2细胞注射到NOD/SCID小鼠的胫骨骨髓腔,随后每隔一天皮下注射rGDPP(0.1mg/kg),对照组注射生理盐水,每周通过IVIS成像监测肿瘤生长,50天后处死小鼠,通过micro-CT分析骨肿瘤体积,免疫组化检测成骨细胞和破骨细胞数量;结果解读:rGDPP处理组的肿瘤负荷显著高于对照组,骨肿瘤体积增大(n=10,P<0.05),成骨细胞和破骨细胞的数量显著增加(n=10,P<0.05),表明GDPP通过增强骨微环境的成骨与破骨过程促进骨转移;产品关联:实验所用关键产品:IVIS Lumina II成像系统(Caliper)、micro-CT(Rigaku,R_mCT2)等。
4. Biomarker研究及发现成果解析
本文鉴定的生物标志物为GDF15前体肽(GDPP),属于循环蛋白类生物标志物,其筛选与验证遵循“组学筛选-细胞验证-临床大样本验证-纵向监测”的完整逻辑链条,同时阐明了其促进骨转移的功能机制,为CRPC骨转移的诊断与治疗提供了新靶点。
Biomarker定位:GDPP是CRPC骨转移的特异性血液生物标志物,筛选逻辑为:首先通过分泌组学从CRPC细胞分泌蛋白中筛选出GDPP,随后通过细胞实验验证其分泌特性,再通过大样本临床队列验证其诊断与预后价值,最后通过纵向监测验证其反映治疗反应的能力。研究过程详述:GDPP的来源为前列腺癌细胞、成骨细胞、破骨细胞分泌至血浆中的蛋白,验证方法为自主研发的ELISA定量检测,特异性方面,GDPP在CRPC骨转移患者中的水平显著高于淋巴结转移患者及局限性前列腺癌患者(n=31 vs n=12,P=0.0124;n=31 vs n=60,P<0.01),ROC曲线AUC=0.92(95% CI未明确提供),敏感性与特异性基于Youden指数确定(文献未明确提供具体数值);核心成果提炼:GDPP是CRPC骨转移的独立预后因素,风险比HR=11.3(95% CI 4.13-31.0,P<0.01),首次发现GDPP通过上调成骨细胞RUNX2、OSX等转录因子和破骨细胞NFATc1、DC-STAMP等转录因子,同时促进成骨与破骨过程,增强骨微环境的“土壤”效应,进而促进CRPC骨转移;该生物标志物的创新性在于首次揭示GDF15前体肽的分泌功能与临床价值,弥补了PSA在CRPC骨转移诊断中的局限性,为CRPC骨转移的早期诊断与动态监测提供了新工具。