1. 领域背景与文献引入
文献英文标题:LINC01559 promotes lung adenocarcinoma metastasis by disrupting the ubiquitination of vimentin;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肺腺癌转移与长链非编码RNA(lncRNA)调控机制
领域共识:肺癌是全球发病率和死亡率最高的恶性肿瘤之一,肺腺癌是其最常见的病理亚型,远处转移是导致肺腺癌患者死亡的主要原因。尽管分子靶向治疗、免疫治疗等手段取得了一定进展,但晚期转移性肺腺癌患者的临床预后仍不理想,亟需深入解析肺腺癌转移的分子机制以开发新的治疗靶点。上皮间质转化(EMT)是肿瘤细胞获得迁移和侵袭能力的关键生物学过程,波形蛋白(vimentin)作为EMT的核心标志物,通过维持细胞骨架结构、降低细胞间黏附性促进肿瘤转移,其表达调控机制是领域研究热点之一。
长链非编码RNA在肿瘤发生发展中的调控作用已被广泛证实,其可通过作为竞争性内源RNA(ceRNA)、结合调控蛋白、参与转录调控等多种方式影响肿瘤进程。目前已有研究报道部分长链非编码RNA参与肺腺癌的增殖、存活等过程,但在肺腺癌转移中的具体调控机制仍存在大量空白,尤其是LINC01559在肺腺癌中的功能尚未被报道。针对这一研究缺口,本研究聚焦LINC01559在肺腺癌转移中的作用及分子机制,为晚期肺腺癌的预后预测和治疗提供新的思路。
2. 文献综述解析
本文作者对领域内现有研究的分类维度主要包括:长链非编码RNA在不同癌症中的功能机制分类(如ceRNA模式、蛋白结合调控模式)、LINC01559在其他癌症中的研究结论对比、肺腺癌转移相关分子调控通路的研究现状。
现有研究显示,长链非编码RNA在肺腺癌中可通过调控抑癌基因、癌基因的表达参与肿瘤进程,例如MILIP通过抑制p53促进肺腺癌发生,LCDR通过维持溶酶体膜完整性促进细胞存活,但这些研究多聚焦于肿瘤增殖或存活,对转移过程的调控机制解析不足。在其他癌症中,LINC01559已被报道参与转移调控,如在胃癌中通过招募IGF2BP2稳定ZEB1表达促进转移,在胰腺癌中通过YAP通路调控细胞迁移,但这些研究的作用机制具有组织特异性,无法直接延伸至肺腺癌领域。此外,现有研究对波形蛋白的调控多集中在转录或磷酸化层面,对其泛素化降解的长链非编码RNA调控机制尚未有报道。
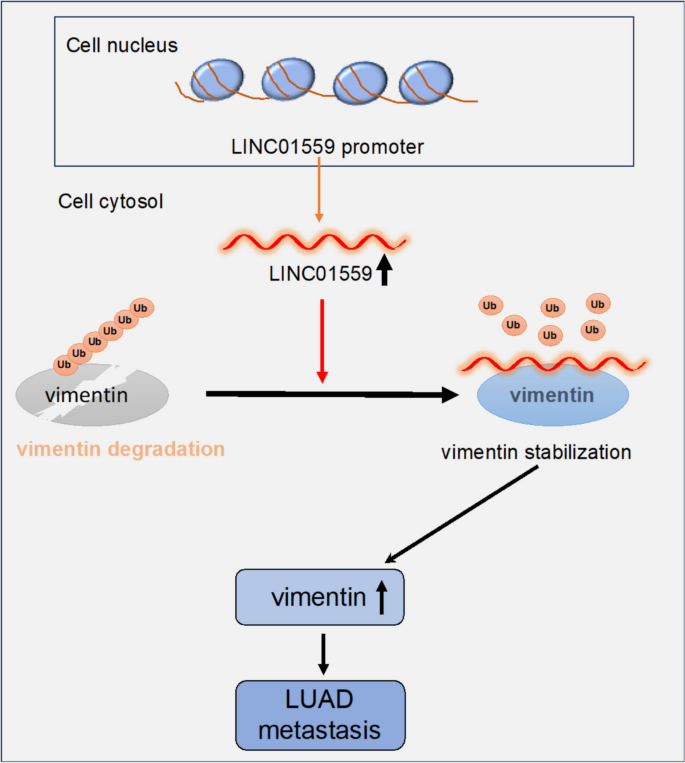
通过对比现有研究的未解决问题,本研究的创新价值凸显:首次在肺腺癌中明确LINC01559的促转移功能,揭示其通过直接结合波形蛋白并阻断其泛素化降解的全新调控机制,同时证实LINC01559可作为肺腺癌患者的独立预后标志物,为肺腺癌转移的机制研究和临床应用提供了新的方向。
3. 研究思路总结与详细解析
本研究的核心目标是明确LINC01559在肺腺癌转移中的功能及分子机制,核心科学问题为“LINC01559如何调控肺腺癌的迁移、侵袭及转移过程”,技术路线遵循“生物信息学筛选→临床样本验证→细胞与动物功能实验→分子机制解析→临床意义验证”的闭环逻辑,系统解析了LINC01559的作用及机制。
3.1 LINC01559在肺腺癌中的表达与预后相关性分析
实验目的:明确LINC01559在肺腺癌组织及细胞系中的表达特征,及其与患者临床病理特征和预后的相关性。
方法细节:首先利用Gene Expression Omnibus(GEO)数据库(GSE11117)和癌症基因组图谱(TCGA)数据库分析LINC01559在肺腺癌中的表达差异;采用原位杂交(ISH)技术检测90例福尔马林固定石蜡包埋(FFPE)肺腺癌样本及配对癌旁组织中LINC01559的表达;通过实时定量PCR(qPCR)检测肺腺癌细胞系(A549、H1299等)及成纤维细胞系中LINC01559的表达;采用Kaplan-Meier生存分析评估LINC01559表达与患者总生存期的关系,多因素Cox回归分析验证其是否为独立预后因素。
结果解读:数据库分析显示,LINC01559在伴有远处转移的肺腺癌组织中表达显著高于无转移组织(TCGA数据集n=453,P<0.05),且肺腺癌组织表达显著高于配对癌旁组织(TCGA数据集n=58,P<0.01);原位杂交验证结果显示,90例临床样本中肺腺癌组织LINC01559的反应评分(RS)显著高于癌旁组织(n=90,P<0.01),高表达与更高的组织学分级(III-IV级)和晚期(AJCC III-IV期)相关;Kaplan-Meier分析显示高表达LINC01559的患者总生存期更短(n=90,P<0.01),多因素Cox回归分析证实其为独立预后因素;细胞系实验显示,3种肺腺癌细胞系中LINC01559表达显著高于成纤维细胞系(n=3,P<0.05)。
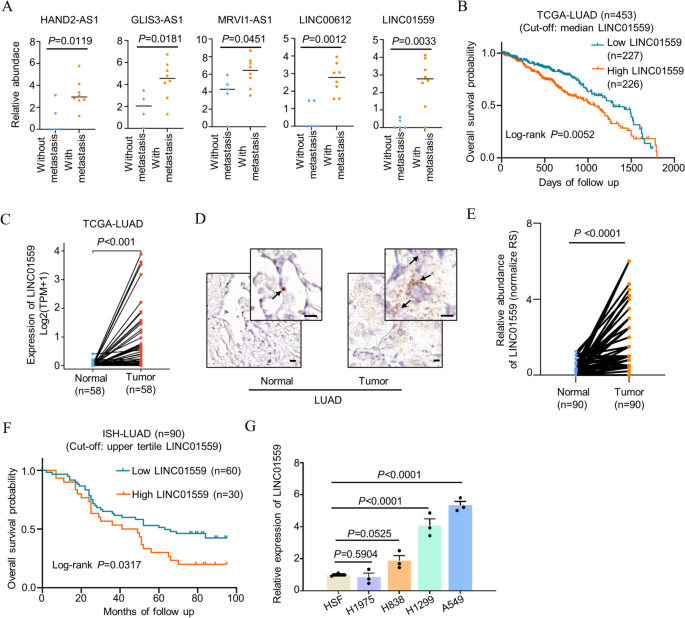
实验所用关键产品:原位杂交使用RNAscope® 2.5 HD Detection Reagent-BROWN(Advanced Cell Diagnostics, #322310),qPCR使用FastPure® Cell/Tissue Total RNA Isolation Kit V2(Vazyme, # RC112)、PrimScript™ RT reagent Kit with gDNA Eraser(TaKaRa, #RR047A)等。
3.2 LINC01559对肺腺癌转移的功能验证
实验目的:在细胞和动物水平验证LINC01559对肺腺癌迁移、侵袭及转移能力的调控作用。
方法细节:细胞实验中,采用小干扰RNA(siRNA)瞬时敲低或短发夹RNA(shRNA)稳定敲低肺腺癌细胞系(A549、H1299)中LINC01559的表达,通过划痕愈合实验、Transwell迁移实验和侵袭实验检测细胞的迁移和侵袭能力;同时构建LINC01559过表达细胞系进行回复验证。动物实验中,将稳定敲低LINC01559的A549细胞通过尾静脉注射至NOD/SCID小鼠体内,8周后计数肺组织转移结节数量,采用苏木精-伊红(H&E)染色进行病理验证。
结果解读:瞬时敲低LINC01559后,A549和H1299细胞的划痕愈合率显著降低(n=3,P<0.01),Transwell迁移和侵袭细胞数分别减少约40%和50%(n=3,P<0.01);稳定敲低LINC01559的A549细胞在小鼠体内形成的肺转移结节数量显著少于对照组(n=6,P<0.01),肺组织重量显著降低,H&E染色证实转移灶面积明显减小;过表达LINC01559可显著增强细胞的迁移和侵袭能力(n=3,P<0.05)。
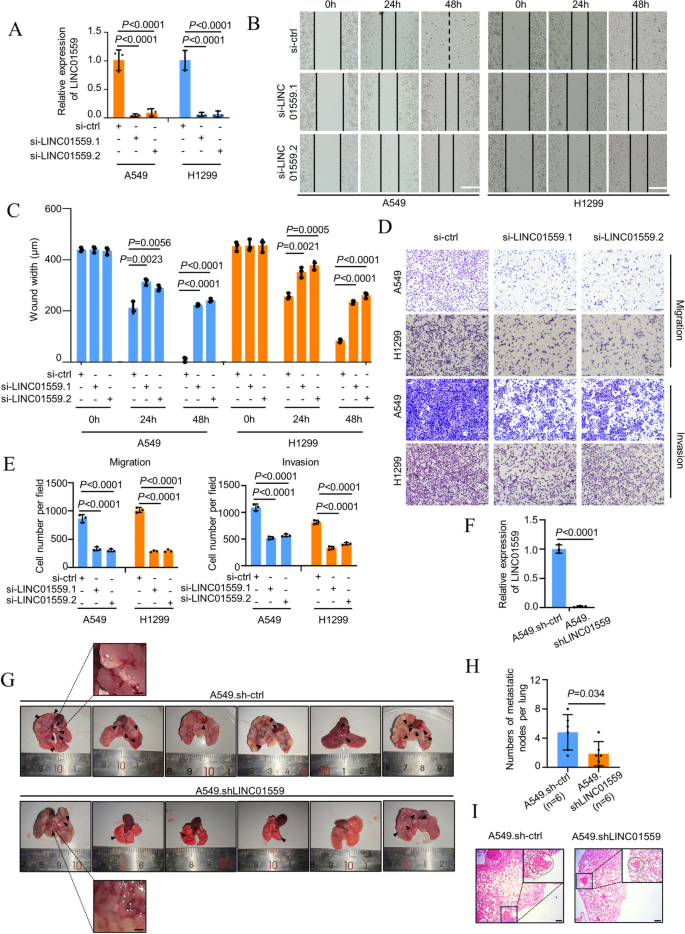
实验所用关键产品:siRNA来自Ribobio,shRNA来自TSINGKE Biological Technology,Transwell小室(Corning, #3422),Matrigel(BD Biosciences, # 356234)等。
3.3 LINC01559与波形蛋白的相互作用鉴定
实验目的:鉴定LINC01559的亚细胞定位及互作蛋白,明确其与波形蛋白的直接结合关系。
方法细节:通过qPCR分析LINC01559在细胞质和细胞核中的分布比例;采用RNA pulldown实验结合质谱分析筛选与LINC01559结合的蛋白;通过RNA pulldown和RNA免疫沉淀(RIP)实验验证LINC01559与波形蛋白的直接结合。
结果解读:亚细胞定位分析显示,LINC01559主要定位于细胞质(占比约75%,n=3);RNA pulldown结合质谱分析结果显示,波形蛋白是与LINC01559结合的最丰富蛋白;RNA pulldown实验证实,LINC01559的反义探针可特异性富集波形蛋白(n=3,P<0.05);RIP实验显示,波形蛋白抗体可特异性富集LINC01559(n=3,P<0.05),两者存在直接相互作用。
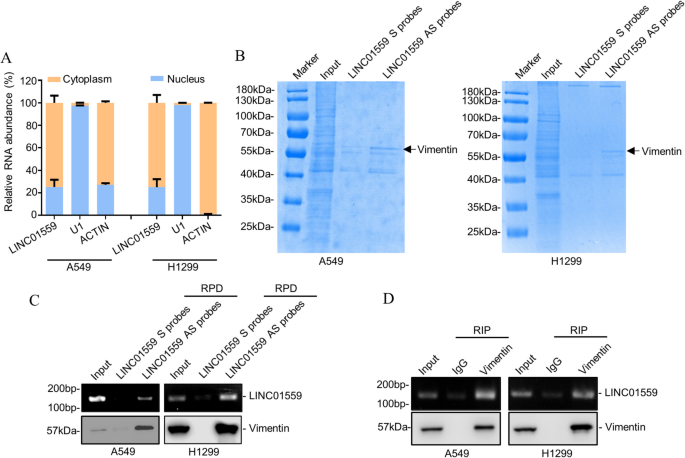
实验所用关键产品:RNA pulldown使用链霉亲和素琼脂糖树脂(ThermoFisher Scientific, #20349),RIP使用磁珠(ThermoFisher Scientific, #26162),波形蛋白抗体(Santa Cruz Biotechnology, #sc-6260)等。
3.4 波形蛋白在LINC01559调控转移中的功能验证
实验目的:明确波形蛋白是否为LINC01559调控肺腺癌转移的下游效应分子。
方法细节:采用siRNA敲低肺腺癌细胞系中波形蛋白的表达,通过Transwell实验检测细胞迁移和侵袭能力;构建LINC01559敲低同时过表达波形蛋白的细胞系,以及LINC01559过表达同时敲低波形蛋白的细胞系,通过Transwell实验进行回复验证。
结果解读:敲低波形蛋白后,A549和H1299细胞的迁移和侵袭能力显著降低(n=3,P<0.01);过表达波形蛋白可完全逆转LINC01559敲低导致的迁移和侵袭能力下降(n=3,P<0.05);敲低波形蛋白可显著抑制LINC01559过表达诱导的迁移和侵袭能力增强(n=3,P<0.05),证实波形蛋白是LINC01559调控转移的必需下游分子。
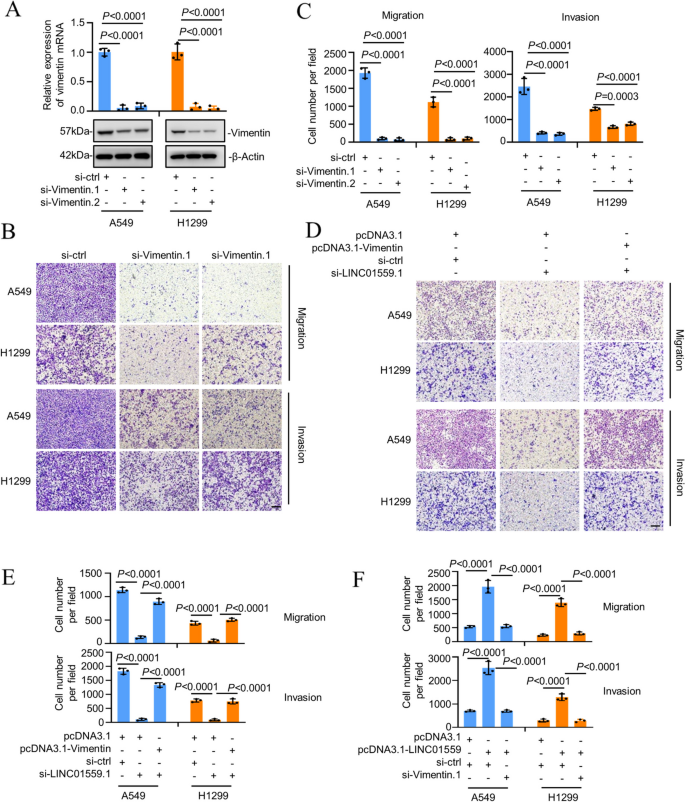
实验所用关键产品:波形蛋白siRNA来自Ribobio,过表达质粒来自TSINGKE Biological Technology等。
3.5 LINC01559对波形蛋白稳定性与泛素化的调控机制
实验目的:解析LINC01559调控波形蛋白表达的分子机制,明确其对波形蛋白泛素化降解的影响。
方法细节:通过qPCR和蛋白免疫印迹(Western blotting)检测敲低或过表达LINC01559后波形蛋白的mRNA和蛋白水平;采用环己酰亚胺(CHX) chase实验检测波形蛋白的蛋白半衰期;通过蛋白酶体抑制剂MG132处理验证降解途径;采用泛素化实验检测波形蛋白的泛素化修饰水平;同时检测小鼠体内转移灶中波形蛋白的表达和泛素化水平。
结果解读:敲低LINC01559不影响波形蛋白的mRNA水平,但显著降低其蛋白表达(n=3,P<0.01);过表达LINC01559可显著升高波形蛋白的蛋白水平,但对mRNA无影响(n=3,P<0.05);CHX chase实验显示,敲低LINC01559后波形蛋白的半衰期从约8小时缩短至约4小时(n=3,P<0.01);MG132处理可完全逆转敲低LINC01559导致的波形蛋白降低,证实其通过蛋白酶体途径降解;泛素化实验显示,敲低LINC01559显著增加波形蛋白的泛素化水平,过表达则显著降低(n=3,P<0.05);小鼠体内转移灶中,敲低LINC01559组的波形蛋白表达显著降低,泛素化水平显著升高(n=5,P<0.05)。
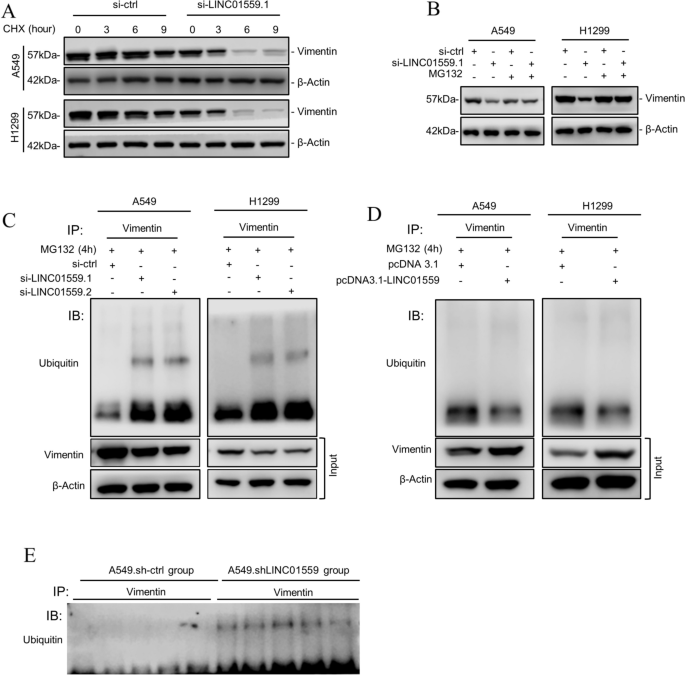
实验所用关键产品:CHX(MedChemExpress, #66-81-9),MG132(Selleckchem, #S2619),泛素抗体(Cell Signaling Technology, #3936S),蛋白免疫印迹使用BCA蛋白定量试剂盒(ThermoFisher Scientific, #23227)等。
4. Biomarker 研究及发现成果解析
本文鉴定的Biomarker为长链非编码RNA LINC01559,属于转录调控类Biomarker,其筛选与验证逻辑为:通过生物信息学数据库筛选出与肺腺癌转移相关的差异表达lncRNA,随后在临床样本中验证其表达特征与预后价值,通过细胞和动物实验验证其功能,最后解析其分子机制以明确Biomarker的生物学意义。
该Biomarker的来源为临床肺腺癌组织样本和细胞系,验证方法包括原位杂交、qPCR、生存分析等。在90例临床样本中,LINC01559在肺腺癌组织中的表达显著高于癌旁组织(n=90,P<0.01),高表达与患者的晚期病理分期、高组织学分级相关,Kaplan-Meier生存分析显示其对患者总生存期具有显著预测价值(n=90,P<0.01),多因素Cox回归分析证实其为独立预后因素(文献未明确提供HR具体数值)。
核心成果方面,LINC01559作为肺腺癌的独立预后Biomarker,可有效区分高风险转移患者,为临床预后分层提供新的指标;同时,其通过结合波形蛋白阻断泛素化降解的机制首次被揭示,为肺腺癌转移的治疗提供了新的潜在靶点。此外,该研究首次将LINC01559与波形蛋白的调控关联起来,拓展了长链非编码RNA调控蛋白泛素化的研究领域,具有重要的学术价值。