1. 领域背景与文献引入
文献英文标题:Bridging the barrier: insights into blood biomarkers and therapeutic strategies targeting choroid plexus and BBB dysfunction in alzheimer’s disease;发表期刊:Biomarker Research;影响因子:未公开;研究领域:阿尔茨海默病、神经退行性疾病、生物标志物研究、精准诊疗。
阿尔茨海默病(AD)是全球最常见的痴呆类型,约占所有痴呆病例的60%-80%,其病理特征包括β-淀粉样蛋白(Aβ)沉积、过度磷酸化tau蛋白形成的神经原纤维缠结、突触功能障碍及神经元丢失。领域发展关键节点涵盖:2024年美国FDA批准首个基于血液的AD诊断设备Lumipulse G,通过检测血浆p-tau217/Aβ₄₂比值辅助诊断;同年脑脊液(CSF)蛋白质组学研究将AD分为5个分子亚型,其中亚型4、5分别以脉络丛(CP)功能障碍和血脑屏障(BBB)功能障碍为核心特征,突破了传统以Aβ/tau为核心的病理认知。当前研究热点聚焦于非侵入性血液生物标志物的开发、亚型特异性诊断模型构建及个性化治疗策略探索,但未解决的核心问题在于:经典Aβ/tau生物标志物无法覆盖CP/BBB功能障碍的非经典AD亚型,缺乏针对该类亚型的特异性血液标志物及靶向治疗方案,导致该类患者难以获得精准诊断与有效干预。
针对这一研究空白,本综述系统整合了AD中CP与BBB功能障碍的病理机制、相关血液生物标志物及潜在治疗策略,旨在为非经典AD亚型的精准诊断提供生物标志物参考,同时为个性化治疗方案的开发提供理论依据,填补了AD亚型特异性诊疗领域的综述研究空白。
2. 文献综述解析
作者对领域内现有研究的分类维度主要包括AD分子亚型(经典Aβ/tau驱动亚型 vs 非经典CP/BBB功能障碍亚型)、生物标志物类型(CP相关、BBB相关)及治疗策略作用机制(抗炎、屏障修复、蛋白清除增强等)。
现有研究的关键结论显示,AD的病理机制具有高度异质性,CSF蛋白质组学分型证实5个分子亚型中,亚型4、5的核心驱动因素为CP/BBB功能障碍而非经典Aβ/tau过度产生,该类亚型患者的CSF tau水平无明显升高,提示病理机制以蛋白清除障碍为主。技术方法层面,CSF蛋白质组学可实现AD的精准分子分型,血液生物标志物检测具有非侵入性、可普及性优势,适合基层医疗场景的早期筛查;但现有研究存在局限性,针对CP/BBB功能障碍的血液标志物大多缺乏直接的成像验证数据,部分标志物的疾病特异性不足,且相关治疗策略多处于临床前或早期临床试验阶段,缺乏大规模多中心临床验证。
通过对比现有研究的未解决问题,本综述的创新价值凸显:现有综述多聚焦于经典AD亚型的生物标志物与治疗,而本研究首次系统整合了非经典AD亚型(CP/BBB功能障碍)的血液生物标志物,涵盖趋化因子、胶质蛋白、代谢蛋白等多类分子,并对应提出亚型特异性治疗策略,为AD的精准诊断与个性化治疗提供了全面的参考框架,弥补了领域内对非经典AD亚型关注不足的缺陷。
3. 研究思路总结与详细解析
本研究的整体框架以“CP/BBB功能障碍在AD中的病理机制→相关血液生物标志物总结→靶向治疗策略梳理”为逻辑闭环,核心科学问题是明确CP/BBB功能障碍在AD中的作用机制,以及如何通过血液标志物识别该类亚型并开发针对性治疗方案,最终为AD的精准诊疗提供依据。
3.1 脉络丛功能障碍相关血液生物标志物解析
本环节的核心目标是总结与CP功能障碍相关的AD血液生物标志物,明确其临床应用价值与病理关联。作者整合了瑞典AD/MCI患者队列、台湾纵向队列、韩国患者队列等多个临床研究数据,涵盖趋化因子、胶质蛋白、蛋白酶、神经损伤标志物等多类分子的研究结果。
CP在AD中表现为体积增大、结构损伤及功能障碍,导致脑脊液产生异常、Aβ清除能力下降(图1)。
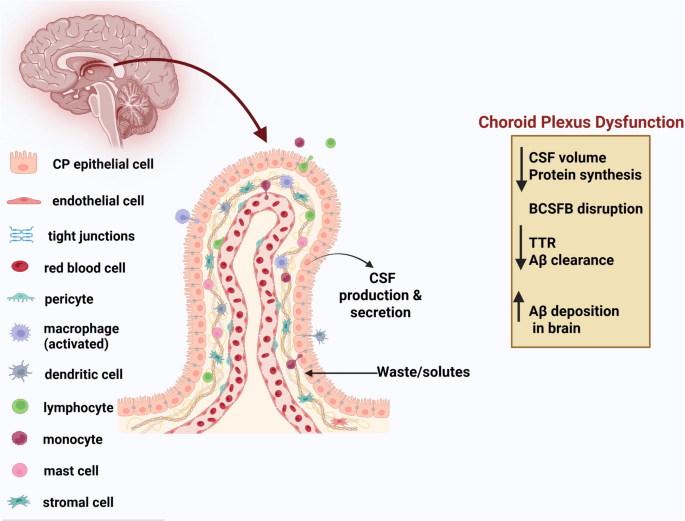
趋化因子CCL2在AD患者血浆中水平显著升高,与简易精神状态检查(MMSE)评分呈负相关(n=310 AD,66 MCI,120健康对照,P<0.05),提示其参与神经炎症进程并影响认知下降速度;几丁质酶3样蛋白1(CHI3L1)在AD患者血浆中浓度高于健康对照和MCI患者(n=61 AD,49 MCI,P<0.05),可作为AD早期筛查的潜在标志物;胶质纤维酸性蛋白(GFAP)作为星形胶质细胞激活标志物,在AD临床前期即出现血浆水平升高,与CP结构完整性降低相关(n=108,22-94岁认知未受损人群,P<0.05);转甲状腺素蛋白(TTR)在AD和MCI患者血浆中水平显著低于健康对照(n=56 AD,55 aMCI,41健康对照,P<0.05),女性患者下降更显著,与疾病严重程度直接相关。此外,CP功能障碍的遗传风险因子包括ABCA7、PICALM、IL-34等(图2),这些基因通过影响Aβ清除、脂质代谢及神经免疫平衡参与AD病理进程。
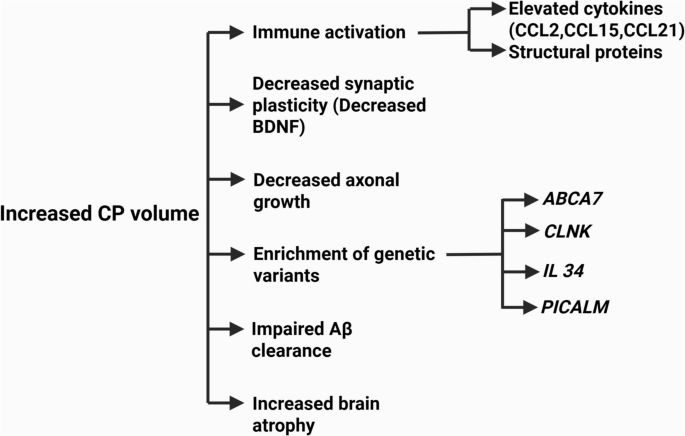
产品关联:文献中提及的检测方法包括酶联免疫吸附试验(ELISA)、液相色谱-质谱联用(LC-MS)等,商用AD血液诊断产品包括Lumipulse G、AlzOn等。
3.2 血脑屏障功能障碍相关血液生物标志物解析
本环节的核心目标是总结BBB功能障碍相关的AD血液生物标志物,揭示其与BBB损伤的病理关联及临床价值。作者整合了AD Neuroimaging Initiative(ADNI)队列、Baltimore纵向衰老研究(BLSA)队列等多个大规模研究数据,涵盖载脂蛋白、急性期蛋白、血管相关因子等多类分子。
BBB在AD中表现为通透性增加、周细胞丢失、紧密连接破坏,导致脑内环境稳态失衡(图4),其遗传风险因子包括APOE ε4、IL-34、APP等(图3),其中APOE ε4在该亚型中的携带比例最高,APP突变通过增加Aβ沉积引发血管损伤。
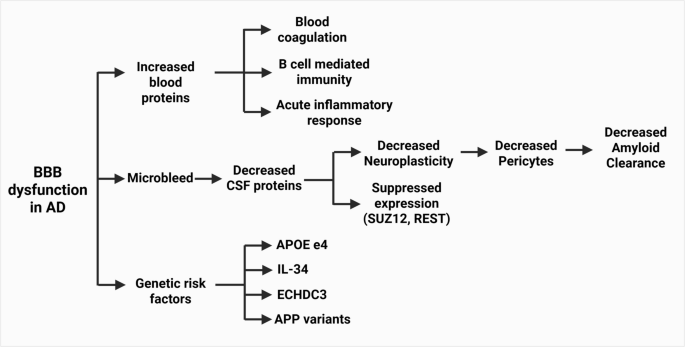
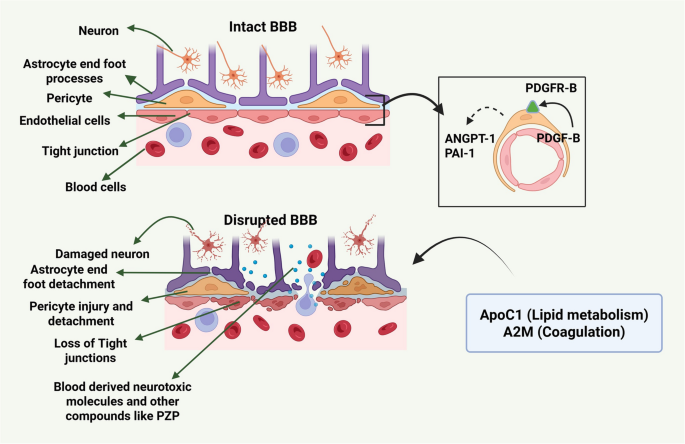
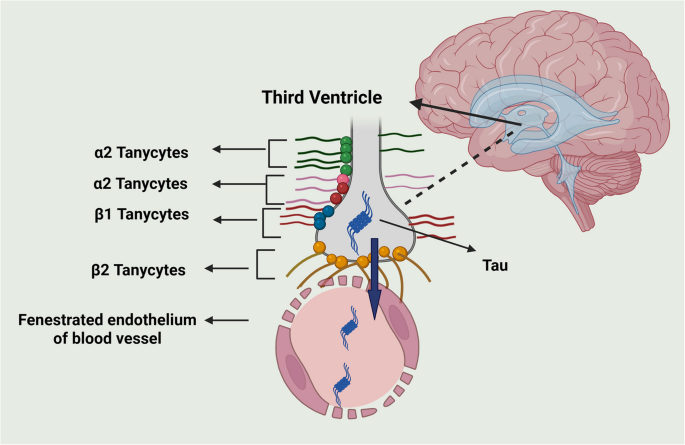
α-2巨球蛋白(A2M)在AD和MCI患者血浆中水平显著升高(n=566 ADNI队列,n=47 BLSA队列,P<0.05),男性AD患者升高更显著,基线水平高的个体发展为AD的风险增加;纤溶酶原激活物抑制剂1(PAI-1)在AD患者血浆中水平随疾病严重程度增加而升高(n=226 Ansan Geriatric队列,P<0.05),PAI-1/脑源性神经营养因子(BDNF)比值与BBB功能障碍及认知下降直接相关;妊娠区带蛋白(PZP)在AD临床前期血清中水平即升高(n=1077 Rotterdam Scan Study队列,60-90岁,P<0.05),与脑内Aβ沉积及神经炎症相关。此外,伸展细胞作为BBB的组成部分,其损伤会影响tau蛋白的脑-血清除(图5),进而参与AD病理进程。
产品关联:文献未提及具体实验产品,领域常规使用酶联免疫吸附试验(ELISA)、液相色谱-质谱联用(LC-MS)等试剂/仪器。
3.3 靶向屏障功能障碍的治疗策略解析
本环节的核心目标是总结针对CP与BBB功能障碍的AD治疗策略,为临床转化提供参考。作者整合了临床前研究、临床试验及药物重定位研究数据,涵盖抗炎治疗、屏障修复治疗、蛋白清除增强治疗、干细胞治疗等多个方向。
抗炎治疗方面,TNF-α抑制剂(如英夫利昔单抗)在AD小鼠模型中可减少Aβ斑块沉积与tau磷酸化,改善认知功能;屏障修复治疗中,白蛋白置换疗法(AMBAR项目)的II/III期临床试验显示,高剂量白蛋白联合静脉注射免疫球蛋白(IVIG)可显著改善AD患者的语言能力与认知处理速度;蛋白清除增强治疗中,靶向CCL2/CCR2轴的药物(如瑞波西汀)可减轻AD小鼠的神经炎症与Aβ沉积;干细胞治疗方面,人多能干细胞(hPSC)来源的周细胞可修复BBB功能,在小鼠卒中模型中促进神经血管恢复。此外,针对周细胞的靶向治疗(如铁死亡抑制剂FER-1、线粒体分裂抑制剂Mdivi-1)也显示出潜在的AD干预价值。
产品关联:文献中提及的治疗药物包括英夫利昔单抗、托珠单抗、阿那白滞素等,白蛋白置换疗法使用5%或20%白蛋白制剂。
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
文献中涉及的生物标志物分为脉络丛功能障碍相关与血脑屏障功能障碍相关两类,筛选与验证逻辑遵循“分子分型确定亚型→临床队列验证血液标志物与亚型的关联→机制研究揭示标志物与屏障功能的病理联系”的完整链条:首先通过CSF蛋白质组学确定CP/BBB功能障碍的AD亚型,随后在多中心临床队列中验证血液标志物与该亚型的相关性,最后通过基础研究明确标志物参与屏障功能障碍的分子机制。
研究过程详述
生物标志物的样本来源包括AD患者、MCI患者及健康对照的血浆/血清样本,验证方法涵盖酶联免疫吸附试验(ELISA)、液相色谱-质谱联用(LC-MS)、磁共振成像(MRI)关联分析等。特异性与敏感性数据显示,GFAP联合年龄、性别、APOE ε4状态的模型可显著提高AD预测准确性(n=206 KARVIAH队列,AUC=0.87);TTR对MCI向AD转化的预测具有一定价值(n=184台湾纵向队列,5年随访,HR=1.23,P<0.05);A2M基线水平高的男性个体发展为AD的风险增加约3倍(n=303 BIOCARD队列,P<0.01)。
核心成果提炼
这些生物标志物的功能关联各有侧重:CCL2参与神经炎症与Aβ清除调控,CHI3L1与神经炎症及神经元损伤直接相关,TTR通过结合Aβ促进其清除,A2M通过RCAN1-钙调神经磷酸酶通路影响tau磷酸化。本研究的创新性在于首次系统总结了非经典AD亚型(CP/BBB功能障碍)的血液生物标志物,为AD的精准分型提供了非侵入性检测依据;同时,针对该类亚型的治疗策略突破了传统Aβ/tau靶向治疗的局限,为AD个性化治疗提供了新方向。统计学结果显示,多数标志物的临床研究均提供了明确的样本量与显著性数据,其中TTR在AD患者中的水平下降具有性别特异性(女性患者P<0.01,男性患者P>0.05),提示性别因素在AD病理进程中具有重要作用。
