1. 领域背景与文献引入
文献英文标题:Advanced single-cell and spatial analysis with high-multiplex characterization of circulating tumor cells and tumor tissue in prostate cancer: Unveiling resistance mechanisms with the CoDuCo in situ assay;发表期刊:Biomarker Research;影响因子:未公开;研究领域:前列腺癌液体活检与耐药机制研究。
前列腺癌是全球第三大常见实体恶性肿瘤,2020年全球新增病例约140万,预计2040年将增至290万。晚期前列腺癌的主要治疗手段为雄激素剥夺疗法(ADT),但多数患者会在治疗后发展为去势抵抗性前列腺癌(CRPC);新型雄激素受体(AR)靶向药物如恩扎卢胺、阿比特龙虽能延长患者生存期,但几乎所有患者最终都会出现继发性耐药。目前已知的耐药机制包括AR通路异常(如AR基因扩增、突变、AR-V7剪接变体表达)和神经内分泌转分化等AR非依赖机制,不同耐药机制对应不同的治疗选择,如AR-V7阳性患者更适合紫杉烷类化疗,神经内分泌前列腺癌患者可选择铂类化疗。然而,临床缺乏基于生物标志物的个体化治疗推荐,也缺乏可行的患者分层和耐药监测工具。
液体活检作为微创监测疾病状态的手段,近年来受到广泛关注,其中循环肿瘤细胞(CTCs)和循环肿瘤DNA(ctDNA)是主要分析物。但现有液体活检技术存在明显局限:ctDNA擅长检测遗传异常,却难以分析转录调控层面的改变;传统CTCs检测技术如抗体染色、PCR技术的多重检测能力有限,无法同时覆盖多种耐药机制相关生物标志物;此前的原位锁式探针(PLP)杂交技术仅能检测3个转录本,且依赖手动图像分析,耗时费力,难以实现临床转化。针对上述空白,本研究开发了组合双色(CoDuCo)原位杂交分析技术,大幅提升多重检测能力,并结合机器学习实现CTCs的自动化分析,为前列腺癌耐药监测和患者分层提供新工具。
2. 文献综述解析
作者对领域内研究的分类维度主要包括:前列腺癌耐药机制的研究进展、液体活检技术的现状与局限、现有CTCs检测技术的不足与改进方向。
现有研究在前列腺癌耐药机制方面已明确AR通路异常和神经内分泌转分化是主要耐药途径,且不同耐药机制对应不同治疗策略,但缺乏可同时检测多种耐药生物标志物的临床工具;液体活检领域中,ctDNA和CTCs的临床应用价值已被证实,但ctDNA无法有效分析转录调控,CTCs检测技术的多重能力不足,难以全面解析肿瘤异质性;传统原位PLP技术虽能实现单细胞水平的转录本检测,但多重能力有限,且图像分析依赖人工,效率低下。现有研究的核心局限性在于无法同时覆盖多种耐药相关生物标志物,且自动化程度不足,难以满足临床大规模应用需求。
本研究的创新价值在于:首次开发了CoDuCo双色编码原位杂交技术,理论上可实现15种转录本的同时检测,实际优化后可稳定检测11种与前列腺癌耐药、分型相关的生物标志物;结合机器学习构建了CTCs自动化分类模型,大幅降低图像分析的人力成本;实现了CTCs异质性、CTC簇的可视化分析,同时可应用于福尔马林固定石蜡包埋(FFPE)组织样本的空间转录组分析,为前列腺癌的耐药监测、患者分层提供了更全面的技术方案。
3. 研究思路总结与详细解析
本研究的核心目标是开发一种高多重、单细胞分辨率的CTCs检测技术,用于前列腺癌耐药机制监测和患者分层;核心科学问题是突破现有原位杂交技术的多重检测瓶颈,实现CTCs的自动化分析,同时解析CTCs的异质性与耐药相关生物标志物的关联;技术路线遵循“技术开发→细胞系验证→机器学习模型构建→临床样本验证→组织样本拓展”的闭环逻辑。
3.1 CoDuCo原位杂交技术开发与细胞系验证
实验目的:突破传统原位PLP技术的多重检测限制,开发可同时检测多种前列腺癌相关生物标志物的原位杂交方法,并在细胞模型中验证其特异性与准确性。
方法细节:采用双色编码策略,利用7通道荧光显微镜(6个信号通道+DAPI核染色),通过两种荧光通道信号的组合区分不同转录本,理论上可产生15种独特组合,实际因通道串扰优化为11种标记。设计针对造血(CD45等)、上皮(KRT、EPCAM)、前列腺特异性(PSA、PSMA、AR-FL、AR-V7)、神经内分泌(SYP、CHGA、NCAM1、DLL3)、间质(VIM)及预测标记(SLFN11)的锁式探针、反转录引物、桥接探针和荧光标记检测探针。将外周血单个核细胞(PBMCs)、前列腺癌细胞系(VCaP、PC-3)、非小细胞肺癌细胞系(NCI-H1299)离心涂片、固定后进行原位杂交,通过Slideview VS200数字切片扫描仪成像。
结果解读:在89%的PBMCs(n=7205)、99%的VCaP细胞(n=10620)、93%的PC-3细胞(n=6912)、100%的NCI-H1299细胞(n=19683)中均检测到特异性信号,不同细胞系呈现独特的基因表达谱:PBMCs高表达造血标记,VCaP细胞高表达AR-FL、PSA等前列腺特异性标记,PC-3细胞高表达VIM和KRT,NCI-H1299细胞高表达KRT和VIM。除SLFN11、AR-V7在PBMCs与PC-3细胞间,EPCAM、PSA、PSMA在PBMCs与NCI-H1299细胞间无显著差异外,其余标记在PBMCs与肿瘤细胞间的表达差异均具有统计学意义(q≤0.05)。
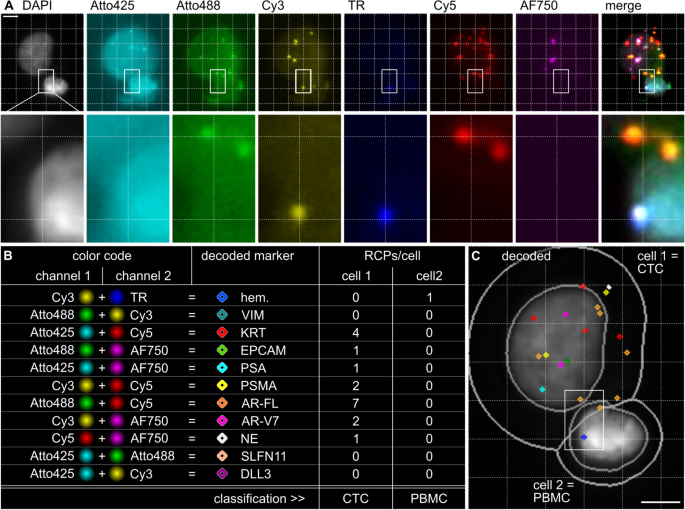
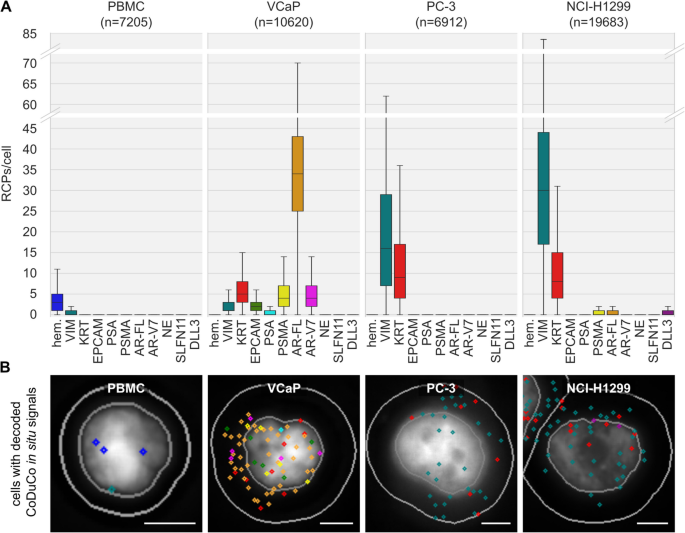
产品关联:实验所用关键产品:Cytogen Smart Biopsy Cell Isolator(CTC富集)、Slideview VS200数字切片扫描仪(成像)、CellProfiler(图像分析)、IDT的寡核苷酸探针、Thermo Fisher Scientific的TranscriptMe反转录酶、RiboLock RNase抑制剂等试剂。
3.2 机器学习CTCs分类模型的训练与验证
实验目的:构建自动化CTCs分类模型,替代手动图像分析,提升CTCs检测的效率与可重复性。
方法细节:构建包含3例健康对照、3例掺入VCaP和PC-3细胞的健康对照的数据集,共137871个细胞,通过专家手动分类为CTCs、PBMCs、人工伪影、原位假阳性细胞、原位阴性细胞5类。随机选取1000个细胞(200个CTCs、500个PBMCs、其余类各100个)训练随机森林分类器,在剩余136871个细胞的测试集中验证模型性能,最后在3例前列腺癌患者样本中测试模型的临床适用性。
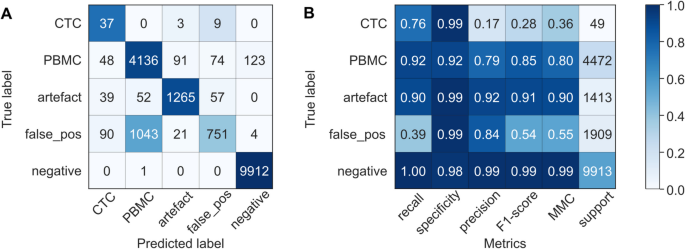
结果解读:在健康对照测试集中,分类器检测CTCs的召回率为0.89、特异性为0.99、精确率为0.88、F1-score为0.89;在患者样本中,召回率为0.76、特异性为0.99、精确率为0.17。进一步分析显示,假阴性CTCs的总信号数显著低于真阳性CTCs(中位数4 vs 35 RCPs/细胞,q≤0.0001),且KRT、PSA、AR-FL、AR-V7的表达水平显著降低;75%的假阴性CTCs无KRT表达,而97%的真阳性CTCs表达KRT,KRT阴性CTCs的分类器召回率仅0.10,远低于KRT阳性CTCs的0.92。
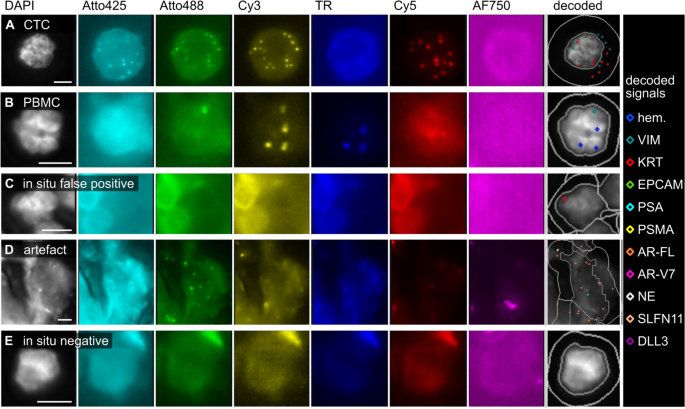
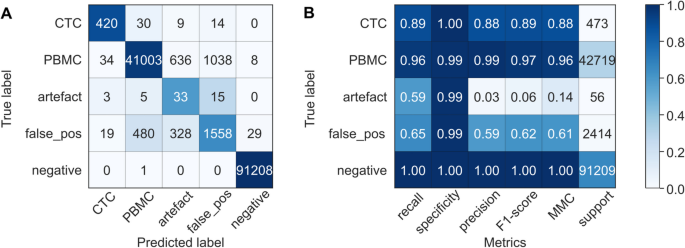
产品关联:文献未提及具体实验产品,领域常规使用Python机器学习库(如scikit-learn)、CellProfiler Analyst等工具进行模型训练与验证。
3.3 临床样本中CTCs异质性与耐药标志物分析
实验目的:验证CoDuCo技术在临床样本中检测CTCs异质性、耐药相关生物标志物的能力,并与临床参数、现有检测技术对比。
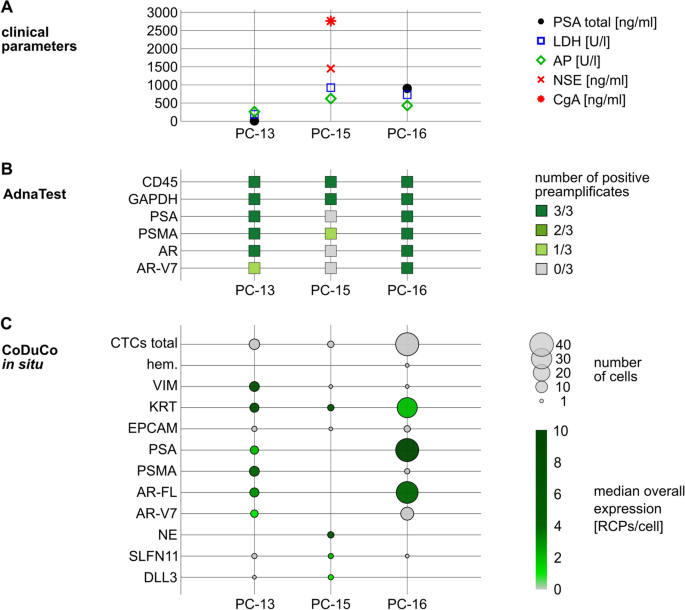
方法细节:对3例晚期前列腺癌患者的外周血样本进行CTC富集、CoDuCo原位杂交、成像,通过机器学习分类结合专家复核分析CTCs的数量、簇形成、基因表达谱,同时对比血清PSA、神经元特异性烯醇化酶(NSE)、嗜铬粒蛋白A(CgA)等临床参数,以及AdnaTest的检测结果。
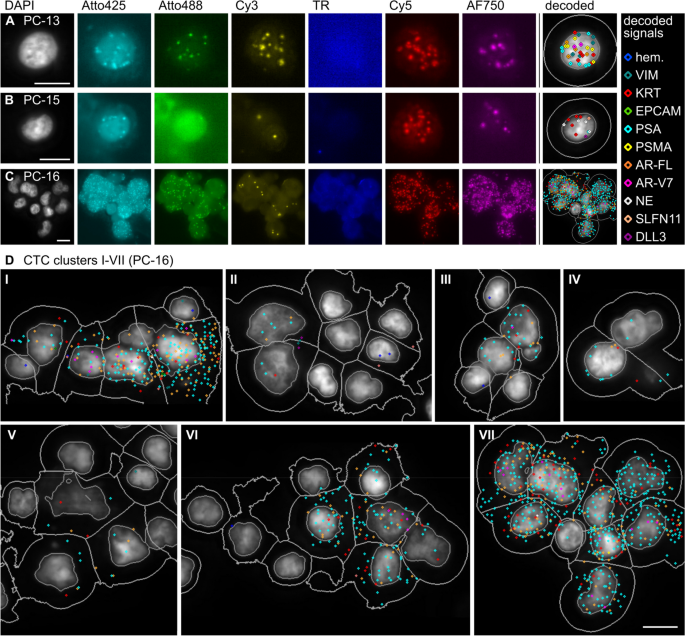
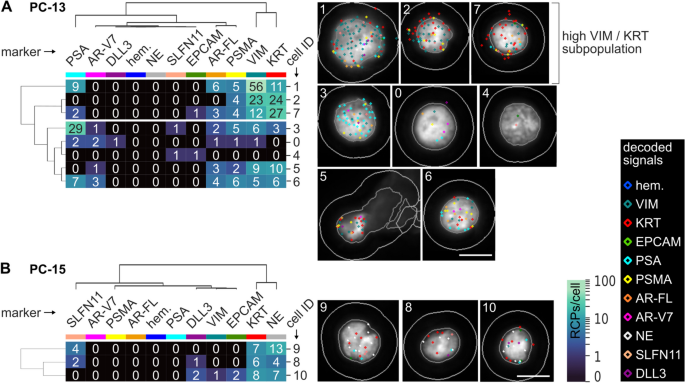
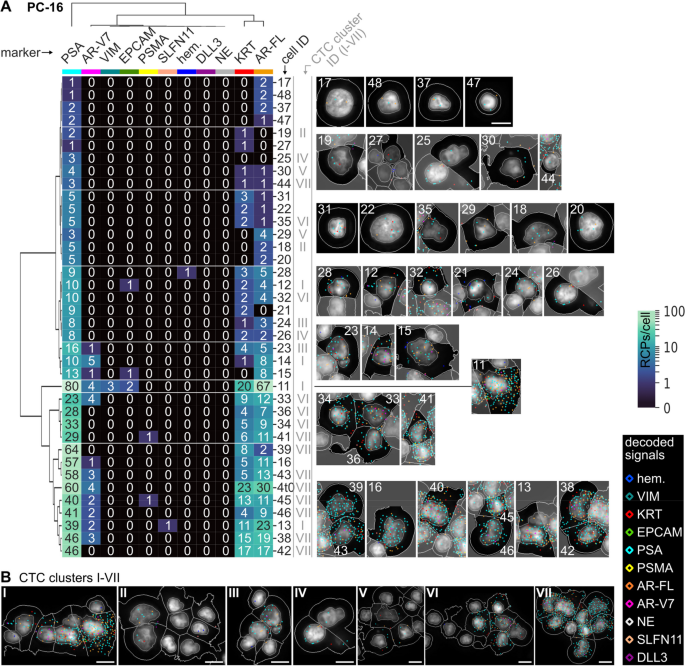
结果解读:3例患者的CTCs数量分别为8、3、38个,其中PC-16样本中26个CTCs以簇形式存在(最多包含9个细胞)。患者间CTCs表达谱存在显著异质性:PC-13的CTCs高表达VIM和KRT,中低表达前列腺特异性标记;PC-15的CTCs无前列腺特异性标记,高表达KRT和神经内分泌标记(SYP、CHGA、NCAM1)及DLL3、SLFN11;PC-16的CTCs高表达PSA,中表达AR-FL,低表达KRT、VIM、PSMA、AR-V7。患者内CTCs也存在异质性,如PC-13存在VIM/KRT高表达和前列腺特异性标记高表达的两个亚群,PC-16的CTCs中PSA、AR-FL、AR-V7的表达水平差异显著。与临床参数的一致性分析显示,血清PSA水平与CTCs中PSA表达水平高度相关(PC-13血清PSA 6.75ng/ml,CTCs中PSA中位数2 RCPs/细胞;PC-16血清PSA 904.06ng/ml,CTCs中PSA中位数10 RCPs/细胞);PC-15患者为治疗相关神经内分泌前列腺癌,血清NSE 1451ng/ml、CgA 2764ng/ml,其CTCs高表达神经内分泌标记。与AdnaTest的对比显示,PSA、PSMA、AR-FL、AR-V7的检测结果基本一致,仅PC-15中AdnaTest检测到低水平PSMA,而CoDuCo技术未检测到。
产品关联:文献未提及具体实验产品,领域常规使用AdnaTest等商业化CTCs检测试剂盒进行对比验证。
3.4 匹配CTCs与FFPE组织样本的空间分析
实验目的:拓展CoDuCo技术的应用场景,验证其在FFPE组织样本中进行空间转录组分析的能力,并对比CTCs与原发肿瘤组织的表达谱差异。
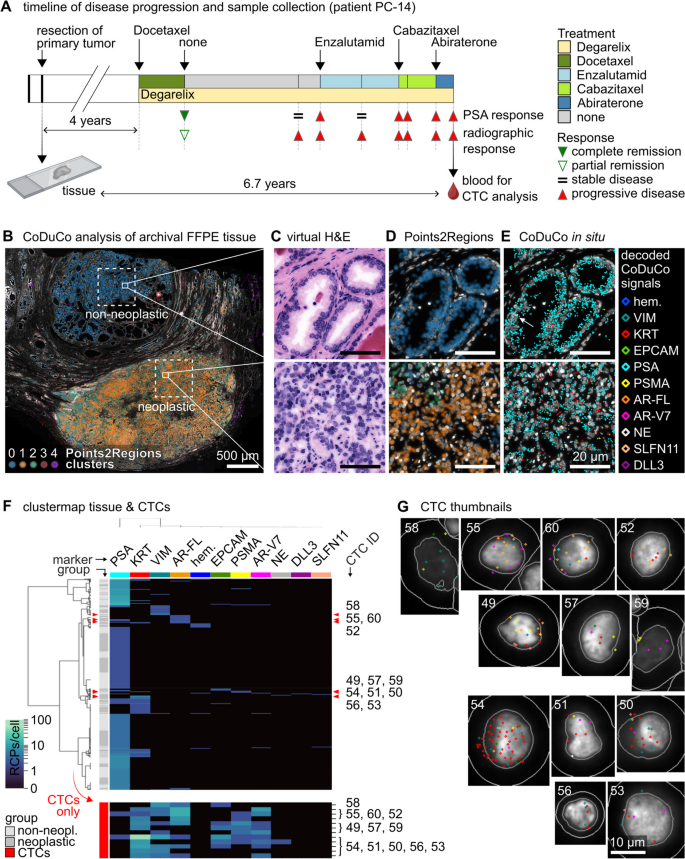
方法细节:对1例前列腺癌患者的原发肿瘤FFPE组织样本(手术切除)和6.7年后的外周血CTCs样本进行CoDuCo原位杂交,通过TissUUmaps进行空间聚类分析,同时通过分层聚类对比CTCs与组织样本的表达谱差异。
结果解读:CoDuCo技术成功应用于FFPE组织样本,空间聚类分析显示非肿瘤上皮、肿瘤组织、基质的表达谱存在显著差异,单细胞水平的分层聚类发现了罕见的神经内分泌细胞。CTCs与原发肿瘤组织的表达谱存在明显差异:CTCs中PSA表达显著降低,KRT、VIM、AR-FL、EPCAM、PSMA、AR-V7的表达水平显著升高,提示肿瘤在长期治疗压力下发生了进化,出现了与耐药相关的表达改变。
产品关联:文献未提及具体实验产品,领域常规使用TissUUmaps、seaborn等工具进行空间转录组与聚类分析。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究涉及的Biomarker包括前列腺特异性标记(PSA、PSMA、AR-FL、AR-V7)、神经内分泌标记(SYP、CHGA、NCAM1、DLL3)、上皮标记(KRT、EPCAM)、间质标记(VIM)、造血标记(CD45等)及预测标记(SLFN11)。筛选逻辑基于前列腺癌的耐药机制、治疗靶点及肿瘤生物学特征,验证逻辑遵循“细胞系验证→机器学习模型构建→临床样本验证→与临床参数/现有技术对比”的完整链条。
研究过程详述
Biomarker的来源为患者外周血CTCs和FFPE组织样本,验证方法为CoDuCo原位杂交技术,通过双色编码信号实现单细胞水平的转录本检测,结合图像分析与机器学习进行细胞分类和信号计数。特异性验证显示,不同细胞系的Biomarker表达具有明显特异性,如PBMCs高表达造血标记,前列腺癌细胞系高表达前列腺特异性标记;敏感性方面,机器学习分类器在患者样本中检测CTCs的召回率为0.76,特异性为0.99,可有效区分CTCs与正常细胞。
核心成果提炼
- 开发了CoDuCo原位杂交技术,可同时检测11种与前列腺癌耐药、分型相关的Biomarker,实现单细胞分辨率的CTCs分析,可可视化CTCs异质性、CTC簇,同时可应用于FFPE组织的空间转录组分析;
- 揭示了CTCs异质性与前列腺癌耐药的关联,如神经内分泌前列腺癌患者的CTCs高表达神经内分泌标记和DLL3、SLFN11,提示神经内分泌转分化耐药机制;
- 验证了CTCs中PSA表达与血清PSA水平的一致性,支持CTCs作为监测前列腺癌治疗反应的Biomarker;
- 发现CTC簇与肿瘤转移潜能的关联,PC-16样本中的CTC簇可能提示不良预后;
- 对比了CTCs与原发肿瘤组织的表达谱差异,揭示了肿瘤在治疗压力下的进化过程,为耐药机制研究提供了新视角。
统计学结果:细胞系验证中,多数Biomarker在PBMCs与肿瘤细胞间的表达差异具有统计学意义(q≤0.05);患者样本中,假阴性与真阳性CTCs的信号数及KRT、PSA、AR-FL、AR-V7的表达差异具有统计学意义(q≤0.0001至q≤0.05);患者间CTCs的VIM、PSMA、PSA、神经内分泌标记、SLFN11、DLL3的表达差异具有统计学意义(q≤0.05)。