1. 领域背景与文献
文献英文标题:Tumor-specific antibody cocktail treatment suppresses colorectal tumor growth in mice;发表期刊:Cancer Immunology, Immunotherapy;影响因子:未公开;研究领域:肿瘤免疫治疗(结直肠癌个性化治疗方向)。
领域共识:结直肠癌是全球第三大常见恶性肿瘤,近年发病率在年轻人群中持续上升,晚期患者缺乏治愈性治疗手段,即使初始治疗响应良好,复发率仍高达60%以上,是全球癌症相关死亡的主要原因之一。领域发展关键节点:2010年后免疫检查点抑制剂逐步应用于结直肠癌治疗,但仅对微卫星高度不稳定的少数患者有效;2018年以来个性化新抗原疫苗、过继性T细胞治疗等精准疗法进入临床,但受限于制备周期长、人类白细胞抗原(HLA)限制性等问题,普及难度较高。当前研究热点为针对肿瘤特异性突变的个性化治疗策略,核心未解决问题为肿瘤异质性导致的传统靶向药物覆盖不足、现有免疫治疗响应率低,缺乏兼具高特异性、普适性的个性化治疗方案。
现有结直肠癌治疗策略多以通用肿瘤相关抗原为靶点,无法匹配不同患者的独特突变图谱,难以克服肿瘤异质性导致的耐药。本研究针对这一空白,开发基于肿瘤特异性突变表面蛋白的个性化多克隆抗体鸡尾酒疗法,将肿瘤异质性从治疗限制因素转化为治疗靶点,为晚期结直肠癌提供新的治疗范式。
2. 文献综述解析
作者的文献综述按“临床需求-现有疗法局限性-新技术潜力”的维度展开,系统梳理了结直肠癌治疗的现有进展与未满足需求,为本次研究的合理性提供充分支撑。
现有研究的核心结论包括:肿瘤异质性是结直肠癌治疗耐药和复发的核心驱动因素,体细胞突变的累积导致不同患者、同一肿瘤内部的细胞抗原表达存在显著差异;抗体类药物具有高特异性和多样性,人体天然抗体库容量可达10^15种,足以覆盖各类肿瘤特异性突变;作者团队前期已在三阴性乳腺癌、黑色素瘤等模型中验证了靶向突变表面蛋白的多克隆抗体鸡尾酒可有效抑制肿瘤生长,验证了该策略的可行性。现有技术的优势包括:全外显子测序可高效识别肿瘤特异性突变,多克隆抗体制备技术成熟,免疫检查点抑制剂可有效激活宿主抗肿瘤免疫。现有研究的局限性包括:传统单克隆抗体仅靶向单个通用靶点,受肿瘤异质性限制响应率低;现有结直肠癌个性化治疗多集中在细胞疗法和疫苗领域,存在制备周期长、依赖宿主T细胞功能等问题,暂无针对结直肠癌的个性化抗体鸡尾酒疗法的相关报道。
本研究的创新价值在于首次将突变表面蛋白靶向的多克隆抗体鸡尾酒策略应用于结直肠癌领域,同时验证了该策略与免疫检查点抑制剂的协同效应,通过癌症基因组图谱(TCGA)临床数据明确了该疗法在人类患者中的可行性,填补了结直肠癌个性化抗体治疗的空白,为克服肿瘤异质性提供了新的研究方向。
3. 研究思路总结与详细解析
本研究的核心目标是验证靶向肿瘤特异性突变表面蛋白的多克隆抗体鸡尾酒对结直肠癌的治疗效果及临床转化潜力,核心科学问题为靶向多个异质性突变位点的抗体能否实现对肿瘤细胞的全覆盖,有效抑制结直肠癌生长并延长生存期,技术路线遵循“靶点筛选-抗体制备-体外验证-体内疗效评估-临床转化潜力分析”的闭环逻辑,所有实验均设置合理对照,数据统计严谨。
3.1 突变表面蛋白靶点筛选与多克隆抗体制备
本环节的核心实验目的是筛选CT26结直肠癌细胞中特异性表达的细胞表面突变蛋白,制备对应的高特异性多克隆抗体。方法细节为:对CT26细胞的全外显子测序数据与BALB/c小鼠参考基因组进行比对,共识别出1354个编码区错义突变,其中11.2%位于质膜蛋白、5.6%位于细胞连接蛋白、2.6%位于细胞外基质蛋白,从中筛选出10个不考虑蛋白功能的表面突变位点,合成包含突变位点的11聚体肽段,通过免疫兔子制备并纯化多克隆抗体,抗体纯度均高于80%。结果解读显示:酶联免疫吸附实验(ELISA)检测结果表明,10种多克隆抗体对对应靶点肽段的半数有效浓度(EC50)范围为1.75×10^-11 M至5.36×10^-11 M,均具备皮摩尔级的高亲和力,验证了抗体制备的有效性。
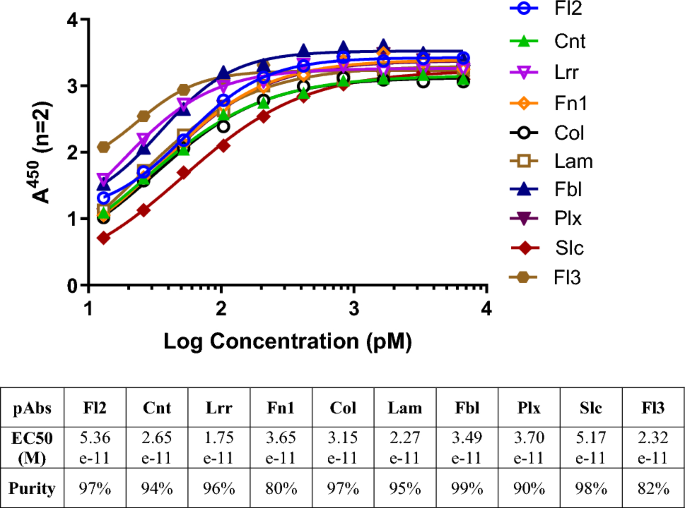
产品关联:实验所用关键产品:金斯瑞的定制多肽合成及多克隆抗体制备服务、赛默飞世尔科技的酶联免疫吸附实验相关试剂,文献未提及具体货号,领域常规使用基因测序、多肽合成、抗体制备类试剂完成该环节实验。
3.2 抗体结合特异性体外验证
本环节的核心实验目的是验证制备的多克隆抗体对CT26肿瘤细胞的特异性结合能力,排除对正常组织的交叉反应,同时验证抗体的累加结合效应。方法细节为:采用免疫荧光(IF)染色检测10种抗体对CT26肿瘤组织切片的结合能力,采用流式细胞术(FCM)检测抗体对活CT26细胞表面的结合能力,同时将10种抗体等浓度混合制备鸡尾酒,检测其对小鼠各正常器官组织的结合情况;通过逐步增加抗体鸡尾酒中的抗体种类,检测结合信号的变化趋势。结果解读显示:免疫荧光染色结果表明10种抗体均可特异性结合CT26肿瘤组织,无明显非特异性染色;流式细胞术检测显示所有抗体对CT26细胞的结合信号均显著高于同型对照抗体,验证了抗体对天然表达靶点的结合能力。
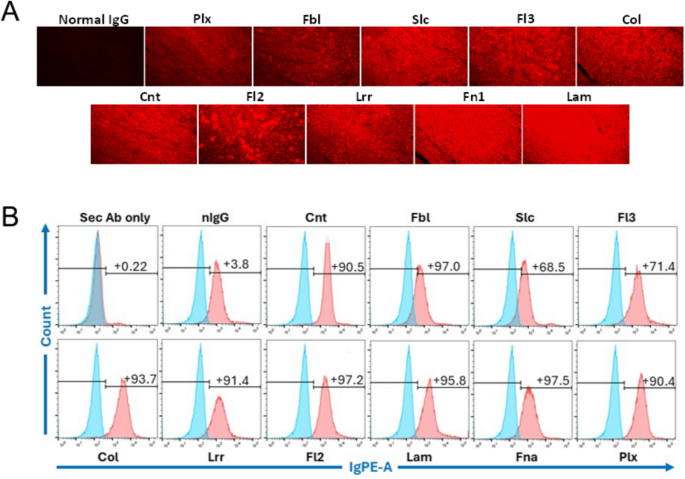
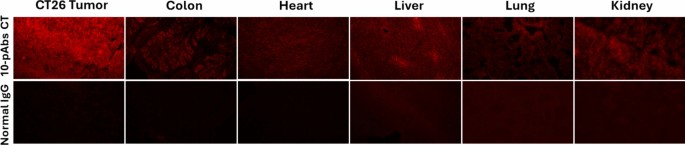
抗体鸡尾酒对CT26肿瘤组织具有强结合信号,但对小鼠心、肝、脾、肺、肾等正常组织仅有极弱的背景结合,提示抗体无明显脱靶效应,安全性良好。
随着抗体鸡尾酒中加入的抗体种类逐步增加,免疫荧光染色信号和流式细胞术的结合信号均呈累加式升高,提示不同抗体可识别肿瘤细胞表面的不同靶点,实现对异质性肿瘤细胞群的全覆盖。
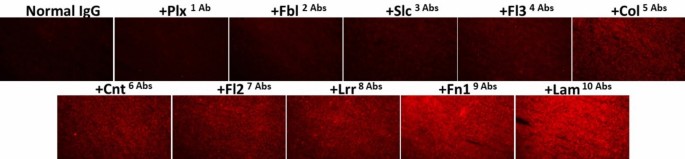
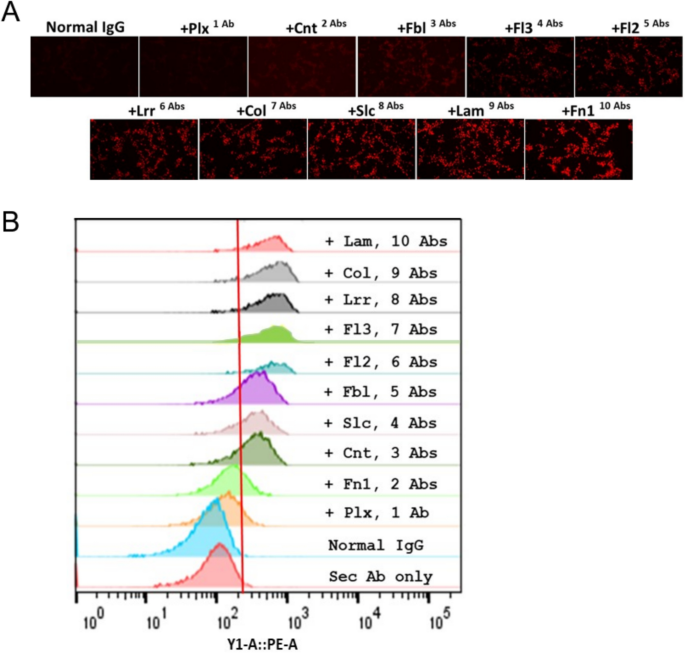
产品关联:实验所用关键产品:宝日医生物的藻红蛋白(PE)标记驴抗兔IgG、立菲泰克的Alexa Fluor 568标记山羊抗兔IgG,文献未提及具体货号,领域常规使用免疫荧光、流式细胞术检测类试剂完成该环节实验。
3.3 体内抑瘤疗效验证
本环节的核心实验目的是验证多克隆抗体鸡尾酒单药及联合程序性死亡受体1(PD-1)抑制剂对结直肠癌的抑瘤效果和生存获益。方法细节为:采用6-7周龄雌性BALB/c小鼠皮下接种1×10^6个CT26细胞构建同源移植瘤模型,接种后3天开始分组给药,共设置6组(n=6/组),分别为未处理组、程序性死亡受体1抑制剂单药组、程序性死亡受体1同型对照组、正常IgG联合程序性死亡受体1组、抗体鸡尾酒单药组、抗体鸡尾酒联合程序性死亡受体1组;抗体鸡尾酒为每日皮下瘤周注射,共给药7天;程序性死亡受体1抑制剂为每2天腹腔注射1次,共给药5次;实验期间每2天检测肿瘤体积和小鼠体重,记录小鼠生存期,肿瘤体积达到2000 mm^3时按伦理要求安乐死。结果解读显示:程序性死亡受体1抑制剂单药组的肿瘤生长情况与对照组无显著差异,抗体鸡尾酒单药组的肿瘤生长较对照组显著抑制(P<0.0001,n=6),抗体鸡尾酒联合程序性死亡受体1抑制剂组的肿瘤生长几乎完全停滞,中位生存期延长至86天,而对照组的中位生存期仅为15.5-19天(P<0.0003,n=6);治疗期间各组小鼠体重无显著下降,提示抗体治疗无明显系统毒性。
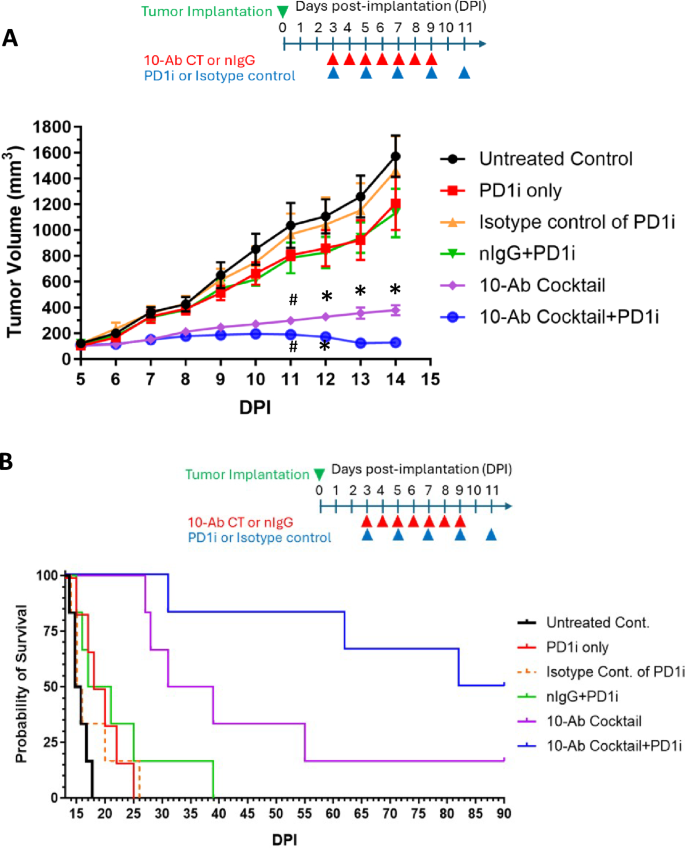
产品关联:实验所用关键产品:博奥信的抗小鼠程序性死亡受体1抗体(克隆号RMP1-14)、大鼠IgG2a同型对照抗体(克隆号2A3),文献未提及具体货号。
3.4 人类结直肠癌临床转化潜力分析
本环节的核心实验目的是验证该抗体鸡尾酒策略在人类结直肠癌患者中的应用可行性。方法细节为:提取癌症基因组图谱数据库中100例结直肠癌患者的全外显子测序数据,比对肿瘤组织与配对正常组织的错义突变,通过UniProt数据库注释突变蛋白的亚细胞定位,筛选位于细胞表面的突变表面蛋白(MSP),统计每例患者的突变表面蛋白数量及不同患者间的突变表面蛋白重合率。结果解读显示:100例患者的中位错义突变数为76.5个(IQR:5-958,n=100),中位突变表面蛋白数量为24.75个(IQR:1-1712,n=100),96%的患者携带至少10个突变表面蛋白,足以支持10种抗体的鸡尾酒疗法的制备;但患者间的突变表面蛋白重合度极低,仅0.088%的突变表面蛋白在3例及以上患者中存在,无突变表面蛋白在超过8例患者中共享,提示该疗法无法采用通用制剂,必须为每位患者个性化制备对应的抗体鸡尾酒。
基于上述结果,作者提出了个性化突变表面蛋白靶向抗体鸡尾酒的临床转化工作流,涵盖患者肿瘤测序、靶点筛选、抗体制备、给药治疗的全流程,为后续临床试验提供了清晰的路径。
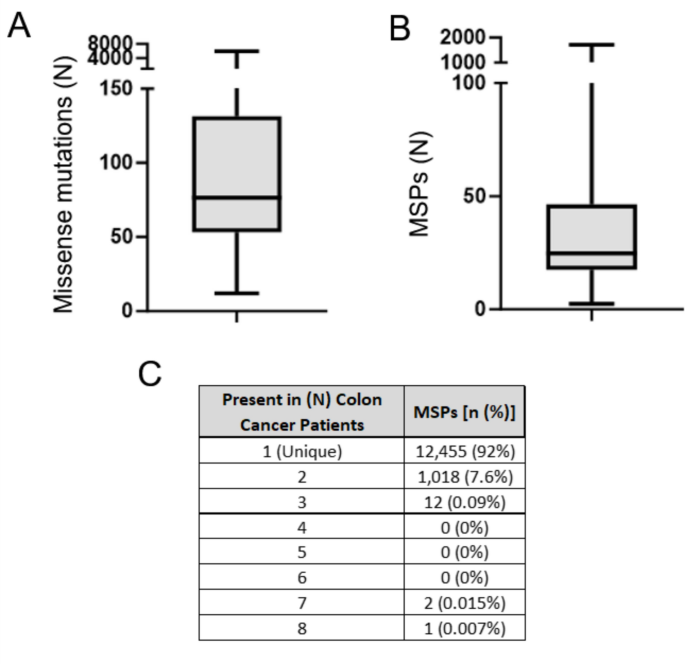
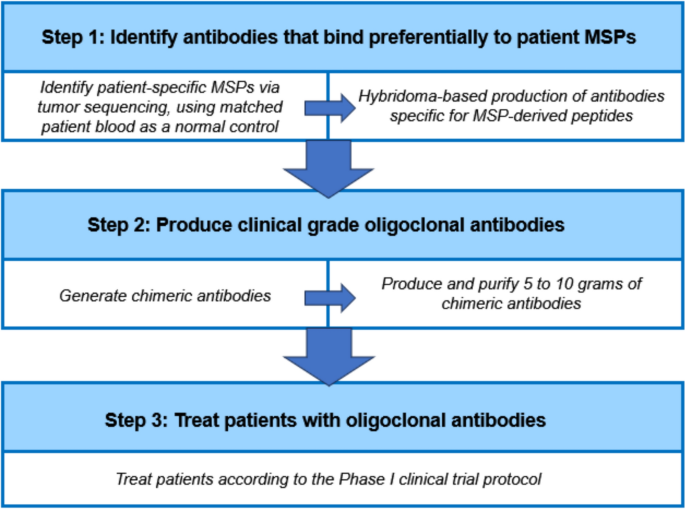
产品关联:文献未提及具体实验产品,领域常规使用R语言、UniProt数据库、癌症基因组图谱公共数据库完成该环节的生物信息学分析。
4. Biomarker 研究及发现成果
本研究涉及的Biomarker为肿瘤特异性突变表面蛋白,属于治疗靶点类Biomarker,筛选验证逻辑为“全外显子测序识别肿瘤特异性突变→亚细胞定位注释筛选表面突变→抗体制备→体外结合验证→体内功能验证→临床人群可行性分析”,逻辑链条完整,数据支撑充分。
突变表面蛋白的来源为肿瘤细胞的体细胞错义突变,仅在肿瘤细胞表面表达,正常组织无对应表达;验证方法包括全外显子测序的突变鉴定、酶联免疫吸附实验的抗体亲和力检测、免疫荧光和流式细胞术的细胞结合特异性检测、体内抑瘤实验的功能验证;特异性数据显示,靶向突变表面蛋白的抗体鸡尾酒对正常组织无明显交叉反应,仅特异性结合肿瘤细胞,累加结合效应可覆盖异质性的肿瘤细胞亚群;敏感性数据显示,单种突变表面蛋白靶向抗体的半数有效浓度可达1.75×10^-11 M至5.36×10^-11 M,联合使用后结合信号随抗体种类增加逐步升高,可实现对低丰度靶点的有效识别。
核心成果方面,突变表面蛋白作为结直肠癌个性化治疗的靶点,对应的多克隆抗体鸡尾酒联合程序性死亡受体1抑制剂可将荷瘤小鼠的中位生存期延长至86天(文献未明确提供风险比(HR)数据,文献未明确提供该数据,基于图表趋势推测,P<0.0003,n=6),较对照组提升4倍以上;创新性为首次在结直肠癌领域验证了靶向个性化突变表面蛋白的抗体鸡尾酒疗法的可行性,突破了传统靶向治疗受限于肿瘤异质性的瓶颈,且96%的人类结直肠癌患者具备足够的突变表面蛋白靶点支持该疗法的应用,具有极高的临床转化价值。统计学结果显示,抗体鸡尾酒单药及联合治疗的抑瘤效果均具有显著统计学差异(P<0.0001,n=6),人类患者的突变表面蛋白中位数量为24.75个(IQR:1-1712,n=100),96%的患者满足靶点数量要求。
